Способы выражения состава растворов
1. Смешали 200 г 20%-ного и 300 г 10%-ного растворов глюкозы. Массовая доля вещества в полученном растворе равна …
| 1) 15% | 2) 18% | 3) 14% | 4) 16% |
2. Объем аммиака (н.у.), необходимый для получения 15% раствора аммиака из 500 г 10% раствора, равен…
| 1) 16,05 л; | 2) 38,75 л; | 3) 32,94 л; | 4) 44,8 л |
3. Масса воды, необходимая для приготовления 400 г 20%-ного раствора нитрата калия, равна …
а) 160 г б) 320 г в) 360 г г) 80 г
4. Для приготовления 2 л раствора соляной кислоты с рН = 1 требуется моль HCl …
а) 0,1 б) 2,0 в) 0,2 г) 1,0
5. Масса растворенного вещества в 500 мл 0,1М раствора серной кислоты равна …
а) 4,9 г б) 49 г в) 9,8 г г) 24,5 г
6. Раствор, в 1 л которого содержится 0,01 моль азотной кислоты, имеет рН, равный…
а) 12 б) 11 в) 4 г) 2
7. Молярная концентрация раствора, в 2 л которого содержится 19,6 г серной кислоты, равна ____ моль/л
а) 0,2 б) 0,1 в) 1,0 г) 0,5
8. Масса соли, необходимая для приготовления 200 мл 10%-ного раствора хлорида натрия (r = 1,1 г/мл), равна …
а) 20 б) 44 в) 22 г) 40
9. 50 г сахарозы растворили в 450 г воды. Массовая доля растворенного вещества в растворе равна …
а) 15% б) 10% в) 22% г) 20%
10. Масса соли, необходимой для приготовления 2 л 0,2М раствора сульфата магния равна
а) 96 б) 48 в) 24 г) 72
11. Массовая доля фосфата калия в растворе, полученном при растворении 0,5 моль соли в 124 мл воды, равна …%.
а) 69 б) 23 в) 46 г) 72
12. Масса растворенного вещества в 500 мл 25%-ного раствора фосфорной кислоты (rr = 1,2 г/мл) равна …
а) 100 г б) 104 г в) 150 г г) 250 г
13. Молярная концентрация 1 л 36,5%-ного раствора соляной кислоты (r = 1,18 г/мл) составляет ____ моль/л
а) 11,8 б) 5 в) 5,6 г) 10
14. В 2 л 10%-ного раствора фосфорной кислоты (r = 1,05 г/мл) содержится ____ граммов растворенного вещества
а) 420 б) 105 в) 200 г) 210
4151. Для приготовления 500 г 10%-ного раствора сульфата калия необходимо навеску соли растворить в ___ граммах воды
а) 50 б) 500 в) 450 г) 400
16. Масса растворенного вещества в растворе, полученном при сливании 160 г 5%-ного и 240 г 10%-ного растворов, равна ____ граммов
а) 32 б) 24 в) 400 г) 40
17. Для приготовления 1 л раствора гидроксида калия с рН 12 необходимо ___ моль KOH
а) 0,02 б) 2 в) 1 г) 0,01
18. В 400 мл 0,2М раствора нитрата натрия содержится ___ граммов соли
а) 6,8 б) 68 в) 34 г) 13,6
19. Масса соли, необходимая для приготовления 2 л 0,2М раствора сульфата магния, равна
а) 24 б) 72 в) 48 г) 96
20. Для приготовления 0,5 л 0,2М раствора глюкозы необходимо растворить ___ г вещества
а) 9 б) 90 в) 45 г) 18
21. В 50 граммах 10%-ного раствора NaCl содержится ___ молекул воды
| 1) 3,01*1024 | 2) 3,01*1023 | 1,505*1024 | 4) 6,02*1024 |
22. Масса HNO3, необходимая для взаимодействия с раствором NaOH объемом 70 мл и концентрацией щелочи 0,5 моль/л, составляет ___ грамма
| 1) 0,5 г | 3) 2,2 г |
| 2) 6,3 | 4) 0,35 |
23. Объем аммиака (н.у.), содержащийся в 50 граммах 20%-ного раствора NH3, составляет
| 1) 13,2 мл | 3) 13,2 л |
| 2) 1,32 л | 4) 1,32 мл |
24. Масса уксусной кислоты, содержащейся в растворе, на нейтрализацию которого израсходовано 250 мл раствора гидроксида натрия с молярной концентрацией 0,2 моль/л, составляет ___ грамма(ов).
| 1) 3,0 | 3) 1,5 |
| 2) 6,0 | 4) 7,5 |
25. Молярная концентрация HNO3 в 250 мл раствора, содержащего 12,6 г кислоты равна ___ моль/л
| 1) 0,2 | 3) 2,0 |
| 2) 0,8 | 4) 8,0 |
26. Массовая доля HCl в растворе соляной кислоты, полученном при растворении 5,6 л хлороводорода (н.у.) в 1 литре воды
| 1) 9% | 3) 0,45% |
| 2) 0,9% | 4) 4,5% |
27. Масса HNO3, необходимая для взаимодействия с раствором NaOH объемом 70 мл и концентрацией щелочи 0,5 моль/л, составляет ___ грамма
| 1) 0,35 г | 3) 0,5 г |
| 2) 6,3 г | 4) 2,2 г |
28. В растворе гидроксида натрия объемом 2 л и концентрацией 0,5 моль/л содержится ___ г растворенного вещества.
| а) 60 | б) 40 | в) 20 | г) 80 |
29. В растворе серной кислоты объемом 0,5 л и концентрацией 0,1 моль/л содержится ___ г растворенного вещества.
| а) 98 | б) 9,8 | в) 4,9 | г) 49 |
30. В 1 л раствора азотной кислоты, имеющего рН = 1, содержится ___ моль кислоты.
| а) 10 | б) 0,5 | в) 0,2 | г) 0,1 |
31. В 1 л раствора гидроксида калия, имеющего рН = 13, содержится ___ моль KOH.
| а) 1 | б) 0,1 | в) 0,5 | г) 0,2 |
32. В 50 граммах 3,65%-ного раствора HCl содержится ___ молекул растворенного вещества
| а) 3,01*1024 | б) 3,01*1022 | в) 3,01*1023 | г) 1,75*1023 |
33. Молярная концентрация раствора, в 200 мл которого содержится 12 г уксусной кислоты, равна ___ моль/л
| а) 1 | б) 0,5 | в) 2 | г) 0,2 |
34. Моляльная концентрация имеет размерность
| а) моль/л | б) г/моль | в) моль/кг | г) л/моль |
35. Мольная доля растворенного вещества может быть выражена в
| а) г/моль | б) процентах | в) моль/кг | г) моль/л |
36. Для приготовления 1 л раствора соляной кислоты, имеющего рН 1, требуется ___ моль HCl.
| а) 0,1 | б) 1,0 | в) 0,5 | г) 0,2 |
37. В 400 г раствора гидроксида натрия с массовой долей растворенного вещества 10% содержится ___ моль NaOH.
| а) 0,5 | б) 0,1 | в) 1 | г) 2 |
38. Для приготовления 500 г с моляльной концентрацией 0,5 моль/кг раст вора CuSO4 требуется ___ г растворенного вещества.
| а) 80 | б) 160 | в) 40 | г) 20 |
39. В растворе нитрата калия объемом 0,5 л и концентрацией 0,1 моль/л, содержится ___ г растворенного вещества.
| а) 50,5 | б) 5,05 | в) 101 | г) 10,1 |
40. Массовая доля растворенного вещества может быть выражена в
| а) моль/кг | в) г/моль |
| б) г/л | г) долях или % |
41. Для приготовления 500 г с моляльной концентрацией 1 моль/кг раствора NaOH требуется ___ г растворенного вещества.
| а) 60 | б) 20 | в) 80 | г) 40 |
42. Мольная доля растворенного вещества может быть выражена в
| а) моль/кг | в) г/моль |
| б) моль/л | г) долях или % |
43. Молярная концентрация раствора, в 500 мл которого содержится 16 г сульфата меди, равна ___ моль/л.
| а) 1 | б) 0,1 | в) 0,2 | г) 2 |
44. Молярная концентрация вдвое меньше молярной концентрации эквивалента для
| а) ZnSO4 | б) HCl | в) KNO3 | г) AlCl3 |
45. Массовая доля сахара в растворе, полученном при растворении 10 г сахара в 190 г воды, равна
| а) 0,4 | б) 0,1 | в) 0,05 | г) 0,01 |
46. Масса серной кислоты, содержащая в 1 л 0,1н раствора
| а) 49 г | б) 98 г | в) 9,8 г | г) 4,9 г |
47. Если концентрация хлорид-ионов в водном растворе хлорида алюминия (AlCl3) равна 0,06 моль/л, то концентрация соли составляет ___ моль/л.
| а) 0,02 | б) 0,04 | в) 0,03 | г) 0,06 |
48. Молярная концентрация эквивалента равна молярности для раствора
| а) ZnSO4 | б) CaCl2 | в) H2SO4 | г) KNO3 |
49. Для нахождения моляльной концентрации раствора нужно воспользоваться формулой
а) 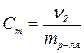 | в) 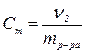 |
б) 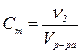 | г) 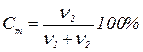 |
50. Для приготовления 200 г раствора с массовой долей хлорида калия 8% навеску соли необходимо растворить в ___ граммах воды.
| а) 84 | б) 184 | в) 192 | г) 92 |
51. Под концентрацией раствора понимают
1) сумму количеств растворенного вещества и растворителя
2) плотность раствора
3) содержание растворенного вещества (в определенных единицах) в единице массы или объема раствора
4) давление насыщенных паров растворителя в зависимости от количества растворенного вещества
52. Величиной, выражающей количественный состав раствора, является
| 1) эквивалентность | 3) концентрация |
| 2) парциальное давление | 4) плотность |
