Агрегатные состояния вещества
МОЛЕКУЛЯРНАЯ ФИЗИКА
- Что называют фазой? Агрегатным состоянием вещества?
- Сравните свойства вещества в трех агрегатных состояниях: твердом жидком и газообразном?
- Что называют фазовым переходом первого рода? второго рода? Приведите примеры этих переходов.
- Что называется испарением, конденсацией?
- Почему испарение происходит при любой температуре?
- Что называют удельной теплотой парообразования?
- Как изменяется скорость испарения с повышением температуры? Повышением давления?
- Чем отличается насыщенный пар от ненасыщенного?
- Подчиняется ли газовым законам насыщенный пар? Ненасыщенный пар?
- От чего зависит давление насыщенного пара?
- Что называют абсолютной влажностью? Относительной влажностью?
- Что такое точка росы? Как по точке росы можно определить абсолютную и относительную влажность воздуха?
- Чем кипение отличается жидкости отличатся от ее испарения?
- Может ли вода кипеть при температуре ниже 100 0С? Выше 100 0С?
- Почему ожог паром сильнее, чем кипятком?
- Какое состояние вещества называют газом? паром?
- Каков физический смысл критической температуры?
- Можно ли при температуре выше критической перевести вещество из парообразного состояния в жидкое?
- Почему при критической температуре теплота парообразования для всех жидкостей равна нулю?
- Объясните механизм уменьшения свободной поверхности жидкости.
- Что называют поверхностной энергией? Силой поверхностного натяжения?
- Как изменяется поверхностное натяжение у вех веществ с увеличением температуры?
- Что представляет собой поверхностно-активные вещества?
- От чего зависит смачивание (несмачивание) жидкостью поверхности твердого тела? Может ли одна и та же жидкость быть смачивающей и несмачивающей? Приведите примеры.
- Что называют полным смачиванием? полным несмачиванием?
- Жидкость налита в сосуд. Когда мениск будет вогнутым? Выпуклым? Дайте объяснение.
- Когда жидкость в капилляре опускается? Поднимается? Дайте объяснение этому явлению.
- Выведите формулу. Определяющую высоту подъема столба жидкости в капилляре.
Ответы
- Часть объема системы, во всех точках которой физические и химические свойства одинаковы, отделенная от других частей системы поверхностью раздела, называют фазой. Агрегатное состояние веществ внутри одной и той же фазы одинаково (твердая фаза, жидкая фаза, газообразная фаза) Агрега́тное состоя́ние вещества (лат. aggrego 'присоединяю') — состояние одного и того же вещества в определённом интервале температур и давлений, характеризующееся определёнными, неизменными в пределах указанных интервалов, качественными свойствами:
- . При Ф. п. первого рода скачком меняются такие термодинамические характеристики вещества, как плотность, концентрация компонент; в единице массы выделяется или поглощается вполне определённое количество теплоты, носящее название теплоты перехода. При Ф. п. второго рода некоторая физическая величина, равная нулю с одной стороны от точки перехода, постепенно растет (от нуля) при удалении от точки перехода в другую сторону. При этом плотность и концентрации изменяются непрерывно, теплота не выделяется и не поглощается. Примеры Ф. п. II рода – появление (ниже определённой в каждом случае температуры) магнитного момента у магнетика при переходе парамагнетик – ферромагнетик, антиферромагнитного упорядочения при переходе парамагнетик – антиферромагнетик, возникновение сверхпроводимости в металлах и сплавах, возникновение сверхтекучести в 3He и 4He, упорядочение сплавов, появление самопроизвольной (спонтанной) поляризации вещества при переходе параэлектрик – сегнетоэлектрик и т.д. К Ф. п. 1 рода относятся: испарение и конденсация, плавление и затвердевание, сублимация и конденсация в твёрдую фазу, некоторые структурные переходы в твёрдых телах, например образование мартенсита в сплаве железо – углерод. В антиферромагнетиках с одной осью намагничивания магнитных подрешёток Ф. п. 1 рода происходит во внешнем магнитном поле, направленном вдоль оси
- Испаре́ние — процесс перехода вещества из жидкого состояния в газообразное, происходящий на поверхности вещества (пар) КОНДЕНСАЦИЯ - переход вещества из газообразного состояния (пара) в жидкое или твёрдое состояние
- - это парообразование с поверхности жидкости.
При этом жидкость покидают более быстрые молекулы, обладающие большей скоростью.
При любой температуре в жидкости находятся такие молекулы, которые обладают достаточной кинетической энергией, чтобы преодолеть силы сцепления между молекулами и совершить работу выхода из жидкости.
Скорость испарения жидкости зависит от:
1) от рода вещества;
2) от площади поверхности испарения;
3) от температуры жидкости;
4) от скорости удаления паров с поверхности жидкости, т.е. от наличия ветра.
Испарение происходит при любой температуре.
С повышением температуры скорость испарения жидкости возрастает, так как возрастает средняя кинетическая энергия ее молекул, а следовательно, возрастает и число таких молекул, у которых кинетическая энергия достаточна для испарения.
Скорость испарения возрастает и при ветре, который удаляет с поверхности жидкости ее пар и тем самым препятствует возвращению молекул в жидкость. - Удельной теплотой парообразования данной жидкости называется отношение теплоты парообразования жидкости к ее массе:
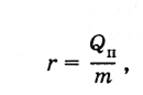
- Увеличивается, потому что при нагревании кинетическая энергия молекул жидкости возрастает и молекулы способны быстрее "вырваться" с поверхности данной жидкости
- Вещество в газообразном состоянии, находящееся в динамическом равновесии с жидкостью, называют насыщенным паром. (Паром называют совокупность молекул, покинувших жидкость в процессе испарения.) Пар, находящийся при давлении ниже насыщенного, называют ненасыщенным.
- Опыт показывает, что ненасыщенные пары подчиняются всем газовым законам, и тем точнее, чем дальше они от насыщения
- от объема, от температуры, от вещества
- Вес, или точнее масса, водяного пара, содержащегося в 1 м3 воздуха, называется абсолютной влажностью воздуха Отношение величины абсолютной влажности воздуха при данной температуре к величине его влагоемкости при той же температуре называется относительной влажностью воздуха.
- Точка Росы определяет то соотношение температуры и влажности воздуха и температуры поверхности, при котором на поверхности начинает конденсироваться вода.
- Кипение и испарение - это процесс, при котором вещество переходит из жидкого состояния в газообразное состояние. Кипение отличается от испарения тем, что кипение происходит при определенной температуре и давлении, а испарение - без внешнего воздействия на вещество.
- Кипит при 100, а замерзает при 0,
- Паром шпариться опаснее только при условии, что масса пара равна массе кипятка. Тогда тело получит разные количества теплоты. От воды только при остывании её от 100 гр до температуры руки, а во втором случае добавится тепло, выделившееся при конденсации.
- Газы (французское gaz; название предложено голланским учёным Я. Б. Гельмонтом), агрегатное состояние вещества, в котором его частицы не связаны или весьма слабо связаны силами взаимодействия и движутся свободно, заполняя весь предоставленный им объём. Паром называется газообразное состояние вещества, температура которого меньше критической,
- При температуре выше критической невозможно существование жидкости и газа,
- Удельная теплота парообразования уменьшается с ростом температуры и при критической температуре становится равной нулю.
- Поверхностное натяжение — термодинамическая характеристика поверхности раздела двух находящихся в равновесии фаз, определяемая работой обратимого изотермокинетического образования единицы площади этой поверхности раздела при условии, что температура, объем системы и химические потенциалы всех компонентов в обеих фазах остаются постоянными. Сила поверхностного натяжения пропорциональна длине того участка контура, на который она действует.
- с повышением температуры поверхностное натяжение жидкости линейно уменьшается
- Пове́рхностно-акти́вные вещества́ (ПАВ) — химические соединения, которые, концентрируясь на поверхности раздела термодинамических фаз, вызывают снижение поверхностного натяжения.
