Элементы квантовой механики
Пояснения к карте-схеме 8.
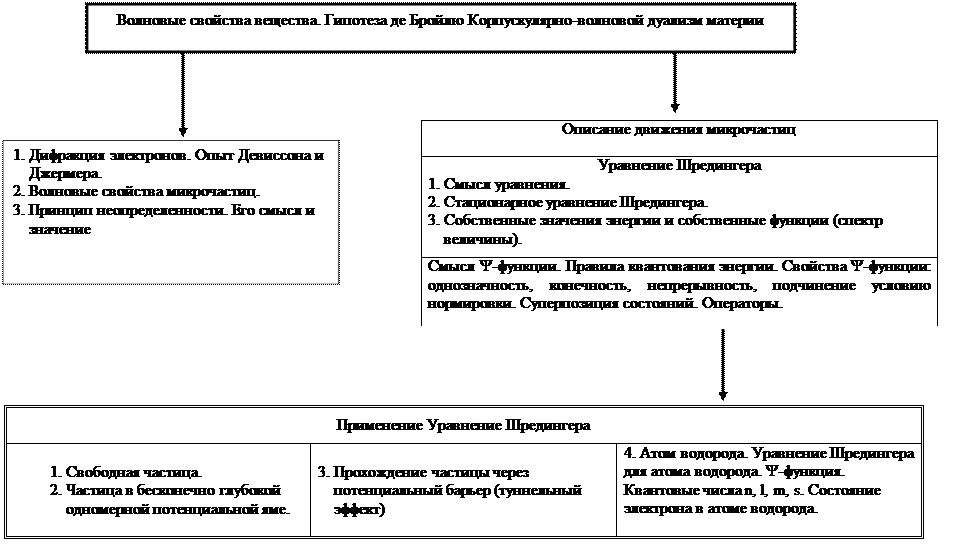
Обратите внимание на основную идею квантовой механики: корпускулярно-волновой дуализм материи, описание волновых свойств частиц, формулу де Бройля, экспериментальное подтверждение гипотезы де Бройля, на опыты Дэвисона и Джермера, Томсона, Фабриканта, Бибермана и др.; на волновые свойства микрочастиц; смысл соотношения неопределенности, уравнения Шредингера и ψ-функции.
Вопросы для самопроверки
1. В чем заключается корпускулярно-волновой дуализм материи? От чего зависит длина
волны де Бройля?
2. Напишите соотношения неопределенности. Объясните их смысл.
3. Как описывается движение микрочастицы?
4. Каков смысл уравнения Шредингера?
5. Напишите уравнение Шредингера для стационарных состояний.
6. Каков физический смысл Ψ-функции?
7. Каким требованиям должна удовлетворять Ψ-функция?
8. Как связаны правила квантования с уравнением Шредингера и его решением?
9. Примените уравнение Шредингера к нахождению собственных функций и собственных
значений для свободных частиц, для частицы в бесконечно глубокой одномерной
потенциальной яме с конечным потенциальным барьером.
10. Опишите туннельный эффект.
8. Карта-схема проработки темы: «Элементы квантовой механики»
 |
АТОМНАЯ ФИЗИКА. МНОГОЭЛЕКТРОННЫЕ АТОМЫ.
РЕНТГЕНОВСКИЕ СПЕКТРЫ
Пояснения к карте-схеме 9.
Обратите внимание на описание состояния электронов в атоме при помощи квантовых чисел, их физический смысл, значение, расчет электронных слоев и оболочек, заполнение электронных оболочек, построение таблицы элементов Менделеева, на формулировку принципа Паули. Особенности рентгеновского излучения, описание двух видов рентгеновских спектров и их закономерностей рекомендуется рассмотреть отдельно.
Вопросы для самопроверки
1. Назовите квантовые числа, опишите их физический смысл. Какие значения принимает каждое из квантовых чисел?
2. Сформулируйте принцип Паули.
3. Что называется термом электрона?
4. Как заполняются электронные слои и оболочки?
5. По каким формулам рассчитывается количество электронов в слое, в оболочке?
6. Чем отличается реальное заполнение таблицы слоев и оболочек от идеализированного, с чем связаны отклонения при их заполнении?
7. Как возникают рентгеновские спектры? Дайте описание каждого из видов рентгеновских спектров.
8. В чем смысл закона Мозли?
9. Карта-схема проработки темы: «Атомная физика. Многоэлектронные атомы. Рентгеновские спектры».
| КВАНТОВЫЕ ЧИСЛА | |||
| n 1. Физический смысл 2. Значения 3. Число значений |  l 1. 2. 3. l 1. 2. 3. | m 1. 2.  3. 3. | s  1. 2. 3. 1. 2. 3. |
| Тормозное и характеристическое излучение |
|
| РЕНТГЕНОВСКИЕ СПЕКТРЫ |
| ПРИНЦИП ПАУЛИ И ЗАПОЛНЕНИЕ СЛОЕВ И ОБОЛОЧЕК | |
| Слои K L Число электронов M в слое N … | Оболочки s p d f q ……..  число электронов в оболочке число электронов в оболочке |
Таблица заполнения слоев и оболочек электронами (идеализированный случай). Отклонения, наблюдающиеся при реальном заполнении оболочек электронами. Таблица элементов Менделеева. Электронная конфигурация для Na  |
ЯДРО АТОМА
