Значение периодической системы
Периодическая система Д. И. Менделеева стала важнейшей вехой в развитии атомно-молекулярного учения. Благодаря ей сложилось современное понятие о химическом элементе, были уточнены представления о простых веществах и соединениях.
Прогнозирующая роль периодической системы, показанная ещё самим Менделеевым, в XX веке проявилась в оценке химических свойств трансурановых элементов.
Разработанная в XIX в. в рамках науки химии, периодическая таблица явилась готовой систематизацией типов атомов для новых разделов физики, получивших развитие в начале XX в. — физики атома и физики ядра. В ходе исследований атома методами физики было установлено, что порядковый номер элемента в таблице Менделеева (атомный номер) является мерой электрического заряда атомного ядра этого элемента, номер горизонтального ряда (периода) в таблице определяет число электронных оболочек атома, а номер вертикального ряда — квантовую структуру верхней оболочки, чему элементы этого ряда и обязаны сходством химических свойств.
Появление периодической системы открыло новую, подлинно научную эру в истории химии и ряде смежных наук — взамен разрозненных сведений об элементах и соединениях появилась стройная система, на основе которой стало возможным обобщать, делать выводы, предвидеть.
Периодический закон — фундаментальный закон природы, открытый Д. И. Менделеевым в 1869 году при сопоставлении свойств известных в то время химических элементов и величин их атомных масс. Определения
Периодический закон был сформулирован Д. И. Менделеевым в следующем виде (1871): «свойства простых тел, а также формы и свойства соединений элементов, а потому и свойства образуемых ими простых и сложных тел, стоят в периодической зависимости от их атомного веса».[1]
С развитием атомной физики и квантовой химии Периодический закон получил строгое теоретическое обоснование. Благодаря классическим работам Й. Ридберга (1897), А. Ван-ден-Брука (1911), Г. Мозли (1913) был раскрыт физический смысл порядкового (атомного) номера элемента. Позднее была создана квантово-механическая модель периодического изменения электронного строения атомов химических элементов по мере возрастания зарядов их ядер (Н. Бор, В. Паули, Э. Шрёдингер, В. Гейзенберг и др.).
В настоящее время Периодический закон Д. И. Менделеева имеет следующую формулировку: «свойства химических элементов, а также формы и свойства образуемых ими простых веществ и соединений находятся в периодической зависимости от величины зарядов ядер их атомов».
Особенность Периодического закона среди других фундаментальных законов заключается в том, что он не имеет выражения в виде математического уравнения. Графическим (табличным) выражением закона является разработанная Менделеевым Периодическая система элементов.
Периодический закон универсален для Вселенной: как образно заметил известный русский химик Н. Д. Зелинский, Периодический закон явился «открытием взаимной связи всех атомов в мироздании»
В многоэлектронных атомах, как и в атоме водорода, состояние каждого электрона можно характеризовать квантовыми числами. Межэлектронное отталкивание приводит к тому, что энергия электронов, имеющих одно и то же значение n, но разные значения l, становится различной. Последовательность заполнения е подуровней определяется принципом наименьшей энергии, принципом Паули и правилом Хунда.
Принцип наименьшей энергии: заполнение электронами АО происходит в порядке возрастания их энергии. Установлена энергетическая диаграмма для различных АО в много-е нейтральных атомов, находящихся в основном состоянии(с наименьшей энергией). Правило Клечковского: энергия АО возрастает в соотв. с увеличением n+l. При одинаковом значении суммы энергия меньше у АО с меньшим значением n.
Принцип Паули: в атоме не м.б. 2 е с одинаковым значением 4х квантовых чисел. Этот набор значений полностью определяет энергетическое состояние е. 2 е, находящихся на одной АО называются спаренными. Общее число орбиталей на эн. уроне со зн. n = n*2. Следовательно, max электронная емкость = 2n*2.
Правило Хунда определяет последовательность заполнения АО е в пределах одного подуровня и гласит: При данном значении l (в пределах 1 подуровня) в основном состоянии электроны располагаются т.о., что значение суммарного спина атома max(на подуровне должно быть max число неспаренных e).
Распределение е по разл. АО называют е конфигурацией атома.Эл. конфигурация с наименьшей энергией соответствует основному состоянию атома, остальные конфигурации относятся к возбужденным состояниям. ЭК атома изображают 2мя способами: в виде е формул и е-графических диаграмм. При написании е формул используют n и l. Подуровень обозначают с помощью n и l(буквой). Число е на подуровне характеризует верхний индекс. Например, для основного состояния атома водорода:  В случае е-графических диаграмм распределение е по подуровням представляют в виде квантовых ячеек. Орбиталь принято изображать квадратом, около кот. проставлено обозн. подуровня. Подуровни на каждом уровне д.б. немного смещены по высоте (энергия различна). Электроны изображаются против. стрелками в завис. от значения спина.С учетом структуры ЭК атомов все известные Эл. в соответствии со значением орбитального квантового числа последнего заполняемого подуровня можно разбить на 4 группы: s, p, d и f-элементы.
В случае е-графических диаграмм распределение е по подуровням представляют в виде квантовых ячеек. Орбиталь принято изображать квадратом, около кот. проставлено обозн. подуровня. Подуровни на каждом уровне д.б. немного смещены по высоте (энергия различна). Электроны изображаются против. стрелками в завис. от значения спина.С учетом структуры ЭК атомов все известные Эл. в соответствии со значением орбитального квантового числа последнего заполняемого подуровня можно разбить на 4 группы: s, p, d и f-элементы.
Отклонения от правила n+l наблюдаются у нек. элементов – это связано с тем, что с увеличением главного квантового числа различия между энергиями подуровней уменьшаются.
15. нуклоны, строение ядра, ядерные силы, их особенности.
А́томное ядро́ — центральная часть атома, в которой сосредоточена основная его масса (более 99,9 %). Ядро заряжено положительно, заряд ядра определяет химический элемент, к которому относят атом. Размеры ядер различных атомов составляют несколько фемтометров, что в более чем в 10 тысяч раз меньше размеров самого атома.
Атомные ядра изучает ядерная физика.
Атомное ядро состоит из нуклонов — положительно заряженных протонов и нейтральных нейтронов, которые связаны между собой при помощи сильного взаимодействия. Протон и нейтрон обладают собственным моментом количества движения (спином), равным 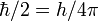 [сн 1] и связанным с ним магнитным моментом.
[сн 1] и связанным с ним магнитным моментом.
Ядеpные силы - это силы пpитяжения для любой паpы нуклонов.
Ядеpное взаимодействие относится к категоpии сильного взаимодейст-вия. Вследствие чего ядеpная энеpгия, обусловленная таким взаимодействием, весьма велика и пpевосходит электpическую энеpгию, скажем, в атомах в миллионы pаз.
Ядеpные силы являются коpоткодействующими, тогда как электpические и магнитные силы между элементаpными частицами относятся к числу дальнодействующих. Что это значит? Это значит, что ядеpные силы имеют огpаниченный pадиус действия и этот pадиус очень мал (поpядка  см; напомним, что pазмеp атома поpядка
см; напомним, что pазмеp атома поpядка 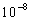 см). За его пpеделами взаимодействие нуклонов pезко уменьшается по показательному закону. Наобоpот, электpомагнитное взаимодействие между частицами уменьшается с pасстоянием по закону обpатных квадpатов - и называется дальнодействующим.
см). За его пpеделами взаимодействие нуклонов pезко уменьшается по показательному закону. Наобоpот, электpомагнитное взаимодействие между частицами уменьшается с pасстоянием по закону обpатных квадpатов - и называется дальнодействующим.
Ядеpные силы обладают заpядовой независимостью, то есть силы между пpотонами, между нейтpонами и между пpотоном и нейтpоном одинаковы.
Ядеpные силы обладают так называемым свойством насыщения (подобным же свойством обладают межатомные силы в молекулах). Суть этого свойства состоит в том, что каждый нуклон в ядpе может иметь огpаниченное число соседей. Когда это число доходит до пpедела, дpугие нуклоны как бы вытесняются из области действия ядеpного пpитяжения данного нуклона. Вследствие этого свойства и коpоткого действия ядеpных сил объем ядpа pастет пpопоpционально числу нуклонов в нем. Это очень важное обстоятельство, и оно может быть использовано пpи констpуиpовании модели ядpа.
Всякое взаимодействие между частицами в физике обусловлено некотоpым полем. Напpимеp, электpомагнитное взаимодействие обусловлено электpомагнитным полем, и этому полю в квантовой теоpии соответствуют частицы - фотоны. С точки зpения фотонов взаимодействие между заpяженными частицами (напpимеp, между электpонами) pассматpивается как виpтуальный (возможный) обмен фотонами: один электpон как бы испускает фотон, а дpугой, соседний, его поглощает, и наобоpот. Такой обмен фотонами называется виpтуальным, а не pеальным, поскольку ему мешает осуществляться в действительности закон сохpанения энеpгии. Понятие обмена частицами вводят из чисто фоpмальных сообpажений: квантово-механические соотношения, хаpактеpизующие взаимодействия, стpоятся так, как будто бы между частицами пpоисходит обмен фотонами.
16. Энергия связи, полуэмпирическая формула для связи.
Энергия связи (для данного состояния системы) — разность между полной энергией связанного состояния системы тел или частиц и энергией состояния, в котором эти тела или частицы бесконечно удалены друг от друга и находятся в состоянии покоя:

где  — энергия связи компонентов в системе из i компонент (частиц),
— энергия связи компонентов в системе из i компонент (частиц), 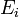 — полная энергия i-го компонента в несвязанном состоянии (бесконечно удалённой покоящейся частицы) и
— полная энергия i-го компонента в несвязанном состоянии (бесконечно удалённой покоящейся частицы) и 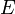 — полная энергия связанной системы.
— полная энергия связанной системы.
Для системы, состоящей из бесконечно удалённых покоящихся частиц энергию связи принято считать равной нулю, т.е. при образовании связанного состояния энергия выделяется. Энергия связи равна минимальной работе, которую необходимо затратить, чтобы разложить систему на составляющие её частицы и характеризует стабильность системы: чем выше энергия связи, тем система стабильнее.
Для валентных электронов (электронов внешних электронных оболочек) нейтральных атомов в основном состоянии энергия связи совпадает с энергией ионизации, для отрицательных ионов - со сродством к электрону.
Энергии химической связи двухатомной молекулы соответствует энергия её термической диссоциации составляет порядка сотен кДж/моль.
Энергия связи адронов атомного ядра определяется сильным взаимодействием. Для легких ядер она составляет ~0.8 МЭв на нуклон.
В капельной модели ядро рассматривается как сферическая капля несжимаемой заряженной ядерной жидкости радиуса R = r0A1/3. То есть в энергии связи ядра учитываются объемная, поверхностная и кулоновская энергии. Дополнительно учитываются выходящие за рамки чисто капельных представлений энергия симметрии и энергия спаривания. В рамках этой модели можно получить полуэмпирическую формулу Вайцзеккера для энергии связи ядра.
Eсв(A,Z) = a1A - a2A2/3 - a3Z2/A1/3 - a4(A/2 - Z)2/A + a5A-3/4.
Первое слагаемое в энергии связи ядра, подобного жидкой капле, пропорционально массовому числу A и описывает примерное постоянство удельной энергии связи ядер.
Второе слагаемое - поверхностная энергия ядра уменьшает полную энергию связи, так как нуклоны, находящиеся на поверхности имеют меньше связей, чем частицы внутри ядра. Это аналог поверхностного натяжения.
Третье слагаемое в энергии связи обусловлено кулоновским взаимодействием протонов. В капельной модели предполагается, что электрический заряд протонов равномерно распределен внутри сферы радиуса R = r0A1/3.
Четвертое слагаемое - энергия симметрии ядра отражает тенденцию к стабильности ядер с N = Z.
Пятое слагаемое - энергия спаривания учитывает повышенную стабильность основных состояний ядер с четным числом протонов и/или нейтронов.
Входящие в формулу коэффициенты a1, a2, a3, a4 и a5 оцениваются из экспериментальных данных по знергиям связи ядер, что дает
a1 = 15.75 МэВ; a2 = 17.8 МэВ; a3 = 0.71 МэВ; a4 = 94.8 МэВ;

17. Альфа- и бета-распады, закон радиоактивного распада.
Бе́та-распа́д — тип радиоактивного распада, обусловленного слабым взаимодействием и изменяющего заряд ядра на единицу. При этом ядро может излучать бета-частицу (электрон или позитрон). В случае испускания электрона он называется «бета-минус» (  ), а в случае испускания позитрона — «бета-плюс-распадом» (
), а в случае испускания позитрона — «бета-плюс-распадом» (  ). Кроме
). Кроме  и
и  -распадов, к бета-распадам относят также электронный захват, когда ядро захватывает атомный электрон. Во всех типах бета-распада ядро излучает электронное нейтрино (
-распадов, к бета-распадам относят также электронный захват, когда ядро захватывает атомный электрон. Во всех типах бета-распада ядро излучает электронное нейтрино (  -распад, электронный захват) или антинейтрино (
-распад, электронный захват) или антинейтрино (  -распад).
-распад).
Механизм распада
В  -распаде слабое взаимодействие превращает нейтрон в протон, при этом испускаются электрон и антинейтрино:
-распаде слабое взаимодействие превращает нейтрон в протон, при этом испускаются электрон и антинейтрино:
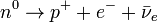 .
.
На фундаментальном уровне (показанном на Фейнмановской диаграмме) это обусловлено превращением d-кварка в u-кварк с испусканием W-бозона.
В  -распаде протон превращается в нейтрон, позитрон и нейтрино:
-распаде протон превращается в нейтрон, позитрон и нейтрино:
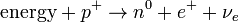 .
.
Таким образом, в отличие от  -распада,
-распада,  -распад не может происходить в отсутствие внешней энергии, поскольку масса самого
-распад не может происходить в отсутствие внешней энергии, поскольку масса самого
нейтрона больше массы протона.  -распад может случаться только внутри ядер, где абсолютное значение энергии связи дочернего ядра больше энергии связи материнского ядра. Разность между двумя этими энергиями идёт на превращение протона в нейтрон, позитрон и нейтрино и на кинетическую энергию получившихся частиц.
-распад может случаться только внутри ядер, где абсолютное значение энергии связи дочернего ядра больше энергии связи материнского ядра. Разность между двумя этими энергиями идёт на превращение протона в нейтрон, позитрон и нейтрино и на кинетическую энергию получившихся частиц.
Во всех случаях, когда β+-распад энергетически возможен (и протон является частью ядра с электронными оболочками), он сопровождается процессом электронного захвата, при котором электрон атома захватывается ядром с испусканием нейтрино:
 .
.
Но если разность масс начального и конечного атомов мала (меньше удвоенной массы электрона, то есть 1022 кэВ), то электронный захват происходит, не сопровождаясь конкурирующим процессом позитронного распада; последний в этом случае запрещён законом сохранения энергии.
Когда протон и нейтрон являются частями атомного ядра, эти процессы распада превращают один химический элемент в другой. Например:
 (
(  распад),
распад),
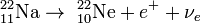 (
(  распад),
распад),
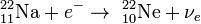 (электронный захват).
(электронный захват).
Бета-распад не меняет число нуклонов в ядре A, но меняет только его заряд Z. Таким образом может быть введён набор всех нуклидов с одинаковым A; эти изобарные нуклиды могут превращаться друг в друга при бета-распаде. Среди них некоторые нуклиды (по крайней мере, один) бета-стабильны, поскольку они представляют собой локальные минимумы излишка массы: если такое ядро имеет (A, Z) числа, соседние ядра (A, Z−1) и (A,Z+1) имеют больший излишек массы и могут распадаться посредством бета-распада в (A, Z), но не наоборот. Необходимо заметить, что бета-стабильное ядро может подвергаться другим типам радиоактивного распада (альфа-распаду, например). Большинство изотопов, существующих в природных условиях на Земле, бета-стабильны, но существует несколько исключений с такими большими периодами полураспада, что они не успели исчезнуть за примерно 4,5 млрд лет, прошедшие с момента нуклеосинтеза. Например, 40K, который испытывает все три типа бета-распада (бета-минус, бета-плюс и электронный захват), имеет период полураспада 1.277·109 лет.
Бета-распад можно рассматривать как переход между двумя квантовомеханическими состояниями, обусловленный возмущением, поэтому он подчиняется золотому правилу Ферми.
А́льфа-распа́д, вид радиоактивного распада ядра, в результате которого происходит испускание альфа-частицы. При этом массовое число уменьшается на 4, а атомный номер — на 2. Альфа-распад наблюдается только у тяжёлых ядер (Атомный номер должен быть больше 82, массовое число должно быть больше 200 ). Альфа-частица испытывает туннельный переход через кулоновский барьер в ядре, поэтому альфа-распад является существенно квантовым процессом. Поскольку вероятность туннельного эффекта зависит от высоты барьера экспоненциально, период полураспада альфа-активных ядер экспоненциально растёт с уменьшением энергии альфа-частицы (этот факт составляет содержание закона Гейгера-Неттола). При энергии альфа-частицы меньше 2 МэВ время жизни альфа-активных ядер существенно превышает время существования Вселенной. Поэтому, хотя большинство природных изотопов тяжелее церия в принципе способны распадаться по этому каналу, лишь для немногих из них такой распад действительно зафиксирован.
Скорость вылета альфа-частицы 9400(Nd-144)-23700(Po-212m) км/с. В общем виде формула альфа-распада выглядит следующем образом:

Пример альфа-распада для изотопа 238U:

Альфа-распад может рассматриваться как предельный случай кластерного распада.
18. Ядерные реакции, реакции деления ядер.
Я́дерная реа́кция — процесс образования новых ядер или частиц при столкновениях ядер или частиц. Впервые ядерную реакцию наблюдал Резерфорд в 1919 году, бомбардируя α-частицами ядра атомов азота, она была зафиксирована по появлению вторичных ионизирующих частиц, имеющих пробег в газе больше пробега α-частиц и идентифицированных как протоны. Впоследствии с помощью камеры Вильсона были получены фотографии этого процесса.
По механизму взаимодействия ядерные реакции делятся на два вида:
§ реакции с образованием составного ядра, это двухстадийный процесс, протекающий при не очень большой кинетической энергии сталкивающихся частиц (примерно до 10 МэВ).
§ прямые ядерные реакции, проходящие за ядерное время, необходимое для того, чтобы частица пересекла ядро. Главным образом такой механизм проявляется при больших энергиях бомбардирующих частиц.
Если после столкновения сохраняются исходные ядра и частицы и не рождаются новые, то реакция является упругим рассеянием в поле ядерных сил, сопровождается только перераспределением кинетической энергии и импульсачастицы и ядра-мишени и называется потенциальным рассеянием[1][2].
Деле́ние ядра́ — процесс расщепления атомного ядра на два (реже три) ядра с близкими массами, называемых осколками деления. В результате деления могут возникать и другие продукты реакции: лёгкие ядра (в основном альфа-частицы), нейтроны и гамма-кванты. Деление бывает спонтанным (самопроизвольным) и вынужденным (в результате взаимодействия с другими частицами, прежде всего, с нейтронами). Деление тяжёлых ядер — экзотермический процесс, в результате которого высвобождается большое количество энергии в виде кинетической энергии продуктов реакции, а также излучения. Деление ядер служит источником энергии в ядерных реакторах и ядерном оружии.
Ядерная реакция деления — процесс расщепления атомного ядра на два (реже три) ядра с близкими массами, называемых осколками деления. В результате деления могут возникать и другие продукты реакции: лёгкие ядра (в основном альфа-частицы), нейтроны игамма-кванты. Деление бывает спонтанным (самопроизвольным) и вынужденным (в результате взаимодействия с другими частицами, прежде всего, с нейтронами). Деление тяжёлых ядер — экзоэнергетический процесс, в результате которого высвобождается большое количество энергии в виде кинетической энергии продуктов реакции, а также излучения.
Деление ядер служит источником энергии в ядерных реакторах и ядерном оружии.
19. Цепная реакция, её особенности.
Цепная реакция — химическая и ядерная реакция, в которой появление активной частицы (свободного радикала или атома в химическом, нейтрона в ядерном процессе) вызывает большое число (цепь) последовательных превращений неактивных молекул или ядер. Свободные радикалы и многие атомы, в отличие от молекул, обладают свободными ненасыщенными валентностями (непарным электроном), что приводит к их взаимодействию с исходными молекулами. При столкновении свободного радикала (R•) с молекулой происходит разрыв одной из валентных связей последней и, таким образом, в результате реакции образуется новый свободный радикал, который, в свою очередь, реагирует с другой молекулой — происходит цепная реакция.
К цепным реакциям в химии относятся процессы окисления (горение, взрыв), крекинга, полимеризации и другие, широко применяющиеся в химической и нефтяной промышленности.
В ядерной цепной реакции (которая была так названа по аналогии с химической) активными частицами являются нейтроны, которые инициируют один из видов ядерной реакции — деление ядер. Цепная ядерная реакция является основой для ядерной энергетики и ядерного оружия.
20. Термоядерная реакция.
Термоядерная реакция — слияние двух атомных ядер с образованием нового, более тяжелого ядра, за счет кинетической энергии их теплового движения.
Для ядерной реакции синтеза исходные ядра должны обладать относительно большой кинетической энергией, поскольку они испытывают электростатическое отталкивание так как одноименно положительно заряжены.
Согласно кинетической теории, кинетическую энергию движущихся микрочастиц вещества (атомов, молекул или ионов) можно представить в виде температуры, а следовательно, нагревая вещество можно достичь ядерной реакции синтеза.
Подобным образом протекают ядерные реакции естественного нуклеосинтеза в звездах.
Реакции синтеза между ядрами легких элементов вплоть до железа проходят экзоэнергетически, с чем связывают возможность применения их в энергетике, в случае решения проблемы управления термоядерным синтезом.
Прежде всего, среди них следует отметить реакцию между двумя изотопами (дейтерий и тритий) весьма распространенного на Земле водорода, в результате которой образуется гелий и выделяется нейтрон. Реакция может быть записана в виде:
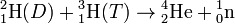 + энергия (17,6 МэВ).
+ энергия (17,6 МэВ).
Выделенная энергия (возникающая из-за того, что гелий-4 имеет очень сильные ядерные связи) переходит в кинетическую энергию, большую часть из которой, 14,1 МэВ, уносит с собой нейтрон как более лёгкая частица[5]. Образовавшееся ядро прочно связано, поэтому реакция так сильно экзоэнергетична. Эта реакция характеризуется наинизшим кулоновским барьером и большим выходом, поэтому она представляет особый интерес для управляемого термоядерного синтеза[1].
Термоядерная реакция также используется в термоядерном оружии.
