Рентгеновские спектры атомов
Физика
Атомная и ядерная физика
Методические указания к расчётно-графическим работам и варианты заданий для студентов бакалавриата
направления 150400
САНКТ-ПЕТЕРБУРГ
УДК 531/534 (073)
Физика. АТОМНАЯ И ЯДЕРНАЯ ФИЗИКА: Методические указания к расчётно-графическим работам и варианты заданий для студентов бакалавриата направления 150400 / Национальный минерально-сырьевой университет «Горный». Сост. Т.В. Стоянова. СПб, 2014. 26 с.
Приведены рекомендации к выполнению расчётно-графических работ, теоретические основы дисциплины, пример решения задачи, библиографический список.
Расчётно-графические работы предназначены для студентов бакалавриата направления обучения 150400
Табл. 2. Ил. 4. Библ.: 5 назв.
Научный редактор доц. Н.А. Тупицкая
| Ó Национальный минерально-сырьевой университет «Горный»,2014 г. |
РЕКОМЕНДАЦИИ К ВЫПОЛНЕНИЮ РАСЧЁТНО-ГРАФИЧЕСКОЙ РАБОТЫ
Вопросы и задачи, содержащиеся в пособие, охватывают большую часть стандартного курса квантовой механики, изучаемого в технических вузах, и способствуют более глубокому усвоению теоретического материала данного раздела.
Выполнение расчётно-графической работы предполагает достаточно большой объём самостоятельной работы студента.
Перед выполнением расчётно-графической работы рекомендуется изучить лекционный курс на тему «Атомная и ядерная физика», познакомиться с соответствующим разделом учебника общего курса физики. Если при самостоятельном изучении теоретического материала возникли вопросы, желательно обсудить их на практических занятиях, но если и после этого остались не ясные моменты, можно получить индивидуальную консультацию преподавателя, ведущего расчётно-графическую работу или лектора.
При изучении физического явления, прежде всего, необходимо выяснить сущность явления, условия при которых оно возможно, определить с помощью каких физических величин, оно характеризуется. Желательно понять, как оно связано с другими явлениями и возможности его применения на практике: При определении физической величины важно обратить внимание на то, какая это величина – скалярная или векторная, какие свойства она характеризует, выяснить её размерность и формулу, определяющую связь с другими физическими величинами. При прочтении закона обратите внимание на границы его применения, определите, между какими явлениями он выражает связь, уточните формулировку и математическое выражение закона.
Расчётно-графическая работа оформляется на компьютере. При выполнении расчётно-графической работы необходимо указать на титульном листе: название института, наименование дисциплины, название работы, фамилию и инициалы студента и ведущего расчётно-графическое задание преподавателя, год выполнения работы.
Необходимо полностью переписать задачу своего варианта, а заданные физические величины выписать отдельно, при этом все числовые значения должны быть переведены в одну систему единиц. При получении расчётной формулы приведите её полный подробный вывод.
Математическое решение должно сопровождаться пояснениями, а в случае необходимости его можно продемонстрировать рисунком. Задачу рекомендуется решить сначала в общем виде (в буквенных обозначениях), поясняя применяемые при написании формул буквенные обозначения, и только после проверки размерности искомой физической величины подставить в выведенную формулу числовые значения. Все необходимые числовые значения величин должны быть выражены в системе «СИ». После получения окончательного результата, для удобства построения графических зависимостей, можно перейти к вне системным единицам. Например, выразить энергию в электрон-вольтах.
Перед построением графиков необходимо получить аналитическое выражение функциональной зависимости. Выбрать удобный масштаб и указать его на осях координат, а так же физические величины и единицы измерения.
На координатной плоскости обязательно должны быть нанесены экспериментальные точки. Кривая, аппроксимирующая функциональную теоретическую зависимость строится в соответствии с методом наименьших квадратов.
СОДЕРЖАНИЕ ОТЧЁТА
1. Титульный лист
2. Теоретическая часть:
2.1. Определения всех физических явлений, законов и величин, встречающихся в данной работе.
2.2. Основные расчётные формулы с пояснениями.
3. Расчётная часть:
3.1. Задание с исходными данными своего варианта.
3.2. Расчёт с пояснениями.
3.3. Графики.
4. Анализ результатов. Заключение.
ТЕОРЕТИЧЕСКИЕ ОСНОВЫ АТОМНОЙ И ЯДЕРНОЙ ФИЗИКИ
Наиболее вероятное расстояние электрона в состоянии n от ядра:
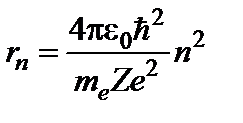 , (1)
, (1)
где me – масса электрона, Z – заряд ядра (атомный номер), n = 1, 2, 3… – главные квантовые числа. При n = 1 и Z = 1 это расстояние совпадает с радиусом первой боровской орбиты.
Одновременное измерение модуля момента импульса и трёх его проекций на оси координат в квантовой механике невозможно. Модуль момента импульса определяется:
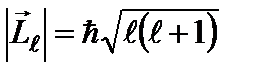 . (2)
. (2)
Число ℓ = 0, 1, 2, …, n-1 называется орбитальным квантовым числом. Проекция момента импульса на любую ось (z) тоже может принимать лишь определенные значения
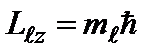 , (3)
, (3)
где mℓ = 0, ± 1, ± 2, …, ± ℓ и называется магнитным квантовым числом. Такое название связано с тем, что оно определяет также проекцию магнитного момента, создаваемого движением электрона вокруг ядра:
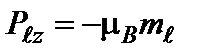 . (4)
. (4)
Модуль магнитного момента электрона
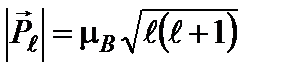 , (5)
, (5)
где 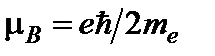 = 0,927∙10-23 Дж/Тл – магнетон Бора. Гиромагнитное отношение для орбитальных магнитного и механического моментов
= 0,927∙10-23 Дж/Тл – магнетон Бора. Гиромагнитное отношение для орбитальных магнитного и механического моментов
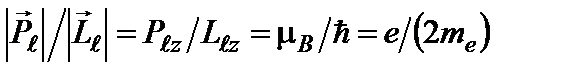 . (6)
. (6)
Электрон обладает также собственным механическим моментом импульса, равным
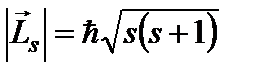 , (7)
, (7)
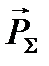 |
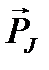 |
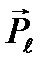 |
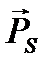 |
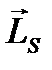 |
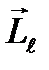 |
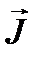 |
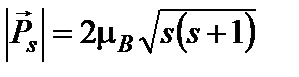 . (8)
. (8)
Проекции спинового момента импульса и магнитного момента на направление внешнего магнитного поля равны
| Рис.1. Сложение моментов. оментовпереходов |
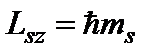 и
и 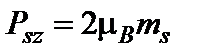 , (9)
, (9) где ms – спиновое квантовое число, может принимать значения ± 1/2.
Гиромагнитное отношение для спиновых магнитного и механического моментов оказывается в два раза больше, чем для орбитальных моментов
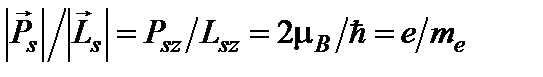 . (10)
. (10)
Орбитальный 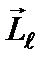 и спиновый
и спиновый 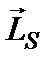 моменты импульса электрона складываются и дают полный момент импульса электрона
моменты импульса электрона складываются и дают полный момент импульса электрона 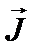 (рис.1). Модуль полного момента импульса квантуется:
(рис.1). Модуль полного момента импульса квантуется:
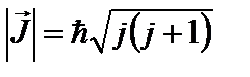 , (11)
, (11)
где 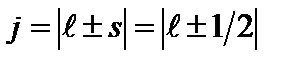 - внутреннее квантовое число. Проекция полного момента импульса на направление внешнего магнитного поля
- внутреннее квантовое число. Проекция полного момента импульса на направление внешнего магнитного поля
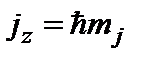 , (12)
, (12)
где mj может принимать 2j +1 значение от – j до j.
Таким образом, для описания состояния электрона в атоме используют четыре квантовых числа: n, ℓ, mℓ и ms. или n, ℓ, j, mj. Из-за разных гиромагнитных отношений для спинового и орбитального моментов суммарный магнитный момент оказывается не параллельным суммарному механическому моменту. Поэтому вводится специальный коэффициент g-фактор Ланде, который есть не что иное, как коэффициент пропорциональности между 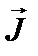 и
и 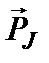 :
:
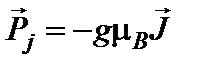 , (13)
, (13)
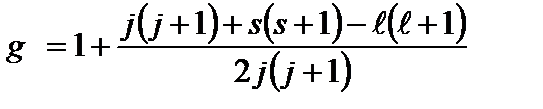 . (14)
. (14)
Порядок заполнения уровней в атоме определяется эмпирическими правилами Клечковского.
Первое правило Клечковского: сначала будут заполняться уровни с наименьшей суммой квантовых чисел n + ℓ.
Второе правило Клечковского: если два уровня имеют одинаковую сумму квантовых чисел n + ℓ, то первым будет заполняться энергетический уровень с меньшим значением n.
Электроны подчиняются принципу Паули: каждый энергетический уровень может быть заселен не более чем двумя электронами с противоположными спинами.
Вырожденные состояния электроны заселяют таким образом, чтобы спин 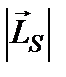 атома был максимален и, при этом по возможности максимальным было значение
атома был максимален и, при этом по возможности максимальным было значение 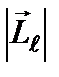 – правило Гунда.
– правило Гунда.
Рентгеновские спектры атомов
Экспериментально строение атомов изучают, исследуя спектры испускания и поглощения атомами электромагнитного излучения. Оптический диапазон соответствует переходам валентных электронов.
Для атома водорода формула, описывающая спектральные линии, подобрана экспериментально и называется формулой Бальмера – в честь ученого, впервые получившего ее для спектрального диапазона видимого излучения. Схема переходов приведена на рис.2.
Длины волн излучаемых атомом водорода определяются по формуле:
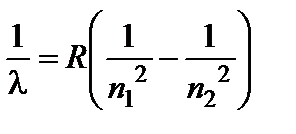 , (15)
, (15)
| Kα |
| Kβ |
| Kγ |
| К-серия |
| L-серия |
| Возбуждение К-серии |
| Возбуждение L-серии |
| К |
| L |
| M |
| N |
| n |
| Рис.2. Схема переходов. |
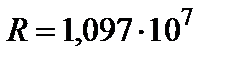 м-1 – постоянная Ридберга;
м-1 – постоянная Ридберга; 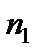 и
и 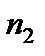 – главные квантовые числа, соответствующие энергетическим уровням, между которыми совершается электронный переход в атоме. Длина волн излучаемых водородоподобными ионами с зарядовым числом ядра Z (число Z определяется по номеру химического элемента в таблице Менделеева), могут быть рассчитаны по формуле:
– главные квантовые числа, соответствующие энергетическим уровням, между которыми совершается электронный переход в атоме. Длина волн излучаемых водородоподобными ионами с зарядовым числом ядра Z (число Z определяется по номеру химического элемента в таблице Менделеева), могут быть рассчитаны по формуле: 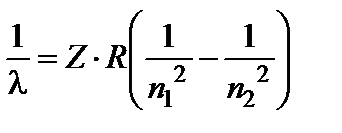 . (16)
. (16)
Водородоподобными ионами называют атомы с одним электроном на внешней оболочке.
Рентгеновское излучение возникает при переходах на внутренних оболочках. Частоты и длины волн соответствующего излучения можно определить, используя закон Мозли:
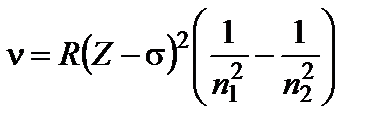 , (17)
, (17)
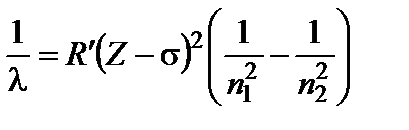 , (18)
, (18)
где Z – порядковый номер элемента в системе Менделеева, R и R' – постоянные Ридберга для частот и длин волн (R = 3,29 ∙ 1015 c-1 и R' = 1,10 ∙ 107 м-1), n1 – номер уровня, с которого переходит электрон, n2 – номер уровня, на который переходит электрон. Величина σучитывает экранировку внутренними электронами Кулоновского взаимодействия ядра и рассматриваемого электрона и называется постоянной экранирования.
Правила отбора для электромагнитных переходов:
Δj = 0, ±1; Δmj = 0, ±1; Δℓ = ±1; Δmℓ = 0, ±1; Δms = 0
