Квантование момента импульса. Спин. Принцип Паули
Главное квантовое число 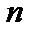 и орбитальное число
и орбитальное число 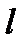 определяют в атоме, соответственно…
определяют в атоме, соответственно…
Какие значения может принимать орбитальное квантовое число 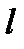 в состоянии с главным квантовым числом n?
в состоянии с главным квантовым числом n?
Состояние электрона в атоме водорода, энергия которого больше энергии основного состояния называется….
Главное квантовое число характеризует
Магнитное квантовое число 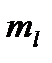 определяет …
определяет …
Орбитальное квантовое число определяет…
Спиновое квантовое число для электрона может принимать значения:
Электрон – частица с …
Спин электрона характеризует
Cпин, равный единице, имеет…
В соответствии с принципом исключения Паули в квантовом состоянии может находиться:
Принцип Паули выполняется для:
Какие значения может принимать магнитное спиновое квантовое число?
Периодичность химических свойств элементов обусловлена
Периодичность химических свойств элементов обусловлена
В любом атоме не может быть двух электронов, находящихся в двух одинаковых стационарных состояниях, определяемых набором
В электронной оболочке атома с главным квантовым числом 2 может находиться максимальное число электронов …
В электронной оболочке атома с главным квантовым числом 1 может находиться максимальное число электронов
В электронной оболочке атома с главным квантовым числом 3 может находиться максимальное число электронов …
Атом водорода
Первый постулат Бора:
где n и k – главные квантовые числа, соответствующие номерам энергетических уровней.
Правило квантования орбит Бора:
(где 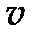 - скорость электрона,
- скорость электрона, 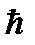 - постоянная Планка,
- постоянная Планка, 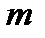 - масса электрона,
- масса электрона, 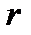 - радиус орбиты)
- радиус орбиты)
Боровский радиус – это радиус …
При переходе электрона в атоме с одной стационарной орбиты с энергией Е2 на другую с энергией Е1 излучается
(h – постоянная Планка )
В видимой области спектра находятся спектральные линии атома водорода, соответствующие серии…
В ультрафиолетовой области спектра находятся спектральные линии атома водорода, соответствующие серии…
В ультрафиолетовой области спектра находятся спектральные линии атома водорода, соответствующие серии…
Атом водорода испускает серию линий в ультрафиолетовой области спектра…
Атом водорода испускает серию линий в видимой области спектра…
На рисунке представлена энергетическая схема уровней атома. Между какими уровнями происходит переход атома с поглощением фотона с максимальной частотой волны.
Водородоподобной системой называется….
В спектре атома водорода могут наблюдаться только те линии, которые возникают при переходах с высших энергетических уровней на низшие при выполнении условия:
