Спин электрона. Принцип Паули
Состояние каждого электрона в атоме определяется четырьмя квантовыми числами:
1) Главное квантовое число 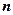 определяет размеры орбиты.
определяет размеры орбиты.
От этого числа зависит энергия электрона в атоме; оно может принимать только целочисленные значения от 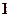 до
до 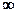
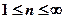
2) Орбитальное квантовое число 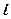 определяет эксцентриситет орбиты или орбитальный момент количества движения электрона и может принимать только целочисленные значения от
определяет эксцентриситет орбиты или орбитальный момент количества движения электрона и может принимать только целочисленные значения от 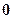 до
до 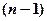 , где
, где 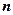 - главное квантовое число, т.е.
- главное квантовое число, т.е.
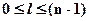
Различные значения числа 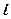 при данном
при данном 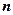 соответствуют движению электронов по эллипсам различной вытянутости. Совокупность всех электронов, движущихся по этим эллипсам, представляет собой электронный слой (оболочку) с данным главным квантовым числом.
соответствуют движению электронов по эллипсам различной вытянутости. Совокупность всех электронов, движущихся по этим эллипсам, представляет собой электронный слой (оболочку) с данным главным квантовым числом.
Слой с 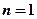 обозначается как
обозначается как 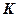 -слой .
-слой .
Слой с 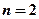 обозначается как
обозначается как 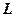 -слой.
-слой.
Слой с 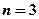 обозначается как
обозначается как 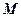 -слой и т.д.
-слой и т.д.
Численные значения 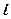 обозначаются буквами по следующей схеме:
обозначаются буквами по следующей схеме:
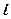 :
: 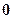 ,
, 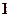 ,
, 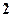 ,
, 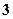 ,
, 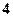 ,
, 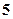
буква: 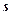 ,
, 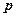 ,
, 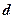 ,
, 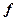 ,
, 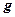 ,
, 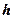
Состояние электронов в слое 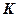 :
: 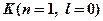 →
→ 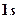
Состояние электронов в слое 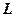 :
: 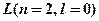 →
→ 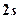
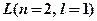 →
→ 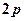
3) Магнитное квантовое число 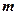 определяет пространственную ориентацию орбиты электрона.
определяет пространственную ориентацию орбиты электрона.
4) Спиновое квантовое число - 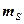 .
.
Собственный момент количества движения электрона называют спином.
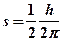
Если 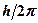 принять за единицу измерения момента количества движения, то
принять за единицу измерения момента количества движения, то 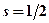 . Проекция спина электрона на любую ось может принимать только два значения:
. Проекция спина электрона на любую ось может принимать только два значения: 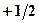 и
и 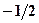 , что соответствует ориентации спина либо параллельно, либо антипараллельно этой оси. В настоящее время установлено, что спином обладает не только электрон, но и большинство элементарных частиц. Спин это особое свойство элементарных частиц. Итак, состояние электрона в атоме характеризуется четырьмя квантовыми числами:
, что соответствует ориентации спина либо параллельно, либо антипараллельно этой оси. В настоящее время установлено, что спином обладает не только электрон, но и большинство элементарных частиц. Спин это особое свойство элементарных частиц. Итак, состояние электрона в атоме характеризуется четырьмя квантовыми числами: 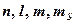 .
.
Согласно принципу Паули, в одном и том же атоме (молекуле) не может быть двух (и более) электронов, у которых были бы одинаковыми все четыре квантовых числа. В основном состоянии атом и электроны в нем обладают наименьшей энергией.
 Пример:
Пример:
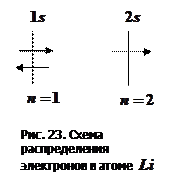
Атом 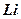 (литий) – имеет 3 электрона (рис. 23). Третий электрон, согласно принципу Паули, не может попасть в слой
(литий) – имеет 3 электрона (рис. 23). Третий электрон, согласно принципу Паули, не может попасть в слой 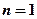 , так как все состояния там заняты. Следовательно, энергия третьего электрона должна быть более высокой, чем первых двух. Он попадает в слой
, так как все состояния там заняты. Следовательно, энергия третьего электрона должна быть более высокой, чем первых двух. Он попадает в слой 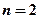 (
( 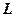 - слой).
- слой). 
Рекомендуемая литература
1. Савельев И.В. Курс общей физики / И.В. Савельев. Т.3.-СПб.: Лань, 2006.
2. Трофимова Т.И. Курс физики / Т.И. Трофимова. - М.: Высшая школа, 2004.
3. Справочное руководство по физике. Ч.2. Колебания, волны, оптика, атомная и ядерная физика: Учеб.-метод. пособие.- Ростов н/Д: Издательский центр ДГТУ, 2009.
4. Федосеев В.Б. Физика / В.Б. Федосеев.- Ростов н/Д: Феникс, 2009.
ОГЛАВЛЕНИЕ
| 1. | Квантовые оптические явления………………………………. | |
| Фотоны. Энергия, масса и импульс фотонов……………. | ||
| Тепловое излучение……………………………………………….. | ||
| Понятие о равновесном тепловом излучении……………… | ||
| Характеристики теплового излучения………………………… | ||
| Законы теплового излучения……………………………………. | ||
| Фотоэффект………………………………………………………….. | ||
| Основные законы фотоэффекта. Уравнение Эйнштейна | ||
| Внутренний фотоэффект…………………………………………… | ||
| Вентильный фотоэффект………………………………………….. | ||
| Давление света…………………………………………………………….. | ||
| Эффект Комптона…………………………………………………………… | ||
| Физика атома……………………………………………………….. | ||
| Спектры. Закономерности в атомных спектрах…………….. | ||
| Модели атома Томсона и Резерфорда………………………… | ||
| Постулаты Бора……………………………………………………….. | ||
| Применение теории Бора к атому водорода……………….. | ||
| Опыты Франка и Герца……………………………………………… | ||
| Достоинства и недостатки теории Бора………………………. | ||
| Люминесценция………………………………………………………… | ||
| Физика атомного ядра и элементарных частиц………… | ||
| Состав и характеристики атомного ядра……………………. | ||
| Дефект массы и энергия связи ядра…………………………. | ||
| Ядерные силы…………………………………………………………. | ||
| Радиоактивность……………………………………………………… | ||
| Правила радиоактивного смещения…………………………. | ||
| Закон радиоактивного распада. Активность………………. | ||
| Методы регистрации радиоактивного излучения………. | ||
| Ядерные реакции…………………………………………………….. | ||
| Термоядерные реакции…………………………………………… | ||
| Элементы квантовой механики…………………………….. | ||
| Гипотеза Луи де Бройля…………………………………………… | ||
| Уравнение Шредингера……………………………………………… | ||
| Частица в одномерной прямоугольной «потенциальной яме» с бесконечно высокими «стенками»…………………… | ||
| Спин электрона. Принцип Паули………………………………… | ||
| Рекомендуемая литература………………………………………….. |
Составители: С.И. Егорова
И.Н. Егоров
Г.Ф. Лемешко
Квантовая оптика.
Атомная и ядерная физика
Учебное пособие
Редактор
Тем. план 2011 г, поз.
ЛР № 04779 от 18.05.01. В печать .
Объём усл. п. л., уч.-изд. л. Офсет. Формат 60x84/64.
Бумага тип №3. Заказ № . Тираж экз. Цена свободная.
Издательский центр ДГТУ
Адрес университета и полиграфического предприятия:
344010, г. Ростов-на-Дону, пл. Гагарина,1.
