Реакция горения оксида углерода может быть описана уравнением
Упругость диссоциации карбонатов.
Карбонаты кальция, магния, железа и марганца широко применяются в металлургии. Наиболее распространенными из них являются:
Карбонат кальция (CaCO3) широко применяется в качестве сырья для производства извести, а также в качестве флюса в мартеновском и доменном производстве.
Карбонат магния (MgCO3) и доломит (CaMg(CO3)2) в обожженном виде применяется в качестве сырья для производства основных огнеупоров.
Карбонат железа (FeCO3) является основным компонентом сидеритовых железных руд.
Карбонат марганца (MnCO3) служит сырьем для получения металлического марганца и марганцевых ферросплавов.
При высоких температурах эти соединения разлагаются на оксид металла и углекислый газ. Поэтому выяснение условий их распада имеет важное значение для выбора условий обжига и анализа процессов, протекающих в различных агрегатах.
Карбонаты образуются по экзотермическим реакциям типа
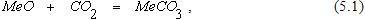
где MeO – оксид двухвалентного металла.
Обратный процесс протекает с поглощением тепла и называется термической диссоциацией карбоната.
Рассмотрим случай, когда участвующие в реакции оксид и карбонат не образуют растворов и представляют собой самостоятельные чистые фазы. Тогда общее число взаимодействующих фаз в системе будет равно трем. В системе присутствуют три вещества, связанных одним уравнением реакции (k = 2). Тогда в соответствии с правилом фаз Гиббса число степеней свободы системы будет равным
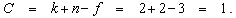
Это означает, что давление углекислого газа в системе
зависит только от температуры.
Реакции термической диссоциации карбонатов являются эндотермическими и протекают с увеличением объема взаимодействующих веществ. Поэтому в соответствии с принципом ЛеШателье протеканию реакции (5.1) в направлении термической диссоциации карбонатов способствуют высокая температура и низкое парциальное давление в газовой фазе.
Константу равновесия реакции термической диссоциации карбонатов в общем случае можно записать в виде
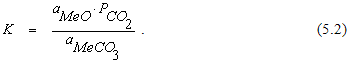
В случае, если оксид и карбонат являются чистыми веществами

Равновесное парциальное давление углекислого газа PCO2(MeCO3) в реакциях образования или термической диссоциации карбонатов принято называть упругостью диссоциации карбонатов. При отсутствии твердых растворов она является функцией только температуры и эквивалентна константе равновесия реакции.
При высоких температурах упругость диссоциации карбонатов поддается непосредственному измерению. При низких температурах она может быть очень малой величиной (например, 10-15 Па и меньше), которую можно определить только путем термодинамических вычислений. При этом она теряет физический смысл давления и становится чисто расчетной величиной
Реакция горения оксида углерода может быть описана уравнением
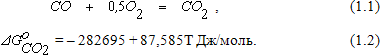
Качественную оценку влияния изменения параметров системы на протекание реакции (1.1) можно выполнить при помощи принципа ЛеШателье и правила фаз Гиббса, согласно которому

Рассматриваемая система состоит из молекул трех веществ, связанных между собой одним уравнением реакции, следовательно k = 2. Все вещества находятся в газовой фазе, поэтому f = 1. Если из внешних факторов, влияющих на состояние равновесия, учитывать только температуру и давление, тогда
С = 2 + 2 – 1 = 3.
Наличие у системы трех степеней свободы означает, что для однозначного определения равновесного состава газа необходимо указать температуру, давление и какую-либо постоянную величину, связанную с концентрацией взаимодействующих веществ.
В соответствии с принципом ЛеШателье при повышении температуры и неизменном давлении равновесие экзотермической реакции (1.1) смещается в направлении диссоциации CO2 на оксид углерода и кислород.
Горение оксида углерода протекает с уменьшением объема взаимодействующих веществ. Поэтому увеличение давления при неизменной температуре способствует протеканию реакции в направлении образования дополнительного количества CO2.
Если для сжигания СО используется воздух, в систему вносится еще один компонент – азот. Введение в систему азота при неизменных температуре и давлении влияет на изменение равновесного состава газовой смеси так же, как уменьшение давления.
Константа равновесия реакции (4.1) определяется из выражения
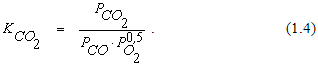
Состав газовой смеси принято выражать в объемных процентах. При этом парциальное давление газа связано с его объемной концентрацией соотношением

где Pi – парциальное давление i-го компонента газовой смеси; (i%) – концентрация компонента i в объемных процентах; Pобщ – общее давление в системе.
Выразив парциальные давления взаимодействующих газов при помощи уравнения (1.5), формулу (1.4) можно привести к виду
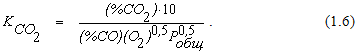
В уравнении (1.6) присутствует величина общего давления в системе. Его изменение при постоянной температуре вызывает изменение равновесных концентраций взаимодействующих веществ, но численное значение константы равновесия реакции остается при этом неизменным.
При заданном составе газовой смеси направление протекания реакции (1.1) можно определить при помощи уравнения
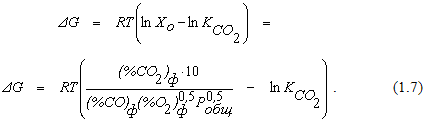
Согласно уравнению (1.7) протекание реакции (1.1) в направлении диссоциации CO2 возможно при соблюдении условия
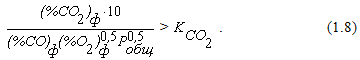
Из уравнения (1.2) формулу для определения константы равновесия реакции (1.1) можно получить в виде
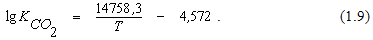
Результаты расчета константы равновесия реакции (1.1) при различных температурах представлены в таблице 1.1.
Таблица 1.1 – Значения константы равновесия реакции (1.1) при различных температурах
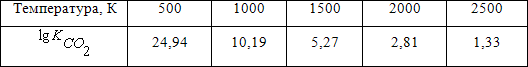
Из таблицы 1.1 можно видеть, что при температурах до 2000К константа равновесия реакции горения оксида углерода имеет очень большие значения. Так как (%CO2) не может быть больше 100%, из уравнения (1.8) следует, что диссоциация CO2 возможна только при малых концентрациях оксида углерода и кислорода или при очень низком давлении смеси газов Pобщ.
Результаты проведенного выше анализа показывают, что заметная диссоциации CO2 возможна только при температурах более 2000 – 2500К. При температурах до 2000К реакцию (1.1) можно считать практически не обратимой и протекающей при благоприятных кинетических условиях до полного исчезновения одного из исходных веществ.
Окислительный потенциал газовой смеси при протекании реакции (1.1) может быть охарактеризован величиной равновесного парциального давления кислорода
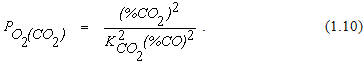
Анализ уравнения (1.10) позволяет сделать следующие выводы: Для газовой смеси с постоянным соотношением между концентрациями CO2 и СО величина равновесного парциального давления кислорода зависит только от температуры. При повышении температуры численное значение константы равновесия реакции (1.1) уменьшается, а окислительный потенциал газовой смеси увеличивается. При неизменной температуре величина равновесного парциального давления кислорода определяется соотношением между объемными концентрациями CO2 и СО в смеси. Окислительный потенциал газовой смеси повышается при увеличении (%CO2) и уменьшается при увеличении (%СО). Реакциягорения водорода может быть описана уравнением 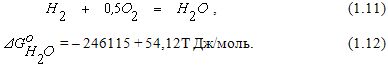 Реакции горения водорода и оксида углерода во многом похожи. Обе они являются сильными экзотермическими реакциями с тепловыми эффектами одного порядка. Стехиометрические соотношения между количествами взаимодействующих веществ в уравнениях реакций (1.11) и (1.1) одинаковы. Поэтому качественная оценка влияния изменения параметров системы на протекание реакций горения водорода и оксида углерода при помощи правила фаз Гиббса и принципа ЛеШателье приводит к одинаковым выводам.Протекание реакции (1.11) в направлении диссоциации H2O становится возможным в условиях, когда
Реакции горения водорода и оксида углерода во многом похожи. Обе они являются сильными экзотермическими реакциями с тепловыми эффектами одного порядка. Стехиометрические соотношения между количествами взаимодействующих веществ в уравнениях реакций (1.11) и (1.1) одинаковы. Поэтому качественная оценка влияния изменения параметров системы на протекание реакций горения водорода и оксида углерода при помощи правила фаз Гиббса и принципа ЛеШателье приводит к одинаковым выводам.Протекание реакции (1.11) в направлении диссоциации H2O становится возможным в условиях, когда 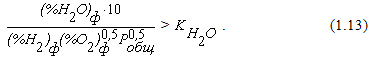 Из уравнения (1.12) формулу для определения константы равновесия реакции (1.11) можно получить в виде
Из уравнения (1.12) формулу для определения константы равновесия реакции (1.11) можно получить в виде
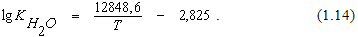 Результаты расчета константы равновесия реакции (1.11) при различных температурах представлены в таблице 1.2. Таблица 1.2 – Значения константы равновесия реакции (1.11) при различных температурах
Результаты расчета константы равновесия реакции (1.11) при различных температурах представлены в таблице 1.2. Таблица 1.2 – Значения константы равновесия реакции (1.11) при различных температурах 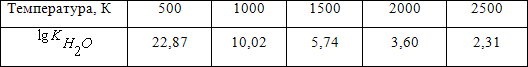 Анализ данных таблицы 1.2 показывает, что при температурах до 2000К константа равновесия реакции (1.11) также имеет очень высокие значения. Это позволяет в широком диапазоне температур считать реакцию горения
Анализ данных таблицы 1.2 показывает, что при температурах до 2000К константа равновесия реакции (1.11) также имеет очень высокие значения. Это позволяет в широком диапазоне температур считать реакцию горения
водорода практически не обратимой. Диссоциация H2O становится возможной только при малых концентрациях водорода и кислорода или очень низком давления смеси газов Pобщ. Окислительный потенциал газовой смеси при протекании реакции (1.11) также может быть охарактеризован величиной равновесного парциального давления кислорода 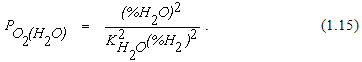 Анализ уравнения (1.15) позволяет сделать следующие выводы: Для газовой смеси с постоянным соотношением между концентрациями H2O и H2 величина равновесного парциального давления кислорода зависит только от температуры. При повышении температуры численное значение константы равновесия реакции (1.11) уменьшается, а окислительный потенциал газовой смеси увеличивается. При неизменной температуре величина равновесного парциального давления кислорода определяется соотношением между объемными концентрациями H2O и H2 в смеси. Окислительный потенциал газовой смеси повышается при увеличении (%H2O) и уменьшается при увеличении (%H2). Между реакциями (1.11) и (1.1) имеются также и некоторые различия. Так как
Анализ уравнения (1.15) позволяет сделать следующие выводы: Для газовой смеси с постоянным соотношением между концентрациями H2O и H2 величина равновесного парциального давления кислорода зависит только от температуры. При повышении температуры численное значение константы равновесия реакции (1.11) уменьшается, а окислительный потенциал газовой смеси увеличивается. При неизменной температуре величина равновесного парциального давления кислорода определяется соотношением между объемными концентрациями H2O и H2 в смеси. Окислительный потенциал газовой смеси повышается при увеличении (%H2O) и уменьшается при увеличении (%H2). Между реакциями (1.11) и (1.1) имеются также и некоторые различия. Так как 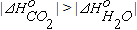 , при повышении температуры константа равновесия реакции горения оксида углерода уменьшается быстрее, чем константа равновесия реакции горения водорода. Расчеты показывают, что при температуре 1083К
, при повышении температуры константа равновесия реакции горения оксида углерода уменьшается быстрее, чем константа равновесия реакции горения водорода. Расчеты показывают, что при температуре 1083К 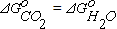 . Это означает, что при соблюдении условия
. Это означает, что при соблюдении условия 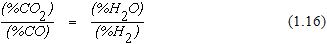 окислительный потенциал газовой смеси при протекании реакций горения оксида углерода и водорода будет одинаковым. При Т < 1083К
окислительный потенциал газовой смеси при протекании реакций горения оксида углерода и водорода будет одинаковым. При Т < 1083К 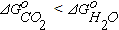 , то есть СО обладает более высоким химическим сродством к кислороду. Поэтому при соблюдении условия (1.16)
, то есть СО обладает более высоким химическим сродством к кислороду. Поэтому при соблюдении условия (1.16) 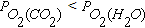 .При Т > 1083К
.При Т > 1083К 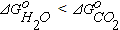 . В этих условиях более высоким хи-мическим сродством к кислороду обладает водород. Поэтому при выполнении условия (1.16)
. В этих условиях более высоким хи-мическим сродством к кислороду обладает водород. Поэтому при выполнении условия (1.16) 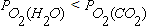 .
.
Реакция водяного газа описывается уравнением 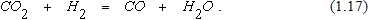 Реакцию (1.17) можно рассматривать как результат последовательного протекания реакций диссоциации CO2и окисления водорода.
Реакцию (1.17) можно рассматривать как результат последовательного протекания реакций диссоциации CO2и окисления водорода. 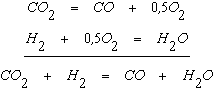
При этом 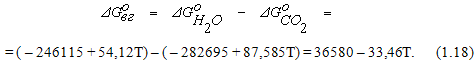 Анализ реакции (1.17) с использованием правила фаз Гиббса показывает, что система состоит из 4 веществ, связанных одним уравнением реакции. Следовательно К = 3. Все они находятся в газовой фазе, поэтому С = 3 + 2 – 1 = 4. Наличие у системы 4 степеней свободы означает, что для однозначной характеристики состава равновесной газовой смеси необходимо указать температуру, давление и содержание двух ее компонентов (или соотношение между ними). В соответствии с принципом ЛеШателье повышение температуры способствует протеканию эндотермической реакции (1.17) в направлении образования дополнительного количества H2O. Так как протекание реакции водяного газа не сопровождается изменением объема взаимодействующих веществ, изменение давления в системе не отражается на величинах их равновесных концентраций. Стандартное значение изменения энергии Гиббса реакции (1.17) становится равным нулю при температуре 1083К. Поэтому любая газовая смесь, соотношение между концентрациями компонентов которой отвечает условию
Анализ реакции (1.17) с использованием правила фаз Гиббса показывает, что система состоит из 4 веществ, связанных одним уравнением реакции. Следовательно К = 3. Все они находятся в газовой фазе, поэтому С = 3 + 2 – 1 = 4. Наличие у системы 4 степеней свободы означает, что для однозначной характеристики состава равновесной газовой смеси необходимо указать температуру, давление и содержание двух ее компонентов (или соотношение между ними). В соответствии с принципом ЛеШателье повышение температуры способствует протеканию эндотермической реакции (1.17) в направлении образования дополнительного количества H2O. Так как протекание реакции водяного газа не сопровождается изменением объема взаимодействующих веществ, изменение давления в системе не отражается на величинах их равновесных концентраций. Стандартное значение изменения энергии Гиббса реакции (1.17) становится равным нулю при температуре 1083К. Поэтому любая газовая смесь, соотношение между концентрациями компонентов которой отвечает условию
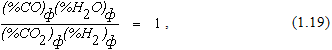 при этой температуре находится в состоянии равновесия. Протекание реакции водяного газа сопровождается малым тепловым эффектом, поэтому изменение температуры не оказывает сильного влияния на величину константы равновесия реакции. Это означает, что в широком интервале температур константа равновесия реакции (1.17) мало отличается от единицы. При этом в составе равновесной газовой смеси могут присутствовать достаточно большие количества каждого из взаимодействующих газов, что позволяет считать реакцию водяного газа практически полностью обратимой.
при этой температуре находится в состоянии равновесия. Протекание реакции водяного газа сопровождается малым тепловым эффектом, поэтому изменение температуры не оказывает сильного влияния на величину константы равновесия реакции. Это означает, что в широком интервале температур константа равновесия реакции (1.17) мало отличается от единицы. При этом в составе равновесной газовой смеси могут присутствовать достаточно большие количества каждого из взаимодействующих газов, что позволяет считать реакцию водяного газа практически полностью обратимой.
ОБЩАЯ ТЕРМОДИНАМИЧЕСКАЯ ХАРАКТЕРИСТИКА РЕАКЦИЙ ГАЗИФИКАЦИИ УГЛЕРОДА. Реакция взаимодействия углерода с углекислым газом.
Взаимодействие углерода с углекислым газом протекает по реакции 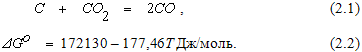
Рассматриваемая система состоит из двух фаз – твердого углерода и газа (f = 2). Три взаимодействующих вещества связаны между собой одним уравнением реакции, следовательно, количество независимых компонентов k = 2. Согласно правилу фаз Гиббса число степеней свободы системы будет равно С = 2 + 2 – 2 = 2 .
Это означает, что равновесные концентрации СО и СО2 являются функциями температуры и давления. Реакция (2.1) является эндотермической. Поэтому согласно принципу ЛеШателье повышение температуры смещает равновесие реакции в направлении образования дополнительного количества СО.
При протекании реакции (2.1) расходуется 1 моль СО2, который при нормальных условиях имеет объем 22400 см3, и 1 моль твердого углерода объемом 5,5 см3. В результате реакции образуется 2 моля СО, объем которых при нормальных условиях равен 44800 см3.
Из приведенных выше данных об изменении объема реагентов при протекании реакции (2.1) следует: Рассматриваемое превращение сопровождается увеличением объема взаимодействующих веществ. Поэтому в соответствии с принципом ЛеШателье повышение давления будет способствовать протеканию реакции в направлении образования СО2. Изменение объема твердой фазы пренебрежимо мало в сравнении с изменением объема газа. Поэтому для гетерогенных реакций с участием газообразных веществ с достаточной точностью можно считать, что изменение объема взаимодействующих веществ определяется только количеством молей газообразных веществ в правой и левой частях уравнения реакции.
Константа равновесия реакции (2.1) определяется из выражения

Если в качестве стандартного состояния при определении активности углерода принять графит, то аС = 1

Численное значение константы равновесия реакции (2.1) можно определить из уравнения
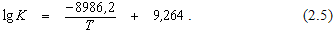
Данные о влиянии температуры на величину константы равновесия реакции приведены в таблице 2.1.
Таблица 2.1 – Значения константы равновесия реакции (2.1) при различных температурах
Из приведенных данных видно, что при температуре около 1000К (700оС) константа равновесия реакции близка к единице. Это означает, что в области умеренных температур реакция (2.1) практически полностью обратима. При высоких температурах реакция необратимо протекает в направлении образования СО, а при низких температурах в обратном направлении.
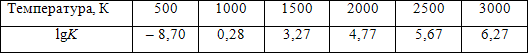
Если газовая фаза состоит только из СО и СО2, выразив парциальные давления взаимодействующих веществ через их объемные концентрации, уравнение (2.4) можно привести к виду
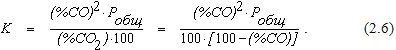
Решение уравнения (2.6) позволяет рассчитать (%СО) в равновесной газовой смеси при различных температурах и давлениях.
В промышленных условиях СО и СО2 получают в результате взаимодействия углерода с кислородом воздуха или дутья, обогащенного кислородом. При этом в системе появляется еще один компонент – азот. Введение азота в газовую смесь влияет на соотношение равновесных концентраций СО и СО2 аналогично уменьшению давления.
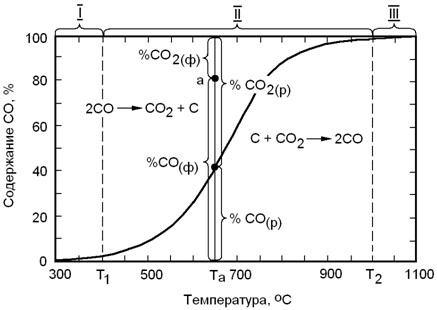
Из уравнения (2.6) видно, что состав равновесной газовой смеси является функцией температуры и давления. Поэтому решение уравнения (2.6) графически интерпретируется при помощи поверхности в трехмерном пространстве в координатах Т, Pобщ и (%СО). Восприятие такой зависимости затруднено. Значительно удобнее изображать ее в виде зависимости состава равновесной смеси газов от одной из переменных при постоянстве второго из параметров системы. В качестве примера на рисунке 2.1 приведены данные о влиянии температуры на состав равновесной газовой смеси при Pобщ = 105 Па.
При известном исходном составе смеси газов судить о направлении протекания реакции (2.1) можно при помощи уравнения
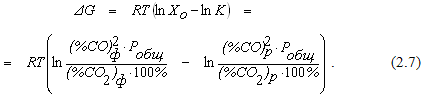
Если давление в системе остается неизменным, соотношение (2.7) можно привести к виду
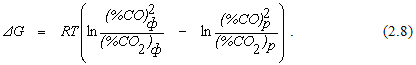
Для газовой смеси, состав которой отвечает точке а на рисунке 2.1, 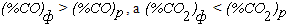 . При этом
. При этом
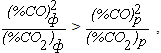
а 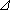 G > 0. Таким образом, точки выше равновесной кривой характеризуют системы, приближение которых к состоянию термодинамического равновесия протекает по реакции
G > 0. Таким образом, точки выше равновесной кривой характеризуют системы, приближение которых к состоянию термодинамического равновесия протекает по реакции
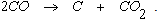
Аналогичным образом можно показать, что точки ниже равновесной кривой характеризуют системы, которые приближаются к равновесному состоянию по реакции
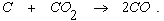
На рисунке 2.1 можно выделить следующие три области: 1 – область низких температур (до 400оС). При низких температурах содержание СО2 в составе равновесной смеси газов приближается к 100%. Поэтому при низких температурах существуют термодинамические
предпосылки для необратимого протекания реакции в направлении распада СО (в реальных условиях распад СО может не наблюдаться по причинам кинетического характера).2 – область умеренных температур (400 – 1000оС). В этой области равновесный газ содержит соизмеримые количества СО и СО2, а реакция является практически полностью обратимой. 3 – область высоких температур (более 1000оС). В этой области содержание СО в равновесном газе приближается к 100%. Это означает, что в присутствии твердого углерода СО2 не устойчив и должен полностью превращаться в СО.
Реакции полного и неполного горения углерода.
Взаимодействие углерода и кислорода может протекать с образованием низшего и высшего оксидов по следующим реакциям:
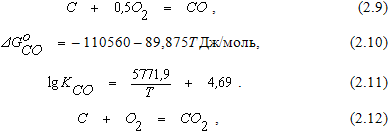
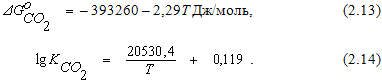
Обе реакции являются экзотермическими, поэтому при повышении температуры константы равновесия этих реакций уменьшаются.
Так как 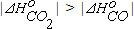 , при повышении температуры константа равновесия реакции (2.12) будет уменьшаться быстрее, чем константа равновесия реакции (2.9).
, при повышении температуры константа равновесия реакции (2.12) будет уменьшаться быстрее, чем константа равновесия реакции (2.9).
Чтобы определить температуру, при которой протекание обеих реакций становится равновероятным, необходимо сравнить значения изменения энергии Гиббса реакций, отнесенные к одному молю кислорода
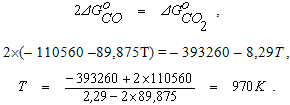
Таким образом при температуре около 700оС реакции окисления углерода до СО и СО2 с точки зрения термодинамики равновероятны.
При температурах менее 700оС 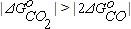 , то есть с точки зрения термодинамики более вероятным является окисление углерода по реакции (2.12). При температурах выше 700оС
, то есть с точки зрения термодинамики более вероятным является окисление углерода по реакции (2.12). При температурах выше 700оС 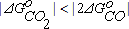 , поэтому при высоких температурах более вероятным является протекание реакции (2.9).
, поэтому при высоких температурах более вероятным является протекание реакции (2.9).
Результаты расчета констант равновесия реакций (2.9) и (2.12) при различных температурах показаны в таблице 2.2.
Таблица 2.2 – Константы равновесия реакций окисления углерода при различных температурах
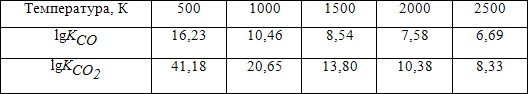
Высокие значения констант равновесия реакций свидетельствуют о том, что обе они необратимо протекают до практически полного исчезновения одного из веществ в левой части уравнения реакции. При этом возможны следующие случаи:
1. При наличии в системе избытка углерода в результате реакций (2.9) и (2.12) кислород будет полностью израсходован и газовая фаза будет состоять из СО и СО2. В этих условиях состав равновесного газа будет определяться протеканием реакции
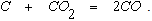
Доля углерода, окисленного по реакциям (2.9) и (2.12), может быть охарактеризована содержанием СО и СО2 в
равновесной газовой фазе. Из рисунка 2.1 видно, что чем выше температура, тем больше отношение (%СО)/(%СО2) в равновесном газе. При температурах более 1000 – 1100оС взаимодействие углерода с кислородом будет протекать только по реакции неполного горения.
2. При наличии в системе избытка кислорода в результате протекания реакций (2.9) и (2.12) углерод будет полностью израсходован, а газовая фаза будет состоять из остатка кислорода, СО и СО2. При этом результат газификации углерода определяется протеканием реакции
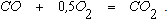
Взаимодействие углерода с водяным паромможет протекать по следующим реакциям
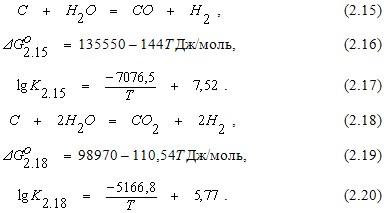
В результате протекания реакция (2.15) и (2.18) образуется газовая фаза, состоящая из СО, СО2, Н2 и Н2О. В газовой фазе такого состава будет протекать реакция водяного газа
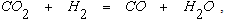
а также реакция между СО2 и твердым углеродом
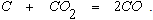
Реакции (2.15) и (2.18) являются эндотермическими. Согласно принципу ЛеШателье при повышении температуры в составе равновесной газовой смеси количество водяного пара будет уменьшаться, а содержание Н2, СО и СО2 будет увеличиваться.
Так как реакции (2.15) и (2.18) протекают с увеличением объема взаимодействующих веществ, при неизменной температуре протеканию реакций в направлении образования Н2, СО и СО2 будет способствовать понижение давления.
Если одновременно с реакциями (2.15) и (2.18) протекает реакция взаи-модействия углерода с углекислым газом и реакция водяного газа, то и повышение температуры и уменьшение давления будут способствовать увеличению соотношения (%СО)/(%СО2) в равновесной смеси.
В таблице 2.3 приведены сведения о влиянии температуры на величину констант равновесия реакций (2.15) и (2.18)
Таблица 2.3 – Константы равновесия реакций (2.15) и (2.18) при различных температурах
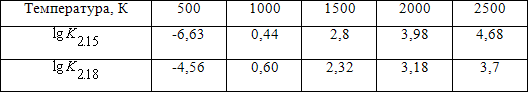
Из приведенных данных видно, что:
1. В области низких температур водяной пар практически не взаимодействует с углеродом.
2. При температурах 400 – 1000оС обе реакции практически полностью обратимы, поэтому в составе равновесного газа присутствуют значительные количества водяного пара.
3. При высоких температурах в присутствии твердого углерода водяной пар практически полностью расходуется в результате протекания реакций (2.15) и (2.18).
В области умеренных температур образовавшаяся в результате реакций (2.15) и (2.18) газовая фаза содержит в значительных количествах Н2О, СО, СО2 и Н2. Равновесный состав газовой фазы определяется протеканием реакции водяного газа.
Реакция водяного газа является эндотермической, поэтому при повышении температуры в составе равновесного газа увеличивается содержание СО, что эквивалентно увеличению количества углерода, газифицированного по реакции (2.15). При понижении температуры в равновесной газовой смеси увеличивается содержание СО2, что эквивалентно газификации углерода преимущественно по реакции (2.18).
При высоких температурах эндотермические реакции водяного газа и взаимодействия углерода с СО2необратимо протекают в направлении образования СО. Это дает основания считать, что при высоких температурах газификация углерода протекает только по реакции (2.15).
