Тепловое излучение. Равновесное излучение.
ЛЕКЦИИ ПО ФИЗИКЕ
Часть 5
КВАНТОВАЯ И ЯДЕРНАЯ ФИЗИКА
Владимир 2015
УДК 530.145 (075)
ББК 22.31я7
Рецензенты:
Доктор технических наук,
профессор, зам. директора Института физики Земли РАН
В.Н. Конешов
Составители: Галкин А.Ф., Прокошева Н.С. «Лекции по физике. Часть 5. Квантовая и ядерная физика»
Учебное пособие содержит двенадцать лекций, посвященных раскрытию физического смысла основных понятий и законов квантовой и ядерной физики, а также вопросы для самоконтроля.
Предназначены для студентов 1-го и 2-го курсов, изучающих дисциплину «Физика», технических специальностей всех форм обучения вуза, а также преподавателей.
Ил. Библиогр:
УДК 530.145 (075)
ББК 22.31я7
ISBN 5-93208-055-8
Введение
Издание продолжает курс лекций по физике и содержит двенадцать лекций по квантовой и ядерной физике.
Материал изложен кратко, доступно, без излишнего математического формализма
Цель авторов- сделать доступными основные понятия и законы квантовой, ядерной физики а также основ физики элементарных частиц.
Чтобы проверить себя, студенту после внимательного изучения теории необходимо ответить на вопросы для самоконтроля после каждой лекции. Параллельно с изучением теоретического материала нужно решать задачи, например из пособия /8/. Максимальное внимание должно быть уделено физическому смыслу изучаемых понятий и законов. Наиболее важные определения, понятия выделены или подчеркнуты.
Пособие рассчитано на всех студентов нашего университета, изучающих физику.
ВНИМАНИЕ! ПОСОБИЕ ОБЛЕГЧАЕТ РАБОТУ СТУДЕНТУ, НО НЕ ЗАМЕНЯЕТ САМИ ЛЕКЦИИ!
Лекция 1.
ЗАКОНЫ ТЕПЛОВОГО ИЗЛУЧЕНИЯ
План
1. Тепловое излучение. Равновесное излучение.
2. Характеристики теплового излучения.
3. Закон Кирхгофа.
4. Закон Стефана-Больцмана и закон смещения Вина.
5. Формула Рэлея-Джинса. Ультрафиолетовая катастрофа.
6. Формула Планка.
Закон Кирхгофа.
Тепловое равновесие имеет динамический характер, т.е. при одинаковых температурах тел излучение и поглощение энергии происходит так, что в единицу времени тело столько же излучает тепла, сколько оно его поглощает. Очевидно, что если два тела обладают различной способностью к поглощению, то их способность к испусканию также неодинакова.
В 1859 г. Кирхгоф сформулировал это утверждение в виде строго количественного закона, играющего важную роль во всех вопросах теплового излучения: отношение испускательной к поглощательной способности не зависит от природы тела, оно является для всех тел одной и той же (универсальной) функцией частоты (длины волны) и температуры:
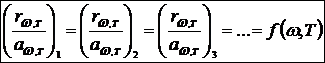 (1.4)
(1.4)
Сами величины аω,Т и rω,Т для различных тел могут сильно отличаться. Отношение же их оказывается одинаковым для всех тел.
Для абсолютно черного тела поглощательная способность равна единице. Следовательно, универсальная функция Кирхгофа 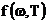 имеет смысл испускательной способности абсолютно черного тела
имеет смысл испускательной способности абсолютно черного тела 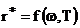 . Определение вида данной функции явилось основной задачей в теории теплового излучения.
. Определение вида данной функции явилось основной задачей в теории теплового излучения.
Лекция № 2.
КВАНТОВЫЕ СВОЙСТВА СВЕТА
План
1. Фотоэлектрический эффект.
2. Фотоны.
3. Эффект Комптона.
Фотоэлектрический эффект.
Квантовая гипотеза Планка привела в дальнейшем к представлению о том, что свет не только испускается, но и поглощается отдельными порциями – квантами. Она нашла свое подтверждение и дальнейшее развитие в ряде явлений таких, как фотоэффект, эффект Комптона и др.
Внешним фотоэффектом называется испускание электронов веществом под действием света. Впервые Герц в 1887 г. обнаружил, что проскакивание искры между шариками разрядника значительно облегчается, если один из шариков осветить ультрафиолетовым светом. Это явление, как показали опыты А.Г.Столетова (1888-1890), обусловлено выбиванием под действием света отрицательных зарядов из металлического катода разрядника. На основании своих опытов Столетов пришел к следующим выводам: 1) наибольшее действие оказывают ультрафиолетовые лучи; 2) сила тока возрастает с увеличением освещенности пластины; 3) испускаемые под действием света заряды имеют отрицательный знак.
Для изучения фотоэффекта пользуются вакуумной трубкой. Катод в фотоэлементе Ф, покрытый исследуемым металлом, освещается монохроматическим светом. Внутри трубки поддерживается высокий вакуум, так как присутствие газов осложняет условия выхода и переноса зарядов. Между анодом и катодом с помощью батареи создается разность потенциалов. Электроны, освобожденные светом, под действием напряжения между анодом и катодом, движутся на анод и далее следуют по проводам через гальванометр Г, замыкая ток в цепи (см. рис.1).
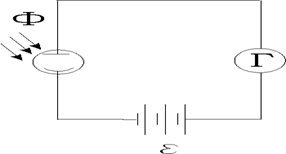 |
Рис.1
При неосвещенном катоде ток в цепи фотоэлемента отсутствует.
Зависимость фототока от напряжения можно представить в виде графика (рис.2)
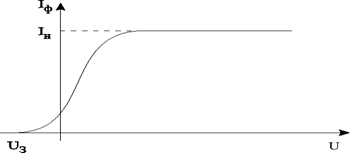 |
Рис.2
Существование фототока в области отрицательных напряжений объясняется тем, что фотоэлектроны обладают отличной от нуля кинетической энергией. За счет уменьшения этой энергии они могут совершать работу против сил задерживающего электрического поля в трубке и достигать анода. Максимальная начальная скорость фотоэлектронов υmax связана с величиной задерживающего напряжения Uзад соотношением
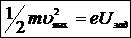 (2.1)
(2.1)
где e и m – заряд и масса электрона.
При 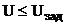 фототок равен нулю. По мере увеличения напряжения ток постепенно возрастает, так как все большее число фотоэлектронов достигает анода. Максимальное значение силы тока Iн называется фототоком насыщения и соответствует таким значениям напряжения, при которых все электроны, выбиваемые из катода, достигают анода.
фототок равен нулю. По мере увеличения напряжения ток постепенно возрастает, так как все большее число фотоэлектронов достигает анода. Максимальное значение силы тока Iн называется фототоком насыщения и соответствует таким значениям напряжения, при которых все электроны, выбиваемые из катода, достигают анода.
Опытным путем установлены следующие основные законы фотоэффекта:
1. Максимальная начальная скорость фотоэлектронов определяется частотой света и не зависит от его интенсивности.
2. Для каждого вещества существует красная граница фотоэффекта, т.е. характерная минимальная частота света ω0 (или максимальная длина волны λ0), при которой еще возможен фотоэффект. Красная граница зависит от химической природы вещества и состояния его поверхности.
3. Количество испускаемых с катода электронов пропорционально интенсивности светового излучения (фототок насыщения пропорционален энергетической освещенности катода).
При объяснении первого и второго законов встретились серьезные трудности. Согласно электромагнитной теории, вырывание свободных электронов из металла должно являться результатом их “раскачивания” в электрическом поле световой волны. Однако в этом случае непонятно, почему максимальная начальная скорость и кинетическая энергия вылетающих фотоэлектронов зависят от частоты света, а не от амплитуды колебаний вектора напряженности электрического поля и связанной с ней интенсивностью волны. Эти факты вызывали сомнения в универсальной применимости волновой теории света.
Законы фотоэффекта находят свое объяснение в рамках квантовой теории. В 1905 году Эйнштейн, изучая проблему возникновения и превращения света, использовал явление фотоэффекта как подтверждение своих идей. Энергетический баланс при фотоэффекте выражается уравнением Эйнштейна
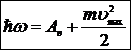 , (2.2)
, (2.2)
где 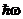 - энергия светового кванта, переданная электрону. Если эта энергия превышает энергию, необходимую для разрыва связи электрона с данным веществом (работу выхода А), то электрон покидает поверхность вещества, обладая кинетической энергией, максимально возможное значение которой определяется из уравнения Эйнштейна.
- энергия светового кванта, переданная электрону. Если эта энергия превышает энергию, необходимую для разрыва связи электрона с данным веществом (работу выхода А), то электрон покидает поверхность вещества, обладая кинетической энергией, максимально возможное значение которой определяется из уравнения Эйнштейна.
Таким образом, внешний фотоэффект возможен только в том случае, когда энергия фотона 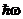 больше или, в крайнем случае, равна работе выхода А. Следовательно, соответствующая красной границе фотоэффекта частота равна
больше или, в крайнем случае, равна работе выхода А. Следовательно, соответствующая красной границе фотоэффекта частота равна 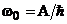 . Она зависит только от работы выхода электрона, т.е. от химической природы металла и состояния его поверхности.
. Она зависит только от работы выхода электрона, т.е. от химической природы металла и состояния его поверхности.
Фотоны.
Чтобы объяснить распределение энергии в спектре равновесного теплового излучения достаточно, как показал Планк, допустить, что свет испускается порциями 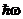 . Для объяснения фотоэффекта достаточно предположить, что свет поглощается такими же порциями. Далее Эйнштейн выдвинул гипотезу, что свет распространяется в пространстве также в виде дискретных частиц - фотонов.
. Для объяснения фотоэффекта достаточно предположить, что свет поглощается такими же порциями. Далее Эйнштейн выдвинул гипотезу, что свет распространяется в пространстве также в виде дискретных частиц - фотонов.
Фотон как частица обладает особыми свойствами хотя бы потому, что он движется со скоростью света. Поэтому формулы классической механики к движению фотона неприменимы, и нужно пользоваться релятивистскими соотношениями. Помимо энергии ε = ћ ω фотон должен обладать массой и импульсом. Формула для массы фотона может быть получена из формулы, выражающей взаимосвязь массы и энергии в теории относительности и формулы энергии фотона
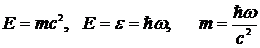 (2.3)
(2.3)
Согласно теории относительности импульс и энергия частицы, движущейся со скоростью v, равны
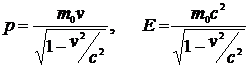 . (2.4)
. (2.4)
Но так как фотон движется со скоростью света, то знаменатель обращается в ноль, и получаем что p = ∞ и Е = ∞. Это означает, что никакое тело нельзя разогнать до скорости света. В случае фотона следует считать, что его масса покоя m0 = 0, т.е. в природе не существует покоящихся фотонов. Ясно, что приведенные формулы (2.4) оказываются непригодными, так как имеем неопределенности типа 0/0. Исключив из (2.4) скорость v , получим соотношение, связывающее импульс и энергию
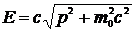
Для фотона m0 =0 и Е= ε = ћ ω, отсюда
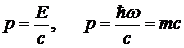 . (2.5)
. (2.5)
Так как фотон обладает импульсом, то, встречая на пути какое-нибудь препятствие, поток фотонов должен оказывать на это препятствие давление, подобно тому, как молекулы газа оказывают давление на стенки сосуда. Впервые русский физик Лебедев экспериментально измерил световое давление и подтвердил существование импульса у фотонов. Однако следует заметить, что в своих исследованиях Лебедев руководствовался не корпускулярной теорией света, а электромагнитной теорией Максвелла, которая тоже приводит к выводу о существовании светового давления. Обе теории дают одну и ту же формулу для вычисления светового давления 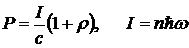 - интенсивность света (n-количество фотонов, падающих на единицу поверхности в единицу времени), ρ – коэффициент отражения света от поверхности тела. Это объясняется тем, что связь между импульсом и энергией фотона идентична связи между энергией и импульсом электромагнитного поля p = E/c.
- интенсивность света (n-количество фотонов, падающих на единицу поверхности в единицу времени), ρ – коэффициент отражения света от поверхности тела. Это объясняется тем, что связь между импульсом и энергией фотона идентична связи между энергией и импульсом электромагнитного поля p = E/c.
Если ввести волновое число 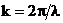 , то выражение (2.4) можно переписать в форме
, то выражение (2.4) можно переписать в форме
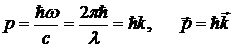 (2.6)
(2.6)
Направление импульса совпадает с направлением распространения света, характеризуемым волновым вектором k, численно равным волновому числу.
Таким образом, фотон подобно любой движущейся частице или телу, обладает энергией, массой и импульсом. Все эти три корпускулярные характеристики фотона связаны с волновыми его характеристиками – длиной волны или частотой. Корпускулярные свойства фотона не должны заставить нас забыть о том, что такие явления как дифракция и интерференция, могут быть объяснены только на основе волновых представлений.
Следовательно, свет обнаруживает корпускулярно-волновой дуализм (двойственность): в одних явлениях проявляется его волновая природа, и он ведет себя как электромагнитная волна; в других – проявляется корпускулярная природа света, и он ведет себя как поток фотонов.
Эффект Комптона.
Квантовые свойства света проявляются в эффекте, который обнаружил Комптон в 1923 г., наблюдая рассеяние монохроматического рентгеновского излучения. Схематически опыт Комптона можно изобразить следующим образом ( рис.1)
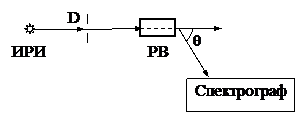 ИРИ – источник рентгеновского излучения
ИРИ – источник рентгеновского излучения
D – фокусирующая диафрагма
РВ - рассеивающее вещество Рис.1
Θ - угол рассеивания
В опыте было установлено, что в рассеянных лучах наряду с излучением первоначальной длины волны λ содержатся также лучи большей длины волны λ´. Разность 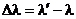 оказалась зависящей только от угла θ, образуемого направлением рассеянного излучения с направлением первичного пучка. С точки зрения классической волновой теории было невозможно объяснить эффект Комптона. Согласно этой теории, рассеяние света есть процесс переизлучения электромагнитных волн электронами. Электроны совершают вынужденные колебания под действием поля электромагнитной волны. Вынужденные колебания происходят на частоте вынуждающей силы. В результате в веществе должны возникать электромагнитные волны той же частоты (или длины волны).
оказалась зависящей только от угла θ, образуемого направлением рассеянного излучения с направлением первичного пучка. С точки зрения классической волновой теории было невозможно объяснить эффект Комптона. Согласно этой теории, рассеяние света есть процесс переизлучения электромагнитных волн электронами. Электроны совершают вынужденные колебания под действием поля электромагнитной волны. Вынужденные колебания происходят на частоте вынуждающей силы. В результате в веществе должны возникать электромагнитные волны той же частоты (или длины волны).
С квантовой точки зрения рассеяние можно рассматривать как процесс упругого соударения рентгеновских фотонов с практически свободными электронами. Свободными можно считать внешние электроны, энергия связи которых в атоме значительно меньше той энергии, которую фотон может передать электрону при соударении.
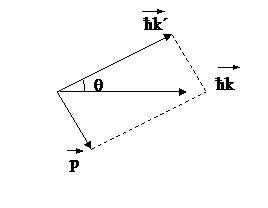
Пусть на покоящийся электрон падает фотон с энергией ħω и импульсом ħk( Рис.2)
Энергия электрона до столкновения 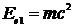
Энергия электрона после столкновения 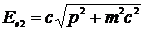
 Импульс электрона до столкновения p = 0.
Импульс электрона до столкновения p = 0.
Импульс электрона после столкновения
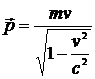
Энергия фотона до столкновения 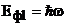
Энергия фотона после столкновения 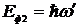
Импульс фотона до столкновения 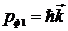 Рис.2
Рис.2
Импульс фотона после столкновения 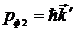
Закон сохранения энергии и импульса
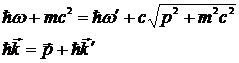 (*)
(*)
Перепишем первое уравнение в виде
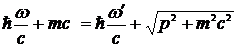 ,
,
или 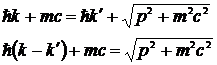 (**)
(**)
Решая систему уравнений (*), с учетом преобразований (**) получим
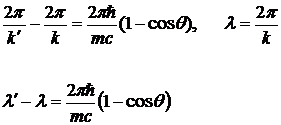
или
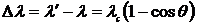 ,
,
где 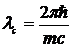 - комптоновская длина волны (в данном случае, электрона).В эффекте Комптона рентгеновский фотон проявляет корпускулярные свойства.
- комптоновская длина волны (в данном случае, электрона).В эффекте Комптона рентгеновский фотон проявляет корпускулярные свойства.
Вопросы для самоконтроля:
1. Как изменится фототок насыщения с уменьшением освещенности при данной частоте?
2. Как будет уменьшаться максимальная кинетическая энергия фотоэлектрона при увеличении частоты падающего излучения? От его интенсивности?
3. Нарисуйте вольт-амперные характеристики соответствующим двум различным частотам (при заданной освещенности).
4. Нарисуйте вольт-амперные характеристики соответствующим двум различным освещенностям (при заданной частоте).
5. Найдите отношение давлений света на зеркальную и черную поверхности.
6. В чем отличие характера взаимодействия при эффекте Комптона и фотоэффекте?
7. В каких случаях свет проявляет корпускулярную, а в каких волновую природу?
Лекция № 3.
СТРОЕНИЕ АТОМА.
План
1. Явления, подтверждающие сложное строение атома.
2. Спектральные закономерности.
3. Модель атома Резерфорда.
4. Постулаты Бора.
5. Атом водорода.
1. Явления, подтверждающие сложное строение атома.
Первоначально высказанная в виде догадки идея об атомном строении вещества по мере развития науки подтверждалась все большим числом опытов и в XIX веке превратилась в общепризнанную теорию. Вплоть до конца XIX века атомы считались вечными неизменными и неделимыми частицами материи, не имеющими внутренней структуры. Однако во второй половине XIX века было обнаружено много таких явлений, которые ставили под сомнение предположение об отсутствии внутренней структуры у атомов. Перечислим основные:
1. Электризация – электрические заряды, как положительные, так и отрицательные, должны входить в состав атомов.
2. Исследование оптических спектров химических элементов – атомы каждого химического элемента дают свое собственное излучение. Из электромагнитной теории света следует, что излучение атомов имеет электромагнитную природу, т.е. должно создаваться тем или иным движением зарядов, входящих в состав атома.
3. Открытая Менделеевым в 1869 г. периодичность свойств химических элементов свидетельствовала о повторяющихся комбинациях электрических зарядов внутри атомов.
4. Законы электролиза, установленные Фарадеем.
5. При опытах с рентгеновскими лучами и по фотоэффекту были обнаружены отрицательные и абсолютно одинаковые частицы, названные в 1891 г. электронами.
6. Открытие Беккерелем в 1896 г. излучения, источником которого являлись урановые руды и природа которого была не ясна. Последующие исследования П. и М. Кюри, Резерфорда показали, что это излучение имеет сложный характер и может быть разделено на лучи трех видов - α, β, γ. α – лучи оказались состоящими из дважды ионизированных атомов гелия, получивших название α-частиц, β-лучи - потоком быстрых электронов (β-частицы), γ-лучи - очень короткими электромагнитными волнами.
Модель атома Резерфорда
Важнейшим шагом вперед явилась попытка непосредственного опытного зондирования внутренних областей атома с целью установления пространственного распределения зарядов в атоме. Такое зондирование осуществил Резерфорд с помощью α – частиц, наблюдая изменение направления их полета (рассеяние) при прохождении через тонкие слои вещества.
Опыты Резерфорда показали, что наряду со случаями отклонения α – частиц в основном на малые углы происходят столкновения, вызывающие отклонения на углы вплоть до 180˚. Проанализировав результаты опыта, Резерфорд пришел к выводу, что столь сильное отклонение α – частиц возможно только в случае, если внутри атома имеется чрезвычайно сильное электрическое поле. Это поле создается зарядом, связанным с большой массой и сконцентрированным в очень маленьком объеме.
Основываясь на этом выводе, Резерфорд предложил в 1911 г. ядерную модель атома: атом представляет собой систему зарядов, в центре которой расположено тяжелое положительное ядро с зарядом Ze, имеющее размеры, не превышающие 10-14м. Вокруг ядра в области с линейными размерами порядка 10-10м расположены Z электронов, распределенных по всему объему, занимаемому атомом. Почти вся масса атома сосредоточены в ядре. Созданная Резерфордом модель напоминала строение солнечной системы, где вокруг массивного Солнца движутся сравнительно легкие планеты, поэтому такую модель строения атома назвали планетарной.
Итак, результаты опытов по рассеянию α – частиц свидетельствуют в пользу ядерной модели Резерфорда. Однако ядерная модель оказалась в противоречии с законами классической механики и электродинамики. Поскольку система неподвижных зарядов не может находиться в устойчивом состоянии – под действием кулоновских сил электроны сразу упали бы на ядро, Резерфорду пришлось отказаться от статической модели атома и предположить, что электроны движутся вокруг ядра, описывая искривленные траектории. Но в этом случае электрон будет двигаться с ускорением, непрерывно излучая электромагнитные волны, согласно классической электродинамике. Процесс излучения сопровождается потерей энергии, так что, в конечном счете, электрон должен упасть на ядро. Такая модель также не объясняла спектральных закономерностей. Электрон, приближаясь к ядру должен двигаться все быстрее, порождая все более короткие электромагнитные волны, в этом случае спектр излучения должен быть сплошным.
Недостатки модели: непрерывная потеря электроном энергии в виде излучения электромагнитных волн; неустойчивость атома; сплошной спектр излучения. В действительности: атом – устойчивая система; излучение имеет линейчатый спектр.
Для объяснения этих противоречий можно было выдвинуть два предположения: либо считать, что предложенная Резерфордом ядерная модель атома не соответствует действительности, либо считать, что законы классической физики имеют ограниченное значение и не могут применяться к движению таких маленьких частиц материи, как электрон.
Заменить ядерную модель атома другой моделью, которая соответствовала бы опытам Резерфорда и не противоречила бы классической физике, не удалось.
Постулаты Бора
Выход из затруднения был предложен Бором. Опираясь на идеи квантовой теории Планка, Бор предположил, что и в случае атома Резерфорда непрерывное излучение, требуемое классической электродинамикой, невозможно. Для истолкования линейчатых спектров Бор предположил, что излучение обладает частотой, определяемой из следующего условия
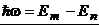 ,
,
где Em и En – энергии системы до и после излучения.
Исходя из этого закона, можно заключить, что спектры не дают нам картины движения частиц в атоме, как принимается в классической теории излучения, а позволяют судить лишь об изменениях энергии при различных возможных процессах в атоме. Дискретный характер спектральных линий свидетельствует о существовании определенных, дискретных значениях энергии, соответствующих особым состояниям атома. Эти состояния Бор назвал стационарными, ибо предположил, что атом может пребывать в каждом из них определенное время и, покидая его, снова попадает в другое стационарное состояние, изменяя свою энергию на конечную величину.
В 1913 г. Бор сформулировал два постулата:
1. Первый постулат (постулат стационарных состояний) - существуют стационарные состояния атома, находясь в которых он не излучает энергию. Этим стационарным состояниям соответствуют определенные (стационарные) орбиты, по которым движутся электроны.
Правило квантования орбит – из всех орбит электрона, возможных с точки зрения классической механики, осуществляются только те, для которых момент импульса равен величине, кратной постоянной Планка 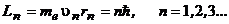 - целое число, m – масса электрона, υ– скорость электрона, r – радиус орбиты.
- целое число, m – масса электрона, υ– скорость электрона, r – радиус орбиты.
2. Второй постулат (правило частот) – при переходе атома из одного стационарного состояния в другое испускается или поглощается один фотон
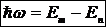 .
.
5. Атом водорода. Рассмотрим электрон, движущийся в поле атомного ядра с зарядом Ze. При Z = 1 такая система соответствует атому водорода, при иных Z – водородоподобному атому, т.е. иону, имеющему порядковый номер Z в таблице Менделеева и один электрон. Согласно закону Кулона между двумя точечными зарядами будет действовать сила
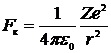
По закону динамики
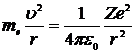 (*)
(*)
Используя правило квантования орбит( первый постулат) и исключая скорость, получим для радиусов допустимых орбит
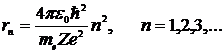 (**)
(**)
Радиус первой боровской орбиты атома водорода
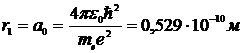
Внутренняя энергия атома складывается из кинетической энергии электрона (ядро неподвижно) и энергии взаимодействия электрона с ядром – потенциальной энергии а также используя (*) получим
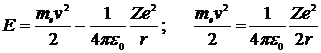
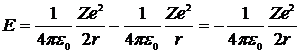
Подставив сюда выражение для радиуса орбиты (**), получим
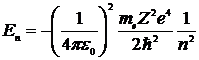 , (***)
, (***)
где n =1,2,3,… - номер орбиты.
Из формулы следует, что энергетические состояния атома водорода образуют последовательность энергетических уровней, изменяющихся в зависимости от числа n. Энергетическое состояние, соответствующее n = 1, называется основнымили невозбужденнымсостоянием. Все состояния с n >1 называются возбужденными.
При возрастании n энергетические уровни сближаются к границе, соответствующей n = ∞. При этом энергия электрона в атоме равна нулю. Знак минус в формуле показывает, что электрон связан в атоме силой притяжения к ядру. Абсолютное значение энергии является энергией связи электрона в атоме, находящимся в состоянии n. Значение энергии связи En = 0 соответствует ионизации атома, т.е. отрыву от него электрона. Для основного состояния энергия ионизации атома водорода, рассчитанная по формуле (***), равна 13,6 эВ.
При переходе атома водорода из состояния m в состояние n , m > n, излучается фотон, так как энергия Em > En по модулю
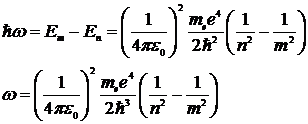
Переписав это соотношение для 1/λ, получим обобщенную формулу Бальмера
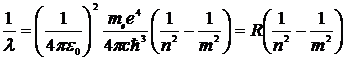 ,
,
Здесь постоянная Ридберга определяется подстановкой численных значений универсальных физических констант и поразительно совпадает с известным из опытов значением этой постоянной.
На рисунке приведена схема энергетических уровней атома водорода. Стрелками указаны переходы, соответствующие излучению различных спектральных серий.

Постулаты Бора о существовании стационарных состояний атомов и правило частот нашли свое экспериментальное подтверждение в опытах Франка и Герца в 1913 г. В опытах изучались столкновения электронов с атомами. Первые опыты были поставлены на парах ртути. Электроны, встречающие на своем пути атомы ртути испытывали с ними соударения двух видов. При упругих столкновениях энергия электронов не изменялась, а изменялось лишь направление их движения. Это, хотя и затрудняло попадание электронов на анод, однако не могло служить причиной полного отсутствия анодного тока, который возрастал с увеличением разности потенциалов. При неупругих столкновениях электрон терял свою энергию, передавая ее атому ртути. В соответствии с постулатами Бора атом не может принять энергию в любом количестве, а лишь определенную порцию, переходя при этом в возбужденное состояние. Ближайшим к основному состоянию атома ртути является возбужденное состояние, отстоящее от основного по шкале энергий на 4,86 эВ. Таким образом, при напряжении 4,86 В должно происходить резкое падение анодного тока, что и наблюдалось в эксперименте. Аналогичная ситуация должна повторяться при напряжениях, кратных 4,86 эВ. Правило частот также подтвердилось на эксперименте. Ртутные пары переходя из возбужденного состояния в основное излучали ультрафиолетовые волны с длиной волны, соответствующей первой резонансной линии в спектре ртути.
Теория Бора сыграла важную роль в создании атомной физики. Особенно велика ее роль в развитии атомной спектроскопии, где огромный экспериментальный материал с помощью теории Бора был систематизирован и сведен к определенным полуэмпирическим закономерностям.
Однако наряду с определенными успехами в теории Бора с самого начала обнаружились существенные недостатки. Теория была внутренне противоречива. Основываясь на механическом соединении классической физики с квантовыми постулатами, теория Бора в ряде проблем привела к существенным трудностям. Наиболее серьезной неудачей в теории Бора явилась абсолютная невозможность с ее помощью создать теорию атома гелия, содержащего помимо ядра два электрона. Постепенно становилось очевидным, что теория Бора представляла собой лишь переходный этап на пути создания последовательной теории атомных и ядерных явлений. Такой последовательной теорией явилась квантовая (волновая) механика. Она объяснила не только многообразие явлений атомной и ядерной физики, но и физическое содержание самих постулатов Бора.
Вопросы для самоконтроля:
1. Каковы недостатки модели атома Резерфорда?
2. Какая серия спектральных линий относится к видимой области спектра? Лаймана? Бальмера? Пашена?
3. Каков смысл постулатов Бора?
4. Как с помощью постулатов Бора объясняется линейчатый спектр атома?
5. Какова суть опытов Франка и Герца?
6. В чем состоят недостатки теории Бора?
Лекция 4.
Гипотеза де Бройля.
Недостатки в теории Бора свидетельствовали о необходимости пересмотра представлений о природе микрочастиц (электронов, протонов). Развитие теории света привело к пониманию того, что фотон подобно любой движущейся частице или телу, обладает энергией, массой и импульсом. Все эти три корпускулярные характеристики фотона связаны с волновыми его характеристиками – длиной волны или частотой. Следовательно, свет обнаруживает корпускулярно-волновой дуализм: в одних явлениях проявляется его волновая природа, и он ведет себя как электромагнитная волна; в других – проявляется корпускулярная природа света, и он ведет себя как поток фотонов.
В 1923 г. Луи де Бройль выдвинул смелую гипотезу, что дуализм не является особенностью одних только оптических явлений, а имеет универсальное значение, т.е. одновременное проявление корпускулярных и волновых свойств присуще любому материальному объекту. Допуская, что частицы вещества наряду с корпускулярными свойствами имеют также и волновые, де Бройль предположил, что если для фотона мы имели энергию 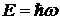 и импульс
и импульс 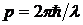 , то для микрочастицы можно определить соответствующую длину волны
, то для микрочастицы можно определить соответствующую длину волны
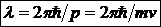
И частоту
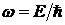
Идея была лишь теоретической гипотезой, так как не существовало фактов, которые подтверждали бы экспериментально существование волновых свойств частиц. В этом заключалось существенное отличие гипотезы де Бройля о волновых свойствах частиц от гипотезы Эйнштейна о существовании фотонов, выдвинутой им после открытия явления фотоэффекта.
Если электрон обладает волновыми свойствами, то он должен проявлять эти свойства в таких принципиально волновых явлениях как интерференция и дифракция.
Лекция 5.
УРАВНЕНИЕ ШРЕДИНГЕРА.
План
1. Вероятностный смысл волн де Бройля.
2. Нестационарное уравнение Шредингера.
3. Стационарное уравнение Шредингера.
4. Уравнение Шредингера для частицы в потенциальной яме.
Лекция 6.
Туннельный эффект.
При преодолении потенциального барьера частица как бы проходит через «туннель» в этом барьере, в связи с чем это явление и получило название туннельного эффекта( рис.3).
С классической точки зрения частица, «находящаяся в туннеле», должна обладать отрицательной кинетической энергией (E < U). 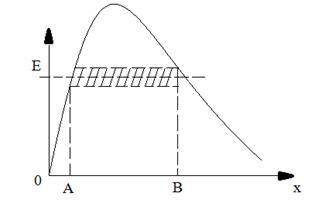
Рис.3
Однако туннельный эффект явление специфически квантовое, не имеющее аналога в классической физике. В квантовой механике деление энергии на кинетическую и потенциальную не имеет смысла, так как противоречит соотношению неопределенности.
Прохождение частиц сквозь потенциальный барьер нашло экспериментальное подтверждение в явлении автоэлектронной эмиссии электронов из металла. Вырывание электронов происходит при напряженностях электрического поля, в сотни раз меньших, чем те которые необходимы для того, чтобы электрон преодолел поверхностную разность потенциалов на границе металл-вакуум и покинул металл. Туннельный эффект играет основную роль в явлениях радиоактивного альфа-распада.
Туннельный эффект уже давно весьма эффективно используется в науке и технике. На нем основан принцип действия многих полупроводниковых приборов (туннельные диоды). Он используется в сверхчувствительных записывающих головках магнитных дисков, сканирующих туннельных микроскопах (1981). В настоящее время пространственная разрешающая способность таких микроскопов ~ 20 нм. Для сравнения, современный оптический микроскоп, конструкция которого была изобретена в 1873 г., имеет разрешающую способность ~ 200 нм.
Лекция 7.
АТОМ ВОДОРОДА.
План
1. Уравнение Шредингера для электрона в атоме водорода.
2. Главное n, орбитальное l и магнитное m квантовые числа; их физический смысл.
3. Условное обозначение состояний электрона. Правило отбора. Его физический смысл.
4. Понятие электронного облака. Его физический смысл.
Лекция 8.
АТОМЫ В МАГНИТНОМ ПОЛЕ
План
1. Орбитальный механический и магнитный моменты электрона.
2. Спин электрона.
3. Опыт Штерна и Герлаха.
1.Орбитальный механический и магнитный моменты электрона.Пусть электрон движется со скоростью v по орбите радиуса r . Через площадку, расположенную в любом месте на пути электрона, за время t переносится заряд q = eνt, где e – заряд электрона, ν – число оборотов в секунду. Следовательно, движущийся по орбите электрон образует круговой ток силы
I = 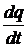 = eν.
= eν.
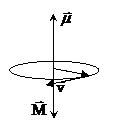 Поскольку заряд электрона отрицателен, направление движения электрона и направление тока противоположны. Магнитный момент создаваемого электроном тока равен
Поскольку заряд электрона отрицателен, направление движения электрона и направление тока противоположны. Магнитный момент создаваемого электроном тока равен
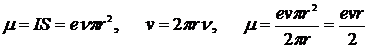 ,
,
где v – скорость движения электрона.
Момент обусловлен движением электрона по орбите, вследствие чего его назвали орбитальным магнитным моментом электрона. Направление вектора μобразует с направлением тока правовинтовую систему, а с направлением движения электрона – левовинтовую.
Орбитальный механический момент импульса 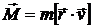 образует с направлением движения электрона правовинтовую систему. Следовательно, вектора μ и М ориентированы перпендикулярно плоскости орбиты и противоположно направлены.
образует с направлением движения электрона правовинтовую систему. Следовательно, вектора μ и М ориентированы перпендикулярно плоскости орбиты и противоположно направлены.
Отношение магнитного момента электрона к его механическому моменту называется гиромагнитным отношением. Получим
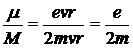
По Бору М = mvr = nћ. Следовательно,
