Растворы. Идеальные растворы. Законы Рауля и Генри. Термодинамическая активность.
Раствором называется однородная, состоящая из 2-х и более веществ система, состав которой может в определенных пределах непрерывно изменяться.
Идеальные растворы – это модели растворов, в которых законы Рауля и Генри выполняются с абсолютной точностью.
Оба закона устанавливают зависимость давления пара компонента над раствором от концентрации этого компонента в растворе.
Первый закон Рауля связывает давление насыщенного пара над раствором с его составом; он формулируется следующим образом:
- Парциальное давление насыщенного пара компонента раствора прямо пропорционально его мольной доле в растворе, причём коэффициент пропорциональности равен давлению насыщенного пара над чистым компонентом.
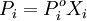
Растворы, для которых выполняется закон Рауля, называются идеальными. Идеальными при любых концентрациях являются растворы, компоненты которых очень близки по физическим и химическим свойствам (оптические изомеры, гомологи и т. п.), и образование которых не сопровождается изменением объёма и выделением либо поглощением теплоты.
Закон Генри: Закон Генри – это положение, согласно которому при постоянной температуре растворимость газа в данной жидкости (выраженная его весовой концентрацией) прямо пропорциональна давлению этого газа над раствором. При этом под растворимостью понимается способность вещества образовывать с другими веществами однородные системы
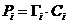 | |||
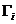 |
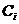 -константа (постоянная) Генри зависит от природы компонентов раствора и от выбранных единиц выражения концентраций.
-константа (постоянная) Генри зависит от природы компонентов раствора и от выбранных единиц выражения концентраций.
-концентрация растворенного компонента.Она может быть выражена в любых единицах, в том числе и в % по массе.
Концентрационный интервал, в котором реальные растворы подчиняются закону Генри, колеблется от долей процента до нескольких процентов.
Под активностью компонента в растворе понимают отношение парциального давления пара компонента над раствором к давлению пара этого же вещества, находящегося в стандартном состоянии
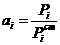 Активность имеет тот же физический смысл, что и концентрация, но учитывает взаимодействие частиц в растворе
Активность имеет тот же физический смысл, что и концентрация, но учитывает взаимодействие частиц в растворе
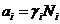 | 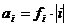 | ||
Термодинамические параметры взаимодействия, их использование в расчетах.
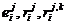 Производные уравнения называются массовыми параметрами взаимодействия первого и второго порядков и обозначаются соответственно
Производные уравнения называются массовыми параметрами взаимодействия первого и второго порядков и обозначаются соответственно
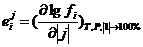
-массовый параметр взаимодействия компонента i с компонентом j первого порядка.
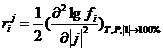
-массовый параметр взаимодействия компонента i с компонентом
j второго порядка
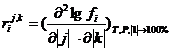
-массовый перекрестный параметр взаимодействия компонента i
второго порядка.
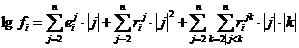
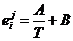 Обычно температурная зависимость параметров взаимодействия имеет вид
Обычно температурная зависимость параметров взаимодействия имеет вид
А и В – компоненты, Т – температура, К.
