Сделайте вывод о выходе продукта реакции
Решение
Кр = 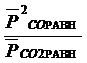 ; Кр = Кс(R*T)∆n , Кс =
; Кр = Кс(R*T)∆n , Кс = 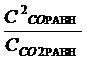
∆rG0Т = - RTlnКр Þ Kp =exp(-∆G0Т /RT)
Кр298 = exp(-120.103/8,31.298) = ехр(-48,5) = 8×10-22;
Kp1000 = exp(+3160/8,31.1000) = ехр(0,38) = 1, 46.
Кс = 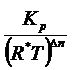 ∆n = 2-1=1
∆n = 2-1=1
Кс 298 = 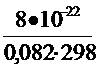 = 3×10-23 Кс 1000 =
= 3×10-23 Кс 1000 = 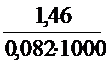 = 0,018
= 0,018
При 298 К - Кр < 0 Þ в равновесной смеси практически отсутствуют продукты и смещение Þв сторону получения исходных веществ.
При 1000 К - Кр > 1 Þ в равновесной смеси преобладают продукты, их выход растет с ↑Т,
Задача 2
Определить равновесные концентрации веществ для реакции: С(к) + СО2(г) = 2СО(г) , если Сисх СО2 = 0,5 моль/л; реакция протекает при:Т = 1000 К в закрытом сосуде и в начальный момент:
продукт отсутствовал; уголь - в избытке и Кс1000 = 0,018
На сколько изменится давление в системе при равновесии по сравнению с исходным?
Решение. Составим таблицу материального баланса
Таблица материального баланса
| Компонент | С | СО2 | СО |
| Начальные концентрации, Сисх , моль/л | - | 0,5 | |
| Изменение концентраций, ∆С, моль/л | - | х | 2 x |
| Равновесные концентрации С равн, моль/л | - | 0,5 – x | 2 x |
Кс=0,018
Запишим выражение константы равновесия:
Кс = 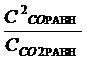 ;
;
Подставив значения находим:
Кс = 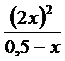 = 0,018. х = 0,0387 моль/л
= 0,018. х = 0,0387 моль/л
ССО равн = 2. 0,0387 = 0,0774 моль/л
С CO2равн = 0,5 - 0,0387 = 0,4613 моль/л
Так как Р = сR*T
То Р0 = сисх R*T = 0,5 . 0,082 .1000 = 41 атм
Рравн= ∑сравн R*T =(0,0774 +0,4613).0,082 .1000 = 44,173атм
Задача 3
Как увеличить выход продуктов реакции
С(к) + СО2(г) = 2СО(г) ∆rH0298 >0
Решение
Чтобы повысить выход продукта СО Þ нужно
равновесие смещать вправо:
а) ↑Т системы, т.к. ∆rH0298 > 0;
б) ↓Рсистемы, т.к прямая реакция идет с ↑числа молей газообразных веществ;
в) ↑РСО2 и ↓РСО(выводить СО из сферы реакции).
Задача 4
Рассчитать ∆r H0298 и ∆r H01000 реакции
С(к) + СО2(г) = 2СО(г),
считая постоянными теплоемкости реагентов в данном температурном интервале.
Решение
∆rН0Т = ∆rН0298 + ∆rС0р (Т - 298)
Справочные данные:
| Вещество | ΔfН0298, кДж/моль | С0р298 ,Дж/(моль.К) |
| С(графит) | 0,0 | 8,54 |
| СО2 (г) | -393,5 | 37,41 |
| СО (г) | -110,5 | 29,14 |
ΔrН0298 = 2ΔfН0298 СО(г) - ΔfН0298 С(к) - ΔfН0298 СО2(г) =
= 2(-110,5) – 0 – (-393,5) = 172,5 кДж.
ΔrН0298 >0 - реакция эндотермическая
∆rС0р = 2С0р298 СО(г) – С0р298 С(к) – С0р298 СО2(г) =
= 2.(29,14) – 8,54 – 37,41 = 12,33 Дж/К.
∆rН01000 =172,5 + 12,33.10-3.(1000 - 298) = 181,16 кДж.
Задача 5
Рассчитать ∆r S0Т реакции
С(к) + СО2(г) = 2СО(г),
при 298К и при 1000К, считая С0pi = const в рассматриваемом температурном интервале.
Решение
∆r S0Т = ∆r S0298 + ∆rС0р ln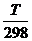
Справочные данные:
| Вещество | S0298, кДж/(моль.K) | С0р298 ,Дж/(моль.К) |
| С(графит) | 5,74 | 8,54 |
| СО2 (г) | 213,68 | 37,41 |
| СО (г) | 197,54 | 29,14 |
Δr S0298 = 2S0298 СО(г) - S0298 С(к) - S0298 СО2(г) =
= 2(197,54)–5,74–213,68=175,66 Дж/K
∆rС0р = 2С0р298 СО(г) – С0р298 С(к) – С0р298 СО2(г) =
= 2.(29,14) – 8,54 – 37,41 = 12,33 Дж/К.
∆r S01000 = 175,66 + 12,33.10-3. ln(1000 / 298) = 190,59 Дж/К
Задача6 Определить температурную область самопроизвольного протекания реакции
С(к) + СО2(г) = 2СО(г),
при стандартных состояниях компонентов.
Решение
Реакция протекает самопроизвольно при стандартных состояниях компонентов, если:
∆r G0Т=∆r H0298+ 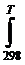 ∆rС0p dT+Т∆r S0298+Т
∆rС0p dT+Т∆r S0298+Т 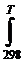 ∆rС0p/T) dT < 0
∆rС0p/T) dT < 0
Допустим: ∆r H0 и ∆r S0 не зависят от температуры:
∆r G0Т = ∆r H0298 - T∆r S0298 < 0
Тогда подставив найденные в задачах4 и5 ∆r H0 и ∆r S0 получаем:
(172,5 – Т∙175,66∙10-3) < 0 Тр = 982 К
Т > 982 К
Справочные данные:
| Вещество | Интервал температур, .К |
| С(графит) | (298 – 2300) К |
| СО2 (г) | (298 – 2500) К |
| СО (г) | (298 – 2500) К |
Следовательно: Область температур протекания реакции: 982 ÷ 2300
Задача1. Во сколько раз изменится скорость реакции
2СО(г) + О2(г)® 2СО2(г)
