Часть 2. Электрохимические системы и электрохимические процессы
Часть 2. Электрохимические системы и электрохимические процессы
В данной части рассматриваются системы, которые совершают полезную работу в ходе химической реакции. Практически единственным результатом такой работы может быть электрическая энергия. Если работа совершается в квазистатических условиях, то для описания этих систем успешно применяются методы классической термодинамики. Существуют методы описания систем, в которых процессы протекают с конечной скоростью. Как правило, они близки к обычному термодинамическому подходу и называются квазитермодинамическими. В нестатических условиях, когда происходит перемещение с конечной скоростью заряженных частиц в растворах, решающую роль могут играть свойства электролитов. Они также изучаются в этой части курса.
Глава 1. Термодинамика гальванического элемента
Гальванический элемент
Гальваническим элементомназывается устройство, в котором в результате химической реакции совершается полезная работа в виде электрической работы.
Рассмотрим, какие условия должны выполняться, чтобы реакция сопровождалась именно этой работой.
Прежде всего необходимо, чтобы реакция осуществлялась с переходом зарядов. Единственным химическим источником электрической работы может быть устройство, в котором протекает реакция окисления - восстановления. Только в ходе этой реакции происходит переход электронов от восстановителя к окислителю.
Второе условие требует, чтобы заряды переносились по всей электрической цепи.
Для пояснения второго условия рассмотрим следующую реакцию окисления - восстановления:
Cu2+ + Zn = Cu + Zn2+.
В этой реакции происходит перенос двух электронов от атома цинка к иону меди.
Однако если поместить цинковую пластинку в раствор, содержащий ионы меди, электрическую работу получить невозможно, так как восстановление ионов меди будет происходить при их прямом контакте с атомами цинка. Для того, чтобы совершалась электрическая работа, электроны должны от атомов цинка пройти к ионам меди по электрической цепи. Поэтому процесс окисления атомов цинка и процесс восстановления ионов меди необходимо пространственно разделить. Таким образом, цинковая пластинка не должна контактировать с ионами меди, содержащимися в растворе электролита. По этой причине цинковую пластинку следует погрузить в раствор, содержащий ионы цинка, а ионы меди должны контактировать с медью.
Следовательно, гальванический элемент состоит из двух основных частей, в одной из которых происходит окисление одного соединения, а в другой - восстановление другого (в данном случае - окисление цинка в одной части устройства и восстановление ионов меди в другой). Эти части называются полуэлементами. В качестве синонима используют другое название - электрод. Каждый из электродов обязательно содержит металл, погруженный в раствор электролита, а в ряде случаев - еще и малорастворимую соль, газ и другие вещества, не содержащиеся в фазе электролита.
Пару полуэлементов необходимо соединить с образованием электрической цепи. Для этого металлическую часть одного полуэлемента соединяют с металлической частью другого полуэлемента металлическим проводником. Цепь можно замкнуть, приведя в контакт растворы электролитов обоих полуэлементов (жидкостное соединение).
Однако по ряду причин для жидкостного соединения используют трубку, заполняемую промежуточным раствором электролита, чаще всего раствором хлорида калия. Такое жидкостное соединение называется солевым мостиком.
Определенный интерес представляет составление цепи в гальваническом элементе в том случае, когда один из элементов содержит неводный электролит. Например, один из полуэлементов может содержать водный раствор электролита, в который погружен малоактивный или даже инертный металл (цинк, медь, ртуть, платина и т.д.), а другой - электролит на основе безводного ацетона с погруженным в него металлическим натрием. Такой гальванический элемент, содержащий водный солевой мостик, а тем более при прямом контакте растворов, не будет стабильным (взаимодействие натрия с водой может привести даже к взрыву). В этом случае для замыкания цепи можно использовать ионизированный газ (Захарченко В.Н., 1974). Между двумя поверхностями растворов электролитов помещают источник ионизирующего излучения. Ионизированный газ содержит газ и электроны, подобен раствору электролита в солевом мостике.
В высокотемпературных гальванических элементах электролитом служат расплавленные вещества, которые называют ионными жидкостями. К ним относятся расплавы солей и расплавы оксидов.
Известны гальванические элементы с твердыми электролитами, например, с таблетированными ионными кристаллами a-AgI или кристаллами a-Ag2HgI4 .
Металл, погруженный в раствор электролита, может непосредственно участвовать в реакции, как это происходит с медью и цинком в приведенном выше примере. Если металл входит в суммарное уравнение химической реакции, протекающей в гальваническом элементе, он называется активным материалом. В других случаях процессы окисления и восстановления могут происходить только на поверхности металла, и он не входит в суммарное уравнение реакции и является лишь переносчиком электронов. Такой металл называется инертным электродным материалом. Наиболее часто в качестве инертных электродных материалов используются углерод и платина.
Гальванический элемент можно изображать графически. Например, в элементе, в котором протекает приведенная выше реакция Cu2+ + Zn = Cu + Zn2+, необходимо изобразить цинковую пластину, погружаемую в сосуд с раствором соединения, диссоциирующего с образованием ионов цинка, и медную пластину, погружаемую в сосуд с раствором, в котором содержатся ионы меди. Далее необходимо показать соединение медной пластины с цинковой и солевой мостик, соединяющий оба раствора электролита (рис. 1-1).
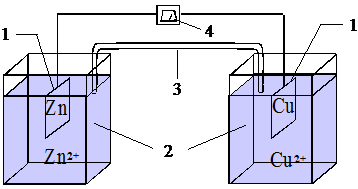 Рис. 1 - 1. Схема гальванического элемента: 1 - электродные материалы, 2 - электролиты, 3 ‑ солевой мостик, 4 - потенциометр. Рис. 1 - 1. Схема гальванического элемента: 1 - электродные материалы, 2 - электролиты, 3 ‑ солевой мостик, 4 - потенциометр. |
Однако многократное изображение гальванического элемента крайне неудобно. Поэтому практически всегда гальванический элемент предпочитают представлять в виде условной записи, которая подчиняется определенным правилам. Международный союз по чистой и прикладной химии (International Union of Pure and Applied Chemistry, IUPAC) рекомендует руководствоваться следующим:
1. Вначале устанавливается, какой из двух электродов данного элемента является более отрицательным.
Общие правила установления соотношения между знаками электродов будут рассмотрены при дальнейшем изложении курса. Для гальванического элемента, в котором происходит восстановление ионов меди атомами цинка, более отрицательным является цинк, а медь имеет более положительный потенциал.
2. Крайним слева записывается электродный материал более отрицательного электрода.
В приводимом случае слева необходимо записать цинк:
Zn.
2а. Если вне фазы электролита находится несколько веществ, включая газы, труднорастворимые соли и др., то их записывают, отделяя друг от друга запятыми, причем крайним слева всегда указывается металл (или другой проводник первого рода) более отрицательного электрода.
Приведем примеры:
Pt, H2; Ag, AgCl; C, C6H4O2, C6H6O2; Hg, Hg2Cl2.
3. Проводится вертикальная черта и указывается состав электролита левого (более отрицательного) электрода.
В рассматриваемом примере реакции между ионами меди и цинком с цинковой пластиной контактирует раствор, содержащий ионы цинка. Следовательно,
Zn ½ Zn2+.
3а. Если раствор электролита содержит несколько видов ионов или других веществ, принимающих участие в реакции, то их записывают, отделяя друг от друга запятыми.
Например,
Pt ½ MnO4 −, Mn2+, H+.
4. В случае соединения растворов электролитов солевым мостиком ставятся две вертикальных черты, правее которых записывается состав раствора электролитов правого (более положительного) электрода.
В рассматриваемом примере у медного электрода электролит содержит ионы меди. Следовательно,
Zn ½ Zn2+ ½½ Cu2+.
4а. Этот пункт правил повторяет пункт 3а для правого электрода.
5. Проводится вертикальная черта и указываются материалы правого электрода, причем крайним справа записывается металл или другой проводник первого рода.
Полная запись гальванического элемента с цинковым и медным электродами такова:
Zn½Zn2+½½Cu2+½Cu.
Классификация электродов
Различают три основных класса электродов:
· электроды с активным электродным материалом, то есть непосредственно входящим в суммарное уравнение электродной реакции,
· электроды с инертным электродным материалом, на поверхности которых протекает электродная реакция и которые не входят в уравнение этой реакции,
· ионоселективные электроды, представляющие собой мембраны, на поверхности которых происходит скачок потенциала.
К электродам с активным электродным материалом относятся электроды 1-го и 2-го рода, а к электродам с инертным электродным материалом относятся простые и сложные окислительно-восстановительные электроды, или редокс-электроды, и газовые электроды.
Из ионоселективных электродов важнейшим является стеклянный электрод.
Электроды 1-го рода
Электрод первого рода состоит из активного металла, погруженного в ненасыщенный раствор соли этого металла.
Обозначим металл M, а катионы, образующиеся при растворении его соли, - Mz+.
С учетом этих обозначений электродную реакцию можно записать следующим образом:
Mz+ + ze = M.
Условная запись электрода принимает следующий вид:
Mz+ôM.
Уравнение для электродного потенциала записывается так:
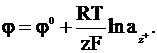 (2 - 1)
(2 - 1)
К электродам 1-го рода относятся медный электрод Cu2+ôCu, цинковый электрод Zn2+ôZn, серебряный электрод Ag+ôAg и др.
Эту группу электродов объединяет то, что их потенциал зависит от активности катиона. Название этой группы - электроды, обратимые по катиону.
Однако к числу электродов 1-го рода относится немногочисленная группа электродов, потенциал которых определяется активностью аниона (их называют электродами, обратимыми по аниону). Наиболее изученными из них являются селеновый электрод и теллуровый электрод, который характеризуется следующим:
2Te + 2e = 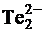 −,
−,

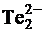 ôTe,
ôTe,
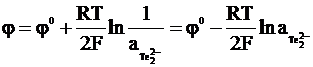 .
.
Электроды 2-го рода
Электроды 2-го рода содержат металл и труднорастворимое соединение этого металла, контактирующие с раствором, содержащим анионы, входящие в состав труднорастворимого соединения.
В зависимости от типа труднорастворимого соединения металла различают металлогалогенидные электроды, содержащие труднорастворимые галогениды металлов, металлосульфатные, содержащие труднорастворимые сульфаты металлов, и др.
Общая запись электродной реакции для электродов 2-го рода такова:
MxAz +xze = xM + zAx-. (а)
Приведенная выше запись результирующей электродной реакции соответствует двум ее основным стадиям:
· растворению труднорастворимой соли
MxAz = xMz+ + zAx-,
· восстановлению ионов металла на катоде
xMz+ + xze = M.
Таким образом, по механизму катодного процесса электроды 2-го рода принципиально не отличаются от электродов 1-го рода.
Отвечающая суммарной реакции (а) условная запись электрода 2-го рода имеет следующий вид:
Ax−ôMz+ , M .
Этой же реакции соответствует выражение для электродного потенциала:
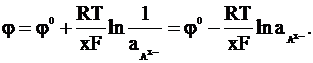 (2 - 2)
(2 - 2)
Потенциал электродов 2-го рода зависит от активности анионов. Поэтому их часто называют электродами, обратимыми по анионам.
Электроды 2-го рода широко применяются при проведении электрохимических измерений. Кроме того, данные по их стандартным электродным потенциалам используются для расчета произведения растворимости PS труднорастворимых солей. С этой целью сравнивают стандартный потенциал электрода 2-го рода 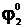 со стандартным потенциалом электрода 1-го рода с соответствующим металлом
со стандартным потенциалом электрода 1-го рода с соответствующим металлом 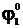 . Так как в системе, содержащей труднорастворимую соль MxAz, устанавливается равновесие
. Так как в системе, содержащей труднорастворимую соль MxAz, устанавливается равновесие
MxAz = xMz+ + zAx-,
характеризуемое константой равновесия
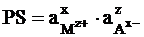 ,
,
то стандартным условиям для электрода 2-го рода ( 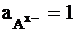 ) отвечает активность ионов металла, равная
) отвечает активность ионов металла, равная 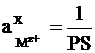 . Таким образом, выполняется условие:
. Таким образом, выполняется условие:
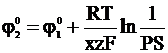 ,
,
из которого следует:
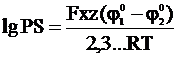 . (2 - 3)
. (2 - 3)
Изучение наиболее известных электродов 2-го рода начнем с класса металлогалогенидных, из которых наиболее распространена группа металлохлоридных электродов.
Каломельный электрод. Его название дано по труднорастворимому хлориду ртути (I) - каломели Hg2Cl2.
Каломельный электрод характеризуют:
· электродная реакция:
Hg2Cl2 + 2e = 2Hg + 2Cl-,
· условная запись:
Cl-ôHg2Cl2, Hg,
· выражение для электродного потенциала:
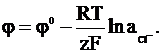
Для изготовления каломельного электрода каломель перетирают с раствором хлорида калия и несколькими каплями ртути до получения однородной пасты, которую наслаивают на поверхность ртути, помещаемой в стеклянную емкость. Сверху на пасту наслаивают раствор хлорида калия. Металлический контакт осуществляют платиновой проволокой, которую впаивают в стекло (платина и лабораторное стекло имеют близкие значения термического коэффициента расширения).
Каломельный электрод отличается прекрасной воспроизводимостью электродного потенциала и очень высокой устойчивостью. Известно, что при хранении свыше 25 лет каломельного электрода не было замечено никакого изменения его электродного потенциала. В связи с этим он широко применялся в качестве практического электрода сравнения. Было предложено использовать следующие типы каломельного электрода:
· децинормальный каломельный электрод, заполняемый 0,1 н. раствором KCl (электродный потенциал такого электрода по отношению к стандартному электроду сравнения при 25°С равен 0,3365 В),
· нормальный каломельный электрод, заполняемый 1 н. раствором KCl (его электродный потенциал по отношению к стандартному электроду сравнения при 25°С равен 0,2828 В),
· насыщенный каломельный электрод, заполняемый насыщенным раствором KCl (потенциал при 25°С равен 0,2438 В).
Наиболее употребительным является насыщенный каломельный электрод. Однако по сравнению с другими типами каломельных электродов у него наибольшая зависимость электродного потенциала от температуры.
Трудности миниатюризации каломельного электрода и работа с ртутью привели к тому, что он повсеместно заменялся серебряногалогенидными электродами.
Серебрянохлоридный электрод является наиболее распространенным представителем группы серебряногалогенидных электродов.
Приводим электродную реакцию, условную запись и выражение для электродного потенциала серебрянохлоридного электрода:
AgCl + e = Ag + Cl-,
Cl−ôAgCl, Ag,
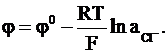
Серебрянохлоридный электрод подобно каломельному электроду имеет хорошую воспроизводимость и устойчивость электродного потенциала. Он широко применяется в качестве практического электрода сравнения (иногда такие электроды называют вспомогательными) не только в водных средах, но и в водных растворах спиртов, кетонов и эфиров.
Для получения серебрянохлоридного электрода тонкую серебряную проволоку покрывают слоем хлорида серебра. С этой целью ее погружают в водный раствор, содержащий хлорид-ионы, и пропускают электрический ток, используя серебряную проволоку в качестве анода. Погруженная в раствор KCl серебряная проволока с электролитическим покрытием AgCl представляет собой готовый электрод сравнения.
Миниатюрные серебрянохлоридные электроды используются в физиологических и биохимических исследованиях.
Ртутносульфатный электродявляется представителем группы металлосульфатных электродов с наиболее устойчивым электродным потенциалом и наиболее высокой воспроизводимостью.
Характеристики этого электрода приводятся ниже:
Hg2SO4 + 2e = 2Hg + SO42-,
SO42-ôHg2SO4, Hg,
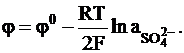
Металлооксидные электроды. В этих электродах анионом, содержащимся в водной среде, служит гидроксид-ион. Частную реакцию на этих электродах можно представить как двухстадийный процесс:
M2Oz + zH2O + 2ze = [2M(OH)z + 2ze]= 2M + 2zOH-.
Электродной реакции соответствует следующая форма условной записи электрода:
OH-ôM2Oz, M.
Выражение для электродного потенциала металлооксидного электрода имеет следующий вид:
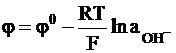 . (2 - 4)
. (2 - 4)
Оно может быть преобразовано с использованием ионного произведения воды
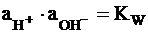
следующим образом:
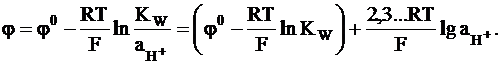
Обозначив
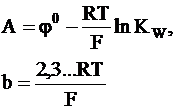

и принимая во внимание, что десятичный логарифм активности водородных ионов представляет собой водородный показатель среды pH, получим
j = A - b×pH.
Входящий в уравнение коэффициент b называется электрохимическим коэффициентом. При 25°С он равен 0,059157 В.
Линейная зависимость между водородным показателем среды и потенциалом металлооксидного электрода предполагает его применение для измерений рН. Такая возможность действительно существует. Однако в кислой среде происходит растворение оксидов и электрод перестает функционировать как рН-метрический.
Примерами металлооксидных электродов могут служить ртутнооксидный и сурьмянооксидный электроды.
Ртутнооксидный электрод характеризуется следующим:
HgO + H2O + 2e = Hg + 2OH-,
OH- ÷ HgO, Hg,
а сурьмянооксидный электрод может быть описан электродной реакцией и условной записью в таком виде:
Sb2O3 + 3H2O + 6e = 2Sb + 6OH-,
OH- ÷ Sb2O3, Sb.
Для изготовления сурьмянооксидного электрода достаточно заполнить стеклянную трубку расплавленной сурьмой и окислить выступающую поверхность сурьмы нагреванием на воздухе.
Электроды на основе металлических сплавов и растворов. Они представляют собой разновидность электродов 1-го и 2-го рода, в которых вместо чистого металла в кристаллической форме используются металлические сплавы или растворы. Многие металлы хорошо растворяются в ртути с образованием амальгамы. В качестве примера амальгамного электрода можно привести кадмиевый амальгамный электрод:
Cd2+ + 2e = Cd (Hg),
Cd2+÷ Cd (Hg),
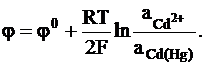
Обращаем внимание на то, что потенциал металла входит в выражение для электродного потенциала, так как в отличие от обычных электродов 1-го и 2-го рода металл не находится в стандартном состоянии.
Газовые электроды
Газовые электроды представляют собой разновидность окислительно-восстановительных электродов, на которых протекают реакции с участием газов. Наибольший интерес из этой группы представляют водородный и кислородный электроды.
Водородный электрод. Этот электрод содержит платинированную платину, погруженную в водный раствор и одновременно контактирующую с пузырьками водорода. Платинированная платина (используются другие названия: черненная платина, серая платина) покрыта электролитическим способом мельчайшими частицами платины, имеет высокую удельную поверхность и обладает каталитическими свойствами, что ускоряет наступление равновесия реакции с участием газообразного водорода.
На водородном электроде протекает реакция:
2H+ + 2e = H2.
Условно водородный электрод записывается следующим образом:
H+ôH2, Pt или H+ôH2 (Pt).
Замечательной особенностью водородного электрода является то, что по предложению В.Нернста стандартный водородный электрод был принят в качестве стандартного электрода сравнения. Следовательно, стандартный потенциал водородного электрода равен 0. Напомним, что стандартным условиям отвечают: активность ионоводорода равна 1 и давление водорода, рассматриваемого как идеальный газ, равно 1 атм или 1,01325×105 Па. Следовательно, если давление водорода выражать в атмосферах, то выражение для электродного потенциала принимает следующий вид:
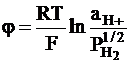 . (2 - 7)
. (2 - 7)
Если же давление выражается в Паскалях, то формула для расчета электродного потенциала может быть записана так:
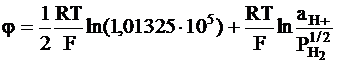 .
.
При постоянном давлении водорода потенциал водородного электрода зависит только от водородного показателя среды:
j = -b×pH.
В связи с этим водородный электрод является главным рН‑ метрическим электродом.
Кислородный электрод. Существуют два варианта рассмотрения кислородного электрода. Первому из них отвечают следующие характеристики:
1/2O2 + H2O + 2e = 2OH-,
OH-ôO2, Pt,
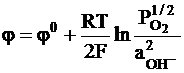 ,
,
j0 = + 0,401 В,
а второй характеризуется следующим:
1/2O2 + 2H+ + 2e = H2O,
H+ôO2, Pt,
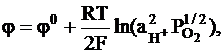
j0 = +1,228 B.
Кроме приведенных реакций на кислородном электроде могут протекать реакции с образованием пероксида водорода и пероксид-ионов. В связи с этим воспроизводимый кислородный электрод реализовать не удается.
Ионоселективные электроды
Электроды этого типа содержат мембрану, обладающую ионообменными свойствами. Твердая мембрана может быть изготовлена из однородного материала или из частиц ионообменного вещества в твердом связующем, чаще всего в пластической массе. На границе мембраны с раствором могут протекать процессы:
Mz+(раствор) = Mz+(мембрана)
или
Аz+(раствор) = Ax−(мембрана),
где Mz+(раствор) или Аz+(раствор) – катионы или анионы, содержащиеся в растворе, Mz+(мембрана) или Ax−(мембрана) - те же ионы, содержащиеся в мембранах.
Равновесному отношению активностей в растворе и мембране отвечает скачок потенциала. Так как скачок потенциала зависит от определенного сорта ионов, то поверхность мембран рассматривается подобно электроду, обладающему избирательными свойствами по отношению к ионам, и называется ионоселективным электродом.
В частности, потенциал поверхности, зависящий от активности катионов Mz+, можно выразить следующим образом:
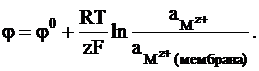 (2 - 8)
(2 - 8)
Самым распространенным ионоселективным электродом является стеклянный электрод, к изучению которого мы приступаем.
Стеклянный электрод представляет собой стеклянную мембрану, разделяющую два раствора, в одном из которых поддерживается постоянной концентрация водородных ионов, а в другом растворе необходимо определить водородный показатель. Потенциал на границе раствор – стеклянная поверхность, на которой протекает процесс:
H+ = H+(ст),
где H+ и H+(ст) означают ионы водорода в растворе и в стекле, может быть выражен формулой:
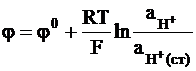 .
.
Способ нахождения отношения активностей ионов водорода в растворе и стекле был предложен Б. П. Никольским на основе представлений об ионном обмене.
Электродное стекло содержит ионы щелочного металла M+, которые могут замещаться ионами водорода. Ионному обмену
M+(ст) +H+ = M+ + H+(ст)
отвечает константа равновесия
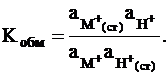
Предполагается, что замещаться могут ионы во всех доступных местах данной мембраны и число замещаемых мест всегда остается постоянным:
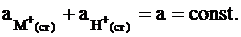
Из двух последних равенств следует
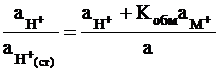
и
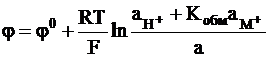 . (2 - 9)
. (2 - 9)
Если константа ионного обмена очень мала, что обеспечивается подбором состава стекла, то выполняется условие: 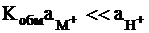 . Для такого образца стекла выражение для электродного потенциала приобретает вид:
. Для такого образца стекла выражение для электродного потенциала приобретает вид:
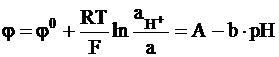 ,
,
где 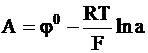 .
.
Для проведения рН-метрических измерений стеклянный электрод из натриевого стекла (содержит SiO2, Na2O и CaO) выдувают из трубки в виде шарика с очень тонкой стенкой (около 0,1 мм). Шарик и частично трубку заполняют внутренним раствором, который часто представляет собой 0,1 М раствор HCl. Во внутренний раствор погружают серебряную проволоку, покрытую AgCl, и трубку тщательно герметизируют, обеспечивая постоянство состава внутреннего раствора. Затем стеклянный электрод погружают в испытуемый раствор, который через солевой мостик контактирует с серебрянохлоридным электродом. Образуется цепь:
Ag, AgClô Cl−, H+ ô стекло ô H+x ôô Cl− ô AgCl, Ag
· внутренний испытуемый ·
(1) раствор раствор (2)
j1 j2 j3 j4
Скачки потенциала в цепи на границах внутреннего электрода сравнения и внутреннего раствора j1, внутреннего раствораôстекло j2, во внешнем электроде сравнения j4 остаются постоянными. Поэтому ЭДС, равная разности потенциалов между точками (2) и (1), должна определяться только активностью ионов водорода H+x испытуемого раствора.
Диапазон значений рН, измеряемых стеклянным электродом, очень велик (приблизительно от 0 до 13 единиц). На стеклянный электрод не действуют соли тяжелых металлов. Он очень удобен для измерений рН в непрозрачных и окрашенных средах.
Стеклянный электрод повсеместно используется в аналитической химии, в промышленности и в биологических исследованиях. Для медицинских целей выпускаются миниатюрные конструкции стеклянного электрода, который можно вводить в вену или артерию для прямых измерений водородного показателя крови.
Стеклянный электрод может быть использован для определения активности ионов щелочных металлов, Ag+, Tl+, NH4+ и некоторых органических катионов. Для этого в стекольную массу вводят оксиды алюминия, бора и др.
Катионная функция (для ионов металлов ее называют металлической функцией) стеклянного электрода объясняется увеличением константы Кобм. В этом случае может быть достигнуто соотношение 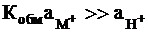 и выражение для электродного потенциала примет следующий вид:
и выражение для электродного потенциала примет следующий вид:
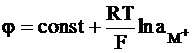 .
.
Избирательность ионоселективных электродов достигает больших величин. Например, содержащий Al2O3 стеклянный электрод позволяет определять активность ионов натрия при 1000-кратном избытке ионов калия.
Мембраны из полимеров и частиц труднорастворимых солей металлов используются для определения в растворах анионов, входящих в состав соли.
Монокристаллы LaF3 были использованы для изготовления лантанфторидных электродов, позволяющих определять содержание фторид-ионов в различных средах, включая слюну.
Диффузионный потенциал
Скачок потенциала, вызываемый различиями коэффициентов диффузии ионов и возникающий между двумя растворами, называется диффузионным потенциалом.
Для расчета диффузионного потенциала можно воспользоваться уравнением, получаемым интегрированием уравнения (5 ‑ 14). Действительно, из уравнения (5 - 14) следует для одномерного движения частиц (движения вдоль одного координатного направления):
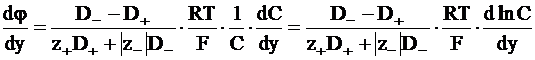 ;
;

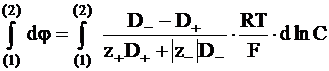 ;
; 
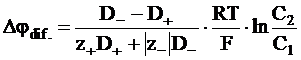 . (5 - 19)
. (5 - 19)
Кроме уравнения (5 - 19), для расчета диффузионного потенциала на границе двух растворов можно воспользоваться уравнением, в котором вместо коэффициента диффузии отдельных ионов используются их абсолютные подвижности. Такое уравнение можно получить, используя равенства типа (5 - 11):
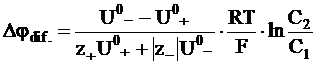 . (5 - 20)
. (5 - 20)
Для достаточно концентрированного бинарного электролита вместо концентрации используется активность электролита:
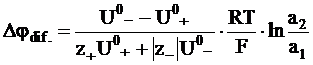 . (5 - 21)
. (5 - 21)
Уравнение (5 - 21) является частным случаем более общего уравнения, полученного М. Планком.
Планк разработал квазитермодинамическую теорию диффузионного потенциала.
Основная идея этой теории заключается в предположении, что пространственное разделение зарядов в результате неодинаковой диффузии ионов сопровождается электрической работой.
Если между граничащими растворами взять предельно узкую часть пространства, ограниченную двумя плоскостями, то ей должна соответствовать разность потенциалов, равная dj. Выбрав такую границу, чтобы через плоскости проходил заряд, равный постоянной Фарадея F, найдем, что электрическая работа равна
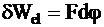 .
.
В предположении, что разделение зарядов в диффузионном процессе происходит квазистатически (это предположение не соответствует полностью термодинамическим представлениям о квазистатическом процессе и по этой причине теория называется квазитермодинамической), можно принять, что при постоянных Р и Т работа происходит за счет убыли энергии Гиббса:
dWel = −dG.
Если при переходе от одной плоскости к другой термодинамическая активность i-го вещества изменяется на dai, то перенос одного моля этого вещества приводит к изменению энергии Гиббса на величину, равную
dGi(1) = RTdlnai.
Перенос ni молей этого вещества приводит к изменению энергии Гиббса на следующую величину:
dGi = niRTdlnai.
Перенос всех веществ через эти плоскости приводит к полному изменению энергии Гиббса:
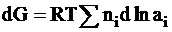 .
.
Таким образом, скачок потенциала между выбранными плоскостями окажется равным
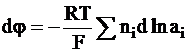 ,
,
а скачок потенциала между двумя растворами, то есть на протяжении всей границы, можно получить как результат интегрирования:
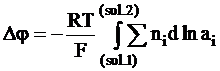 . (5 - 22)
. (5 - 22)
Заряд, переносимый данным сортом ионов i, при условии, что заряд одного иона в а.е.з. равен zi, а число моль ионов равно ni, будет выражен zini.
Введем новое понятие – число переноса, которое представляет собой переносимую данным сортом ионов долю общего заряда, проходящего по цепи.
В соответствии с этим определением число переноса ti может быть выражено равенством
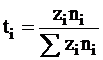 . (5 - 23)
. (5 - 23)
Так как было условлено, что суммарный заряд, переносимый по цепи, равен постоянной Фарадея, то в этом случае Szini = 1, ti =zini и ni =ti/zi. Следовательно, уравнению (5 - 22) можно придать следующий вид:
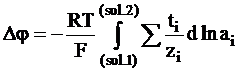 . (5 - 24)
. (5 - 24)
Для бинарного электролита число переноса равно отношению абсолютной подвижности данного сорта ионов к сумме абсолютных подвижностей обоих сортов ионов и мы вновь приходим к уравнению (5 - 21).
Экспериментальные данные показывают, что диффузионный потенциал может достигать нескольких десятков милливольт. Таким образом, при расчете стандартных электродных потенциалов может вкрасться серьезная ошибка.
Уравнение (5 - 21) позволяет понять, каким образом можно устранить влияние диффузионного потенциала.
Диффузионный потенциал окажется минимальным, если растворы соединяют солевым мостиком, содержащим концентрированный раствор электролита, образующего ионы с близкими абсолютными подвижностями.
Гравитационные цепи
Работу в такой цепи осуществляет металл, опускающийся под действием силы тяжести.
Первая гравитационная цепь была составлена в 1875 г. Р.А.Колли. Она содержит две стеклянные трубки с расположенными внизу пористыми керамическими мембранами. При заполнении трубок ртутью и погружении их в раствор, содержащий соли ртути, металлическая ртуть не вытекает через поры мембраны, но в то же время контактирует с раствором электролита. Если уровни ртути в трубках различны, то происходит переход ионов из металлической ртути в раствор из донной части трубки с более высоким уровнем и разряд ионов на поверхности ртути в трубке с низким уровнем. Ртуть в трубке с более высоким уровнем оказывается катодом, а с более низким уровнем - анодом.
Электродная реакция для ртутного электрода такова:
Hg22+ + 2e = 2Hg.
Следовательно, при образовании или растворении 2 моль по цепи протекают 2 фарадея электричества.
Работа, совершаемая ртутью при опускании ее от верхнего уровня h1 до нижнего h2, равна:
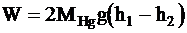 .
.
ЭДС такой цепи равна:
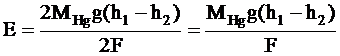 .
.
ЭДС гравитационной цепи очень мала (при разности уровней ртути в 1 м она составляет около 20 мкВ). В связи с этим силу тяжести можно заменить на центробежную силу. Такие цепи называются центробежными.
Аллотропические цепи
В цепях этого типа источником работы является переход из одной кристаллической формы металла в другую.
Аллотропическую цепь можно записать в следующей форме:
MaôMz+, Ax−ôMb,
где Ma и Mb - кристаллические формы металла.
По данным ЭДС аллотропической цепи можно экспериментально определить термодинамические характеристики перехода
Ma ® Mb.
Так как электрическая работа цепи равна убыли энергии Гиббса - DG, то
DG = −zFE.
К.В. Захарченко использовал аллотропическую цепь для определения термодинамической активности аморфного кобальта (аморфные металлы образуются при чрезвычайно быстром охлаждении расплавленного металла). Цепь, содержащая один электрод из аморфного кобальта, а другой из кристаллического металла, позволила по данным ЭДС найти термодинамическую активность аморфного кобальта, которая оказалась в зависимости от скорости охлаждения равной от 15 до 27. По температурной зависимости ЭДС, используя уравнение Гиббса - Гельмгольца, были вычислены изменения энтальпии и энтропии при переходе кобальта из кристаллического в аморфное состояние.
Концентрационные цепи
Существует несколько типов концентрационных цепей.
Например, используя в качестве электродов амальгаму кадмия разной концентрации, можно получить цепь
Cd(Hg)ôCdНаши рекомендации
