Работа № 4. ОПРЕДЕЛЕНИЕ КОЭФФИЦИЕНТА РАСПРЕДЕЛЕНИЯ ВЕЩЕСТВА В ДВУХ НЕСМЕШИВАЮЩИХСЯ ЖИДКОСТЯХ
Целью работы является изучение коэффициента распределения ионов меди между водой и органической жидкостью при комнатной температуре.
При подготовке к работе следует ознакомиться со следующими разделами теоретического курса: правило фаз Гиббса, закон распределения, активности компонентов разбавленных, идеальных и реальных растворов.
Теоретические сведения
Рассмотрим систему из двух чистых жидкостей, нерастворимых друг в друге, при этом жидкости образуют два слоя. Если в такую систему добавить третье вещество, растворимое в обеих жидкостях (третий компонент), то после достижения равновесия этот третий компонент распределится между обоими слоями, образуя два раствора различной концентрации.
Согласно правилу фаз Гиббса число степеней свободы трехкомпонентной ( 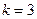 ) двухфазной (
) двухфазной ( 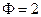 ) системы равно трем:
) системы равно трем:
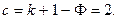 | (40) |
Таким образом, из трех параметров, характеризующих равновесие системы (температура 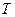 и концентрации растворенного вещества в двух фазах
и концентрации растворенного вещества в двух фазах 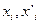 ), произвольно можно изменять лишь два. Третий параметр является функцией двух независимых переменных. При постоянной
), произвольно можно изменять лишь два. Третий параметр является функцией двух независимых переменных. При постоянной 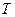 концентрация растворенного вещества «i» в одной из фаз является функцией его концентрации в другой фазе, т.е.
концентрация растворенного вещества «i» в одной из фаз является функцией его концентрации в другой фазе, т.е. 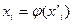 . Другими словами, при равновесии двух фаз концентрации растворенного вещества «i» в них взаимно связаны. Эта связь выражается законом распределения вещества между двумя несмешивающимися жидкостями, согласно которому константа распределения, равная отношению активностей растворенного вещества в разновесных фазах является однозначной функцией температуры.
. Другими словами, при равновесии двух фаз концентрации растворенного вещества «i» в них взаимно связаны. Эта связь выражается законом распределения вещества между двумя несмешивающимися жидкостями, согласно которому константа распределения, равная отношению активностей растворенного вещества в разновесных фазах является однозначной функцией температуры.
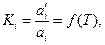 | (41) |
Вывод уравнения (41) основан на условии равновесия системы: химические потенциалы растворенного вещества одинаковы в обеих фазах, т.е. 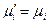 .
.
Используя известное соотношение
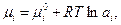 | (42) |
в котором 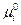 относится к стандартному состоянию, и приравнивая потенциалы
относится к стандартному состоянию, и приравнивая потенциалы 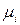 и
и 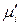 вещества «i», приходим к равенству:
вещества «i», приходим к равенству:
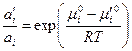 . . | (43) |
Поскольку стандартные потенциалы компонента «i» в каждой из фаз 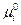 и
и 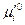 зависят лишь от температуры, отношение активностей компонента, называемое константой распределения, является также функцией только температуры и не зависит от состава растворов.
зависят лишь от температуры, отношение активностей компонента, называемое константой распределения, является также функцией только температуры и не зависит от состава растворов.
В реальных растворах активность компонента
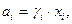 | (44) |
поэтому вместо константы распределения удобнее использовать коэффициент распределения 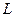 , равный отношению концентраций растворенного вещества в равновесных фазах
, равный отношению концентраций растворенного вещества в равновесных фазах
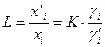 . . | (45) |
Коэффициент распределения является функцией состава, поскольку коэффициенты активности 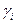 и
и 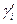 зависят от концентрации раствора.
зависят от концентрации раствора.
В бесконечно разбавленных растворах коэффициент активности растворенного вещества постоянен, поэтому здесь не только константа, но и коэффициент распределения не зависят от состава равновесных фаз.
В бесконечно разбавленном растворе все величины, характеризующие состав, пропорциональны друг другу ( 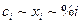 ). Поэтому здесь коэффициент распределения может быть выражен через отношение равновесных концентраций в любых единицах, например,
). Поэтому здесь коэффициент распределения может быть выражен через отношение равновесных концентраций в любых единицах, например,
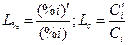 . . | (46) |
Значения 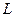 при этом получаются различными, но во всех случаях они не зависят от состава.
при этом получаются различными, но во всех случаях они не зависят от состава.
Измерение коэффициента распределения позволяет определять активности растворенного вещества. Для этого бинарный раствор с известной зависимостью активности компонентов от состава приводят в контакт с несмешивающейся жидкостью, содержащей общий с первой фазой компонент, активность которого неизвестна. После установления равновесия измеряют концентрации 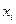 и
и 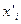 растворенного вещества в каждой из фаз для растворов различного состава. Находят соответствующие значения отношений
растворенного вещества в каждой из фаз для растворов различного состава. Находят соответствующие значения отношений 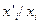 и строят график зависимости этого отношения от концентрации третьего компонента в растворах с известными активностями. Экстраполируя полученную линию до нулевой концентрации (
и строят график зависимости этого отношения от концентрации третьего компонента в растворах с известными активностями. Экстраполируя полученную линию до нулевой концентрации ( 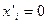 ), на оси ординат получают значение константы распределения для бесконечно-разбавленного раствора. Для таких растворов, как уже отмечалось, отношение концентраций растворенного вещества не зависит от состава растворов. Зная это отношение и величины активностей растворенного вещества в одном из растворителей, рассчитывают активности третьего компонента в другом растворителе при всех исследованных концентрациях.
), на оси ординат получают значение константы распределения для бесконечно-разбавленного раствора. Для таких растворов, как уже отмечалось, отношение концентраций растворенного вещества не зависит от состава растворов. Зная это отношение и величины активностей растворенного вещества в одном из растворителей, рассчитывают активности третьего компонента в другом растворителе при всех исследованных концентрациях.
Закон распределения имеет и другое важное практическое значение. Из предыдущих уравнений следует, что для понижения концентрации растворенного вещества в одной фазе при постоянных температуре и давлении необходимо понизить его концентрацию в другой. Последнее может быть достигнуто разбавлением одной из фаз. В частности, при производстве стали для очистки металла от вредных примесей (фосфора, серы и др.) либо увеличивают количество шлака, либо удаляют шлак, содержащий вредную примесь, и наводят новый. Так как при постоянной температуре константа распределения примеси остается величиной постоянной, то часть примеси переходит из металла в новый шлак и концентрация ее в металле уменьшается. Такое извлечение растворенного вещества из раствора называется экстракцией.
Очевидно, экстракция будет тем эффективнее, чем больше коэффициент распределения отличается от единицы. Коэффициент распределения можно менять, добавляя в растворы вещества, меняющие коэффициенты активности данного компонента «i». Так, введение вещества, имеющего большее сродство к данному компоненту, чем растворитель, снижает коэффициент активности этого компонента и, следовательно, изменяет величину коэффициента 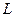 .
.
Порядок выполнения работы
Работа выполняется на виртуальной модели, которые часто применяются в случае, если изучение объекта экономически не обосновано, осложнено экспериментально или не безопасно. Виртуальная модель включает в себя смысловую модель, на основе которой разрабатывается математическая модель. По уравнениям мат. модели с помощью компьютера осуществляется графическое представление процесса.
Выполняемая виртуальная работа основана на реальном процессе выделения ионов меди из водного раствора при соприкосновении данного раствора с органической фазой представляющей собой раствор Д2ЭГФК ( Ди 2-этил-гексил фосфорная кислота) 30 мас.% в керосине. При протекании такого процесса основное количество Cu2+ переходит в органическую фазу, а концентрация Cu2+ в водном растворе существенно снижается.
Для выполнения работы следует подать в емкость 1 (Рис.8) по трубке 3 с помощью нажатия соответствующей кнопки-клапана необходимое кол-во водного раствора Vр (от 100 до 190 мл, синего цвета), добавить клапаном 4 жидкой органической фазы. После чего включить магнитную мешалку и перемешать растворы в течение 30 сек.
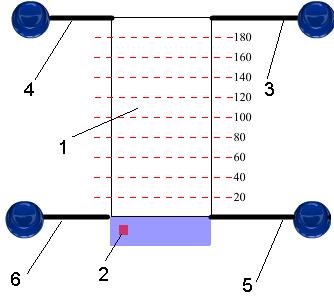
Рис. 8. Схема установки для разделения ионов меди между двумя несмешивающимися жидкостями: 1 – емкость для разделения (экстрактор), 2 – кнопка включения магнитной мешалки, трубки для подачи/слива: 3 – водного раствора содержащего ионы меди, 4 – органической фазы, 5 – на отбор проб для титрования, 6 – растворов в отстойник
Затем полученной эмульсии дают отстояться, и когда установятся два слоя, нижний (воду) в количестве 20 мл сливают нажатием на клапан трубки 5 в колбу для титрования 7 (Рис.9).
С помощью клапана 8 в бюретку 9 заливают титрующий раствор (водный раствор тиосульфата натрия) до выбранного уровня. К исследуемому раствору в колбе 7 добавляют 2 г KJ и 2 мл крахмала с помощью кнопки 10. При добавлении избытка KJ в исследуемый раствор вся медь содержащаяся в нем превращается в иодид и осаждается на дно сосуда.
| 2Cu 2+ +4I- = 2 CuI + I2 | (47) |
В ходе этой реакции происходит выделение молекулярного йода J2 , который в присутствии крахмала придает раствору ярко синюю окраску.
Далее с помощью крана 11 начинают титрование, приливая титрующий раствор из бюретки в колбу 7. При этом осуществляется реакция:
| I2 + 2 Na2S2O3 = 2 NaI + Na2S4O6. | (48) |
Тиосульфат натрия взаимодействует с йодом, уменьшая его количество. В момент времени, когда весь молекулярный йод прореагирует по реакции (48), окраска раствора резко изменит свой цвет с синего на бесцветный. Как только раствор обесцветился титрование прекращают и фиксируют потраченное количество титрующего раствора Vт. Зная концентрацию тиосульфата натрия (Na2S2O3) в титрующем растворе, равную 0,1 моль/л, рассчитывают по реакциям (1 и 2) концентрацию меди в исследуемом растворе Ср1. В соответствии с реакцией (47) 2 моля прореагировавших ионов меди приходится 1 моль выделившегося иода. И по реакции (48) для нейтрализации 1 моля иода необходимо 2 моля тиосульфата натрия.
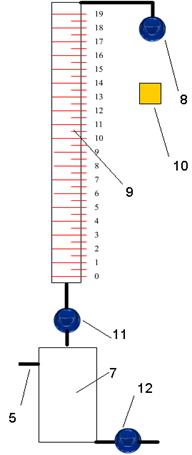
Рис. 9. Схема установки для титрования
7 – колба, 9 – бюретка, 10 – добавление KJ,
8,11, 12 – клапаны
То есть 1 моль прореагировавших Cu2+ приведет к затратам при титровании 1 моль Na2S2O3:
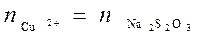 . . | (49) |
Следовательно концентрацию Ср1 можно определить по формуле:
| Ср1= 0,1*Vт/20. | (50) |
При выполнении работы на экране в правом нижнем углу отображается начальная концентрация ионов меди в растворе подаваемом в экстрактор C0 от 0,01 до 0,05 моль/л. До процесса экстракции водный раствор содержал количество меди равное 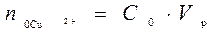 . После того как произошло перераспределение, в растворе остались ионы меди в количестве
. После того как произошло перераспределение, в растворе остались ионы меди в количестве 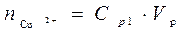 . Следовательно в органическую фазу перешло количество меди равное
. Следовательно в органическую фазу перешло количество меди равное 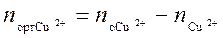 . Зная перераспределившееся количество меди, определяют равновесную концентрацию меди в органической фазе Ср2.
. Зная перераспределившееся количество меди, определяют равновесную концентрацию меди в органической фазе Ср2.
В емкости, где происходит разделение, остался раствор в количестве достаточном для повторного осуществления операции титрования. Поэтому клапаном 12 сливают из колбы 7 раствор после титрования и проводят химический анализ повторно. Определение концентрации меди в исследуемом растворе осуществляют 3 раза. По результатам трех измерений определяют средние значения концентраций.
Используя уравнение (46) находят коэффициент распределения ионов меди между водой и органической фазой для одной равновесной концентрации ионов меди в воде. Изменяя соотношения объемов органической фазы и водной (водный раствор добавляется в количестве 190, 180, 170, 160, 150 мл; органический до метки в 200 мл), изменяют равновесную концентрацию ионов меди. Определяют зависимость коэффициента распределения L от концентрации. Результаты измерения и расчетов помещают в таблицу 5.
Таблица 5
Результаты работы
| № опыта | Количество раствора тиосульфата, V, мл | Концентрация, моль/л | Коэффициент распределения L | |||||
| № пробы | Vср, мл | С0 | Ср1 | Ср2 | ||||
Вопросы для самоконтроля
1. Что называют константой распределения; от каких факторов зависит константа распределения?
2. Что называют коэффициентом распределения; в каком случае коэффициент распределения не зависит от состава раствора?
3. Чему равно число степеней свободы системы, состоящей из двух несмешивающихся индивидуальных жидкостей и распределенного между ними третьего вещества?
4. В каком случае по результатам опытов можно говорить о независимости коэффициента распределения от состава раствора?
5. В условиях задачи требуется очистить изоамиловый спирт от уксусной кислоты при помощи 1 литра воды. Коэффициент распределения равен 1. Как выгоднее ее использовать для этой цели: залить ли ее всю в делительную воронку сразу или отдельными порциями?
6. Изменится ли коэффициент распределения, если между двумя несмешивающимися фазами поместить третью фазу?
7. В чем состоит практическое значение определения коэффициента распределения вещества в двух несмешивающихся жидкостях?
