Элементы квантовой физики атомов
МОЛЕКУЛ И ТВЕРДЫХ ТЕЛ
Теория атома водорода по Бору
Основные формулы и законы
· Первый постулат Бора (постулат стационарных состояний)
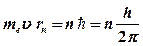 (
( 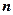 = 1, 2, 3,…),
= 1, 2, 3,…),
где 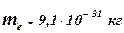 – масса электрона;
– масса электрона; 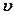 – скорость электрона на
– скорость электрона на 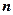 -й орбите, радиус которой равен
-й орбите, радиус которой равен 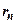 ;
;
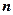 – номер стационарного состояния;
– номер стационарного состояния; 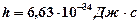 – постоянная Планка.
– постоянная Планка.
· Второй постулат Бора (правило частот)
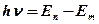 ,
, 
где 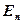 ,
, 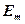 – энергии стационарных состояний атома соответственно до и после излучения (поглощения);
– энергии стационарных состояний атома соответственно до и после излучения (поглощения); 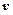 – частота излученного (поглощенного) кванта энергии.
– частота излученного (поглощенного) кванта энергии.
· Обобщенная формула Бальмера, описывающая серии линий в спектре атома водорода:
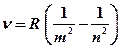 ,
,
где 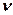 – частота спектральных линий в спектре атома водорода;
– частота спектральных линий в спектре атома водорода;
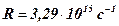 - постоянная Ридберга;
- постоянная Ридберга; 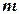 – целое число, определяет серию линий в спектре атома водорода:
– целое число, определяет серию линий в спектре атома водорода: 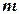 = 1 – серия Лаймана (расположена в ультрафиолетовой части спектра);
= 1 – серия Лаймана (расположена в ультрафиолетовой части спектра); 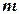 = 2 – серия Бальмера (расположена в видимой части спектра);
= 2 – серия Бальмера (расположена в видимой части спектра);
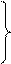
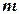 = 3 – серия Пашена;
= 3 – серия Пашена;
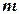 = 4 – серия Брэкета;
= 4 – серия Брэкета;
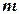 = 5 – серия Пфунда; расположены в инфракрасной
= 5 – серия Пфунда; расположены в инфракрасной
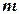 = 6 – серия Хэмфри. части спектра
= 6 – серия Хэмфри. части спектра
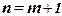 – определяет отдельные линии соответствующей серии
– определяет отдельные линии соответствующей серии 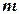 .
.
· Радиус 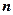 -й орбиты электрона в атоме водорода
-й орбиты электрона в атоме водорода
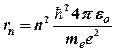 ,
,
где 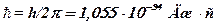 – постоянная Планка;
– постоянная Планка;
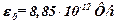 – электрическая постоянная;
– электрическая постоянная; 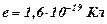 – заряд электрона;
– заряд электрона; 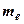 – масса электрона.
– масса электрона.
· Энергия 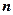 -го стационарного состояния атома водорода:
-го стационарного состояния атома водорода:
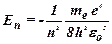 ,
,
где 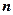 – номер стационарной орбиты.
– номер стационарной орбиты.
· Энергия электрона в атоме водорода
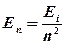 ,
,
где 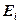 – энергия ионизации атома водорода.
– энергия ионизации атома водорода.
· Потенциал ионизации
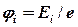 .
.
· Потенциал возбуждения
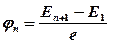 .
.
Задания
4.1.Определить радиусы первых трех стационарных орбит в атоме водорода. [0,53∙10-10 м; 2,12∙10-10 м; 4,77∙10-10 м].
4.2.Определить скорости электрона на первых трех стационарных орбитах в атоме водорода. [2,19∙106 м/c; 1,1∙106 м/c; 0,73∙106 м/c].
4.3.Определить период обращения электрона на первой стационарной орбите в атоме водорода. [1,43∙10-16 c].
4.4.Определить угловую скорость электрона на первой стационарной орбите в атоме водорода. [4,4∙1016 рад/c].
4.5.Определить кинетическую, потенциальную и полную энергии электрона на первой стационарной орбите в атоме водорода. [21,76∙10-19 Дж; – 43,52∙10-19 Дж; – 21,76∙10-19 Дж].
4.6.Определить наибольшую и наименьшую длину волны в серии Лаймана. [121,6 нм; 91,2 нм].
4.7.Определить наибольшую и наименьшую частоту волны в серии Бальмера. [0,82∙1015 Гц; 0,45∙1015 Гц].
4.8.Определить потенциал ионизации и первый потенциал возбуждения атома водорода. [13,6 В; 10,2 В] .
4.9.Максимальная длина волны спектральной линии в серии Лаймана равна 0,122 мкм. Полагая, что постоянная Ридберга неизвестна, определить максимальную длину волны в серии Бальмера. [0,656 мкм].
4.10.1). Какую наименьшую энергию (в электронвольтах) должны иметь электроны, чтобы при возбуждении атомов водорода ударами этих электронов появились все линии всех серий спектра водорода? 2). Какую наименьшую скорость должны иметь эти электроны? [13,6 эВ; 2,2 ∙106 м/с].
4.11.Используятеорию Бора, определить орбитальный магнитный момент электрона, движущегося по первой орбите атома водорода. [0,93∙10-23 А∙м2].
4.12.Предполагая, что в опыте Франка и Герца вакуумная трубка наполнена не парами ртути, а разреженным атомарным водородом, определить, через какие интервалы ускоряющего потенциала возникнут максимумы на графике зависимости силы анодного тока от ускоряющего потенциала. [10,2 В].
4.13.Атомарный водород освещается ультрафиолетовым излучением с длиной волны 100 нм. Определить, какие спектральные линии появятся в спектре излучения атомарного водорода. [λ1,2 = 121,6 нм; λ 1,3 = 102,6 нм; λ 2,3 = 656,3 нм].
4.14.В спектре излучения атомарного водорода интервал между двумя линиями, принадлежащими серии Бальмера, составляет 1,71∙10-7 м. Определить с помощью этой величины постоянную Ридберга.
4.15.Основываясь на том, что энергия ионизации атома водорода равна 13,6 эВ, определить в электронвольтах энергию фотона, соответствующую самой длинноволновой линии серии Пашена. [0,48 эВ].
Элементы квантовой механики
Основные формулы и законы
· Длина волны де Бройля
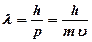 ,
,
где 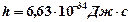 – постоянная Планка;
– постоянная Планка; 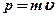 – импульс частицы (
– импульс частицы ( 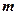 – масса частицы;
– масса частицы; 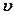 – её скорость).
– её скорость).
· Связь импульса частицы 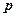 с ее кинетической энергией
с ее кинетической энергией 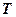 :
:
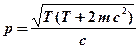 ,
,
где 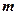 – масса покоя частицы. При малых скоростях
– масса покоя частицы. При малых скоростях 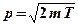 .
.
· Соотношение неопределенностей Гейзенберга
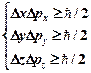
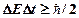 ,
,
где 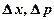 ,
, 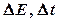 – соответственно неопределенности координаты, импульса, энергии и времени,
– соответственно неопределенности координаты, импульса, энергии и времени, 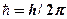 .
.
· Нестационарное уравнение Шредингера
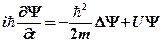 .
.
· Уравнение Шредингера для стационарных состояний
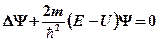 ,
,
где 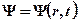 – волновая функция микрочастицы;
– волновая функция микрочастицы; 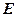 – полная энергия микрочастицы;
– полная энергия микрочастицы; 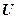 =
= 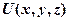 – потенциальная энергия частицы;
– потенциальная энергия частицы; 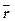 – пространственная координата (
– пространственная координата ( 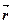 =
= 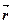
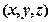 ); t – время, ∆ =
); t – время, ∆ = 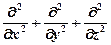 – оператор Лапласа (записан в декартовых координатах);
– оператор Лапласа (записан в декартовых координатах); 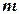 – масса микрочастицы;
– масса микрочастицы; 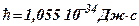 – постоянная Планка;
– постоянная Планка; 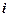 =
= 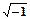 – мнимая единица.
– мнимая единица.
· Одномерное уравнение Шредингера для стационарных состояний
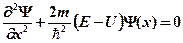 .
.
· Условие нормировки волновой функции
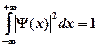
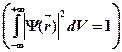 .
.
· Плотность вероятности
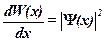
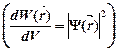 ,
,
где 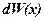 – вероятность того, что частица может быть обнаружена вблизи точки с координатой
– вероятность того, что частица может быть обнаружена вблизи точки с координатой 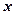 на участке
на участке 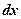 .
.
· Вероятность обнаружения частицы в интервале от 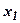 до
до 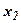
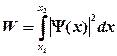 .
.
· Решение уравнения Шредингера для одномерного, бесконечно глубокого, прямоугольного потенциального ящика шириной 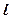 (0 ≥
(0 ≥ 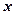 ≥
≥ 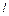 )
)
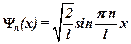 (собственная нормированная волновая функция)
(собственная нормированная волновая функция)
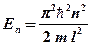 (собственное значение энергии),
(собственное значение энергии),
где 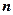 – главное квантовое число (
– главное квантовое число ( 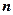 = 1, 2, 3,…). В области 0≥
= 1, 2, 3,…). В области 0≥ 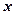 ≥
≥ 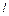
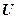 = ∞ и
= ∞ и 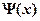 = 0.
= 0.
· Коэффициент прозрачности прямоугольного потенциаль-ного барьера
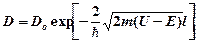 ,
,
где 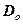 – постоянный множитель (можно приравнять единице);
– постоянный множитель (можно приравнять единице); 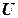 – высота барьера;
– высота барьера; 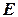 – полная энергия частицы;
– полная энергия частицы; 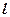 – ширина барьера.
– ширина барьера.
· Энергия квантового осциллятора
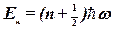 ,
,
где 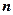 – главное квантовое число (
– главное квантовое число ( 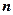 =0, 1, 2,…);
=0, 1, 2,…); 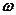 – собственная частота колебаний осциллятора.
– собственная частота колебаний осциллятора.
· Для частиц с целочисленными спинами (бозонов) справедлива статистика Бозе-Эйнштейна, а для частиц с полуцелыми спинами (фермионов) справедлива статистика Ферми-Дирака. Обобщенное уравнение для квантовых статистик
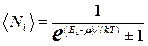 ,
,
где 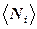 - среднее число частиц в состоянии с номером i,
- среднее число частиц в состоянии с номером i,
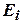 – энергия частицы в этом состоянии; m – так называемый химический потенциал, определяемый из условия
– энергия частицы в этом состоянии; m – так называемый химический потенциал, определяемый из условия 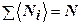 , т. е. сумма всех частиц равна полному числу
, т. е. сумма всех частиц равна полному числу 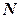 частиц в системе, знак минус (-) перед единицей в знаменателе соответствует статистике бозонов (распределению Бозе-Эйнштейна, а знак плюс (+) соответствует статистике фермионов (распределению Ферми-Дирака).
частиц в системе, знак минус (-) перед единицей в знаменателе соответствует статистике бозонов (распределению Бозе-Эйнштейна, а знак плюс (+) соответствует статистике фермионов (распределению Ферми-Дирака).
Задания
