Дросселирование газов и паров
Если на пути движения потока газа или пара имеется местное сопротивление, т. е. резкое сужение проходного сечения (например, диафрагма с небольшим отверстием в центре), то в месте сужения скорость резко возрастает, а давление понижается. При последующем понижении скорости из-за завихрений давление восстанавливается не полностью, как показано на графике. Перепад давления 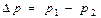 тем больше, чем меньше отношение fo / f1.
тем больше, чем меньше отношение fo / f1.
 Понижение давления газа или пара при прохождении его через какое-либо местное сопротивление называется дросселированием.
Понижение давления газа или пара при прохождении его через какое-либо местное сопротивление называется дросселированием. 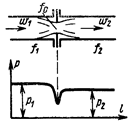 Процесс дросселирования идет без теплообмена с окружающей средой и не сопровождается производством технической работы, поэтому аналитическое выражение первого закона термодинамики для горизонтального потока принимает вид:
Процесс дросселирования идет без теплообмена с окружающей средой и не сопровождается производством технической работы, поэтому аналитическое выражение первого закона термодинамики для горизонтального потока принимает вид:
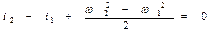 или
или 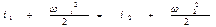
Изменение скорости при дросселировании может быть весьма значительным, но даже при очень больших скоростях кинетическая энергия потока столь несущественна по сравнению с его энтальпией, что вторыми слагаемыми можно пренебречь. Тогда получаем
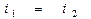
т.е. при дросселировании газа или пара его энтальпия практически не изменяется.
 При дросселировании идеального газа, для которого
При дросселировании идеального газа, для которого 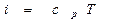 причем сp = const, получаем
причем сp = const, получаем
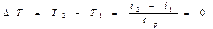 ,
,
т.е. температура идеального газа при дросселировании не изменяется.
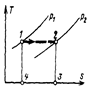
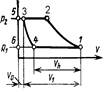
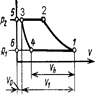
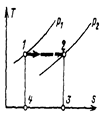 Если в Ts–диаграмме точка 1 соответствует состоянию идеального газа до дросселирования, то точка 2, соответствующая состоянию его после дросселирования, лежит с ней на одной горизонтали и располагается правее (поскольку изобара р2 находится правее изобары p1).
Если в Ts–диаграмме точка 1 соответствует состоянию идеального газа до дросселирования, то точка 2, соответствующая состоянию его после дросселирования, лежит с ней на одной горизонтали и располагается правее (поскольку изобара р2 находится правее изобары p1).
График показывает, что дросселирование идеального газа сопровождается ростом его энтропии, несмотря на то, что процесс идет без теплообмена с окружающий средой. Это очевидно, поскольку этот процесс является необратимым.
 Энтропия является функцией состояния и, следовательно, ее изменение не зависит от пути, по которому газ переходит из состояния 1 в состояние 2. Это означает, что оно будет таким же, как при обратимом изотермическом процессе 1-2, т. е. может быть определено по формуле:
Энтропия является функцией состояния и, следовательно, ее изменение не зависит от пути, по которому газ переходит из состояния 1 в состояние 2. Это означает, что оно будет таким же, как при обратимом изотермическом процессе 1-2, т. е. может быть определено по формуле:
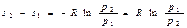
 Горизонтальную прямую 1-2 можно рассматривать как линию процесса дросселирования лишь условно, поскольку в принципе графическому изображению поддаются лишь обратимые процессы и фактически линия 1-2 изображает не дросселирование, а обратимое изотермическое расширение газа.
Горизонтальную прямую 1-2 можно рассматривать как линию процесса дросселирования лишь условно, поскольку в принципе графическому изображению поддаются лишь обратимые процессы и фактически линия 1-2 изображает не дросселирование, а обратимое изотермическое расширение газа.
Равным образом нельзя рассматривать реальный процесс дросселирования и как изоэнтальпийный, т. е. протекающий при i=const.
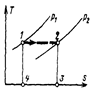 Легко видеть, что эти два процесса, изображающиеся одной и той же линией, но в принципе совершенно различны:
Легко видеть, что эти два процесса, изображающиеся одной и той же линией, но в принципе совершенно различны:
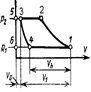
в изотермическом процессе площадь 1-2-3-4-1, лежащая под линией процесса, представляет собой внешнюю теплоту, за счет которой и совершается работа расширения газа;
в процессе дросселирования эта площадь представляет собой внутреннюю теплоту, получаемую газом за счет превращения в тепловую энергию работы расширения, полностью затрачиваемой на вихреобразование.
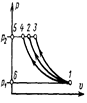
Процесс дросселирования водяного пара.
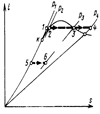
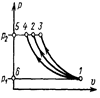
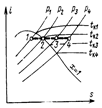 Из графика видно, что влажный пар в области умеренных давлений (точка 1) при дросселировании подсушивается, сухой насыщенный пар (точка 2) перегревается, а перегретый (точка 3) увеличивает свой перегрев.
Из графика видно, что влажный пар в области умеренных давлений (точка 1) при дросселировании подсушивается, сухой насыщенный пар (точка 2) перегревается, а перегретый (точка 3) увеличивает свой перегрев.
Температурный эффект дросселирования перегретого пара на Δр бар даёт понижение температуры 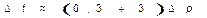 ,0С.
,0С.
 В области высоких давлений, близких к критическому, перегретый пар (точка 1) сначала переходит в сухой насыщенный (точка 2), затем увлажняется, затем снова подсушивается, становясь сухим насыщенным (точка 3), и, наконец, вновь становится перегретым (точка 4).
В области высоких давлений, близких к критическому, перегретый пар (точка 1) сначала переходит в сухой насыщенный (точка 2), затем увлажняется, затем снова подсушивается, становясь сухим насыщенным (точка 3), и, наконец, вновь становится перегретым (точка 4).
Кипящая вода (точка 5) при дросселировании частично испаряется и переходит в смесь воды с насыщенным паром (точка 6).
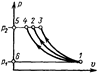
 С помощью is–диаграммы можно показать, что дросселирование сопряжено с потерей располагаемой работы.
С помощью is–диаграммы можно показать, что дросселирование сопряжено с потерей располагаемой работы.
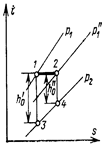
Если до дросселирования пар имел давление 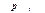 (точка 1), то располагаемое теплопадение было равно h'o, после дросселирования, когда его давление снизилось до
(точка 1), то располагаемое теплопадение было равно h'o, после дросселирования, когда его давление снизилось до 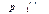 (точка 2), располагаемое теплопадение стало равным h"o.
(точка 2), располагаемое теплопадение стало равным h"o.
А т.к. точка 4 располагается выше точки 3, очевидно, что 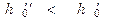 .
.
