Зависимость функции распределения Максвелла от массы молекул и температуры газа
На рисунке 2.8 показана зависимость f(υ) при различных температурах и массах молекул газа.
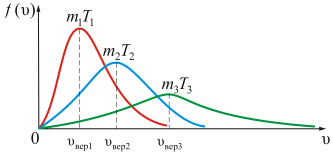
Рис. 2.8
Из рисунка 2.8 можно проследить за изменением f(υ) при изменении m и T. В данном случае 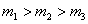 (при T = const ) или
(при T = const ) или 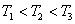 (при m = const). Площадь под кривой величина постоянная, равная единице (
(при m = const). Площадь под кривой величина постоянная, равная единице ( 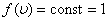 ), поэтому важно знать как будет изменяться положение максимума кривой:
), поэтому важно знать как будет изменяться положение максимума кривой:
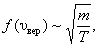 | кроме того | 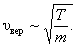 |
Максвелловский закон распределения по скоростям и все вытекающие следствия справедливы только для газа в равновесной системе. Закон статистический, и выполняется тем лучше, чем больше число молекул.
Вопрос №59
Обозначим 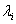 – длина свободного пробега молекулы.
– длина свободного пробега молекулы.
Медленность явлений переноса, например диффузии ароматических веществ – «распространение запаха», - при относительно высокой скорости теплового движения молекул (103 м/с) объясняется столкновениями молекул. Молекула газа время от времени сталкивается с другими молекулами. В момент столкновения молекула резко изменяет величину и направление скорости своего движения. Расстояние, проходимое молекулой в среднем без столкновений, называется средней длиной свободного пробега. Средняя длина свободного пробега равна:
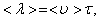 |
где 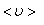 – средняя скорость теплового движения, τ – среднее время между двумя столкновениями. Именно
– средняя скорость теплового движения, τ – среднее время между двумя столкновениями. Именно 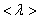 - средняя длина свободного пробега нас интересует (рис. 3.1).
- средняя длина свободного пробега нас интересует (рис. 3.1).
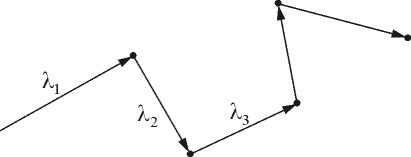
Рис. 3.1
Модель идеального газа – твёрдые шарики одного диаметра, взаимодействующие между собой только при столкновении. Обозначим σ – эффективное сечение молекулы, т.е. полное поперечное сечение рассеяния, характеризующее столкновение между двумя молекулами (рис. 3.2).
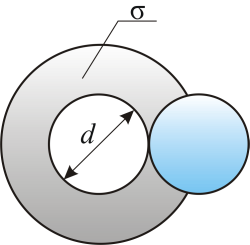
Рис. 3.2
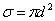 – площадь, в которую не может проникнуть центр любой другой молекулы. Здесь
– площадь, в которую не может проникнуть центр любой другой молекулы. Здесь 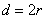 – диаметр молекулы.
– диаметр молекулы.
За одну секунду молекула проходит путь, равный средней арифметической скорости 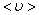 . За ту же секунду молекула претерпевает ν столкновений. Следовательно,
. За ту же секунду молекула претерпевает ν столкновений. Следовательно,
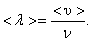 | 3.2.1 |
Подсчитаем число столкновений ν.
Вероятность столкновения трех и более молекул бесконечно мала.
Предположим, что все молекулы застыли, кроме одной. Её траектория будет представлять собой ломаную линию. Столкновения будут только с теми молекулами, центры которых лежат внутри цилиндра радиусом d (рис. 3.3).
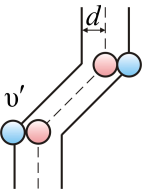
Рис. 3.2
Путь, который пройдет молекула за одну секунду, равен длине цилиндра 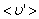 . Умножим объём цилиндра
. Умножим объём цилиндра 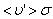 на число молекул в единице объёма n, получим среднее число столкновений в одну секунду:
на число молекул в единице объёма n, получим среднее число столкновений в одну секунду:
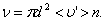 | 3.2.1 |
На самом деле, все молекулы движутся (и в сторону, и навстречу друг другу), поэтому число соударений определяется средней скоростью движения молекул относительно друг друга.
По закону сложения случайных величин
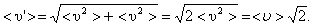 | (3.2.1) |
А так как средняя длина свободного пробега 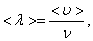 то получим:
то получим:
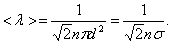 | (3.2.2) |
Уравнение состояния идеального газа позволяет нам выразить n через давление P и термодинамическую температуру Т.
Так как 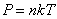 , то есть
, то есть 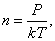 то
то
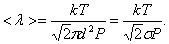 | (3.2.3) |
Таким образом, при заданной температуре средняя длина свободного пробега обратно пропорциональна давлению Р:
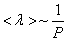 |
Например, при d = 3 Å = 3×10-10 м, Р = 1 атм., Т = 300 К, 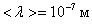 а, т.к.
а, т.к. 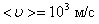 , то
, то 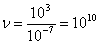 столкновений.
столкновений.
Вопрос №60
Сопоставим уравнения переноса. 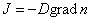 или
или 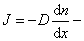 уравнение Фика для диффузии.
уравнение Фика для диффузии.
Коэффициент диффузии 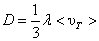 .
.
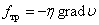 или
или 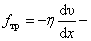 уравнение Ньютона для трения.
уравнение Ньютона для трения.
Коэффициент вязкости 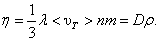
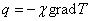 или
или 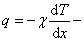 уравнение Фурье для теплопроводности.
уравнение Фурье для теплопроводности.
Коэффициент теплопроводности 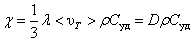 .
.
Все эти законы были установлены опытно, задолго до обоснования молекулярно-кинетической теорией. Эта теория позволила установить, что внешнее сходство уравнений обусловлено общностью лежащего в их основе молекулярного механизма перемешивания молекул в процессе их теплового хаотического движения.
Однако к концу XIX века, несмотря на блестящие успехи молекулярно-кинетической теории, ей недоставало твёрдой опоры – прямых экспериментов, доказывающих существование атомов и молекул. Это дало возможность некоторым философам, проповедовавшим субъективный идеализм, заявлять, что схожесть формул – это произвол учёных, упрощённое математическое описание явлений.
Но это, конечно, не так. Все вышеуказанные коэффициенты связаны между собой и все выводы молекулярно-кинетической теории подтверждены опытно.
Зависимость коэффициентов переноса от давления Р
Так как скорость теплового движения молекул 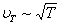 и не зависит от давления Р, а коэффициент диффузии D ~ λ, то и зависимость D от Р должна быть подобна зависимости λ(Р). При обычных давлениях и в разряженных газах
и не зависит от давления Р, а коэффициент диффузии D ~ λ, то и зависимость D от Р должна быть подобна зависимости λ(Р). При обычных давлениях и в разряженных газах 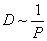 ; в высоком вакууме D = const.
; в высоком вакууме D = const.
С ростом давления λ уменьшается и затрудняется диффузия ( 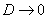 ).
).
В вакууме и при обычных давлениях 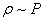 , отсюда
, отсюда 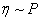 и
и 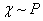 .
.
С увеличением Р и ρ, повышается число молекул, переносящих импульс из слоя в слой, но зато уменьшается расстояние свободного пробега λ. Поэтому вязкость η и теплопроводность χ, при высоких давлениях, не зависят от Р (η и χ – const). Все эти результаты подтверждены экспериментально.
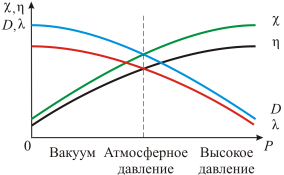
Рис. 3.7
На рисунке 3.7 показаны зависимости коэффициентов переноса и длины свободного пробега λ от давления Р. Эти зависимости широко используют в технике (например, при измерении вакуума).
