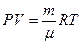Что такое изотермический процесс?
Процесс, происходящий в системе при постоянной температуре (T = PV = const).
Что такое обратимый процесс? Какие процессы являются обратимыми?
Обратимый процесс – это процесс, который может проходить как в прямом, так и в обратном направлении, проходя через одинаковые промежуточные состояния, причём система возвращается в исходное состояние без затрат энергии и без макроскопических изменений окружающей среды. Например: цикл Карно.
(Принцип Карно, состоит в том, что для получения работы в тепловой машине необходимы, по крайней мере, два источника теплоты с разными температурами.
Карно предложил идеальный цикл тепловой машины, где используются два источника теплоты с постоянными температурами: источник с высокой температурой - нагреватель и источник с низкой температурой - холодный источник. Поскольку цикл идеальный, то он состоит из обратимых процессов теплообмена между рабочим телом и источниками теплоты, протекающим по двум изотермам, и двух идеальных адиабат перехода рабочего тела с одной изотермы на другую.)
256. Что такое необратимый процесс? Приведите примеры необратимых процессов?
Необратимый процесс – это процесс, который нельзя провести в обратном направлении через все те же промежуточные состояния. Все реальные процессы необратимы. Например: диффузия, теплопроводность и др. процессы, при которых происходит направленный пространственный перенос вещества, энергии, импульса или заряда.
(Диффузия - проникновение одного вещества в другое при их соприкосновении. Теплопроводность - процесс переноса внутренней энергии от более нагретого тела к менее нагретому, из-за хаотического движения частиц (атомов, молекул…)).
Дайте определение идеального газ с точки зрения термодинамики.?
Идеальный газ – это система материальных точек (точечных молекул), которые взаимодействуют только путём упругих соударений (т.е. отсутствуют силы взаимодействия на расстоянии). Между молекулами отсутствуют силы взаимного притяжения и отталкивания, а их размеры намного меньше межмолекулярных расстояний. Термодинамика изучает макроскопические свойства тел и явлений природы, не интересуясь их микроскопической картиной.
Дайте определение идеального газ с точки зрения молекулярной физики. ?
Молекулярно-кинетическая теория изучает свойства тел (те, которые можно непосредственно наблюдать на опыте - давление, температура…) как суммарный результат действия молекул и не рассматривает движение отдельных частиц.
Каково значение средней концентрации молекул при нормальных условиях?
Нормальные условия: P = 10⁵ Па; T = 273 K; k=1.38 × 10⁻²³ Дж/К.
Найдем концентрацию из уравнения состояния идеального газа:
P = nkT
n = P / kT
Подставим числа:
n = 10⁵ / 1.38 × 10⁻²³ × 273 = 2.65 × 10²⁵ м⁻³
Какой вид имеет термическое уравнение состояния идеального газа?
Термическое уравнение состояния связывает макроскопические параметры системы, причём один из этих параметров — температура. Для системы с постоянным числом частиц его общий вид можно записать так: f (P,V,T) = 0.
Для идеального газа уравнение состояния (термическое) - это уравнение
Менделеева-Клапейрона 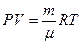
Напишите уравнение Клапейрона-Менделеева для произвольной массы газа.