Обеспечение химической стабильности.
Основными способами стабилизации глазных капель являются регулирование значений рН и введение в состав растворов, содержащих легкоокисляющиеся вещества, антиоксидантов. Для регулирования значения рН используются буферные растворители. Чаще всего в качестве буферного растворителя применяется борная кислота 1,9 - 2%. В качестве антиоксидантов: натрия сульфит, натрия метабисульфит и трилон Б.
В качестве вспомогательных веществ используют буферные растворы и др. стабилизаторы для повышения стабильности при хранении, натрия хлорид для обеспечения изотоничности, пролангаторыСократить частоту истилляций глазных капель и одновременно увеличить время контакта с тканями глаза можно путем пролонгирования является включение в состав глазных капель вязких растворителей, которые замедляют быстрое вымывание ЛВ из конъюктивального мешка. В качестве таких веществ раньше использовали масла (подсолнечное рафинированное, персиковое или абрикосовое). Однако более эффективными пролонгаторами для глазных капель оказались синтетические гидрофильные ВМС, такие, как МЦ (0,5% - 2%), Na - соль КМЦ (0,5 - 2%) поливинол (1,5%), микробный ПС аубазидан (0,1 - 0,3%), полиглюкин и др. Эти вещества не раздражают слизистую оболочку глаза, а также совместимы со многими ЛВ и консервантами.
В настоящее время в виде суспензий для офтальмологии применяют препараты стероидных гормонов. С целью предотвращения образования агрегатов или хлопьев, плохо смачивающихся дисперсионной средой, в. их состав рекомендуется вводить ПЭГ-400 и 0,1—0,15% раствор натрия хлорида.
Использование консервантовв производстве препаратов парентерального назначения. Одна из причин снижения качества лекарственных средств — их микробная контаминация в процессе производства или применения, которая может привести к снижению терапевтического эффекта препаратов или развитию у больного различного рода заболеваний. В связи с этим инъекционные лекарственные формы можно применять только при отсутствии в них микроорганизмов, т. е. стерильными. Введение консервантов в растворы проводится в тех случаях, когда сохранение стерильности гарантировать нельзя
Каждое антимикробное вещество, используемое для консервации лекарств, должно обеспечивать безопасность больного и необходимое качество лекарственного препарата. Исходя из этого к консервантам предъявляются следующие требования:
— широкий спектр антимикробного действия при низких концентрациях;
— хорошая растворимость;
совместимость с большинством лекарственных и вспомогательных веществ, упаковочными материалами;
- стабильность в широком интервале рН и температуры среды в течение срока годности лекарственного препарата;
— отсутствие влияния на органолептические свойства лекарственного препарата;
— отсутствие способности к образованию устойчивой формы микроорганизмов. Консерванты не должны снижать фармакологическую эффективность действующего
вещества или оказывать токсическое, аллергизирующее и раздражающее действие на организм человека.
Производство тюбик-капельницВполне обоснованно считается, что только в условиях фармацевтического предприятия могут быть созданы условия, позволяющие обеспечить весь комплекс необходимых требований, предъявляемых к глазным лекарствам на современном этапе научно-технической революции. В настоящее время преобладающее большинство глазных капель отпускается в тюбик-капельницах.
Тюбик-капельница представляет собой полиэтиленовый контейнер емкостью 1,5±0,15 мл для упаковки, транспортирования, стерильного хранения и инстилляции водных растворов лекарств для глаз. Она состоит из корпуса, свариваемого в асептических условиях после заполнения стерильным раствором, и защитного колпачка с прокалывающим устройством.
Общая технология производства тюбик-капельницы.
Технологический процесс приготовления раствора:
— растворение ингредиентов;
— подготовка помещений для фильтрации и розлива;
— подготовка аппаратов для приема раствора;
— подготовка фильтров и стерильная фильтрация.
Растворы в тюбик-капельницах готовятся в помещениях 2-го класса чистоты в условиях асептики. Помещение и аппаратура подвергаются влажной уборке, дезинфекции 3—5% раствором фенола и стерилизации бактерицидными лампами в течение 2 ч.
Растворы лекарственных веществ готовят в никелированных аппаратах из нержавеющей стали в соответствии с прописью лекарственной формы.
После проведения анализа раствор передается на стерильную фильтрацию и далее поступает в стерилизованный аппарат для последующего наполнения тюбик-капельниц.
Для получения готовой продукции используется вибрационная установка, представляющая собой герметически закрытый агрегат, внутри его поддерживается избыточное давление стерильного воздуха. В установке периодически движется непрерывная конвейерная цепь, по которой подаются отдельные детали тюбик-капельницы.
Перед сборкой тюбик-капельницы и колпачки промываются дистиллированной водой и подвергаются газовой стерилизации при 40—50 °С смесью этиленоксида и 10% углерода диоксида в течение 2 ч, после чего остатки газа удаляют выдерживанием изделий в течение 12 ч в стерильном помещении. Далее в асептических условиях в установке для сборки происходит навинчивание колпачков на корпус, наполнение его раствором лекарственного вещества и запайки термосвариванием. На печатной машине одновременно с двух сторон на корпус наносится надпись с названием лекарственного препарата, указанием его концентрации и объема.

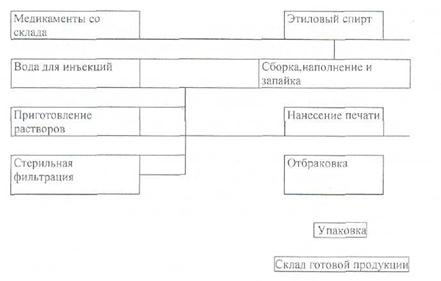
Рис. 2. Общая схема производства тюбик-капельницы
Тюбик-капельницы подвергаются визуальному контролю на отсутствие механических включений на белом и черном фоне. Помимо оптического просмотра проводят также дополнительную выборочную проверку по всем показателям — 5% от каждой партий.
Упаковывают тюбик-капельницы в одноместные футляры, в картонные коробки или в полихлорвиниловую пленку).
Кроме этой упаковки, по ГОСТу 17768-80 для глазных капель рекомендуют стеклянные флаконы с пробкой-пипеткой из нестабилизированного полиэтилена низкой плотности Перед наполнением раствор стерилизуют фильтрованием, а пробки-пипетки — газовой стерилизацией этиленоксидом с 10% углерода диоксида.
Методы стерилизации
По требованиям Государственной фармакопеи XI издания все готовые лекарственные препараты должны выдерживать тест на микробиологическую чистоту. Поэтому процесс стерилизации имеет большое значение при изготовлении всех лекарственных форм, а особенно инъекционных.
Под стерилизацией (обеззараживание, обеспложивание) понимают совокупность физических, химических и механических способов освобождения от вегетативных и покоящихся форм микроорганизмов (Н. Horn, 1984).
ГФ XI издания определяет стерилизацию как процесс умерщвления в объекте или удаления из него микроорганизмов всех видов, находящихся на всех стадиях развития.
От правильно подобранного метода стерилизации зависит качество производимой стерильной продукции.
В технологии лекарственных форм промышленного производства в настоящее время используют 3 группы методов стерилизации:
— механические;
— химические;
— физические.
Механические методы стерилизации
Стерилизующая фильтрация. Микробные клетки и споры можно рассматривать как нерастворимые образования с очень малым (1—2 мкм) размером частиц. Подобно другим выключениям, они могут быть отделены от жидкости механическим путем —фильтрованием сквозь мелкопористые фильтры. Этот метод стерилизации включен в ГФ XI для стерилизации термолабильных растворов.
По механизму действия фильтрующие перегородки, используемые для стерильной фильтрации, подразделяют на глубинные и поверхностные (мембранные) с размером пор не более 0,3 мкм.
Глубинные фильтры характеризуются сложным механизмом задержания микроорганизмов (ситовым, адсорбционным, инерционным). Ввиду большой толщины таких фильтров удерживаются и частицы меньшего размера, чем размер пор фильтрующей перегородки.
Глубинные фильтры классифицируют на: керамические и фарфоровые (размер пор 3—^ мкм), стеклянные (около 2 мкм), бумажно-асбестовые (1—1,8 мкм). Недостатками керамических и фарфоровых фильтров является продолжительность стерилизации, потеря раствора в порах толстого фильтра, образование микротрещин из-за хрупкости материала и, следовательно, ненадежность стерилизации.
Так, стеклянные и бумажно-асбестовые фильтры несовершенны. Стеклянные фильтры малопроизводительны, бумажно-асбестовые фильтры не рекомендуются для стерилизации инъекционных растворов, поскольку они состоят из волокнистых материалов и имеется угроза отрыва волокон от фильтра. Попадая в организм с раствором, такие волокна могут вызывать различные патологические реакции.
В последние годы большое распространение для стерилизующей фильтрации получили микропористые мембранные фильтры. Они лишены недостатков, присущих стеклянным и бумажно-асбестовым фильтрам.
Мембранные фильтры представляют собой тонкие (100— 150 мкм) пластины из полимерных материалов, характеризующиеся ситовым механизмом задержания микроорганизмов и постоянным размером пор (около 0,3 мкм). Во избежание быстрого засорения фильтра мембраны используют в сочетании с префильтрами, имеющими более крупные поры. При стерилизации больших объемов растворов оптимальным является применение фильтров обоих типов.
Использование глубинных и мембранных фильтров обеспечивает необходимую чистоту, стерильность и апирогенность растворов для инъекций.
Стерилизующая фильтрация имеет преимущества по сравнению с методами термической стерилизации. Для многих растворов термолабильных веществ (апоморфина гидрохлорид, викасол. барбитал натрия и другие) его признают единственно доступным методом стерилизации. Метод весьма перспективный в производстве глазных капель.
Химические методы стерилизации
Методы основаны на высокой специфической (избирательной) чувствительности микроорганизмов к различным химическим веществам, что обусловливается физико-химической структурой их клеточной оболочки и протоплазмы. Механизм антимикробного действия многих таких веществ еще недостаточно изучен. Считают, что некоторые вещества вызывают коагуляцию протоплазмы клетки, другие — действуют как окислители. Ряд веществ влияет на осмотические свойства клетки, многие химические факторы вызывают гибель микробиологической клетки благодаря разрушению ферментной системы. Основа любого варианта химической стерилизации — взаимодействие бактерицидного вещества с компонентами микробной клетки или споры.
Химическая стерилизация подразделяется на стерилизацию растворами (веществами) и стерилизацию газами (газовая стерилизация).
Стерилизация растворами или веществами. Стерилизацию растворами (веществами) серийно выпускаемой инъекционной продукции в заводских условиях не используют, так как введение в раствор постороннего биологически активного вещества нежелательно из-за возможных химического взаимодействия стерилизующего агента с действующими компонентами и побочных действий этого агента на организм человека. Еще однопринципиальное ограничение данного метода связано с тем, что практически любое бактерицидное вещество обладает определенной селективностью и его эффективность проявляется при высоких концентрациях или часто в определенных интервалах рН. недопустимых для живых организмов. Этот вид стерилизации используют для обеззараживания различной аппаратуры, трубопроводов и другого оборудования, применяемого в производстве стерильной продукции.
Газовая стерилизация. К своеобразной химической стерилизации следует отнести метод стерилизации газами. Преимущество метода — возможность стерилизации объектов в пластмассовой упаковке, проницаемой для газов. В герметическую камеру вводят стерилизант —■ смесь этиленоксида и углерода диоксида в соотношении 9:1. Углекислый газ добавляют в связи со взрывоопасностью окиси этилена. При стерилизации стерилизант поступает в аппарат под давлением до 2 кгс/см2 (196133 Н/м2) при температуре 43—^5 °С. Продолжительность стерилизации зависит от проницаемости упаковки, толщины слоя материала и продолжается от 4 до 20 ч. Затем этиленоксид удаляют продуванием стерильным воздухом (азотом) или путем вакуумирования.
При химической стерилизации газами погибают все вегетативные формы микроорганизмов и плесневые грибы.
Для стерилизации донорского материала, растворов кровезаменителей или продуктов, полученных из крови, широко применяют е-пропиолактон.
Главный недостаток, химических методов стерилизации — необходимость освобождения простерилизованного объекта от остатков стерилизанта и продуктов возможного взаимодействия. Широкое распространение метода затруднительно из-за длительности стерилизации, высокой стоимости, возможности побочного действия химического агента на обслуживающий персонал. Тем не менее для ряда лекарственных препаратов — это единственно надежный способ стерилизации в современных условиях.
Использование консервантов. Добавление консервантов условно можно отнести к методам химической стерилизации. Введение консервантов в растворы проводится в тех случаях, когда нельзя гарантировать сохранение стерильности. При этом возможно снижение температуры стерилизации или сокращение времени ее проведения.
Механизмы воздействия консервантов на микроорганизмы очень различны и определяются их химическим строением. Как к основному результату при этом следует отнести нарушение жизненных функций клетки, в частности инактивацию белковой части клеточных ферментов. В зависимости от степени инактивации наступает либо гибель клетки. либо замедление ее жизненных функций.
Физические методы стерилизации
Тепловая (термическая) стерилизация. В настоящее время монопольное положение среди возможных методов стерилизации в фармацевтическом производстве занимает тепловая стерилизация.
В зависимости от температурного режима тепловая стерилизация подразделяется на стерилизацию:
— паром под давлением (автоклавирование);
— текучим паром;
— тиндализацию;
— воздушную.
Стерилизация паром под давлением. Автоклавирование — стерилизация растворов, устойчивых к нагреванию, паром под давлением 1,1 атм при температуре 119—121 °С. В данных условиях погибают не только вегетативные, но и споровые микроорганизмы за счет коагуляции белка клетки.
Этот традиционный способ стерилизации сегодня предпочтителен по трем причинам. Во-первых, он дает возможность стерилизации препаратов в конечной герметичной упаковке,что исключает опасность вторичной контаминации. Во-вторых, благодаря длительной практике использования он обеспечен достаточно надежной аппаратурой. И в-третьих, на сегодняшний день он наиболее экономичен.
При применении данного метода происходит комбинированное воздействие на микроорганизмы высокой температуры и влажности, при этом погибают самые стойкие споры. Коагуляция белковых веществ в этих условиях начинается при температуре 56 °С.
Стерилизацию паром под давлением проводят в стерилизаторах различной конструкции цилиндрической или квадратной формы. Стерилизаторы квадратной формы типа АП-7 (рис. 19.25), АП-18 имеют двери с двух сторон: через одну происходит загрузка нестерильной продукции; через другую — выгрузка простерилизованной. Корпус автоклава нагревается глухим паром, чтобы не было его конденсации в рабочей камере. Затем в камеру для вытеснения воздуха подается острый пар. Отсчет времени стерилизации начинается с момента достижения заданного давления по манометру. Стерилизаторы оснащены, автоматической контрольной аппаратурой, с помощью которой на контрольной ленте записывается давление и время стерилизации. Условия стерилизации продукции указаны в промышленных регламентах или другой нормативно-технической документации.

Рис. 21. Устройство парового стерилизатора АП-7:
/ — корпус; 2 —- крышка; 3 — теплоизоляция; 4 — стерилизационная камера;
5 — клапан предохранительный; б — пульт управления; 7 — полка;
8 —• подача острого пара
Стерилизацию растительных масел и жиров в заводских условиях осуществляют паром под давлением в герметически закрытых сосудах при температуре 119—-121 °С и давлении 1,0— 1,1 атм в течение 2 ч.
Автоклавированию также подвергаются установки для стерилизующего фильтрования, фильтрующие перегородки и другой вспомогательный материал, используемый в технологическом процессе производства инъекционных лекарственных форм.
Среди недостатков метода можно выделить невозможность стерилизации растворов, содержащих термолабильные вещества, опасность работы с паром под давлением, отсыревание многих материалов во время стерилизации и др.
Стерилизация текучим паром. Растворы веществ термически малоустойчивые иногда стерилизуют при 100 °С текучим паром (без примеси воздуха и избыточного давления). Насыщенный пар убивает только вегетативные формы микроорганизмов и при наличии в объекте споровых форм метод неэффективен.
Тиндализация (дробная стерилизация). Для термолабильных веществ, а также для растворов в шприц-ампулах стерилизацию иногда проводят методом тиндализации. Суть метода заключается в трехкратном нагревании растворов до 40—60 °С с перерывами в сутки, i течение которых объекты термостатируют при температуре 37±1 °С для прорастания :поровых форм в вегетативные.
Стерилизация сухим жаром (воздушная стерилизация). Стерилизация сухим жаром, [роводимая в аэростерилах или других аппаратах этого типа, также высокоэффективна. 1огибают все формы микроорганизмов за счет пирогенетического разложения белковыхвеществ. Однако высокая температура нагрева (160— 200 °С), длительное время воздействия (1—2 ч) и сухой горячий воздух оказывают повреждающее действие на стерилизуемые объекты и, следовательно, ограничивают возможности данного Способа.
Инъекционные растворы не подвергают стерилизации сухим жаром, так как из-за низкой теплопроводности воздух не обеспечивает быстрый нагрев растворов до температуры стерилизации, а длительный прогрев -— приводит к разложению большинство лекарственных веществ.
Сухим жаром стерилизуют некоторые термостойкие порошки, масла, стеклянную тару (ампулы, флаконы и необходимую посуду), вспомогательные материалы.
Лучшими считают стерилизаторы с ламинарным потоком стерильного воздуха, нагретого до требуемой температуры, что улучшает создание равномерного температурного поля и устраняет загрязнения от обогреваемых стенок камеры и из воздуха, попадаемого в момент выгрузки объекта.
Радиационная стерилизация. Лучистая энергия губительно действует на клетки живого организма, в т. ч. и на различные микроорганизмы. Принцип стерилизующего эффекта этих излучений основан на способности вызывать в живых клетках при определенных дозах поглощенной энергии такие изменения, которые неизбежно приводят их к гибели за счет нарушения метаболических процессов и коагуляции белка.
Источником ионизирующих у-излучений служат долгоживущие изотопы 60Со2?, b7Cs66 , ускорители электронов прямого действия и линейные ускорители электронов. Для бактерицидного эффекта достаточно от 15 до 25 кГр, причем верхний предел необходим для инактивации споровых форм.
В настоящее время накоплен большой опыт применения этого метода, точно установлены типичные дозы излучения, необходимые для надежной стерилизации, разработано радиационное оборудование для высокопроизводительного процесса стерилизации, решены вопросы безопасности работы установок для обслуживающего персонала.
Этот метод по экономическим показателям превосходит асептическое изготовление растворов со стерильной фильтрацией, но несколько уступает тепловой стерилизации. Однако в будущем может приблизиться к ней из-за неизбежного снижения относительной стоимости изотопов — побочных продуктов атомной энергетики.
Ультразвуковая стерилизация. Прохождение ультразвука (УЗ) в жидкой среде сопровождается чередующимися сжатиями, разрежениями и большими переменными ускорениями. В жидкости образуются разрывы, называемые кавитационными полостями. В момент сжатия эти полости захлопываются. Избыточное давление, создаваемое УЗ-волной, накладывается на постоянное гидростатическое и суммарно может составлять в пузырьках несколько атмосфер. В качестве «зародышей» кавитационных полостей могут быть пузырьки газа, пара в жидкости, твердые частицы и места неровностей твердой поверхности. Большие импульсные давления кавитаций приводят к разрушению целостности клеточной мембраны микроорганизмов, споровых образований и других частиц. Важно установить оптимальные параметры процесса стерилизации, так как высокие импульсные давления могут приводить к механическому разрушению ампул. Стерилизующая частота звука должна быть в пределах 18—22 кГц.
И хотя метод очень эффективен, он не нашел широкого применения из-за сложности аппаратурного оснащения и возможных сложных химических превращений компонентов растворов. Вопросы стабильности компонентов при УЗ-стерилизации имеют много общего с аналогичными проблемами радиационной стерилизации. Для повышения устойчивости лекарств при ультразвуковом воздействии необходимо подобрать такие условия стерилизующей обработки, которые обеспечивают снижение вводимой в систему энергии на тех частотах ультразвука, которые одновременно со стерилизацией не приводят к разложению компонентов лекарственных препаратов.Чаще метод применим при производстве эмульсий и суспензий с целью лучшего диспергирования веществ в них и одновременно получения стерильных гетерогенных систем для парентерального применения.
Стерилизация токами высокой и сверхвысокой частоты. К настоящему времени нет единой точки зрения на механизм инактивации микроорганизмов при ВЧ- и СВЧ-облучении. Существует мнение об исключительно тепловом механизме действия токов высокой частоты на биологические объекты. Принцип действия высокочастотного поля заключается в его активном воздействии на ориентацию молекул вещества. Изменение направленности поля вызывает изменение ориентации молекул и поглощение части энергии поля веществом. В результате происходит быстрый нагрев вещества во всех точках его массы. Менее широко распространены представления о том, что. помимо тепловых процессов, на гибель микроорганизмов оказывает влияние специфическое действие ВЧ- и СВЧ-излучения.
С помощью СВЧ-энергии возможно стерилизовать в расфасованном виде готовую продукцию: глазные мази, пасты в тубах, лекарственные средства в конвалютах, порошки, таблетки, пористые лиофилизированные массы, не содержащие гидрофильные жидкости. Стерилизация ампулир о ванных растворов и жидких лекарственных форм, укупоренных герметически — нежелательна, так как в замкнутой емкости возникает избыток давления паров испарившейся жидкости, взрывающий ее. В результате наступает разгерметизация в виде растрескивания стенок ампул или срыва укупорочного материала.
Метод также не нашел широкого применения из-за сложности аппаратурного оснащения и возможности неблагоприятного воздействия быстрого кратковременного нагрева инъекционного раствора.
Стерилизация ультрафиолетовым излучением. Из-за возможности образования ядовитых продуктов и возможности разложения биологически активных компонентов инъекционных растворов под действием УФ-излучения, метод не нашел применения для стерилизации препаратов для инъекций. Однако он широко используется для стерилизации порошков, воды для инъекций, вспомогательных материалов, воздушной среды производственных помещений, технологического оборудования и других объектов.
При стерилизации воздушной среды производственных помещений в качестве источников УФ-радиации используют специальные лампы БУВ (бактерицидная увиолевая), которые изготавливают в виде трубки из специального увиолевого стекла, способного пропускать УФ-лучи, с электродами из длинной вольфрамовой спирали, покрытой бария и стронция гидрокарбонатами. В трубке находится ртуть и аргон при давлении в несколько мм рт. ст. Источник УФ-лучей — разряд ртути, происходящий между электродами при подаче на них напряжения. Излучение лампы БУВ обладает большим бактерицидным действием, так как максимум излучения лампы близок к максимуму бактерицидного действия (254 нм).
Количество и мощность бактерицидных ламп подбирается так, чтобы при прямом облучении на 1 м~ объема помещения приходилось не менее 2—2,5 Вт мощности излучателя. Промышленностью выпускаются лампы БУВ-15, БУВ-30, БУВ-60 и др. (цифра обозначает мощность в ваттах), а также бактерицидные облучатели: настенный ОБН, состоящий из двух ламп БУВ-30; потолочный ОБП — из 4 ламп БУВ-30; передвижной маячного типа ОБПЕ — из 6 ламп БУВ-30. Облучатели используют только при отсутствии в помещении людей.
Для стерилизации воды применяют аппараты с погруженными и. непогруженными источниками УФ-радиации. В аппаратах первого типа источник УФ-излучения (бактерицидная увиолевая лампа, покрытая кожухом из кварцевого стекла) помещается внутри водопровода и обтекается водой. Данный способ стерилизации больших объемов воды для инъекций считается наиболее экономичным.
В аппаратах с непогруженными лампами они помещаются над поверхностью облучаемой воды. В связи с тем что обычное стекло практически непроницаемо для ультрафиолетовых лучей, водопровод в местах облучения изготавливают из кварцевого стекла, а это значительно повышает стоимость аппарата. В настоящее время разработан способ, приприменении которого имеется возможноств замены кварцевого стекла полиэтиленовым, свободно пропускающим УФ-радиацию.
Как положительный фактор 'следует отметить, что при стерилизации воды не происходит накопления пероксидных соединений и под действием УФ-излучения инактивируются некоторые пирогенные вещества, попавшие в воду.
Стерилизация ИК- и лазерным излучением. Электронная стерилизация.
Эти перспективные виды стерилизации практически не находят сегодня применения, хотя возможности для этого имеются.
Облучение инъекционных водных систем инфракрасным (ИК) излучением в областях поглощения воды (К—2,1 мкм) может быть эффективным средством ее нагрева и тем самым является, по сути, еще одним вариантом тепловой стерилизации. Наличие достаточно мощных источников ИК-излучения позволяет надеяться на возможность создания оборудования для высокопроизводительной технологии. Преимуществом этого метода перед традиционным автоклавированием может считаться возможноств отказа от небезопасного в обслуживании и нетехнологичного перегретого пара.
Принципиально возможны способы стерилизации с применением лазерного и электронного излучения, при этом можно достигнуть высокой эффективности стерилизации как путем интенсивного нагрева вследствие поглощения мощного излучения в воде, так и за счет селективного поглощения излучения макромолекулами микроорганизмов в многоквантовых процессах. Однако исчерпывающих исследований применительно к какой-либо конкретной системе, совокупность которых дала бы основание о создании хотя бы основ таких методов стерилизации, пока не проведено.
Методы контроля СТЕРИЛЬНОСТИ
Определение стерильности растворов проводится путем посева и инкубации на специальных тест-средах образцов каждой серии продукции. При обнаружении роста микроорганизмов хотя бы в одной пробирке испытание повторяют на таком же количестве сосудов. И только при отсутствии роста при повторном посеве серия считается стерильной. Определению стерильности подвергают ампулы или флаконы каждой серии, одновременно подвергавшиеся стерилизации в одном стерилизующем аппарате.
Метод мембранного фильтрования при определении стерильности рекомендован при выраженном антимикробном действии лекарственного вещества и испытании растворов в больших объемах.(более 100 мл). Отбирается 30 ампул, их делят на 3 группы по 10 штук, 20 используют для испытания на стерильность, 10 — для контроля полноты отмывания мембраны от лекарственного вещества. Для фильтрования применяют установку с мембраной диаметром 47 мм и размером пор 0,45±0,02 мкм. Фильтры стерилизуют при температуре 121±1 °С 20 мин. Если испытывают порошок, его растворяют в воде для инъекций, фильтруют через стерильную мембрану, которую промывают от раствора 3—5 порциями растворителя по 100 мл, разрезают стерильными ножницами на 2 части, одну из них помещают в колбу с тиогликолевой средой, вторую — в среду Сабуро, 7 дней инкубируют при ежедневном просмотре. Все операции проводят в асептических условиях. При отсутствии роста на двух средах делают заключение о стерильности серии.
Вопрос 3. Folia Salviae (Folia Salviae qfflcinalis) — листья шалфея {Salviae folium (Salviae qfficinalis folium) — шалфея лист)
Шалфея лекарственного (Salvia officinalis L) из сем. губоцветных — Lamiaceae (Labia-tae); используют в качестве лекарственного средства и лекарственного сырья.
Химический состав. Листья содержат 1-2,5 % эфирного масла. Масло состоит из цинеола (до 15 %), пинена, камфоры, туйона, сальвена и других терпеноидов. Листья содержатдубильные вещества, тритерпеноидные кислоты — урсоловую и олеаноловую, дитерпеноиды (карнозоли розманол), фенольные кислоты.

количественное определение.Аналитическую прооу сырья измельчают до размера частиц, проходящих сквозь сито с отверстиями диаметром 2 мм.
Содержание эфирного масла определяют в 30 г измельченного сырья методом 1 или 2 (ГФ XI, вып. 1, с. 290). Время перегонки 2 ч.
Заготовка сырья, первичная обработка, сушка.Заготавливают вполне развитые листья в течение лета. Сбор производят главным образом механизированным способом, иногда вручную. Траву скащивают косилками, высушивают на токах или в сушилках, затем обмолачивают, отделяют листья от стеблей путем просеивания через решёта.
Хранение.Хранят сырье в сухих прохладных помещениях на стеллажах или подтоварниках, в защищенном от света месте, отдельно от других видов сырья. В аптеках хранят в закрытых фанерных ящиках. Срок годности 1,5 года (предельный).
Использование.Листья шалфея в аптеки поступают в фасованном виде. Листья входят в состав грудных сборов, а также применяются в форме настоя — вяжущего, противовоспалительного средства для полосканий полости рта. глотки, гортани при катарах верхних дыхательных путей.
Из листьев шалфея получают также суммарный препарат «Сальвин»,обладающий вяжущим и антимикробным действием. Шалфей лекарственный применяется в гомеопатии и используется в БАДах.
При приеме препаратов шалфея возможны следующие побочные эффекты: опухание губ, сухость во рту. Противопоказано их назначение при беременности. При сильном кашле, бронхиальной астме, гастрите с повышенной секрецией и нефрите рекомендуется применять с осторожностью.
Вопрос 4. Рецепт выписан верно. Срок действия рецепта - 2 мес. Рецепт отдается
больному с указание на обороте количества отпущенного препарата и даты отпуска и не
хранится в аптеке. По истечении срока действия рецепт гасится штампом «Рецепт не
действителен».
Способ применения ЛС обозначается на русском или русском и национальном языках с
указанием дозы, частоты, времени приема и его длительности.
ПРИКАЗ МИНЗДРАВА РФ ОТ 04.03 2003 N 80 (С ИЗМ ОТ 30 01 2004) "ОБ
УТВЕРЖДЕНИИ ОТРАСЛЕВОГО СТАНДАРТА "ПРАВИЛА ОТПУСКА (РЕАЛИЗАЦИИ)
ЛЕКАРСТВЕННЫХ С (приказ должен быть на экзамене).
В аптечной организации в удобных для ознакомления местах торгового зала
должны быть размещены:
- копии лицензий на фармацевтическую деятельность и другие виды деятельности в соответствии с действующим законодательством Российской Федерации;
информация о телефонах и адресах органов управления здравоохранением и фармацевтической деятельностью;
- книга отзывов и предложений;
- информация о группах населения, имеющих право на бесплатное и льготное обеспечение внеочередное обслуживание, в соответствии с действующим законодательством Российской Федерации;
- информация о лице, ответственном за лекарственное обеспечение инвалидов Великой Отечественной войны и приравненных к ним категорий населения по льготам (для аптечных организаций, осуществляющих льготный отпуск лекарственных препаратов):
- информация о номерах телефонов и режиме работы справочной фармацевтической службы;
- информация о наименованиях отделов или зон отпуска соответствующих групп товаров;
- информация о сроках хранения лекарственных препаратов, изготовленных в аптеке (аптечном пункте)]
- ценники на предлагаемые безрецептурные лекарственные препараты и другие товары, разрешенные отпуску из аптечных организаций;
информация о сотрудниках аптечной организации. непосредственно обслуживающих население (таблички, бейджи и прочие с указанием ФИО и должности);
- информация о дежурном администраторе (ФИО, должность) и нахождении кнопки сигнального вызова дежурного администратора (за исключением аптечного киоска);
- при наличии пункта проката, информация о перечне предметов, выдаваемых на прокат;
- копия или выписка из Федеральногозакона "О защите прав потребителей"

|>илет 16. Вопрос]/ Суспензии — жидкая лекарственная форма, содержащая в качестве дисперсной^фазйГодно или несколько измельченных порошкообразных лекарственных веществ, распределенных в жидкой дисперсионной среде.
Различают суспензии для внутреннего, наружного и парентерального применения. Суспензии для парантерального применения вводят только внутримышечно. Они должны соответствовать статье «Инъекции», если нет других указаний в частных статьях.
Суспензии могут быть готовыми к применению, а также в виде порошков или гранул для суспензий, к которым перед применением прибавляют воду или другую подходящую жидкость; количество воды или другой жидкости должно быть указано в частных статьях.
В качестве вспомогательных используют вещества, увеличивающие вязкость дисперсионной среды, поверхностно-активные и буферные вещества, корригенты, консерванты, антиокислители, красители и другие, разрешенные к медицинскому применению. Перечень вспомогательных веществ должен быть указан в частных статьях. Не допускается изготовление суспензий, содержащих ядовитые вещества.
Отклонение в содержании действующих веществ в 1 г (мл) суспензии не должно превышать±10 %.
Перед употреблением суспензии взбалтывают в течение 1—2 мин, при этом должно наблюдаться равномерное распределение частиц твердой фазы в жидкой дисперсионной среде. Время седиментационной устойчивости суспензии или размер частиц твердой фазы должны быть указаны в частных статьях.
Маркировка. Для суспензий, полученных из порошков или гранул, должны быть указаны условия и время хранения после прибавления воды. Все виды суспензий должны иметь указание: «Перед употреблением взбалтывать».
Упаковка. С соответствующим дозирующим устройством.
Хранение. В упаковке, обеспечивающей стабильность при хранении и транспортировании и. если необходимо, в прохладном месте.
Расчеты. Количество стабилизатора при изготовлении водных суспензий рассчитывают с учетом степени гидрофобности лекарственных веществ. Так, для не резко гидрофобных веществ желатозу берут в соотношении 0,5 г на 1,0 г стабилизируемого вещества, для резко гидрофобных соотношение составляет 1 : 1. В тех же соотношениях могут
