Фармацевтические факторы, влияющие на высвобождение лекарственных веществ из лекарственных форм
Биофармация в современной технологии лекарственных форм является научной основой поиска, создания и исследования высокоэффективных лекарственных препаратов. Она изучает зависимость действия лекарственных препаратов от фармацевтических факторов, влияющих на терапевтическую эффективность. В специальной литературе термин «фармацевтические факторы» получил распространение в последние 3 десятилетия прежде всего в связи с клиническим подтверждением экспериментальных данных о существовании зависимости между эффективностью лекарственных препаратов и методами их получения. Роль фармацевтических факторов в развитии лечебного действия впервые удалось установить при исследовании терапевтической неэквивалентности лекарственных препаратов, полностью соответствующих требованиям «Государственной фармакопеи» (ГФ), содержащих равные количества одного и того же лекарственного вещества в одних и тех же лекарственных формах, но отличающихся методом изготовления или используемыми вспомогательными веществами и в связи с этим оказывающих различный терапевтический эффект. Тщательные исследования процессов всасывания лекарственных веществ показали, что на терапевтическую эффективность особое влияние оказывают следующие факторы, которые и названы фармацевтическими:
1) физическое состояние лекарственного вещества
(размер частиц, форма кристаллов, наличие или от
сутствие заряда на поверхности частиц и др.);
2) химическая природа лекарственного вещества
(соль, кислота, основание, количество гетероциклов,
эфирные связи, комплексные соединения и т. д.);
3) вспомогательные вещества, их природа, физи
ческое состояние, количество;
4) вид лекарственной формы и пути ее введения;
5) фармацевтическая технология.
Среди перечисленных факторов в практической деятельности провизора-технолога наибольшее значение имеют такие факторы, как физическое состояние лекарственного вещества, наличие вспомогательных веществ и их природа. Эти факторы необходимо учитывать при выборе технологии лекарственных препаратов, механизации стадий технологического процесса. Обычно химическая природа лекарственных веществ, так же как и лекарственная форма, регламентируется прописью рецепта,, где врач указывает лекарственное вещество (соль, кислоту и т. д.) и форму. Однако при разработке новых лекарственных препаратов обязательно учитывают химическую природу лекарственного вещества и рациональную лекарственную форму. Например, назначение амидопирина в порошках и суппозиториях с последующим определением этого лекарственного вещества в моче больных показало, что при применении амидопирина в суппозиториях он обнаруживается в моче больных через 5 мин, а в порошках — через 15—20 мин. Таким образом, при назначении амидопирина в форме суппозиториев его болеутоляющее действие наступает быстрее, чем при применении порошков. При выборе лекарственной формы важно знать цель применения лекарственного вещества и препарата. Например, в офтальмологии применяются глазные капли, глазные пленки. В том случае, когда требуется кратковременное действие лекарственного вещества — расширение зрачка для просмотра сосудов глазного дна — более рационально использовать атропина сульфат в глазных каплях. Наоборот, применение пилокарпина гидрохлорида, используемого при лечении глаукомы (повышенного внутриглазного давления) , целесообразно в виде глазных пленок, так как это позволяет вводить препарат 1—2 раза в сутки по сравнению с глазными каплями, инстилляцию которых проводят через каждые 2—3 ч. Перспективны в этом плане интраокулярные лекарственные пленки, созданные на основе коллагена, которые так же, как и глазные пленки, впервые разработаны на кафедре технологии лекарственных форм I ММИ им. И. М. Сеченова. Пленки используются в хирургической практике. Их вводят в переднюю камеру глаза при офтальмохирур-гических вмешательствах с целью исключения повторного инфицирования глаза, которое может возникнуть на 5—7-е сутки после операции. Пленки, содержащие
гентамицина сульфат, заменяли субконъюнктивальные инъекции. Коллагеновые пленки лизировались на 10— 12-е сутки. Таким образом, правильный выбор лекарственной формы — необходимое условие обеспечения оптимального действия лекарственного вещества.
При изготовлении экстемпоральных лекарственных форм наибольшее влияние на биологическую доступность оказывают физическое состояние лекарственного вещества, правильный выбор вспомогательных веществ и фармацевтическая технология, которые освещены в материале по каждой лекарственной форме.
Правильное введение лекарственного вещества в состав лекарственной формы зависит от знания провизором-технологом свойств лекарственного вещества: растворимости в том или ином растворителе (в первую очередь —. в воде); степени гидрофобности и т. д. Если лекарственное вещество невозможно ввести в растворенном виде, то его измельчают.
ИЗМЕЛЬЧЕНИЕ
Вопросам измельчения в фармацевтической технологии придается особое значение. Известно, что с уменьшением размера частиц резко увеличивается поверхностная энергия измельчаемого лекарственного вещества. При тонком измельчении лекарственные вещества лучше растворяются, быстрее и полнее участвуют в химических реакциях и т. д. Измельчение может существенным образом влиять на терапевтическую активность лекарственных веществ вследствие изменения процессов их всасывания. Это происходит при изменении растворимости лекарственных веществ, скорость которой прямо пропорциональна площади поверхности и обратно пропорциональна величине частиц вещества. Например, при назначении одинаковых доз сульфадимезина микронизированного и полученного в заводском производстве без дополнительного измельчения выявлено, что в первом случае в плазме крови людей содержание вещества на 40 % выше, максимальная концентрация достигается на 2 ч раньше, а общее количество всосавшегося вещества на 20 % больше, чем во втором случае. При уменьшении размера частиц кислоты ацетилсалициловой до микро-низированных увеличивалось приблизительно в 2 раза
ее анальгетическое, жаропонижающее и противовоспалительное действие.
Убедительные результаты о влиянии размера частиц лекарственных веществ на высвобождение и всасывание получены при изучении суспензий и мазей. Например, сульфадиметоксин микронизированный (3— 12 мкм), введенный животным в виде 2 % водной суспензии из расчета 500 мг/кг, всасывался в кровь значительно быстрее по сравнению с лекарственным веществом, отвечающим требованиям нормативно-технической документации. Его максимальная концентрация через 1—2 ч составляла от 18,5 до 21,9мг/мл, в то время как в контрольной группе максимальный уровень вещества в крови достигался через 4 ч и составлял лишь 5 мг/мл.
Аналогичные результаты получены при использовании суспензии сульфамонометоксина.
В аптечной практике необходимый размер частиц порошка получают при соблюдении следующих условий измельчения: выбор ступки, время измельчения, применение аппаратов, порядок смешивания, особые правила и приемы технологии (см. главу 8). Технология других лекарственных форм, например суспензий, мазей, где возможно растворение или измельчение лекарственных веществ, также имеет свои особенности. Специфика технологии каждой лекарственной формы рассмотрена в соответствующих разделах курса.
3.3. ВСПОМОГАТЕЛЬНЫЕ ВЕЩЕСТВА
Не менее важное значение в технологии лекарственных форм имеет правильный выбор вспомогательных веществ. Ни один из фармацевтических факторов не оказывает столь сложного и значительного влияния на действующие вещества, как вспомогательные ингредиенты. Это связано не только с тем, что вспомогательные вещества присутствуют в каждом лекарственном препарате. Будучи своеобразным «носителем» лекарственных веществ, постоянно контактируя с ними, вспомогательные вещества сами обладают определенными физико-химическими свойствами, которые в различных условиях могут проявляться по-разному. Вспомогательные вещества не являются индифферентными и всегда так или иначе воздействуют на высвобождение лекарственного вещества. Чаще всего в
качестве индифферентного вещества называют сахар молочный. Однако его присутствие, например, ускоряет всасывание тестостерона, но снижает активность изониазида. Поэтому в каждом конкретном случае выбор вспомогательного вещества должен быть индивидуальным по отношению к лекарственному веществу.
В качестве примера рассмотрим влияние вспомогательных веществ на активность лекарственных веществ в мазях и суппозиториях. Среди факторов, влияющих на высвобождение лекарственных веществ, наибольшее внимание уделяют основе, ее типу (гидрофильная, гидрофобная, эмульсионная), вязкости, физико-химическим свойствам и концентрации применяемых эмульгаторов, наличию поверхностно-активных веществ (ПАВ) и других активаторов всасывания.
Влияние типа основы различно в зависимости от способа введения лекарственного вещества. Установлено, например, что кислота борная не оказывает бак-териостатического действия при использовании жировых основ, но эффективна при изготовлении мазей на гидрофильных основах, в которых содержится большое количество воды. По-видимому, терапевтическое действие проявляет образующийся раствор кислоты борной. Иод, напротив, малоактивен в основах, содержащих большое количество воды.
Структурно-механические свойства мазевых основ, в частности вязкость и предельное напряжение сдвига, являются факторами, влияющими на скорость диффузии лекарственных веществ, т. е. на скорость того процесса, который происходит при наложении мази на кожу или слизистую оболочку и от которого в известной мере зависит лечебный эффект. Изменение вязкости мазевых оскоз при введении 5—8 % аэросила приводит к увеличению пластической вязкости и тиксо-тропности систем, в результате высвобождение, например, кислоты салициловой уменьшается.
Изучено влияние реологических свойств желатин-но-глицериновых основ по величине модуля упругости (Ei), эластичности (£2) и пластической вязкости (л) на резорбцию кислоты ацетилсалициловой из суппозиториев. На рис. 3.1 показано, что при концентрации желатина ниже 10 % масса плавится и резорбция лекарственного вещества (R) из таких студней незначительна. При повышении концентрации желатина в
| CM | СЧ | |
| s | ||
| о | ||
| X | ||
| с; | Ч | |
| ю |
Г О О
| uJ -5,0 | HI -50 | ; А. | |
| 4,0 | -40 | ||
| 3,0 | -30 | ||
| - | |||
| 2,0 | -20 | /У | |
| 1,0 | - 10 | - ^ ! 1 1 1 |
0 10 20 30 40 50 С, %
Рис. 3.1. Зависимость модуля упругости (Ei), модуля эластичности (Е2) и резорбции (R) от концентрации (С) желатина в студне при температуре 37 °С.
R
«IК Г/МЛ
! 30 |"
] j
H
| 10 20 30 40 Е9-Ю~&дин/см2 |
Рис. 3.2. Зависимость резорбции (R) кислоты ацетилсалициловой от модуля эластичности основ
студне упругость и пластичность увеличиваются и параллельно повышается резорбция. Однако при больших концентрациях желатина (более 40%) упругость увеличивается, а эластичность уменьшается. При этом уменьшается также и резорбция лекарственного вещества. Следовательно, процесс резорбции зависит от степени эластичности (рис. 3.2).
Введение в состав мазевых и суппозиторных основ эмульгаторов, ПАВ и других активаторов всасывания является одним из важных факторов, оказывающих

Время, ч
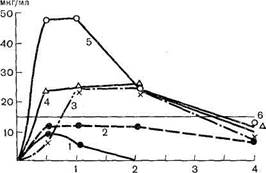
Рис. 3.3. Уровень стрептомицина сульфата в крови кроликов после введения его в виде суппозиториев с различными ПАВ. 1 — без ПАВ (контроль); 2 —с сорбитанолеатом; 3 —с натрия лаурил-сульфатом; 4 — с эмульсионным воском; 5 — с твином-80; 6 — уровень терапевтической концентрации стрептомицина в крови.
влияние на активность лекарственных веществ. Натрия лаурилсульфат способствует увеличению резорбции микрокристаллического сульфапиридазина из гидрофильной основы. Показана способность диметилсуль-фоксида легко проникать через неповрежденную кожу, транспортировать, депонировать и пролонгировать при этом поступление лекарственных веществ в организм.
Изучено влияние ПАВ на кинетику стрептомицина сульфата, вводимого в суппозиториях, изготовленных на масле какао, к которому добавляли по 5 %: эмульгатор № 1, эмульгатор Т-2, полиоксил-30-олеат, твин-80, воск эмульсионный, сорбитанолеат, пентол, полиок-сил-40-стеарат или 1 % натрий-лаурилсульфат. Результаты, полученные в эксперименте, представлены на рис. 3.3. Стрептомицина сульфат ограниченно всасывается при ректальном введении суппозиториев, изготовленных на масле какао. Добавление ПАВ (наилучший эффект обеспечивает твин-80) позволяет создать в крови кроликов терапевтические концентрации антибиотиков (выше 15 мкг/мл) в течение 4 ч и обеспечить противотуберкулезное действие.
Особое значение для научного понимания роли вспомогательных веществ имеет изучение их взаимодействия с лекарственными веществами и другими компонентами лекарственного препарата: образование
водородных связей, соединения-включения ван дер ваальсовы силы, ковалентные связи (свободноради кальные взаимодействия, реакции, связанные с пере носом элементарных частиц). Однако независимо от природы связи в подавляющем большинстве случаев конечным результатом в системе лекарственное вещество — вспомогательное вещество являются реакции комилексообразования и адсорбции. Это может быть обнаружено только с помощью специальных исследований. Образующиеся комплексы могут быть весьма прочными или, наоборот, легко распадаться, характеризоваться высокой поверхностной активностью, могут усиливать или ослаблять основную фармакологическую реакцию лекарственного вещества и т. д.
Интенсивность технологических процессов при производстве лекарственных препаратов может существенно влиять на реакцию комплексообразования, ускоряя ее или направляя в соответствующую сторону Особенно важными в этом отношении являются стадии растворения и фильтрования, плавления, смешивания и другие стадии, при которых происходит изменение агрегатного состояния лекарственного и вспомогательного веществ, интенсификация и рост числа контактов между ними.
Перспективным вспомогательным веществом в технологии мазей, суппозиториев, растворов для инъекций, глазных лекарственных пленок и других лекарственных форм является коллаген (см. главу 5). Предполагается, что лекарственное вещество, попадая в «петли» молекул коллагена, образует соединения-включения типа клатратов, обеспечивая тем самым пролонгированное действие. Последнее для ряда лекарственных веществ, имеющих с коллагеном одинаковые функциональные группы, например карбоксила-мидные, объясняется химическим взаимодействием Перспективность применения коллагена убедительно доказана при изучении анестезирующей активности о ^ пиромекаиновых мазей, которые обеспечивают анестезию в течение 200 мин, в хо время как другие основы — от 25 до 115 мин. Это вполне удовлетворяет требованиям практической стоматологии, для нужд которой (прежде всего) разрабатывалась мазь. Концентрация пиромекаина в мази на основе коллагена снижена с 5 до 3 %. Правильный выбор вспомогатель-
ных веществ позволяет снизить концентрацию лекарственного вещества при сохранении терапевтического эффекта.
Таким образом, при разработке состава и технологии любого лекарственного препарата особое внимание следует уделять способности высвобождения действующего вещества, которая, как показано на примерах, в значительной степени зависит от фармацевтических факторов, в аптечной практике — прежде всего от размера частиц, правильного выбора вспомогательных веществ, технологии лекарственных форм.
Контрольные вопросы
1. Какова роль биофармации в разработке терапевтически эффек
тивных лекарственных препаратов?
2. Какова зависимость между фармацевтическими факторами и
эффективностью лекарственных форм?
3. Как влияет размер частиц лекарственных веществ на кинетику
их высвобождения?
4. Какова взаимосвязь между эффективностью действия лекар
ственных препаратов и физическим состоянием лекарственных
веществ?
5. От каких условий зависит оптимальное измельчение лекарствен
ных веществ?
6. Каково влияние вспомогательных веществ на терапевтическую
эффективность лекарственных препаратов?
7. Какова взаимосвязь факторов, от которых зависит рациональный
выбор основ для мазей и суппозиториев, и максимальное высво
бождение лекарственных веществ?
8. Какие факторы, с точки зрения биофармации, обеспечивают в
аптечной практике рациональную технологию лекарственных
препаратов?
Приведите конкретные примеры.
Гл ав а 4
