Изотермический процесс
Процесс, протекающий при постоянной температуре, называется изотермическим. Линия, изображающая изотермический процесс графически,
называется изотермой и в p-v – диаграмме представляет собой гиперболу, которая соединяет точки начального и конечного состояния газа (рис. 1.1.).
Для изотермического процесса идеального газа
p1v1 = p2v2 , (1.19)
или
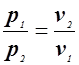 . (1.20)
. (1.20)
При T = const количество подведенной к рабочему телу теплоты численно равно работе изменения объема, т.е.
qt1-2 = l = p1v1 ln 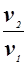 = p1v1 ln
= p1v1 ln 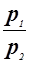 . (1.21)
. (1.21)
Энтальпия и внутренняя энергия идеального газа в изотермическом процессе не меняются и равны нулю
dh=0; du=0.
Изотермический процесс на T-s – диаграмме изображается прямой, параллельной оси абсцисс (рис.1.1.).
Изменение энтропии определится из следующего уравнения:
S2-S1=R ln 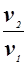 = R ln
= R ln 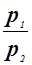 . (1.22)
. (1.22)
Теплоту, участвующую в изотермическом процессе, можно определить по формуле:
q = T(S2-S1). (1.23)
Адиабатный процесс
Адиабатным называется процесс, в котором к системе не подводится и от системы не отводится теплота, т.е. процесс протекает без теплообмена с окружающей средой, поэтому
dq = 0. (1.24)
Обратимый адиабатный процесс можно осуществить в цилиндре с абсолютно нетеплопроводными стенками при бесконечно медленном перемещении поршня. В общем случае для обратимого процесса
dq = T·ds, (1.25)
поэтому для обратимого адиабатного процесса
ds = 0 и s = const, (1.26)
т.е. энтропия системы сохраняется постоянной. Обратимый адиабатный процесс является одновременно изоэнтропным процессом.
Уравнение адиабаты идеального газа записывается в следующем виде:
Pvk = const, (1.27)
где k – показатель адиабаты.
На диаграмме p-v адиабата протекает круче изотермы и является неравнобокой гиперболой (рис.1.1.), а на диаграмме T-s изображается вертикальной прямой.
Из уравнения адиабаты следует, что



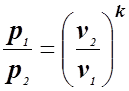
 и
и 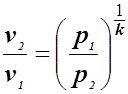 . (1.28)
. (1.28)
Эти выражения дают возможность получить соотношения между температурами и объемами
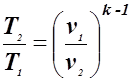 , (1.29)
, (1.29)
или между температурами и давлениями
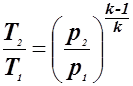 . (1.30)
. (1.30)
Работа при адиабатном процессе совершается только за счет уменьшения внутренней энергии
l = u1-u2 (1.31)
и её можно определить из следующих выражений:
l = 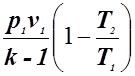 ; (1.32)
; (1.32)
l = 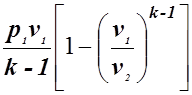 ; (1.33)
; (1.33)
l = 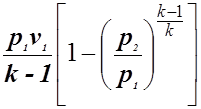 . (1.34)
. (1.34)
Все записанные выше зависимости между p, T, v справедливы при условии k = const. В реальных процессах показатель адиабаты k = 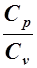 зависит от температуры. Тогда в расчетах принимают среднее значение k, которое соответствует изменению температуры в процессе
зависит от температуры. Тогда в расчетах принимают среднее значение k, которое соответствует изменению температуры в процессе
k = CP
Политропные процессы
Политропным процессом является такой термодинамический процесс изменения параметров состояния рабочего тела, при котором в течение всего процесса теплоемкость с и показатель политропы n, который может иметь любое значение в пределах от - ∞ до + ∞, остаются постоянными.
Уравнение политропного процесса имеет вид
pv 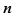 = const, (1.36)
= const, (1.36)
где n – показатель политропы.
Политропный процесс является обобщающим по отношению к рассмотренным термодинамическим процессам – изохорному, изобарному, изотермическому, адиабатному. Каждому частному процессу соответствует следующее значение величины показателя политропы n:
изохорному – n = ± ∞;
изобарному – n = 0;
изотермическому – n = 1;
адиабатному – n = k = const.
Физический смысл показателя политропы определяется следующим уравнением :
12
n = 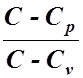 . (1.37)
. (1.37)
Значения показателя политропы n определяет расположение и характер протекания политропного процесса (рис.1.1.).
Связь между параметрами газа в двух состояниях при политропном процессе выражается формулами
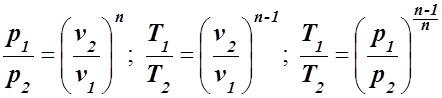 (1.38)
(1.38)
