Количественное определение микроорганизмов
СЕВЕРНЫЙ ГОСУДАРСТВЕННЫЙ МЕДИЦИНСКИЙ УНИВЕРСИТЕТ
КУРС ФАРМАЦИИ КАФЕДРЫ ФАРМАКОЛОГИИ
ОСОБЕННОСТИ АНАЛИЗА ГОТОВЫХ ЛЕКАРСТВЕННЫХ ФОРМ
( Часть II)
Методические указания
К лабораторным занятиям по фармацевтической химии
Для студентов IV курса фармацевтического факультета
(8 часов)
Архангельск 2006
УДК
Авторы: канд. фарм. наук Струсовская О.Г.
Рецензенты: доктор мед. наук, доц. Айвазова Е.А.
доктор мед наук, профессор Буюклинская О.В.
УТВЕРЖДЕНО
на заседении ЦМС СГМУ
«__»____________2006 г
председатель ЦМС
проф…………………………….
Методические указания ставят своей целью более глубокое усвоение студентами особенностей анализа готовых лекарственных форм: мазей, паст, линиментов и суппозиториев, целенаправленное приобретение умений и навыков будущего специалиста.
Лабораторная работа 1.
Тема: Анализ мазей заводского изготовления.
Цель занятия: Изучение особенностей анализа мазей, паст и линиментов.
Объекты:
1. Мазь состава: кислоты салициловой - 13,33
кислоты бензойной - 6,67
вазелина - 80,00;
2. Мазь цинковая;
3. Линимент стрептоцида 5%;
4. Паста салицилово-цинковая.
Литература:
1. Государственная фармакопея ХI издания.- М.: Медицина, 1990.-вып. 2, с. 154-160.
2. Лекционный материал.
3. Методические указания «Особенности анализа готовых лекарственных форм».-Архангельск.-2006.
4. Беликов В.Г. Фармацевтическая химия. Ч. 2. Специальная фармацевтическая химия.- Пятигорск, 1996.- С. 182-185, 267-268.
Вопросы для самоподготовки:
1. Каковы принципы классификации мягких лекарственных форм?
2. Дайте определение суппозитория и приведите классификацию.
3. Дайте определение мазей и приведите их классификацию.
4. Какие по ГФ ХI особенности анализа суппозиториев вы знаете?
5. Какие по ГФ ХI особенности анализа мазей, паст и линиментов вы знаете?
6. Какие реакции можно использовать для идентификации ингредиентов изучаемых лекарственных форм?
7. Перечислите физико-химические и объемные методы анализа, которые можно использовать для количественного определения ингредиентов анализируемых лекарственных форм.
План занятия:
1. Входной контроль.
2. Теоретический разбор материала:
3. Распределение индивидуальных заданий.
4. Самостоятельная работа студентов:
4.1. Выполнение анализа мазей, паст, линиментов.
5. Проверка полученных результатов.
6. Оформление протокола по результатам анализа.
7.Устный итоговый контроль.
Практические умения к занятию №1
Анализ мазей, паст и линиментов заводского изготовления
При выполнении анализа студент должен уметь:
1. отвешивать мазь, пасту или линимент для анализа;
2. проводить извлечение действующего вещества из мазевой основы;
3. идентифицировать действующие вещества в мазях, линиментах, пастах и проводить их количественное определение;
4. рассчитывать количественное содержание веществ и отклонения в их содержании;
5. делать заключение о соответствии мазей, паст и линиментов требованиям НД;
6. решать задачи
с этой целью на занятии студент должен закрепить следующие умения:
- проверять упаковку, маркировку и срок годности лекарственных препаратов в соответствии с требованиями НД;
- делать заключение о соответствии внешнего вида лекарственной формы требованиям НД;
- устанавливать подлинность лекарственных веществ в лекарственных формах;
- проводить количественное определение действующих веществ и соответствующие расчеты;
- делать заключение о качестве мазей, линиментов, паст в соответствии с требованиями НД.
Информационный блок
МАЗИ
Мази - мягкая лекарственная форма, предназначенная для нанесения на кожу, раны и слизистые оболочки. Мази состоят из основы и лекарственных веществ, равномерно в ней распределенных. По типу дисперсионных систем различают мази гомогенные (сплавы, растворы), суспензионные, эмульсионные и комбинированные, а в зависимости от консистентных свойств - собственно мази, пасты, кремы, гели и линименты.
Для приготовления мазей используют основы:
- липофильные (вазелин, сплавы углеводородов), жировые (природные, гидрогенизированные жиры и их сплав с растительными маслами и жироподобными веществами), силиконовые и др.; и гидрофильные – гели высокомолекулярных углеводов и белков (эфиры целлюлозы, крахмала, желатина, агара), гели неорганических веществ (бентонита), гели синтетических высокомолекулярных соединений (полиэтиленоксида, поливинилпирролидона и т.д.);
- гидрофильно-липофильные – безводные сплавы липофильных основ с эмульгаторами (сплав вазелина с ланолином или с другими эмульгаторами);
- эмульсионные основы типа вода/масло (сплав вазелина с водным ланолином) и масло/вода ( в качестве эмульгаторов используют натриевые, калиевые соли жирных кислот, твин-80) и др.
Мази изготавливают на основе, указанной в частной статье.
Требования, предъявляемые к мазям, обусловлены как способом применения, так и сложностью состава этой лекарственной формы. Для достижения необходимого терапевтического эффекта и точности дозирования, лекарственные вещества в мазях должны быть максимально диспергированы и равномерно распределены по всей массе мази. Поэтому согласно общих требований Государственной Фармакопеи ХI издания необходимо определение размера частиц.
МЕТОД ОПРЕДЕЛЕНИЯ РАЗМЕРА ЧАСТИЦ ЛЕКАРСТВЕННЫХ ВЕЩЕСТВ В МАЗЯХ
Размер частиц лекарственных веществ в мазях определяют на биологическом микроскопе, снабженном окулярным микрометром МОВ-I при увеличении окуляра 15Х и объектива 8Х. Цену деления окулярного микрометра выверяют по объект-микрометру для проходящего света (ОМП). Пробу мази отбирают, как указано в статье «Отбор проб лекарственных средств», и она должна составлять не менее 5 г.
Если концентрация лекарственных веществ в мазях превышает 10 %, то их разбавляют соответствующей основой до содержания около 10 % и перемешивают. При отборе проб следует избегать измельчения частиц.
Методика определения. Из средней пробы мази берут навеску 0,05 г и помещают на необработанную сторону предметного стекла. Другая сторона предметного стекла обработана следующим образом: на середине его алмазом или каким-либо другим абразивным материалом наносят квадрат со стороной около 15 мм и диагоналями. Линии окрашивают с помощью карандаша по стеклу. Предметное стекло помещают на водяную баню до расплавления основы, прибавляют каплю 0,1 % раствора судана III для жировых, углеводородных и эмульсионных основ типа вода/масло или 0,15% раствора метиленового синего для гидрофильных и эмульсионных основ типа масло/вода и перемешивают.
Пробу накрывают покровным стеклом (24 Х 24 мм), фиксируют его путем слабого надавливания и просматривают в 4 полях зрения сегментов, образованных диагоналями квадрата. Для анализа одного препарата проводят 5 определений средней пробы. В поле зрения микроскопа должны отсутствовать частицы, размер которых превышает нормы, указанные в частных статьях.
ОТБОР ПРОБ (ВЫБОРОК) ЛЕКАРСТВЕННЫХ СРЕДСТВ
Заключение о качестве лекарственных средств производится на основании анализа пробы (выборки), отобранной в соответствии с приведенными ниже требованиями, если нет специальных указаний в частных статьях.
Общие правила
Пробы (выборки) отбирают от отдельных серий (партий) лекарственного средства.
Упаковочную тару (ящики, бутыли, барабаны, коробки и т. д.) подвергают наружному осмотру для проверки соответствия требованиям нормативно-технической документации.
Пробы (выборки) отбирают только из неповрежденных, укупоренных и упакованных согласно нормативно-технической документации упаковочных единиц.
При отборе проб (выборок) необходимо принимать меры предосторожности, учитывая токсичность, взрывоопасность, огнеопасность, гигроскопичность и другие свойства лекарственных средств, а также предохранять их от загрязнений.
При отборе проб (выборок) ядовитых и наркотических лекарственных средств следует руководствоваться правилами работы, предусмотренными соответствующими приказами, инструкциями и положениями, утвержденными Министерством здравоохранения РФ, а также с учетом требований частных статей на эти лекарственные средства.
Для проведения испытаний лекарственных средств на соответствие требованиям нормативно-технической документации проводят многоступенчатый отбор проб (выборок).
При многоступенчатом отборе пробу (выборку) образуют по ступеням и продукцию в каждой ступени отбирают случайным образом в пропорциональных количествах из единиц, отобранных в предыдущей ступени. Число ступеней определяется видом упаковки.
I ступень: отбор единиц упаковочной тары (ящиков, коробок, мешков и др.).
II ступень: отбор упаковочных единиц, находящихся в упаковочной таре (коробок, флаконов, банок и др.).
III ступень: отбор продукции в первичной упаковке (ампул, флаконов, туб, контурных упаковок и др.).
Для расчета отбора количества продукции на каждой ступени используют формулу 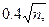 где n - количество упаковочных единиц данной ступени одной серии (партии). Полученное в результате подсчета по формуле дробное число округляют в сторону увеличения до целого числа, оно должно быть не менее 3 и не более 30.
где n - количество упаковочных единиц данной ступени одной серии (партии). Полученное в результате подсчета по формуле дробное число округляют в сторону увеличения до целого числа, оно должно быть не менее 3 и не более 30.
В случае недостаточного количества упаковочных единиц для проведения испытания повторно отбирают упаковочные единицы, как указано выше.
Из отобранных на последней ступени упаковочных единиц после контроля по внешнему виду берут пробу (выборку) для исследования препарата на соответствие требованиям нормативно-технической документации в количестве, необходимом для 4 полных физико-химических анализов (для контролирующих организаций - на шесть полных физико-химических анализов).
Порядок отбора проб (выборок) для контроля лекарственных средств на стерильность, пирогенность, токсичность, наличие веществ гистаминного действия и на другие специальные виды контроля указан в частных и соответствующих общих статьях ГФ XI.
Отобранную пробу (выборку) упаковывают и хранят в соответствии с требованиями нормативно-технической документации на лекарственное средство.
ОТБОР ВЫБОРОК ГОТОВЫХ ЛЕКАРСТВЕННЫХ СРЕДСТВ
(ШТУЧНОЙ ПРОДУКЦИИ)
Выборка готовых лекарственных средств должна состоять из ненарушенных заводских упаковочных единиц.
Отбор выборок готовых лекарственных средств для инъекций на отсутствие в них механических включений должен производиться согласно соответствующей документации, утвержденной. Министерством здравоохранения РФ.
Отбор выборки аэрозолей, азота закиси проводят в соответствии с требованиями частных статей.
Серия (партия) - количество продукции одного наименования, произведенной в одном технологическом цикле или в течение определенного интервала времени, в одних и тех же условиях и одновременно представленной на контроль. Качество серии (партии) должно быть удостоверено одним документом.
Проба - количество нештучной продукции, отобранной из контролируемой серии (партии), состоящее из нескольких точечных проб.
Выборка - количество штучной продукции, отобранной из контролируемой серии (партии).
Упаковочная единица – упаковка, содержащая установленное количество продукции.
Точечная проба – количество нештучной продукции, отобранной одномоментно.
Мази должны быть стабильны, и не содержать механических включений.
При анализе мазей определяют:
- массу содержимого упаковки, которая должна быть не менее, указанной на этикетке. Каждую банку или тубу взвешивают с точностью до 0,1 г и тщательно освобождают от содержимого. На тубе предварительно делают продольный разрез. Остатки препарата удаляют горячей водой, а влагу – фильтровальной бумагой и снова взвешивают.
- подлинность лекарственных веществ (как с помощью цветных качественных реакций, так и с помощью физико-химических констант и показателей);
- количественное содержание действующих веществ после выделения их из мазевой основы титриметрическими и физико-химическими методами;
- микробиологическую чистоту, если нет других указаний в частных фармакопейных статьях.
ИСПЫТАНИЕ НА МИКРОБИОЛОГИЧЕСКУЮ ЧИСТОТУ
Лекарственные средства (таблетки, капсулы, гранулы, растворы, экстракты, сиропы, мази и др.), не стерилизуемые в процессе производства, могут быть контаминированы микроорганизмами и поэтому должны быть испытаны на микробиологическую чистоту.
Испытание на микробиологическую чистоту включает количественное определение жизнеспособных бактерий и грибов, а также выявление определенных видов микроорганизмов, наличие которых недопустимо в нестерильных лекарственных средствах.
Испытание проводят в асептических условиях, применяя методы и питательные среды для контроля всех видов нестерильных лекарственных средств, а также сырья, используемого в их производстве.
Определяют действие лекарственного средства в отношении следующих тест-микроорганизмов:
Bacillus subtilis (Bacillus cereus),
Escherichia coli,
Pseudomonas aeruginosa,
Staphylococcus aureus,
Candida albicans.
Количественное определение микроорганизмов
Испытание проводят двухслойным агаровым методом в чашках Петри диаметром 90-100 мм. Образец лекарственного средства в количестве 10 г (мл) растворяют, суспендируют или эмульгируют в фосфатном буферном растворе рН 7,0 так, чтобы конечный объем раствора (суспензии, эмульсии) был 100 мл.
Посевы просматривают ежедневно.
Определение общего числа бактерий. Приготовленный раствор (суспензию, эмульсию) образца вносят по 1 мл в каждую из двух пробирок с 4 мл расплавленной и охлажденной до температуры от 45 до 50º С среды №1.
Среда № 1:
пептона ферментативного сухого 10 г
натрия хлорида 5 г
глюкозы 1 г
агара микробиологического 13 г
мясной воды (1:2) 1000 мл
Быстро перемешивают содержимое пробирки и переносят в чашку Петри, содержащую 15-20 мл застывшей питательной среды №1. Быстрым покачиванием чашки Петри равномерно распределяют верхний слой агара. После застывания среды чашки переворачивают и инкубируют в течение 5 сут при температуре от 30 до 35º С. Через 48 ч и окончательно через 5 сут подсчитывают число бактериальных колоний на двух чашках, находят среднее значение и, умножая его на показатель разведения, вычисляют число бактерий в 1 г (мл) образца.
Для получения достоверных результатов учитывают только те чашки, на которых выросло от 30 до 300 колоний. Если при разведении образца 1: 10 нет роста, результаты отмечают следующим образом: «В 1 г (мл) лекарственного средства (сырья) менее 10 бактерий».
Если число колоний на чашке превышает 300, делают ряд дальнейших последовательных разведений образца (1:100, 1:1000 и т. д.), выбирая для посева разведение, наиболее соответствующее указанному выше уровню.
Определение общего числа грибов. Испытание проводят двухслойным агаровым методом, используя среду №2.
Среда № 2 (Сабуро):
пептона ферментативного сухого 10 г
глюкозы 40 г
агара микробиологического 13 г
воды очищенной 1000 мл
Посевы инкубируют в течение 5 сут при температуре от 20 до 25º С. Через 72 ч и окончательно через 5 сут подсчитывают общее число колоний дрожжевых и плесневых грибов на двух чашках. Находят среднее значение и, умножая его на показатель разведения, т. е. на 10, вычисляют число грибов в 1 г (мл) образца. В случае, если число колоний грибов на чашке превышает 300, делают ряд дальнейших разведений образца. На чашке учитывают все колонии грибов, даже если их число менее 30.
Мази выпускают в тубах и склянках, если необходимо, то темного стекла.
Хранение. Как правило, мази хранят в прохладном, сухом, защищенном от света месте, если нет других указаний в частных статьях.
ЛИНИМЕНТЫ
Линиментами или втираниями называется обособленная группа жидких лекарственных веществ для наружного употребления, применяемых чаще всего путем втирания в кожу. В настоящее время линименты рассматривают как категорию жидких мазей.
Большинство линиментов – это текучие жидкости, обладающие различной степенью вязкости - от легкоподвижных до имеющих консистенцию жидкой сметаны или густых сливок.
Небольшая часть линиментов обладает сравнительно плотной консистенцией и представляет собой механически непрочные системы, легко плавящиеся при температуре человеческого тела.
По физико-химической природе линименты представляют собой дисперсные системы, образованные в жидких дисперсионных средах. По характеру дисперсионной среды линименты удобно классифицировать на четыре группы: жирные, спиртовые, мыльно-спиртовые, вазолименты.
Жирные линименты. Эта группа втираний характеризуется наличием в их составе какого-нибудь жира или жироподобного вещества. Жирные линименты могут быть гомогенными или гетерогенными.
Спиртовые линименты. В качестве спиртовых линиментов используются лекарственные спирты, их смеси, а также различные приготовленные по мере надобности спиртовые растворы лекарственных веществ.
Сапонименты. В состав сапониментов входят спиртовые растворы мыла, играющего роль дисперсионной среды.
Вазолименты. Это разновидность линиментов, приготовляемых на основе вазелинового масла.
Сложные вазолиментыпредставляют собой растворы различных препаратов, растворимых в жирах, в обыкновенном или простом вазолименте.
Линименты должны быть стабильны и не содержать механических включений.
При анализе линиментов определяют:
массу содержимого упаковки, которая должна быть не менее указанной на этикетке;
подлинность лекарственных веществ, как с помощью цветных качественных реакций, так и с использованием физико-химических констант и показателей;
количественное содержание действующих веществ (после выделения их из основы).
В случае прямого титрования лекарственного вещества в мазях, линиментах и пастах и отсутствия контрольного опыта на индикатор или титрованный раствор, содержание действующего вещества (g, г) рассчитывают по формуле:

где Р- 100 г мази или 1 г мази ( в зависимости от указаний НД).
Задачи и тесты для самостоятельного решения:
1. Рассчитайте теоретический объем 0,1 М раствора натрия нитрита (К=l,00), который пошел на титрование 2,0635 г линимента стрептоцида 5% (Мr стрептоцида=172,2), если содержание стрептоцида в линименте составило 5,05%.
2. Соответствует ли мазь цинковая 50,0 г требованиям ФС 42-3663-97 по массе содержимого упаковки, если масса банки с мазью составила 198,3 г, а пустой банки 149,6 г. Допустимое отклонение ±4%.
3. Для количественного определения цинка оксида в мази цинковой 0,4237 г лекарственной формы поместили в колбу вместимостью 100 мл. Прибавили 5 мл кислоты хлористоводородной разведенной и 25 мл воды. Раствор нагрели до расплавления основы, охладили, прибавили 10 мл хлороформа и титровали 0,05 М раствором трилона Б (К=0,99). Объем титранта 10,75 мл. Мr цинка оксида равна 81,36. Рассчитайте содержание цинка оксида в мази (%).
4. Соответствует ли мазь состава: кислоты салициловой 13,33 г, кислоты бензойной 6,67 г, вазелина 80,0 г, требованиям ФС 42-2282-84 по количественному содержанию салициловой кислоты, если из 0,9903 г мази извлечения проводили водно-спиртовой смесью, после разделения слоев водный слой помещали в мерную колбу вместимостью 100 мл и доводили до метки. Затем к 25 мл раствора прибавляли 25 мл 0,1 М раствора бромата калия и определение проводили с помощью обратного броматометрического титрования. На титрование основного опыта пошло 29,8 мл, а контрольного опыта 15,3 мл 0,1 М раствора натрия тиосульфата (К=1,00). Mr салициловой кислоты 138,0. В препарате должно содержаться от 12,0 г до 14,6 г салициловой кислоты.
5. Рассчитайте теоретический объем 0,1 М раствора едкого натра (К=l,01), который пойдет на титрование навески мази салициловой 3% массой 1,0 г. Мr кислоты салициловой 138,1.
6. С каким реактивом цинка оксид образует белый студенистый осадок?
а) (NH4)2SO4
б) КзFе(СN)6, НСl
в) NН40H (избыток)
г) K4Fe(CN)6, НС}
д) NaOH (избыток).
7. Количественное определение кислоты салициловой в мази по ФС выполняют методом броматометрии:
KBrO3 + 5KBr = 6HCl  3Br2 + 6KCl + 3H2O
3Br2 + 6KCl + 3H2O
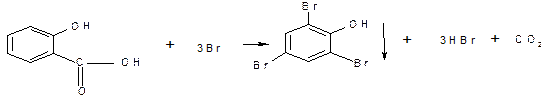
Br2 = 2KI  2KBr = I2
2KBr = I2
I2 + 2Na2S2O3  2NaI + Na2S4O6
2NaI + Na2S4O6
Чему равен фактор эквивалентности кислоты салициловой?
а) 1/3;
б) 1/6;
в) ½
г)1/4
8. Какой индикатор по ФС используют при количественном определении мази цинковой?
а) фенолфталеин
б) тропеолин 00;
в) кислотный хром черный специальный;
г) крахмал.
9. Укажите реактивы, с которыми кислота салициловая образует окрашенные продукты:
а) FeCl3
б) 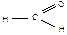 , H2SO4 конц.
, H2SO4 конц.
в) CuSO4, NaOH
г) 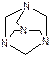 , H2SO4, конц.
, H2SO4, конц.
а) правильный ответ: 1,2,3,4
б) правильный ответ: 1,2,3
в) правильный ответ: 1,2
г) правильный ответ: 1,3,4.
