Гемоглобиновая буферная система
Наибольшей мощностью обладает гемоглобиновый буфер, который можно рассматривать как часть белкового. На него приходится до 30% всей буферной емкости крови.
В буферной системе гемоглобина существенную роль играет гистидин, который содержится в белке в большом количестве.
Изоэлектрическая точка гистидина равна 7,6, что позволяет гемоглобину легко принимать и легко отдавать ионы водорода при малейших сдвигах физиологической рН крови (в норме 7,35-7,45).
Данный буфер представлен несколькими подсистемами:
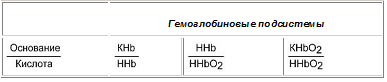
Пара ННb/ННbО2 является основной в работе гемоглобинового буфера.
Соединение ННbО2 является более сильной кислотой по сравнению с угольной кислотой, HHb - более слабая кислота, чем угольная. Установлено, что ННbО2 в 80 раз легче отдает ионы водорода, чем ННb.
Присоединение ионов водорода к остатку гистидина дезоксигемоглобина выглядит так:
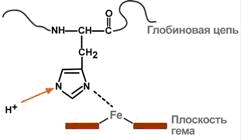
Работа гемоглобинового буфера неразрывно связана с дыхательной системой (к вопросу о значении пранаямы! - ALG)
В легких после удаления СО2 (угольной кислоты) происходит защелачивание крови.
При этом присоединение О2 к дезоксигемоглобину H-Hb образует кислоту ННbО2 более сильную, чем угольная. Она отдает свои ионы Н+ в среду, предотвращая повышение рН:
Н-Hb + O2 > [H-HbO2] > НbO2 + Н+
В капиллярах тканей постоянное поступление кислот (в том числе и угольной) из клеток приводит к диссоциации оксигемоглобина НbO2 (Эффект Бора) и связыванию ионов Н+ в виде Н-Hb:
НbO2+ Н+ > [H-HbO2] > Н-Hb + O2
Длительная стабилизация сдвигов рН
Это так называемая физиологическая компенсация нарушений кислотно-основного состояния, которая происходит прежде всего за счет работы дыхательной системы и почек, и в меньшей степени - за счет печени и костной системы.
Дыхательная система
Легочная вентиляция обеспечивает удаление угольной кислоты, образованной при функционировании бикарбонатной буферной системы. По скорости реакции на изменение рН – это вторая система после буферных систем.
Дополнительная вентиляция легких приводит к удалению СО2, а значит и Н2СО3, и повышает рН крови, что компенсирует закисление межклеточной жидкости и плазмы крови продуктами метаболизма, в первую очередь, органическими кислотами.
Сдвиги значений рО2 не являются сильно значимыми для изменения легочной вентиляции. Только снижение рО2 до 8 кПа в артериальной крови (норма 11,04-14,36 кПа или 83-108 мм рт.ст.) приводит к увеличению активности дыхательного центра.
Более существенным фактором для активации дыхательной системы является концентрация ионов Н+.
Накопление ионов Н+ в крови уже через 1-2 минуты вызывает максимальную (для данной их концентрации) стимуляцию дыхательного центра, повышая его активность до 4-5 раз, что приводит к снижению рСО2 до 10-15 мм рт.ст.
И, наоборот, снижение кислотности крови понижает активность дыхательного центра на 50-75%, рСО2 при этом способен возрастать до 60 мм рт.ст и выше.
Костная ткань
Это наиболее медленно реагирующая система. Механизм ее участия в регуляции рН крови состоит в возможности обмениваться с плазмой крови ионами Са2+ и Na+ в обмен на протоны Н+. Происходит растворение гидроксиапатитных кальциевых солей костного матрикса, освобождение ионов Са2+ и связывание ионов НРО42– с Н+ с образованием дигидрофосфата, который уходит с мочой.
Параллельно при снижении рН (закисление) происходит поступление ионов H+внутрь остеоцитов, а ионов калия – наружу.
Печень
Существенную, но пассивную роль в регуляции кислотно-основного состояния крови берет на себя печень, в которой происходит метаболизм низкомолекулярных органических кислот (молочная кислота и др). Кроме этого, кислые и щелочные эквиваленты выделяются с желчью.
Почки
Развитие почечной реакции на смещение кислотно-основного состояния происходит в течение нескольких часов.
Регуляция концентрации ионов H+ осуществляется опосредованно, через потоки ионов Na+, движущихся по градиенту концентрации, и через перераспределение потоков ионов К+ и Н+, которые выходят из эпителиоцитов (секретируются) в обмен на ионы Na+.
Также для обеспечения электронейтральности внутри- и внеклеточной жидкости при реабсорбции ионов Na+ усиливается реабсорбция ионов Cl–, однако их не хватает, поэтому возникает необходимость в усилении реабсорбции и дополнительном синтезе ионов HCO3– (и вот тут-то как раз и играет свою роль сода - бикарбонат натрия NaHCO3. Если мы поставляем организму дополнительное количество ионов HCO3 посредством соды, мы существенно снижаем нагрузку с почек и помогаем им в работе - ALG)
В почках активно протекают три процесса, связанных с уборкой кислых эквивалентов. Благодаря этим процессам рН мочи в состоянии снижаться до 4,5-5,2 :
1. Реабсорбция бикарбонатных ионов HCO3–.
2. Ацидогенез – удаление ионов Н+ с титруемыми кислотами (в основном в составе дигидрофосфатов NaH2PO4).
3. Аммониегенез – удаление ионов Н+ в составе ионов аммония NH4+.
