Образование мочевины
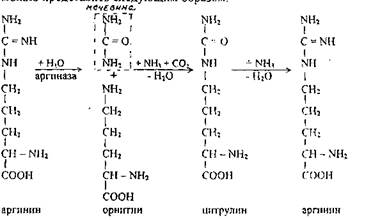
Синтез мочевины - это главный путь обезвреживания аммиака в оранизме. Мочевина - конечный азотистый продукт, выделяющийся с мочой у человека и млекопитающих. Образование ее происходит в печени. В 1932 г. возникла теория синтеза мочевины, известная под названием цикла Кребса, согласно которой в синтезе мочевины принимают участие 3 аминокислоты - аргинин, орнитин и цитрулин. Причем образование мочевины по циклу Кребса происходит в срезах печени в аэробных условиях. Схематически образование мочевины по циклу Кребса можно представить следующим образом:
Суммирование реакций цикла образования мочевины приводит к следующему уравнению:
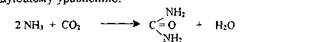
Образование мочевины по указанному циклу получило свое подтверждение и является общепринятым. Однако в последствии цикл Кребса подвергся существенной детализации. Из приведенных выше реакций можно видеть, что в образовании мочевины участвуют свободный аммиак и углекислый газ. Между тем известно, что аммиак, по мере своего образования в тканях, устраняется с образованием глутамина. Далее известно, что реакции переаминирования, которые активно происходят в различных тканях, приводят к тому, что аминогруппы подвергающихся распаду аминокислот не освобождаются в виде аммиака, а переносятся на кетокислоты. Естественно возникает вопрос, откуда же в печени берется аммиак, необходимый для синтеза мочевины? Ответ на этот вопрос дают проведенные Ратнер с сотр. исследования, показывающие, что в синтезе мочевины помимо свободного аммиака участвуют аминогруппы, входящие в состав аминокислот, в частности аспарагиновой, без предварительного отщепления их в виде аммиака. Таким образом, последовательность синтеза мочевины можно представить следующими реакциями:
1) Аммиак взаимодействует с углекислым газом под действием
фермента карбамоилфосфатсинтетазы, образуется карбамоилфосфат
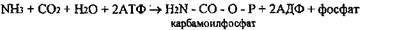
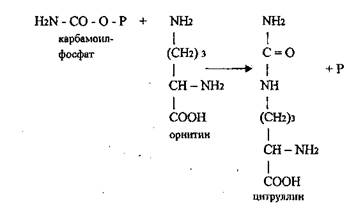
2) Карбамоилфосфат взаимодействует с орнитином, образуется
цитруллин и фосфат (катализатор - орнитин - карбамоилфосфат-
трансфераза)
3) Цитруллин взаимодействует с аспарагиновой кислотой с
образованием аргининсукцината:
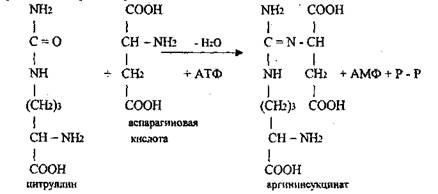
Катализирует реакцию аргининсукцинатсинтетаза.
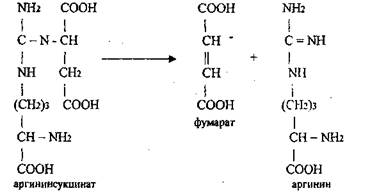
4) Аргининсукцинат расщепляется аргининсукцинатлиазой на фумарат
и аргинин:
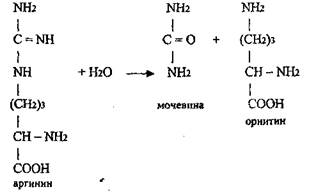
5) Аргинин под действием аргиназы расщепляется гидролитически на
мочевину и орнитин:
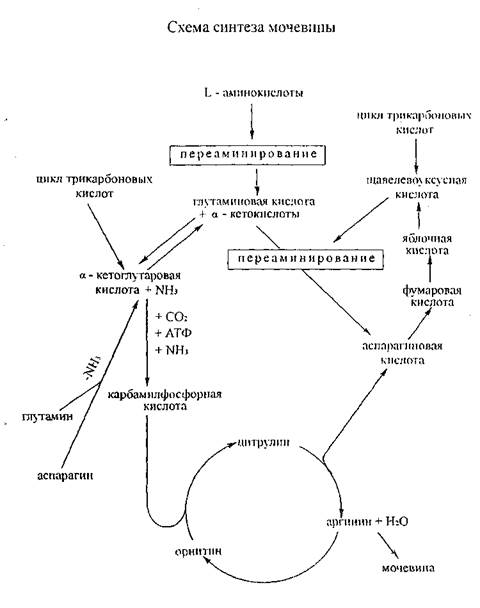 |
Из приведенных реакций можно заключить, что одна группа NH2 молекулы мочевины образуется из аммиака, а другая из аминогруппы аспарагиновой кислоты. Отсюда следует вывод, что аминогруппы 50% аминокислот, подвергающихся в организме превращению путем переаминироваиия (через глутаминовую кислоту), включаются в шавелевоуксусную кислоту с образованием аспарагиновой кислоты. Аминогруппа аспарагиновой кислоты, как мы видели, непосредственно используется для синтеза мочевины. Использование азота аминокислот (аминогрупп) для синтеза мочевины видно из схемы, показывающей связь между синтезом мочевины и циклом трикарбоновых кислот.
Обезвреживание аммиака в тканях может происходить и путем синтеза глутамина и аспарагина. Однако большая часть NH3 утилизируется за счет синтеза мочевины.
Обмен сложных белков
ОБМЕН НУКЛЕОПРОТЕИДОВ
В ЖКТ под действием соляной кислоты, пепсина, трипсина и др. ферментов от нуклеопротендов отщепляется белковая часть и гидролизуется до аминокислот. Простетическая группа - нуклеиновые кислоты - разрушаются до мононуклеотидов под действием нуклеаз. Мононуклеотнды частично всасываются, а большей частью под действием фосфатаз и нуклеотидаз расщепляются на составные компоненты: азотистые основания, пентозы и фосфорную кислоту, которые, как водорастворимые вещества, активно всасываются. Фосфорная кислота пополняет запасы фосфора в организме, пентозы принимают участие в процессах окисления и синтеза новых НК, а азотистые основания
подвергаются различным превращениям. Так пуриновые азотистые основания после дезаминирования превращаются в ксантин, а затем под действием ксантиноксидазы - в мочевую кислоту, которая выводится из организма почками.
Конечными продуктами распада пиримидиновых азотистых
оснований являются аммиак, CO2 и простые азотистые соединения. Так
урацил распадается на NH3, СО2 и b- аланин. Пути превращения NH3 и CО2
мы же рассматривали, а b-аланин участвует в синтезе КоА.
Одновременно с распадом в клетках осуществляется постоянный синтез нуклеиновых кислот. Это сложный процесс, в котором участвует большое число исходных соединений: пентозы, глицин, глутамин, аспарагиновая кислота, активная форма СО2, АТФ и соответствующие ферменты. В ходе синтеза образуются сначала мононуклеотиды: АМФ, ГМФ, УМФ, последнее соединение служит стартовым веществом для образования ТМФ и ЦМФ.
Для синтеза самих НК необходимы все типы нуклеотидтрифосфатов, набор ферментов и ДНК, на матрице которой строятся новые дочерние молекулы ДНК и молекулы РНК.
ОБМЕН ХРОМОПРОТЕИДОВ.
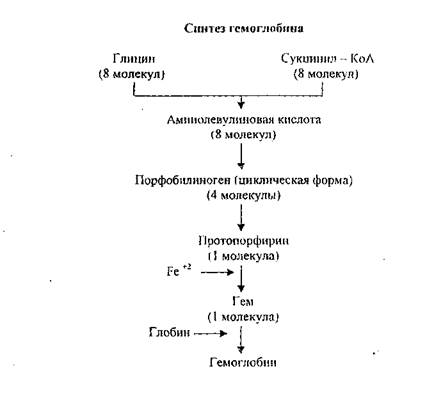
Из многих представителей хромопротеидов для человека наибольшее значение имеет гемоглобин, обмен которого мы и рассмотрим.
Поступающий с пищей гемоглобин (НЬ) в ЖКТ распадается на свои составные части - гем и глобин. Глобин гидролизуется до аминокислот, которые всасываются в кровь, а гем окисляется до гематина и выводится с калом, т.е. экзогенный гем не используется.
Обмен эндогенного Hb протекает весьма интенсивно и связан с периодом существования эритроцитов, в которых содержится весь НЬ. Этот период составляет 110 -120 дней, после чего эритроциты распадаются, процесс активно протекает в печени, селезенке, костном мозге и др. тканях РЭС. Часть же эритроцитов распадаегся в кровеносном русле, освободившийся при этом НЬ адсорбируется в крови гаптоглобином и транспортируется в печень, где распадается по вышеуказанной схеме.
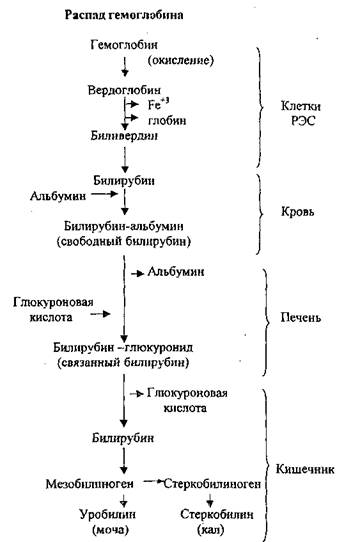
В клетках РЭС НЬ вначале окисляется под действием гем-оксигеназы до вердоглобина (зеленого цвета). Последний спонтанно (самопроизвольно) распадается на свои составные части: глобин, Fe3+ и оставшуюся часть гема-биливердин (пигмент зеленого цвета). Глобин гидролизуется до аминокислот. Fe3+ захватывается трансферрином и кровью доставляется в печень, где освобождается от белка-переносчика и откладывается про запас в виде ферритина (соединение Fe с особым белком). Этот комплекс по мере надобности распадается, Fe вновь адсорбируется трансферрином, доставляется в клетки, где участвует в синтезе НЬ, цитохромов и пр.
Биливердин восстанавливается в билирубин- пигмент желто-красного цвета, который является водонерастворимым и весьма токсичным веществом. Поэтому он быстро выводится из клеток РЭС, поступает в кровь, где адсорбируется альбумином, образуя растворимый в воде и нетоксичный комплекс, называемый свободным билирубином (непрямым). Он транспортируется в печень, где распадается и билирубин попадает в гепатоциты. Здесь он взаимодействует с активной формой глюкуроновой кислоты (УДФКГ) с образованием моно- и диглюкуронидбилирубина, являющегося нетоксичным иводорастворимым соединением, называемым связанным билирубином(прямым). Связанный билирубин поступает в желчный пузырь, входит в состав желчных пигментов, выделяется с желчью в кишечник, где от него отщепляется глюкуроновая кислота. Освободившийся билирубин подвергается воздействию ферментов микроорганизмов с образованием мезобилиногена, азатем – стсркобилиногена,который окисляетсякислородом воздухадо стеркобилинаи выводится с калом.Небольшая часть мезобилиногена всасывается в кровь и по воротной вене доставляется в печень, где расщепляется до диперролов (2 пиррольных кольца), которые задерживаются печенью ине поступают в общий кровоток. Большая же часть мезобилиногена, превратившаяся в стеркобилиноген, в нижних отделах толстой кишки всасывается в кровь и через геморроидальные вены попадает в систему большого круга кровообращения, а затем выводится с мочой в виде уробилиногена,окисляющегося на воздухе в уробилин.
Таков в обших чертах основной путь распада НЬ.
Но для нормальной жизнедеятельности организма постоянно требуется определенное количество НЬ, синтез которого осуществляется по следующей схеме.