Соединения стероидной природы: холестерин, стероидные гормоны, желчные кислоты. Представление о химическом строении и биологической роли
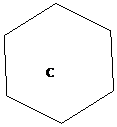
Стероиды – это производные тетрациклического насыщенного углеводорода циклопентанпергидрофенантрена, метилированного в положениях 10, 13. Структура имеет 3 шестичленных кольца и 1 пятичленные. Обозначение колец: А, В, С, D. Нумерация начинается с А-кольца. В положениях 10, 13- СН3 – группы. СН3


 12 17
12 17
 11 13 16
11 13 16
СН3 D



 1 9 14 15
1 9 14 15
2 8
3 7
4 6
Рис. 12. Структура циклопентанпергидрофенантрена
Важнейшим представителем этого класса липидов является холестерин (и его производные).
 Холестеринимеет в 17 положении 8-углеродную боковую цепь; в 3 положении – ОН-группу, между 5 и 6 углеродными атомами – двойная связь..
Холестеринимеет в 17 положении 8-углеродную боковую цепь; в 3 положении – ОН-группу, между 5 и 6 углеродными атомами – двойная связь..
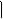 |
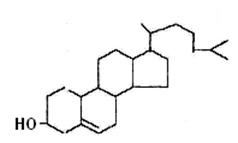 |
Рис. 13.Структура холестерина (холестерола)
Функции холестерина:
1. Входит в состав клеточных мембран.
2. Предшественник в синтезе других стероидов:
а) жёлчных кислот;
б) стероидных гормонов (глюкокортикоидов, минералкортикоидов, половых гормонов (андрогенов и эстрогенов)).
3. Витамин D3 (антирахитический) синтезируется в коже при УФ-излучении вследствие разрыва В-цикла. Витамин D3 является предшественником гормона кальцитриола, регулирующего обмен Са2+ в организме и остеогенез (формирование костной ткани).
Жёлчные кислоты
Жёлчные кислоты синтезируются из холестерина в печени. Известны четыре желчных кислоты: холевая (3,7,12 – тригидроксихолановая кислота), хенодезоксихолевая (3, 7 – дигидроксихолановая кислота), дезоксихолевая (3, 12,- дигидроксихолановая кислота) и литохолевая (3-гидроксихолановая кислота) (рис. 19). Первые две ЖК синтезируются в печени человека, а две другие - в кишечнике под действием ферментов микроорганизмов.
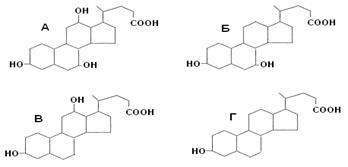 |
Рис. 14. Структуры желчных кислот (А – холевая, Б-хенодезоксихолевая, В – дезоксихолевая, Г – литохолевая)
Жёлчные кислоты соединяются с аминокислотами глицином (Н2N-СН2-СООН) или таурином (Н2N-СН2-ОSО3Н),образуя парные кислоты - гликохолевую, таурохолевую и другие. В конъюгированном виде они поступают в кишечник и участвуют в переваривании липидов (рис. 15).
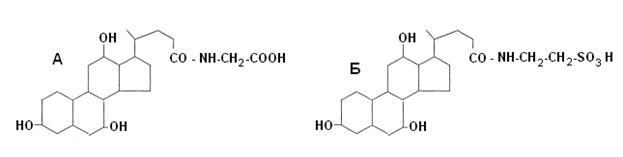
Рис. 15. Конъюгированные желчные кислоты (А – гликохолевая, Б – таурохолевая)
Стероидные гормоны
Стероидные гормоны – физиологически активные вещества ряда стероидов, вырабатываемые железами внутренней секреции. По химическому строению и биологическому действию различают гормоны коры надпочечников (кортикостероиды), мужские половые гормоны (андрогены) и женские половые гормоны (гестагены и эстрогены). Каждому типу стероидных гормонов соответствует углеводород, который составляет основу их углеродного скелета. Для кортикостероидов и гестагенов это – прегнан, андрогенов – андростан, эстрогенов – эстран.
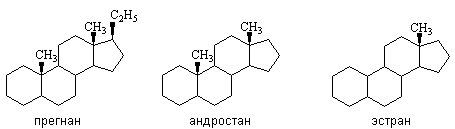
На рисунке приведены примеры некоторых стероидных гормонов, вырабатываемые разными железами внутренней секреции.
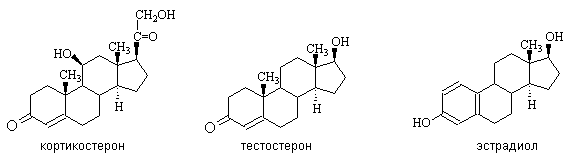
Кортикостерон – гормон коры надпочечников, регулирует углеводный обмен, действует как антагонист инсулина, повышая содержание сахара в крови. Тестостерон – мужской половой гормон, стимулирует развитие вторичных половых признаков. Эстрадиол – женский половой гормон, контролирует менструальный цикл.
8. Особенности физико-химических свойств мембран, влияние факторов на изменение свойств, «текучесть» мембраны.
В живых клетках биологическая мембрана пребывает в жидкокристаллическом состоянии. В жидком кристалле сочетаются свойства кристалла (дальний порядок организации и двулучепреломление) и жидкости (текучесть и образование капель), что приводит к возникновению качественно новых свойств. Термин «жидкий кристалл» существует в науке с конца XIX в. В1888 г. ботаник Ф. Райнитцер синтезировал эфир холестерина (холестерилбензоат) и изучил его свойства. Оказалось, что при температуре (Т) ниже 145 °С он был твердым кристаллом, при Т > 178 °С − прозрачной жидкостью, а в промежутке между этими температурами − мутной жидкостью. В следующем году физик О. Леман при исследовании мутной жидкости холестерилбензоата (при 145 < Т < 178 °С) в поляризационном микроскопе обнаружил анизотропию (типичное свойство кристалла) и назвал это промежуточное (между кристаллом и жидкостью) состояние холестерилбензоата жидкокристаллическим. Позднее оно было обнаружено у многих веществ при разных температурах и других параметрах среды (рН, росм и т. д.).
Бимолекулярный слой фосфолипидов, образующий биомембраны, в физиологических условиях (при температуре тела, нормальных рН и ионном составе интерстиция и цитозоля) представляет собой жидкий кристалл.
При понижении температуры и под влиянием ряда других факторов фосфолипидный каркас биомембран приобретает свойства твердого (димерного) кристалла, сохраняя бимолекулярную (в профиле) структуру. В обоих состояниях молекулы фосфолипида имеют гексагональную упаковку в плоскости биомембраны, но плотность их упаковки различна. Например, молекула лецитина занимает в твердокристаллическом состоянии поверхность в 0,46 − 0,48 нм2, а в жидкокристаллическом − 0,6 − 0,8 нм2. Чем больше двойных связей в ненасыщенных жирных кислотах, входящих в состав фосфолипидов, тем ниже температура, при которой они становятся твердыми кристаллами.
В физиологических условиях текучесть биологических мембран уменьшается при повышении в них содержания холестерина, ионов кальция и магния. Двухвалентные ионы в зависимости от концентрации нейтрализуют в той или иной степени отрицательный заряд на головках фосфолипидов и ослабляют их взаимное отталкивание, что приводит к более плотной упаковке молекул в биомембране. Местные анестетики (новокаин и родственные ему соединения) повышают степень текучести клеточных мембран, влияя на их жидкокристаллическое состояние. Оно изменяется при росте и развитии клеток, а также при некоторых патологических состояниях (раке, дистрофиях и др.).
Характерным свойством жидких кристаллов (ЖК) является их способность к фазовым переходам, т. е. к преобразованию в твердые кристаллы (ТК) и возвращению в прежнее состояние (ЖК ←→TK) при определенных условиях. В биологических мембранах фазовые переходы происходят в физиологических условиях под действием ряда агентов (раздражителей). Важно, что это может совершиться не во всем объеме мембраны, а в небольших ее участках (там, где появляются такие агенты).
Фазовый переход: ЖК ←→ TK в фосфолипидном каркасе существенно изменяет свойства ферментов, каналов, переносчиков и других функционально значимых компонентов биомембраны, находящихся в том ее участке, где совершается кооперативный процесс. Там изменяется проницаемость, нарушаются биохимические реакции, рецепторные и другие процессы, которые приводят к сдвигам в физиологическом состоянии организма. Кстати говоря, самим мембранным белкам также свойственно жидкокристаллическое состояние, и они могут испытывать фазовый переход.
Количество молекул, образующих участок биомембраны, где совершается кооперативный процесс, называется размером кооперативной единицы. В однородной среде он больше, чем в неоднородной. Белки и холестерин, встроенные в более или менее однородный фосфолипидный каркас, нарушают его однородность и тем самым уменьшают размер кооперативной единицы. Так обеспечивается высочайшая степень локальности фазовых переходов в клеточных мембранах.
Природа жидкокристаллического состояния биомембран обусловлена необычайно высокой подвижностью мембранных компонентов.
Вязкость биомембран.Биомембрана как жидкокристаллическая структура с присущей ей текучестью характеризуется определенной вязкостью, которая измерена методами ЭПР (электронный парамагнитный резонанс) и дифференциальной сканирующей микрокалориметрии (ДСК). Результаты измерений вязкости разными методами совпали. Вязкость БМ составляет от 0,03 до 0,1 Па · с (30 − 100 мПа · с = 30 − 100 сП), т. е. в 30-100 раз больше, чем у воды, и примерно такая же, как у оливкового масла.
При изменении температуры, молекулярного состава и других параметров БМ меняется ее вязкость вследствие возникновения фазового перехода: жидкий кристалл ←→ твердый кристалл (структура в виде относительно жестких вытянутых палочек). При температуре 310 − 311 К фосфолипиды с ненасыщенными углеводородными цепями пребывают в жидкокристаллическом состоянии, а при замене на полностью насыщенные цепи они образуют двухмерный кристалл. Регулируя молекулярный (прежде всего, фосфолипидный) состав клеточных мембран, живой организм может изменять их фазовые состояния при постоянной температуре и, напротив, сохранять жидкокристаллическое состояние при понижении температуры. Последнее свойственно бактериям и растениям, заменяющим в своих клеточных мембранах насыщенные липиды на ненасыщенные при охлаждении. Так они сохраняют жидкокристаллическое состояние, а значит, нормальную вязкость и зависящую от нее проницаемость мембран при низкой температуре окружающей среды.
Смена фосфолипидного состава БМ на «морозоустойчивый» присуща и пойкилотермным животным, которые используют этот механизм для адаптации к холоду. Строгое постоянство температуры тела гомойотермных животных избавляет их от необходимости осуществлять столь серьезные молекулярные перестройки своих клеточных мембран. Из сказанного следует, что одним из важных достоинств гомойотермии (постоянства температуры) является постоянное поддержание БМ в жидкокристаллическом состоянии, обеспечивающем стабильность транспорта веществ через них. Интересно, что у пингвинов температура нижних конечностей падает в дистальном направлении и, соответственно, мембраны клеток все более обогащаются ненасыщенными жирными кислотами (в тканях стопы их гораздо больше, чем в тканях бедра).
Вязкость БМ претерпевает существенные изменения при многих заболеваниях, а также под действием электромагнитных излучений (особенно ионизирующих), ряда фармакологических препаратов, гормонов и некоторых других факторов. Во многих случаях влияние на вязкость клеточных мембран опосредовано изменением содержания в них холестерина. При нормальной температуре тела повышение содержания холестерина в БМ увеличивает их вязкость, а понижение − уменьшает ее. В этом причина разжижения мембран в клетках злокачественных опухолей (например, лейкоцитарных мембран при лейкозе). Вязкость всех клеточных мембран падает при тиреотоксикозе, а также под действием наркотических веществ (например, хлороформа). Возможно, что наркотический эффект непосредственно связан с изменением физико-химических свойств биомембран. Так, головастик, помещенный в раствор хлороформа, утрачивает двигательную активность и способность реагировать на стимуляцию. Его удается «оживить», уплотнив клеточные мембраны путем повышения атмосферного давления. Однако при слишком высоком давлении головастик снова теряет подвижность и чувствительность. Их можно восстановить, добавив в среду наркотик. Известно, что дыхательная смесь, содержащая наряду с кислородом газ, оказывающий на организм наркотизирующее воздействие при атмосферном давлении, теряет этот эффект на большой глубине.
Приведенный пример позволяет сделать вывод, что жизнеспособность организма страдает как при понижении, так и при повышении мембранной проницаемости, которая, в свою очередь, зависит от вязкости БМ. Ее оптимальные значения поддерживаются в клеточных мембранах, пребывающих в жидкокристаллическом состоянии.
Лабораторная работа:
1. Растворимость жиров в органических растворителях
В пробирку поместите 1 каплю масла и 5 капель этилового спирта. Встряхните пробирку – получается эмульсия масла в спирте. Добавьте еще 5 капель спирта и вновь встряхните. Жидкость не просветляется, что указывает на плохую растворимость масла в спирте. Нагрейте раствор до кипения и дайте отстояться (на дне образуется большая капля масла). Слейте мутную жидкость и вновь нагрейте. Жидкость станет прозрачной, но при охлаждении помутнеет.
Если же к 1 капле масла добавить 5 капель хлороформа или эфира, то происходит растворение масла.
Сделайте вывод о различной растворимости жиров в органических растворителях.
2. Омыление жиров.
В небольшую фарфоровую чашечку поместите 0,5 мл масла и 4 капли 35% р-ра едкого натра, стеклянной палочкой хорошенько размешайте щелочь с маслом до получения однородной эмульсии. Затем поставьте чашку на электрическую печь и при незначительном подогревании продолжайте помешивать. Пока не получится однородная, прозрачная, слегка желтоватая жидкость. Затем добавьте 2 мл дистиллированной воды и вновь нагрейте, тщательно перемешивая, до полного упаривания воды. Снимите чашечку с электрической печки. Получится кусочек твердого белого мыла.
Тристеарат глицерина + 3 NаОН → глицерин + стеарат натрия
3. Растворение мыла в воде
Полученное натриевое мыло поместите в большую пробирку, добавьте 5 мл дистиллированной воды, хорошенько взболтайте. Подогрейте пробирку на спиртовке, убедитесь, что при нагревании мыло растворяется быстрее. При встряхивании содержимого пробирки наблюдается обильное пенообразование. Сделаете вывод о растворимости мыла в воде.
4. Образование нерастворимых кальциевых мыл
В пробирку поместите 5 капель р-ра мыла, 1-2 капли хлористого кальция. Выпадает белый осадок нерастворимых в воде кальциевых мыл. Кальциевое мыло выделяется при мытье в жесткой воде, что ухудшает моющие свойства мыла.
 2С17Н35СООNа + СаСl2 2 NаСl + (С17Н35СОО)2Са↓
2С17Н35СООNа + СаСl2 2 NаСl + (С17Н35СОО)2Са↓
5. Образование нерастворимого в воде свинцового мыла
В пробирку поместите 5 капель р-ра мыла, 1-2 капли 0,1% р-ра уксуснокислого свинца. Выпадает белый осадок нерастворимого свинца мыла. Олеат свинца применяется при изготовлении свинцового пластыря.
