Задания для тестового контроля
УКАЖИТЕ СООТВЕТСТВИЯ!
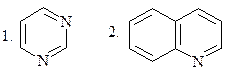 1. а) пиридин
1. а) пиридин
б) пиримидин
в) хинолин
г) пиррол
д) пурин
2.
а) пиридин
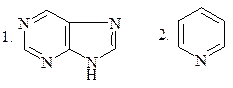 б) пиримидин
б) пиримидин
в) хинолин
г) пиррол
д) пурин
УКАЖИТЕ ПРАВИЛЬНЫЙ ОТВЕТ (ОТВЕТЫ)!
3.
ПИРИМИДИН ЯВЛЯЕТСЯ АРОМАТИЧЕСКИМ СОЕДИНЕНИЕМ, Т.К.
1. все атомы цикла sp2-гибридизованы
2. в наличии замкнутая p,π-сопряжённая система
3. в наличии замкнутая π,π-сопряжённая система
4. каждый азот отдаёт в сопряжение по 1 электрону, т.е. 4n+2=6
5. каждый азот отдаёт в сопряжение по 2 электрона, т.е. 4n+2=10
4.
ЭЛЕКТРОННАЯ КОНФИГУРАЦИЯ АТОМА АЗОТА В ПИРИДИНЕ:
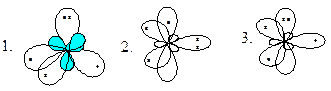 |
5.
ПИРИМИДИН ЯВЛЯЕТСЯ АРОМАТИЧЕСКИМ СОЕДИНЕНИЕМ, Т.К.
6. все атомы цикла sp2-гибридизованы
7. в наличии замкнутая p,π-сопряжённая система
8. в наличии замкнутая π,π-сопряжённая система
9. каждый азот отдаёт в сопряжение по 1 электрону, т.е. 4n+2=6
10. каждый азот отдаёт в сопряжение по 2 электрона, т.е. 4n+2=10
6.
ПО МЕХАНИЗМУ ЭЛЕКТРОФИЛЬНОГО ЗАМЕЩЕНИЯ В ПИРИДИНЕ
ПРОТЕКАЮТ РЕАКЦИИ:
1. бромирования 3. гидроксилирования
2. сульфирования 4. аминирования
7.
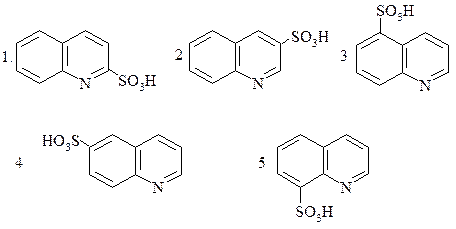 В РЕАКЦИИ СУЛЬФИРОВАНИЯ ХИНОЛИНА ПРЕИМУЩЕСТВЕННО
В РЕАКЦИИ СУЛЬФИРОВАНИЯ ХИНОЛИНА ПРЕИМУЩЕСТВЕННО
ОБРАЗУЮТСЯ:
8.
В РЕАКЦИИ НИТРОВАНИЯ ХИНОЛИНА ПРЕИМУЩЕСТВЕННО ОБРАЗУЮТСЯ:
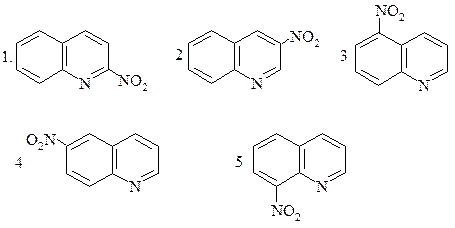 |
9.
В РЕАКЦИИ ПИРИДИНА С АМИДОМ НАТРИЯ ОБРАЗУЕТСЯ:
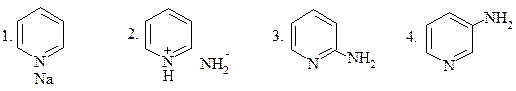 |
10.
В РЕАКЦИИ ГИДРОКСИЛИРОВАНИЯ ПИРИДИНА (KOH, 300oC) ОБРАЗУЕТСЯ:
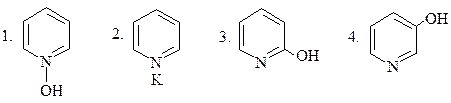 |
11.
ПО МЕХАНИЗМУ НУКЛЕОФИЛЬНОГО ЗАМЕЩЕНИЯ В ПИРИДИНЕ
ПРОТЕКАЮТ РЕАКЦИИ:
1. бромирования 3. гидроксилирования
2. сульфирования 4. аминирования
12.
ОСНОВНЫЕ СВОЙСТВА ПИРИДИНА ПРОЯВЛЯЮТСЯ ЗА СЧЁТ:
1. неподелённой электронной пары азота, участвующей в сопряжении
2. неподелённой электронной пары азота, не участвующей в сопряжении
3. повышенной электронной плотности в ароматическом кольце
4. пониженной электронной плотности в ароматическом кольце
13.
ОСНОВНЫЕ СВОЙСТВА ПИРИДИНА ПРОЯВЛЯЮТСЯ В РЕАКЦИЯХ С:
1. HCl 4. NaNH2
2. NaOH 5. CH3-I
3. H2O
14.
ПРИ ВЗАИМОДЕЙСТВИИ ПИРИДИНА С HCl ОБРАЗУЕТСЯ:
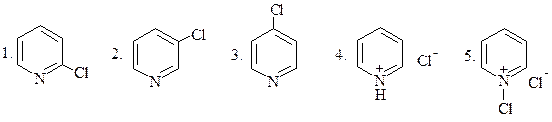
15.
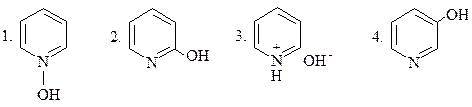 |
ПРИ ВЗАИМОДЕЙСТВИИ ПИРИДИНА С ВОДОЙ ОБРАЗУЕТСЯ:
16.
ОСНОВНЫЕ СВОЙСТВА ПИРИМИДИНА ПРОЯВЛЯЮТСЯ В РЕАКЦИИ С:
4. HCl 4. NaNH2
5. NaOH 5. CH3-I
6. H2O
17.
ПРИ ВЗАИМОДЕЙСТВИИ ПИРИМИДИНА С HCl ОБРАЗУЕТСЯ:
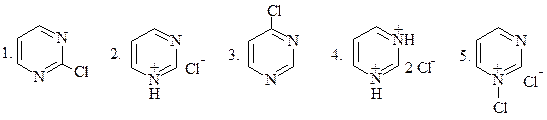 |
18.
В РЕАКЦИИ ПИРИДИНА С МЕТИЛИОДИДОМ ОБРАЗУЕТСЯ:
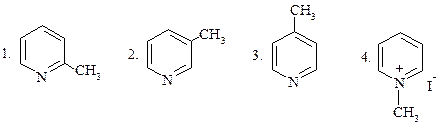 |
19.
НУКЛЕОФИЛЬНЫЕ СВОЙСТВА ПИРИДИНА ПРОЯВЛЯЮТСЯ ЗА СЧЁТ:
5. неподелённой электронной пары азота, участвующей в сопряжении
6. неподелённой электронной пары азота, не участвующей в сопряжении
7. повышенной электронной плотности в ароматическом кольце
8. пониженной электронной плотности в ароматическом кольце
20. ЗАПОЛНИТЕ СХЕМУ!
(вставьте в квадраты номера нужных ответов)
ПОРЯДОК УВЕЛИЧЕНИЯ АКТИВНОСТИ СОЕДИНЕНИЙ В РЕАКЦИЯХ
ЭЛЕКТРОФИЛЬНОГО ЗАМЕЩЕНИЯ:
 |  |  |


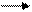
 1 [ ] 2 [ ] 3 [ ] 1. бензол
1 [ ] 2 [ ] 3 [ ] 1. бензол
2. пиридин
3. пиримидин
ВПИШИТЕ НЕДОСТАЮЩИЕ СЛОВА!
21.
ОСНОВНЫЕ СВОЙСТВА ПИРИМИДИНА ___________________, ЧЕМ У ПИРИДИНА, ТАК КАК ДВА АТОМА АЗОТА В КОЛЬЦЕ ОКАЗЫВАЮТ ДРУГ НА ДРУГА ЭЛЕКТРОНО___________________ ВЛИЯНИЕ.
22.
В РЕАКЦИИ С ЙОДИСТЫМ ЭТИЛОМ ПИРИДИН ПРОЯВЛЯЕТ ____________________ СВОЙСТВА.
23.
ПРОИЗВОДНЫЕ 8-ГИДРОКСИХИНОЛИНА ОБЛАДАЮТ ____________________
ДЕЙСТВИЕМ.
УКАЖИТЕ СООТВЕТСТВИЯ!
24.
реакции пиридина их механизм
1. гидроксилирование а) SE в) AE
2. бромирование б) SN г) AN
25.
РЕАКЦИИ В ПИРИДИНЕ:
реагент механизм реакции
1. к. H2SO4, to а) электрофильное замещение
2. KOH, to б) нуклеофильное замещение
в) электрофильное присоединение
г) нуклеофильное присоединение
26.
реакции пиридина их механизм
3. нитрование а) SE в) AE
4. аминирование б) SN г) AN
27.
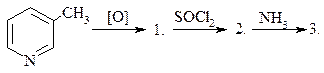
а) никотиновая кислота д) хлорникотиновая кислота
б) изоникотиновая кислота е) изониазид (тубазид)
в) хлорангидрид никотиновой кислоты ж) никотинамид
г) хлорангидрид изоникотиновой кислоты
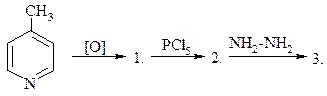 |
28.
а) никотиновая кислота д) хлорникотиновая кислота
б) изоникотиновая кислота е) изониазид (тубазид)
в) хлорангидрид никотиновой кислоты ж) витамин PP
г) хлорангидрид изоникотиновой кислоты
29.
лекарственный препарат гетероцикл, производным которого
он является
1. никотиновая кислота а) пиридин
2. 5-НОК (нитроксолин) б) пиримидин
3. кофеин в) пурин
30.
препарат медицинское применение
1. никотинамид а) для лечения пеллагры
2. гидразид изоникотиновой б) жаропонижающее средство
кислоты (изониазид) в) противотуберкулёзное средство
г) местный анестетик
д) противовоспалительное средство
УКАЖИТЕ ПРАВИЛЬНЫЙ ОТВЕТ (ОТВЕТЫ)!
31.
СТРУКТУРА КОМПЛЕКСА 8-ОКСИХИНОЛИНА С ИОНАМИ Co2+:
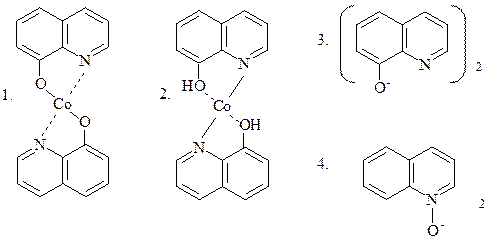 |
Co
 |
Co
32.
БАРБИТУРОВАЯ КИСЛОТА ЯВЛЯЕТСЯ ПРОИЗВОДНЫМ:
1. пиридина 3. пурина
2. пиримидина 4. хинолина
33.
БАРБИТУРОВАЯ КИСЛОТА ПРОЯВЛЯЕТ ВЫСОКИЕ КИСЛОТНЫЕ СВОЙСТВА ЗА СЧЁТ СУЩЕСТВОВАНИЯ В:
1. кето-форме 3. лактамной форме
2. енольной форме 4. лактимной форме
34.
ОБЩАЯ ФОРМУЛА БАРБИТУРАТОВ
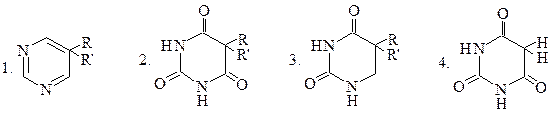 |
35.
БАРБИТУРАТЫ СПОСОБНЫ К ОБРАЗОВАНИЮ СОЛЕЙ
ЗА СЧЁТ СУЩЕСТВОВАНИЯ В:
1. кето-форме 3. лактамной форме
2. енольной форме 4. лактимной форме
36.
СТРУКТУРА НАТРИЕВОЙ СОЛИ БАРБИТАЛА
(5,5-ДИЭТИЛБАРБИТУРОВОЙ КИСЛОТЫ)
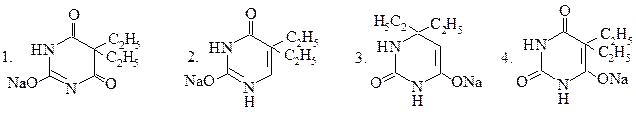
37.
БАРБИТУРАТЫ ПРИМЕНЯЮТ КАК:
1. противовоспалительные средства
2. жаропонижающие средства
3. седативные и снотворные средства
4. диуретики
38. НУМЕРАЦИЯ АТОМОВ В ПУРИНЕ:
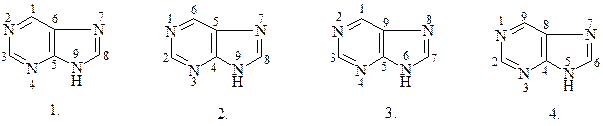
39.
К МЕТИЛИРОВАННЫМ КСАНТИНАМ ОТНОСЯТСЯ:
1. кофеин 4. мочевая кислота
2. теофиллин 5. пурин
3. ураты
40.
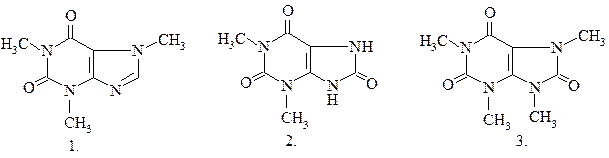 |
СТРУКТУРА КОФЕИНА:
УКАЖИТЕ СООТВЕТСТВИЯ!
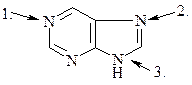 41.
41.
Тип азота
а) пиридиновый
б) пиримидиновый
в) пиррольный
42.
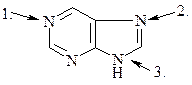 |
Вклад в сопряжённую систему
а) 1 электрон
б) 2 электрона
в) не участвует в сопряжении
43.
ТАУТОМЕРИЯ КСАНТИНА:
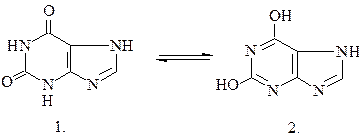 |
а) лактамная флома в) кето-форма
б) лактимная форма г) енольная форма
44.

45. ВПИШИТЕ НЕДОСТАЮЩЕЕ СЛОВО!
УРАТЫ – ЭТО СОЛИ ____________________ КИСЛОТЫ.
Занятие № 12
ИТОГОВОЕ ЗАНЯТИЕ ПО ТЕМЕ «МЕТАБОЛИТЫ
И РОДОНАЧАЛЬНИКИ ВАЖНЕЙШИХ ГРУПП ЛЕКАРСТВЕННЫХ ПРЕПАРАТОВ»
Мотивация цели. Большинство биологически активных соединений, участвующих в процессах метаболизма, в том числе лекарственных препаратов, относится к гетерофункциональным соединениям. Для лучшего понимания зависимости строения, свойств и биологической роли гетерофункциональных соединений и их производных следует повторить и обобщить учебный материал.
Цель самоподготовки. Необходимо повторить свойства гетерофункциональных производных алифатического и ароматического рядов, а также гетероциклических соединений.
Рекомендуемая литература
См. задания № 9-11.
Вопросы для самоконтроля
1. Запишите формулы молочной и α-гидроксимасляной кислот. Назовите их по IUPAC. Отметьте хиральные центры молекул, запишите формулы стереоизомеров, определите их относительную конфигурацию. Дайте определение понятиям «энантиомеры», «рацемическая смесь».
2. Приведите схемы реакций молочной кислоты по карбоксильной группе (образование солей и сложных эфиров) и по гидроксильной группе (реакции ациирования и окисления).
3. Дайте определение понятию «гетерофункциональные соединения» и общую характеристику свойств гетерофункциональных соединений.
4. Приведите строение пировиноградной, ацетоуксусной и щавелевоуксусной кислот. Назовите их по номенклатуре IUPAC.
5. Приведите по одному примеру реакций ацетоуксусной кислоты по каждой функциональной группе и специфическую реакцию (декарбоксилирование).
6. Приведите схемы реакций пировиноградной и ацетоуксусной кислот по карбоксильной группе (образование солей и сложных эфиров).
7. Приведите схемы реакций пировиноградной и щавелевоуксусной кислот по оксогруппе (восстановление, реакции с синильной кислотой и гидроксиламином). Назовите полученные продукты.
8. Дайте определение понятия «таутомерия». Приведите схему кето-енольной таутомерии этилового эфира ацетоуксусной (β-кетомасляной) кислоты. Объясните причину таутомерных превращений.
9. Приведите схему взаимных превращений «кетоновых тел»:
β-гидроксимасляной и ацетоуксусной кислот, ацетона.
10. Охарактеризуйте кислотно-основные свойства п-аминофенола и п-аминобензойной кислоты (по одному примеру реакций по кислотному и основному центрам).
11. Приведите схему реакции ацилирования п-аминофенола уксусным ангидридом. Дайте медицинское название полученного лекарственного препарата.
12. Приведите схемы реакций получения лекарственных препаратов – производных п-аминобензойной кислоты анестезина и новокаина, укажите их применение в медицине.
13. Приведите схемы реакций получения натрия салицилата и ацетилсалициловой кислоты из салициловой кислоты. Укажите применение этих препаратов в медицине.
14. Приведите схемы реакций получения фенилсалицилата из салициловой кислоты (через хлорангидрид). Как применяется фенилсалицилат в медицине?
15. Приведите примеры реакций, иллюстрирующих кислотно-основные свойства сульфаниловой кислоты. Запишите формулу биполярного иона сульфаниловой кислоты. Приведите строение стрептоцида (сульфаниламида) и общую структурную формулу сульфаниламидных препаратов. Объясните принцип их фармакологического эффекта.
16. Дайте определение понятию «гетероциклические соединения». Объясните, почему пиррол и фуран являются ароматическими соединениями и почему их называют π-избыточными циклами.
17. Сравните активность бензола и фурана в реакциях электрофильного замещения (на примере бромирования). Ответ поясните.
18. Приведите строение индола (бензпиррола) и схему реакции, доказывающей его кислотные свойства.
19. Приведите схемы реакций окислительного (до серотонина) и неокислительного (до триптамина) декарбоксилирования аминокислоты триптофан.
20. Приведите схему реакции получения 5-нитрофурфурола из фурфурола. Каким биологическим действием обладают медицинские препараты нитрофуранового ряда?
21. Приведите структуру пиразола, объясните, почему он является ароматическим соединением. Приведите примеры двух реакций, иллюстрирующих кислотные и основные свойства пиразола.
22. Запишите формулу пиразолона-3 (5), укажите тривиальные названия лекарственных препаратов – производных пиразолона и их фармакологический эффект.
23. Приведите примеры двух реакций, иллюстрирующих кислотные и основные свойства имидазола.
24. Приведите схему реакции декарбоксилирования α-аминокислоты гистидина.
25. Приведите строение пиридина, объясните, почему он относится к π-недостаточным циклам. Сравните активность бензола и пиридина в реакциях электрофильного замещения (на примере бромирования). Объясните различия.
26. Объясните, почему пиридин проявляет основные свойства. Приведите схему реакции, иллюстрирующей основные свойства пиридина.
27. Приведите схему реакций получения никотиновой кислоты и её амида из соответствующего пиколина. Укажите их биологическую роль.
28. Приведите схему реакций получения изоникотиновой кислоты и её гидразида из соответствующего пиколина. Каким фармакологическим эффектом обладает гидразид изоникотиновой кислоты?
29. Приведите схемы реакций сульфирования и нитрования хинолина. Назовите механизм этих реакций.
30. Каким фармакологическим эффектом обладают препараты – производные 8-оксихинолина? Объясните механизм их действия (приведите структуру комплекса 8-гидроксихинолина с ионами Fe2+).
31. Приведите строение пиримидина и его производного – барбитуровой кислоты (2,4,6-тригидроксипиримидина) в наиболее устойчивой таутомерной форме. Объясните причину высоких кислотных свойств барбитуровой кислоты (приведите схему кето-енольной таутомерии). Приведите схему реакции образования соли с одним молем щелочи.
32. Приведите общую структурную формулу барбитуратов, объясните причину их кислотных свойств (приведите схему лактам-лактимной таутомерии). Приведите схему реакции образования соли барбитурата с одним молем щёлочи. Укажите применение барбитуратов в медицине.
33. Приведите строение пурина. Назовите гетероциклы, из которых состоит эта конденсированная гетероциклическая система. Объясните, почему пурин является ароматическим соединением.
34. Приведите структуру ксантина (2,6-дигидроксипурина) и его метилированного производного – кофеина (1,3,7-триметилксантина).
35. Приведите строение мочевой кислоты (2,6,8-тригидроксипурина), её кислой и средней натриевых солей. Укажите их растворимость в воде.
План работы на предстоящем занятии
3. Обобщение материала изученных тем.
4. Компьютерное тестирование.
Занятие № 13
