Биохимические основы энзимотерапии, применение ферментов в энзимотеравии (примеры)
Энзимотерапия – применение ферментов животного, бактериального или растительного происхождения и регуляторов активности ферментов с лечебной целью.
1) Протеолитические ферменты применяются при нарушении пищеварения.
Пример:
a. Экстракты слизистой оболочки желудка, основным действующим веществом которых является пепсин. Их в основном используют для коррекции секреторной дисфункции желудка.
b. Панкреатические энзимы, представленные амилазой, липазой, трипсином и химотрипсином. Их используются для коррекции нарушений процесса пищеварения, а также для регуляции функций поджелудочной железы.
c. Комбинированные ферменты, содержащие панкреатин в комбинации с компонентами желчи, гемицеллюлозой. Их назначают при недостаточной внешнесекреторной функции поджелудочной железы в сочетании с патологией печени, желчевыводящей системы, при нарушении жевательной функции, малоподвижном образе жизни, кратковременных погрешностях в еде.
d. Растительные энзимы, представленные папаином, грибковой амилазой, протеазой, липазой и др. ферментами. Папаин и протеазы гидролизируют белки, грибковая амилаза - углеводы, липаза - жиры.
e. Дисахаридазы.
2) Протеолитические препараты применяют местно, в виде аппликаций или орошений, при первичной обработке ран и ожогов. Гидролизуя белки некротизированных тканей, ферменты способствуют очищению раны, уменьшению воспаления и ускорению заживления.
Пример:
a. Коллагеназа вызывает деструкцию коллагена при этом жизнеспособные мышцы, грануляционная ткань и эпителий остаются интактными. При гнойных ранах коллагеназа способствует быстрому очищению от нежизнеспособных тканей и экссудата, более раннему появлению грануляционной ткани и эпителизации, предупреждает развитие грубых рубцов, способствует сохранению функции суставов.
b. Гиалуронидазы – ферменты, специфическим субстратом которых является гиалуронованная кислота, основа межклеточного матрикса соединительной ткани. Показателями к их применению являются рубцы после ожогов и операций, гематомы, контрактуры суставов и т.д. Лечебный эффект проявляется размягчением рубцов, рассасыванием гематом, появлением подвижности в суставах.
c. Протеолитические ферменты применяют для предотвращения и лечения тромбозов, эмболии, инфаркта миокарда, закупорки сосудов сетчатки глаза.
d. Нуклеазы (ДНК-аза, РНК-аза) используют при лечении некоторых вирусных заболеваний. Фермент разрушает ДНК вируса, не повреждая вместе с тем ДНК клеток макроорганизма.
e. Бактериолитические ферменты. Препарат обладает наибольшей бактерицидной активностью по отношению к грамположительным бактериям: стафилакоккам, стрептококкам, а также менингококкам, гонококкам. Особенность, препарат показывает высокую бактерицидную эффективность вне зависимости от устойчивости бактерий к действию антибиотиков.
Энзимотерапию применяют в случае недостаточности ферментов, либо вместе с другими препаратами.
Цикл Кребса - схема реакций, ферменты, коферменты, энергетический баланс одного оборота. Тканевые особенности в детском возрасте, Регуляция.
Цикл Кребса.
ЩУКа "съела" ацетат,
Получается цитрат.
Через cis-аконитат
Будет он - изоцитрат.
Водороды отдав НАД,
Он теряет СО 2.
Этому безмерно рад
Альфа -кето- глутарат.
Окисление грядет:
НАД похитит водород,
В 1 и липоат
С коэнзимом А спешат,
Отбирают СО 2.
А энергия едва
В сукциниле появилась,
Сразу АТФ родилась.
И остался сукцинат.
Вот добрался он до ФАДа -
Водороды тому надо.
Водороды потеряв,
Стал он просто фумарат.
Фумарат воды напился,
Да в малат и превратился.
Тут к малату НАД пришел,
Водороды приобрел.
ЩУКа снова объявилась
И тихонько затаилась
Караулить ацетат...
Ферменты в этой схеме есть.
Коферменты - это НАД, НАДФ, АТФ, ГТФ? Тогда есть.
Схема:
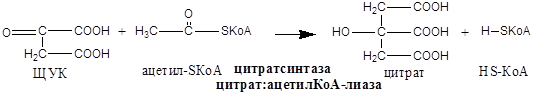
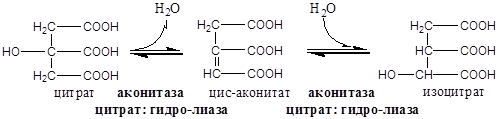
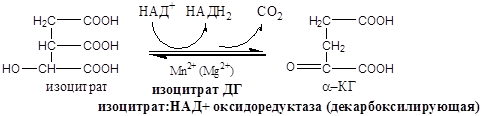
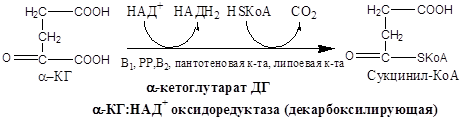
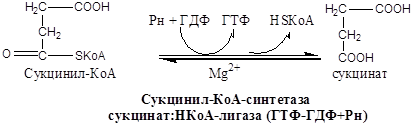
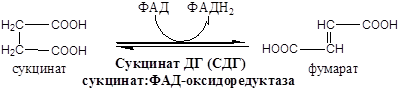
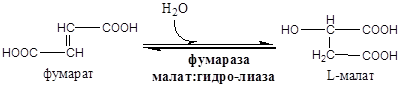
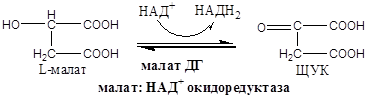
Образовавшиеся молекулы ЩУК реагируют с новой молекулой Ацетил-КоА и цикл повторяется вновь.
Энергетический баланс одного оборота:3 НАДН2 + 1 ФАДН2 (направляются далее в дыхательную цепь окислительного фосфорилирования) + 1 ГТФ (НАДН2 -> 3 АТФ, ФАДН2 -> 2 АТФ, ГТФ -> 1 АТФ) = 12 АТФ.
Регуляция ЦТК: 4 регуляторных фермента: цитратсинтазы, изоцитрат ДГ, α-КГ ДГ и СДГ. ЦТК ингибируется в основном НАДН2 и АТФ, которые являются продуктами ЦТК и цепи окислительного фосфорилирования. Активируют ЦТК в основном НАД+ и АДФ.
Оксидазный путь использования кислорода в клетке - митохондриальное окислительное фосфорилирование. Состав дыхательных комплексов редокс-цепи, локализация и функции, тканевые особенности в детском возрасте. Регуляция.
Оксидазный путь использования кислорода в клетке:
Протекает в митохондриях, потребляет 90% О2 и обеспечивает процесс окислительного фосфорилирования.
Окислительное фосфорилирование - синтез АТФ из АДФ и Н3РО4 за счет энергии движении электронов по дыхательной цепи.
Оно является основным источником АТФ в аэробных клетках
Окислительное фосфорилирование состоит из процессов окисления и фосфорилирования.
1) Процесс окисления
Процесс окисления происходит при движении электронов по дыхательной цепи от субстратов тканевого дыхания на кислород. Дыхательная цепь окислительного фосфорилирования состоит из 4 белковых комплексов, встроенных во внутреннюю мембрану митохондрий и небольших подвижных молекул убихинона и цитохрома С, которые циркулируют в липидном слое мембраны между белковыми комплексами.
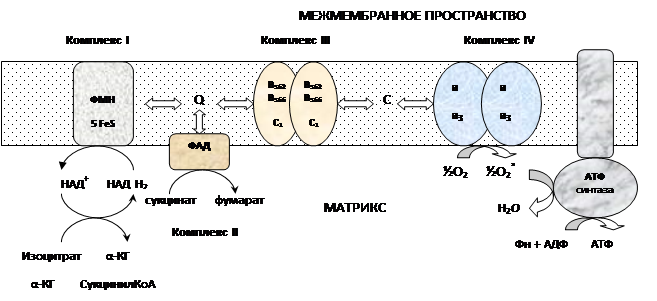
a. Комплекс I – НАДН2 дегидрогеназный комплекс–самый большой из дыхательных ферментных комплексов, в качестве коферментов содержит ФМН и 5 железосерных (Fe2S2 и Fe4S4) белков.
b. Комплекс II – СДГ. В качестве коферментов содержит ФАД и железосерный белок.
c. Комплекс III – Комплекс b-c1 (фермент QH2 ДГ). Каждый мономер содержит 3 гема, связанных с цитохромами b562, b566, с1, и железосерный белок.
d. Комплекс IV – Цитохромоксидазный комплекс. Каждый мономер содержит 2 цитохрома (а и а3) и 2 атома меди.
e. Коэнзим Q (убихинон). Переносит по 2Н+ и 2е-.
f. Цитохром С. Периферический водорастворимый мембранный белок. Содержит молекулу гема.
Этапы движения е- по дыхательной цепи
a. 2е- от НАДН2, проходят через I комплекс (ФМН→SFe белок) на КоQ, высвобождаемая при этом энергия обеспечивает перекачку Н+.
b. КоQ с 2е- забирает у воды 2Н+ из матрикса и превращается в КоQН2 (восстановление КоQ проходит также с участием комплекса II).
c. КоQН2 переносит 2е- на комплекс III, а 2Н+ в межмембранное пространство.
d. Цитохром С переносит е- c III комплекса на IV комплекс.
e. IV комплекс сбрасывает е- на О2, высвобождаемая при этом энергия обеспечивает перекачку Н+.
Образовавшийся на внутренней мембране митохондрий электрохимический потенциал используется для:
a. фосфорилирования АДФ в АТФ;
b. транспорта веществ через мембрану митохондрий;
c. теплопродукцию.
2) Процесс фосфорилирования
Процесс фосфорилирования осуществляется АТФ-синтетазой (Н+-АТФ-аза), которая потребляет 40-45% свободной энергии, выделившейся при окислении. Н+-АТФ-аза интегральный белок внутренней мембраны митохондрий, она состоит из 2 белковых комплексов F0 и F1.
a. Гидрофобный комплекс F0 погружён в мембрану и служит основанием, которое фиксирует АТФ-синтазу в мембране. Он состоит из нескольких субъединиц, образующих канал, по которому протоны переносятся в матрикс.
b. Комплекс F1 выступает в митохондриальный матрикс. Он состоит из 9 субъединиц (3α, 3β, γ, δ, ε). Субъединицы α и β уложены попарно, образуя «головку»; между а- и β-субъединицами располагаются 3 активных центра, в которых происходит синтез АТФ; γ, δ, ε – субъединицы связывают комплекс F1, с F0.
АТФ-синтетаза обеспечивает обратимое взаимопревращение энергии электрохимического потенциала и энергии химических связей.
Электрохимический потенциал внутренней мембраны заставляет Н+ двигаться из межмебранного пространства по каналу АТФ-синтазы в матрикс митохондрий. При каждом переносе протонов через канал Fo энергия электрохимического потенциала расходуется на поворот стержня, в результате которого циклически изменяется конформация а- и β-субъединиц и все 3 активных центра, образованных парам α- и β-субъединиц, катализируют очередную фазу цикла: 1) связывание АДФ и Н3РО4; 2) образование фосфоангидридной связи АТФ; 3) освобождение конечного продукта АТФ.
