Задания для тестового контроля. УКАЖИТЕ СООТВЕТСТВИЯ!
УКАЖИТЕ СООТВЕТСТВИЯ!
1.
1. восстанавливающий дисахарид а) мальтоза
2. невосстанавливающий дисахарид б) лактоза
в) сахароза
г) манноза
2.
моносахаридное звено
1. сахароза а) глюкопираноза
2. мальтоза б) фруктофураноза
в) галактопираноза
г) глюкофураноза
3.
моносахаридное звено
1. целлобиоза а) глюкопираноза
2. лактоза б) фруктофураноза
в) галактопираноза
г) глюкофураноза
ВПИШИТЕ НЕДОСТАЮЩЕЕ СЛОВО!
4.
ДИСАХАРИД, ПОСТРОЕННЫЙ ИЗ ДВУХ ОСТАТКОВ ГЛЮКОПИРАНОЗЫ,
СВЯЗАННЫХ β-1,4-ГЛИКОЗИДНОЙ СВЯЗЬЮ, НАЗЫВАЕТСЯ _________________.
5.
ДИСАХАРИД, ПОСТРОЕННЫЙ ИЗ ДВУХ ОСТАТКОВ ГЛЮКОПИРАНОЗЫ,
СВЯЗАННЫХ α-1,4-ГЛИКОЗИДНОЙ СВЯЗЬЮ, НАЗЫВАЕТСЯ _________________.
УКАЖИТЕ ПРАВИЛЬНЫЙ ОТВЕТ (ОТВЕТЫ)!
6.
В МОЛЕКУЛЕ ЦЕЛЛОБИОЗЫ ДВА МОНОСАХАРИДНЫХ ОСТАТКА СВЯЗАНЫ:
1. α-1,4-гликозидной связью 4. β-1,6-гликозидной связью
2. α-1,6-гликозидной связью 5. β-1,3-гликозидной связью
3. β-1,4-гликозидной связью
7.
МОНОСАХАРИДНЫМИ ЗВЕНЬЯМИ ЛАКТОЗЫ ЯВЛЯЮТСЯ:
1. глюкопираноза 3. галактопираноза
2. фруктофураноза 4. фруктопираноза
8.
ВОССТАНАВЛИВАЮЩИЕ СВОЙСТВА ДИСАХАРИДОВ ПРОЯВЛЯЮТСЯ
ЗА СЧЁТ:
1. циклической таутомерной формы 3. полуацетального гидроксила
2. открытой таутомерной формы 4. спиртовых гидроксилов
4. реакции гидролиза
9.
ПРИ ОБРАЗОВАНИИ МОЛЕКУЛЫ ВОССТАНАВЛИВАЮЩЕГО ДИСАХАРИДА:
1. полуацетальный гидроксил одного моносахарида взаимодействует со спиртовым гидроксилом другого моносахарида
2. полуацетальный гидроксил взаимодействует с полуацетальным
3. спиртовой гидроксил взаимодействует со спиртовым
10.
ПРИ ОБРАЗОВАНИИ МОЛЕКУЛЫ НЕВОССТАНАВЛИВАЮЩЕГО
ДИСАХАРИДА:
4. полуацетальный гидроксил одного моносахарида взаимодействует со спиртовым гидроксилом другого моносахарида
5. полуацетальный гидроксил взаимодействует с полуацетальным
6. спиртовой гидроксил взаимодействует со спиртовым
11.
МОНОСАХАРИДНЫМИ ЗВЕНЬЯМИ САХАРОЗЫ ЯВЛЯЮТСЯ:
1. α-D-глюкопираноза 5. β-D-фруктопираноза
2. β-D-глюкопираноза 6. β-D-фруктофураноза
3. α-D-фруктопираноза 7. β-D-галактопираноза
4. α-D-фруктофураноза
12.
В МОЛЕКУЛЕ ЛАКТОЗЫ ДВА МОНОСАХАРИДНЫХ ОСТАТКА СВЯЗАНЫ:
1. α-1,4-гликозидной связью 4. β-1,6-гликозидной связью
2. α-1,6-гликозидной связью 5. β-1,3-гликозидной связью
3. β-1,4-гликозидной связью
13.
ВОССТАНАВЛИВАЮЩИМ ФРАГМЕНТОМ ДИСАХАРИДА ЯВЛЯЕТСЯ:
1. альдегидная группа 3. спиртовой гидроксил
2. полуацетальный гидроксил 4. О-гликозидная связь
14.
ВОССТАНАВЛИВАЮЩИМИ СВОЙСТВАМИ ОБЛАДАЮТ:
1. мальтоза 4. целлюлоза
2. сахароза 5. амилоза
3. лактоза
15.
В МОЛЕКУЛЕ САХАРОЗЫ ДВА МОНОСАХАРИДНЫХ ЗВЕНА СВЯЗАНЫ:
1. α-1,4-гликозидной связью 3. α-1.6-
2. β-1,4- 4. 1,2-
16.
ГАЛАКТОЗА ЯВЛЯЕТСЯ МОНОСАХАРИДНЫМ ЗВЕНОМ:
1. мальтозы 3. лактозы
2. целлобиозы 4. сахарозы
17.
В МОЛЕКУЛЕ МАЛЬТОЗЫ ДВА МОНОСАХАРИДНЫХ ЗВЕНА СВЯЗАНЫ:
1. α-1,4-гликозидной связью 4. β-1,6-гликозидной связью
2. α-1,6-гликозидной связью 5. β-1,3-гликозидной связью
3. β-1,4-гликозидной связью
18.
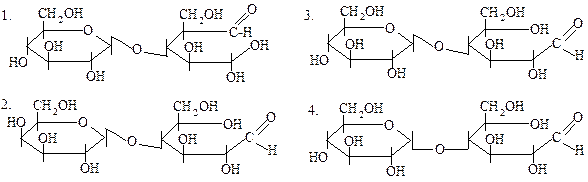 СТРУКТУРА ОТКРЫТОЙ ТАУТОМЕРНОЙ ФОРМЫ ЦЕЛЛОБИОЗЫ:
СТРУКТУРА ОТКРЫТОЙ ТАУТОМЕРНОЙ ФОРМЫ ЦЕЛЛОБИОЗЫ:
19.
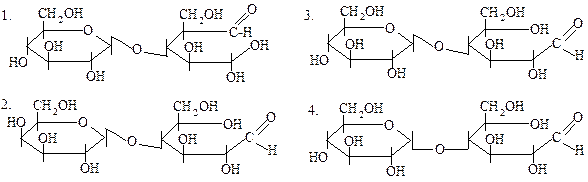 СТРУКТУРА ОТКРЫТОЙ ТАУТОМЕРНОЙ ФОРМЫ МАЛЬТОЗЫ:
СТРУКТУРА ОТКРЫТОЙ ТАУТОМЕРНОЙ ФОРМЫ МАЛЬТОЗЫ:
20.
РЕАКЦИЯ «СЕРЕБРЯНОГО ЗЕРКАЛА» ХАРАКТЕРНА ДЛЯ:
1. мальтозы 4. лактозы
2. сахарозы 5. целлюлозы
3. глюкозы
21.
МОНОСАХАРИДНЫМИ ЗВЕНЬЯМИ β-МАЛЬТОЗЫ ЯВЛЯЮТСЯ:
5. α-D-глюкопираноза 5. β-D-фруктопираноза
6. β-D-глюкопираноза 6. β-D-фруктофураноза
7. α-D-фруктопираноза 7. β-D-галактопираноза
8. α-D-фруктофураноза
УКАЖИТЕ СООТВЕТСТВИЯ!
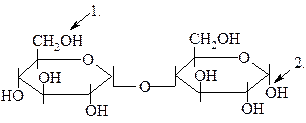 22.
22.
а) образование гликозидов
б) образование простых эфиров
в) образование сложных эфиров
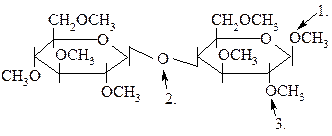 |
23. а) гликозидная связь
б) сложноэфирная связь
в) простая эфирная связь
г) ангидридная связь
24.
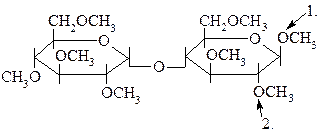 |
а) гидролизуется только в
кислой среде
б) гидролизуется только в
щелочной среде
в) гидролизуется и в кислой,
и в щелочной среде
г) не подвергается гидролизу
УКАЖИТЕ ПРАВИЛЬНЫЙ ОТВЕТ (ОТВЕТЫ)!
25.
ПРИ ВЗАИМОДЕЙСТВИИ ЛАКТОЗЫ С ЭТАНОЛОМ В ПРИСУТСТВИИ СУХОГО ХЛОРОВОДОРОДА ОБРАЗУЕТСЯ:
1. О-этиллактоза 3. октаэтиллактоза
2. О-этиллактозид 4. октаацетиллактоза
26.
ЗА СЧЁТ НАЛИЧИЯ СВОБОДНОГО ПОЛУАЦЕТАЛЬНОГО ГИДРОКСИЛА
ДЛЯ ЦЕЛЛОБИОЗЫ ХАРАКТЕРНЫ:
1. реакция кислотного гидролиза
2. реакция щелочного гидролиза
3. образование простых эфиров
4. цикло-цепная таутомерия
5. реакция образования гликозидов
27.
ПРИ КИСЛОТНОМ ГИДРОЛИЗЕ О-МЕТИЛЛАКТОЗИДА ОБРАЗУЮТСЯ:
1. лактоза 4. галактоза
2. глюкоза 5. фруктоза
3. манноза 6. метанол
7. CH3Cl
28.
ПРИ КИСЛОТНОМ ГИДРОЛИЗЕ О-МЕТИЛМАЛЬТОЗИДА (В ПРИСУТСТВИИ HCl) ОБРАЗУЮТСЯ:
1. мальтоза 4. глюкоза
2. CH3OH 5. CH3Cl
3. галактоза
29.
ПРИ ЩЕЛОЧНОМ ГИДРОЛИЗЕ ДАННОГО СОЕДИНЕНИЯ (NaOH) ОБРАЗУЮТСЯ:
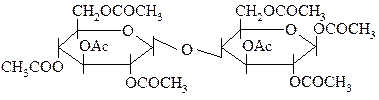 |
1. глюкоза 4. лактоза
2. мальтоза 5. CH3COOH
3. целлобиоза 6. CH3COONa
30.
В РЕАКЦИИ МАЛЬТОЗЫ С Cu(OH)2 ПРИ КОМНАТНОЙ ТЕМПЕРАТУРЕ
НАБЛЮДАЕТСЯ:
1. выпадение кирпично-красного осадка
2. образование ярко-синего раствора
3. выпадение голубого студенистого осадка
4. появление аптечного запаха
5. выпадение белого кристаллического осадка
31.
СЛОЖНОЭФИРНЫЕ СВЯЗИ В ОКТААЦЕТИЛЦЕЛЛЮЛОЗЕ
1. гидролизуются только в кислой среде
2. гидролизуются только в щелочной среде
3. гидролизуются и в кислой, и в щелочной среде
4. не подвергаются гидролизу
32.
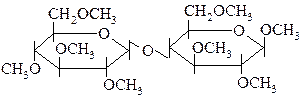 ПРИ КИСЛОТНОМ ГИДРОЛИЗЕ (В ПРИСУТСТВИИ HCl)
ПРИ КИСЛОТНОМ ГИДРОЛИЗЕ (В ПРИСУТСТВИИ HCl)
ОБРАЗУЮТСЯ:
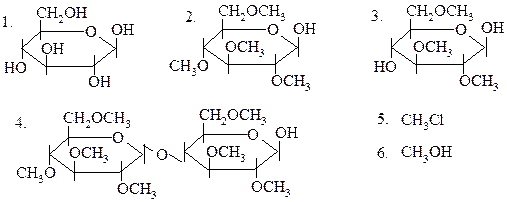 |
33.
ПРИ КИСЛОТНОМ ГИДРОЛИЗЕ ДАННОГО СОЕДИНЕНИЯ
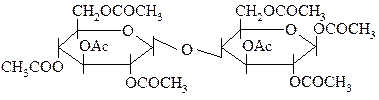 ОБРАЗУЮТСЯ:
ОБРАЗУЮТСЯ:
1. целлобиоза 4. лактоза
2. мальтоза 5. CH3COOH
3. глюкоза 6. CH3COONa
34.
ПРИ КИСЛОТНОМ ГИДРОЛИЗЕ О-ЭТИЛЦЕЛЛОБИОЗИДА (В ПРИСУТСТВИИ HCl) ОБРАЗУЮТСЯ:
1. целлобиоза 4. галактоза
2. C2H5Cl 5. C2H5OH
3. глюкоза
35.
O-ГЛИКОЗИДНЫЕ СВЯЗИ ГИДРОЛИЗУЮТСЯ:
1. только в щелочной среде
2. только в кислой среде
3. и в кислой, и в щелочной среде
4. не подвергаются гидролизу
УКАЖИТЕ СООТВЕТСТВИЯ!
36.
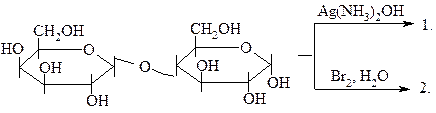 |
а) различные продукты окисления г) целлобионовая кислота
б) лактобионовая кислота д) целлобиаровая кислота
в) мальтобионовая кислота е) лактобиаровая кислота
37. 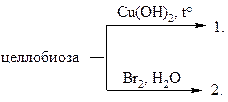
а) различные продукты окисления
б) целлобиаровая кислота
в) целлобионовая кислота
г) целлулитная кислота
д) целлобиат меди
38.
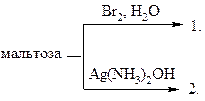 |
а) различные продукты окисления
б) мальтобионовая кислота
в) мальтобиаровая кислота
г) мальтаровая кислота
д) глюконовая кислота
ВПИШИТЕ ЦИФРУ!
39.
ОБРАЗОВАНИЕ ГЛИКОЗИДОВ ВОЗМОЖНО ЗА СЧЕТ ГИДРОКСИЛА,
ОБОЗНАЧЕННОГО ЦИФРОЙ ____ .
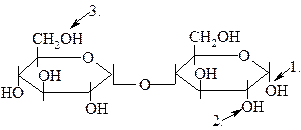 |
УКАЖИТЕ ПРАВИЛЬНЫЙ ОТВЕТ!
40.
В РЕАКЦИИ САХАРОЗЫ С Cu(OH)2 ПРИ КОМНАТНОЙ ТЕМПЕРАТУРЕ
НАБЛЮДАЕТСЯ
1. выпадение кирпично-красного осадка
2. образование ярко-синего раствора
3. выпадение голубого студенистого осадка
4. появление аптечного запаха
5. выпадение белого кристаллического осадка
УКАЖИТЕ СООТВЕТСТВИЯ!
41.
основной тип связи между
моносахаридными остатками полисахарид
1. α-1,4- а) амилоза
2. β-1,4- б) амилопектин
в) гликоген
г) целлюлоза
42.
тип связей
1. амилопектин а) α-1,4- в) α-1,6-
2. целлюлоза б) β-1,4- г) β-1,6-
43.
тип связей между моносахаридными звеньями
1. гликоген а) α-1,4- в) α-1,6- д) β-1,3-
2. амилоза б) β-1,4- г) β-1,6-
44.
тип связи
1. амилопектин а) α-1,4- в) β-1,4 д) β-1,3-
2. целлюлоза б) α-1,6- г) β-1,6-
УКАЖИТЕ ПРАВИЛЬНЫЕ ОТВЕТ (ОТВЕТЫ)!
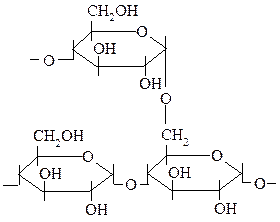 45.
45.
ДАННЫЙ ФРАГМЕНТ МОЖЕТ БЫТЬ
УЧАСТКОМ МОЛЕКУЛ:
1. амилозы
2. амилопектина
3. целлюлозы
4. гликогена
46.
ГЛИКОГЕН ГИДРОЛИЗУЕТСЯ:
1. в присутствии ферментов
2. в кислой среде
3. в щелочной среде
4. гидролиз невозможен
47.
КРАХМАЛ ГИДРОЛИЗУЕТСЯ:
1. в кислой среде
2. в щелочной среде
3. в присутствии ферментов
4. гидролиз невозможен
48.
АМИЛОПЕКТИН ГИДРОЛИЗУЕТСЯ:
1. в кислой среде
2. в щелочной среде
3. в присутствии ферментов
4. гидролиз невозможен
49. ВПИШИТЕ НЕДОСТАЮЩИЕ СЛОВА!
КАЧЕСТВЕННОЙ РЕАКЦИЕЙ НА АМИЛОЗУ ЯВЛЯЕТСЯ ВЗАИМОДЕЙСТВИЕ
С _____________ С ОБРАЗОВАНИЕМ ________________ ОКРАШИВАНИЯ.
Занятие № 15
α-АМИНОКИСЛОТЫ. ПЕПТИДЫ И БЕЛКИ
Мотивация цели.Аминокислоты играют важную роль в живом организме как мономеры для построения молекул пептидов и белков. Кроме того, они являются материалом для биосинтеза многих ферментов, гормонов, витаминов, антибиотиков, медиаторов. Отдельные аминокислоты используются как лекарственные препараты (цистеин, метионин, глутаминовая кислота). Пептиды выполняют в организме регуляторную функцию (гормоны, антибиотики). Белки составляют материальную основу химической деятельности клетки (ферменты, гормоны, структурные, транспортные защитные белки).
Цель самоподготовки. Необходимо усвоить классификацию и строение наиболее часто встречающихся α-аминокислот, химические превращения α-аминокислот in vitro и in vivo, принципы строения пептидов, пространственную организацию молекул белка.
План изучения материала
1. Строение, классификация и стереоизомерия α-аминокислот.
1.1. Классификация природных α-аминокислот по характеру радикала и по числу карбоксильных и аминогрупп. Строение и номенклатура 20 важнейших α-аминокислот.
1.2. Пространственная изомерия α-аминокислот (оптическая изомерия), её причины. Отнесение стереоизомеров к D- и L-стереохимическим рядам.
1.3. Незаменимые аминокислоты.
2. Химические свойства аминокислот in vitro.
2.1. Кислотно-основные свойства аминокислот. Биполярная структура. Строение в кислой и щелочной среде. Изоэлектрическая точка.
2.2. Реакции по карбоксильной группе – образование солей, сложных эфиров, галогенангидридов.
2.3. Реакции по аминогруппе – образование солей, ацилирование, взаимодействие с альдегидами (как основа пиридоксалевого катализа), дезаминирование (под действием азотистой кислоты).
2.4. Специфические реакции α-аминокислот – декарбоксилирование, образование внутрикомплексных солей, реакция с нингидрином.
2.5. Реакции отдельных групп α-аминокислот:
- реакция на ароматические аминокислоты (ксантопротеиновая);
- реакция на серусодержащие аминокислоты.
3. Реакции α-аминокислот in vivo: декарбоксилирование, дезаминирование (окислительное и неокислительное), переаминирование, образование пептидов.
4. Первичная структура пептидов и белков.
4.1. Электронное и пространственное строение пептидной связи.
4.2. Состав и аминокислотная последовательность пептидов. Их кислотно-основные свойства, изоэлектрическая точка.
4.3. Установление состава пептидов. Гидролиз пептидов, условия.
4.4. Установление аминокислотной последовательности (Самостоятельная работа № 9).
4.5. Качественные реакции на белки (биуретовая, ксантопротеиновая, с нингидрином, с ацетатом свинца).
5. Пространственное строение молекул белков.
5.1. Вторичная структура белков (α-спираль, β-складчатая структура). Связи, фиксирующие вторичную структуру.
5.2. Третичная структура белков. Связи, фиксирующие её (дисульфидные и ионные).
Рекомендуемая литература
А - с. 314-346, 349-360, 363-367.
А* - с. 313-321, 322-324, 326-331, 333-340, 343-345, 351, 361-366,
369-370, 371-372.
А** - с. 296-305, 307-309, 312-314. 316-317, 318-320, 325, 332-338, 341-343, 347-348.
Б – тема 3.1, обучающие задачи 2, 3, 5 (с. 182-186, 189-190).
Вопросы для самоконтроля(вопросы, обозначенные*, обязательны для выполнения в письменном виде)
1. Напишите проекционные формулы энантиомеров серина, валина, глутаминовой кислоты, гистидина. Какие из этих аминокислот являются незаменимыми?
2*. Приведите формулы биполярных ионов Ала, Сер, Гли, Лиз, Асп. В какой области значений pH находятся их ИЭТ?
3. Приведите строение Ала в сильнокислой среде, Гли - в сильнощелочной среде.
4. Запишите схемы реакций декарбоксилирования аминокислот Гис, Сер, Три. Укажите условия протекания реакций in vivo и in vitro.
5. Приведите схемы реакций дезаминирования in vitro и in vivo (окислительное) аминокислот Ала, Иле, Тир.
6*. Приведите схемы реакций взаимодействия Ала со следующими реагентами: NaOH, HCl, SOCl2, (CH3CO)2O, C2H5OH, формальдегидом. Назовите продукты реакций.
7*. Приведите схемы реакций переаминирования аланина щавелевоуксусной кислотой; глутаминовой кислоты пировиноградной кислотой. Назовите полученные аминокислоты.
8. Запишите структурные формулы трипептидов: Гли-Вал-Иле, Ала-Вал-Фен, Гис-Лиз-Три. В какой области значений pH находятся ИЭТ этих трипептидов?
9. Приведите схемы кислотного и щелочного гидролиза дипептидов Сер-Вал, Ала-Фен, Иле-Цис, Сер-Лиз, Гли-Ала, Вал-Тре, Мет-Гис.
10. Покажите взаимодействие между пространственно сближенными участками белковой молекулы, содержащими остатки лизина и аспараниновой кислоты; два остатка цистеина.
План работы на предстоящем занятии
1. Определение исходного уровня знаний (тестовый контроль).
2. Разбор основных вопросов темы.
3. Выполнение лабораторной работы:
- Реакция глицина с нингидрином;
- Реакция глицина с азотистой кислотой;
- Образование комплексной медной соли глицина;
- Биуретовая реакция на пептидную связь;
- Ксантопротеиновая реакция белков;
- Реакция на присутствие серусодержащих α-аминокислот.
4. Оформление лабораторного журнала, контроль выполнения лабораторной работы.
Лабораторная работа
