Строение и биологическая роль протеиногенных аминокислот
А) Строение и биологическая роль ациклических аминокислот.
1. Моноаминомонокарбоновые
Глицин(гли, аминоуксусная к-та):
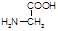
Биологическая роль:
1. Протеиногенная.
2. Глюкогенная (гли ®сер®ПВК…).
3. Донор одноуглеродных фрагментов, необходимых для синтеза:
· пиррола,
· пуринсодержащих молекул (нуклеотидов, нуклеиновых кислот),
· гемсодержащих соединений (гемоглобина, хлорофилла),
· холина (и соответственно ацетилхолина – медиатора парасимпатической системы),
· креатина (креатинфосфат участвует в мышечном сокращении).
4. Необходим для синтеза трипептида – глютатиона.
Аланин(ала, a-аминопропионовая к-та):
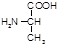
Биологическая роль:
1. Протеиногенная.
2. Глюкогенная (ала ® сер ®ПВК…).
Серин(сер, a-амино-b-гидроксипропионовая к-та):
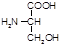
Биологическая роль:
1. Протеиногенная.
2. Глюкогенная (сер ®ПВК…).
3. Входит в состав активных центров ферментов (30%).
4. Необходим для синтеза фосфопротеинов (казеин молока).
5. Необходим для синтеза заменимой аминокислоты цис.
Цистеин(цис, a-амино-b-тиопропионовая к-та):
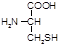
Биологическая роль:
1. Протеиногенная.
2. Глюкогенная (цис®сер®ПВК…).
3. Входит в состав активных центров ферментов.
4. Необходим для формирования 2-, 3-, и 4-тичной структуры белков, т. к. способен образовывать дисульфидные связи.
5. Содержит самую реакционно активную при физиологических условиях функциональную группу, которая легко вступает во многие реакции:
· окислительно-восстановительные (образуется цистин, глютатион);
· способен связывать тяжёлые металлы – входит в состав металлотионеинов (содержит до 30% цистеина), одна молекула такого белка может связать 7 атомов Ме.
6. Является донором сульфид- и сульфат-группы и необходим для синтеза серосодержащих соединений:
· таурина (для синтеза желчных кислот);
· при декарбоксилировании образуется меркаптоэтиламин (необходим для синтеза КоА-SH).
7. Много в хрусталике глаза, применяется в медицинской практике для профилактики катаракты (в качестве препарата «Витеин» – 3¢-фосфоаденозин-5¢-фосфосульфат, в состав которого входят цистеин, глутамин и глюконат).
Треонин( тре, a-амино-b-гидроксимасляная к-та):
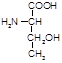
Биологическая роль:
1. Протеиногенная.
2. Глюкогенная (гли ®сер ®ПВК…).
3. Необходим для синтеза фосфопротеинов.
Метионин(мет, a-амино-g-метилтиомасляная кислота):
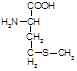
Биологическая роль:
1. Протеиногенная (особенно много в казеине молока).
2. Является донором метильной группы (в виде S-аденозин-метионина), необходим для синтеза:
· холина;
· фосфолипидов (липитропный эффект) – в медицинской практике назначается при токсических поражениях и жировой инфильтрации печени.
Валин(вал,a-амино-изовалерьяновая кислота):
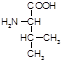
Биологическая роль:
1. Протеиногенная.
2. Глюкогенная.
3. Кетогенная.
Лейцин(лей, a-амино-изокапроновая кислота):
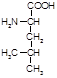
Биологическая роль:
1. Протеиногенная.
2. Глюкогенная.
3. Кетогенная.
Изолейцин(иле, a-амино-изокапроновая кислота):
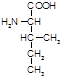
Биологическая роль:
1. Протеиногенная.
2. Глюкогенная.
3. Кетогенная.
2. Моноаминодикарбоновые аминокислоты
Аспартат(асп, аминосукцинат):
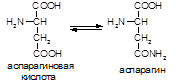
Биологическая роль:
1. Протеиногенная, в состав белков входят и аспартат и его амид (асн).
2. Глюкогенная (асп®ЩУК…).
3. Входит в активный центр ферментов.
4. Является донором аминогруппы.
5. Необходим для синтеза пиримидиновых оснований.
6. Участвует в обезвреживании аммиака.
Глутамат(глу, аминоглутарат):
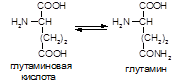
Биологическая роль:
1. Протеиногенная, в состав белков входят и глутамат и его амид (глн).
2. Глюкогенная (глу® a-кетоглутарат ®ЩУК…).
3. Входит в активный центр ферментов.
4. Является донором аминогруппы.
5. Необходим для синтеза пуриновых оснований.
6. Необходим для синтеза трипептида глютатиона.
7. Участвует в обезвреживании аммиака.
8. При декарбоксилировании образуется g-аминомасляная кислота (оказывает тормозящее действие на ЦНС).
9. Как нейромедиатор улучшает функцию головного мозга (передача синапсов симпатической системы), содержится в сером и белом веществе головного мозга; в медицинской практике назначают при лечении заболеваний ЦНС, психических расстройствах, дистрофии мышц.
3. Диаминомонокарбоновые
Аргинин(арг, a-амино-d-гуанидилвалерьяновая кислота):
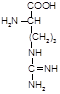
Биологическая роль:
1. Протеиногенная (особенно много в эмбриональных тканях и опухолевых клетках).
2. Основной источник образования NO, необходимого для регуляции апоптоза, деления и дифференцировки клеток.
3. Участвует в синтезе мочевины.
4. Необходим для синтеза:
· аргининфосфата (используется при мышечном сокращении),
· креатинфосфата (из арг, гли и мет), необходимого для мышечного сокращения.
Лизин(лиз, a,e-диаминокапроновая кислота):
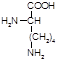
Биологическая роль:
1. Протеиногенная.
2. Глюкогенная (глу®a-кетоглутарат®ЩУК…).
3. Из лиз образуются нестандартные аминокислоты:
· 5-гидроксилизин (для синтеза коллагена);
· N-метиллизин (в миозине);
· десмозин (в эластине).
4. При декарбоксилировании образуется трупный яд кадаверин.
4. Диаминодикарбоновые (цистин, лактионин)
Б) Строение и биологическая роль циклических аминокислот
1. Гомоциклические:
Фенилаланин(фен, a-амино-bфенил-пропионовая кислота):
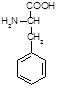
Биологическая роль:
1. Протеиногенная.
2. Глюкогенная.
3. Кетогенная.
4. Необходим для синтеза гормонов:
· гормонов мозгового слоя надпочечников (адреналина и норадреналина);
· гормонов щитовидной железы (тироксина).
5. Необходим для синтеза меланина.
Тирозин(тир, a-амино-b-парагидроксифенил-пропионовая кислота):
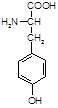
(легко образуется из фен и выполняет те же функции).
2. Гетероциклические аминокислоты
Триптофан(три, a-амино-b-индолил-пропионовая кислота):
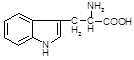
Биологическая роль:
1. Протеиногенная.
2. Необходим для синтеза витамина РР.
3. Необходим для синтеза биогенных аминов:
· серотонина (медиатор ЦНС);
· триптамина (повышает АД, сужает сосуды).
Гистидин(гис, a-амино-b-имидозолил-пропионовая кислота):
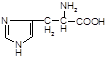
Биологическая роль:
1. Протеиногенная.
2. Глюкогенная (Гис ® глу ®…).
3. Входит в активный центр ферментов.
4. Необходим для синтеза биогенного амина (при декарбоксилировании) – гистамина (понижает давление, расширяет кровеносные сосуды).
5. Необходим для синтеза экстрактивных веществ скелетной мышцы – карнозина и ансерина (специфические дипептиды скелетных мышц позвоночных, участвуют в сокращении, увеличивают амплитуду сокращения мышцы после утомления).
3. Гетероциклические иминокислоты
Пролин(про, пирролидин-a-карбоновая кислота):
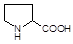
Биологическая роль:
1. Протеиногенная (больше всего в коллагене).
2. Глюкогенная (Гис ® глу ®…).
3. Дестабилизирует пространственную структуру белка, вызывая излом a-цепи).
Применение аминокислот в медицинской
и фармацевтической практике
1. В промышленности и медицине:
· ежегодно производят в мире более 200 тыс. тонн аминокислот, в основном как пищевые добавки и компоненты кормов для скота;
· традиционные методы получения – ферментативный гидролиз, химический и ферментативный синтез;
· больше всего производят лиз и глу, а также гли и мет.
2. В качестве лекарственных препаратов:
· в основном применяются мет, гис, глу и асп, а также арг, фен и цис (например, на основе ГАМК создан препарат гаммалон (аминолон), применяемый при нарушениях мозгового кровообращения после инсульта, при атеросклерозе мозговых сосудов, потере памяти);
· асп – способствует повышению потребления кислорода сердечной мышцей. В кардиологии применяют панангин – препарат, содержащий К и аспартат Mg (его применяют для лечения аритмий и ишемической болезни сердца);
· мет – назначают при отравлениях эндотоксинами, для защиты от экзотоксинов, обладает радиопротекторными свойствами, в геронтологии – в качестве профилактического средства;
· гли – как ГАМК, является медиатором торможения ЦНС. Применяют для лечения хронического алкоголизма, производный глицина – бетаин – эффективный гепатопротектор;
· вал – входит в состав комплексонов для выведения радио-нуклидов из организма.
3. В пищевой промышленности:
· для улучшения вкуса мяса, консервирования – глу;
· D-триптофан (слаще сахарозы);
· в качестве антиоксидантов в пищевой промышленности используют гли и цис, лиз – как стабилизатор витаминов;
· сладкий на вкус гли применяют при производстве приправ и безалкогольных напитков.
2. Примерные варианты контрольной работы по теме «Аминокислоты: классификация, структура
И биологическая роль»
Вариант 1
1. Приведите примеры гетероциклических аминокислот, производных пропионовой кислоты. Напишите их формулу, укажите название, биологическую роль.
2. Какие из перечисленных аминокислот относятся к полярным незаряженным: лейцин, глутамин, фенилаланин, треонин, валин? Напишите их формулы.
Вариант 2
1. Пролин и гидроксипролин (классификация, структура, биологическая роль).
2. Напишите формулы серосодержащих аминокислот, укажите их биологическую роль.
Вариант 3
1. Напишите формулу аминокислоты, не имеющей стереоизомеров. К какому классу по классификации Ленинджера она относится? Укажите ее биологическую роль.
2. Пирролидин-α-карбоновая кислота. Напишите ее формулу, укажите тривиальное название, классификацию и биологическую роль.
Вариант 4
1. Напишите формулу гомоциклических аминокислот. К каким классам по классификации Ленинджера они относятся? Укажите их биологическую роль.
2. Лизин (структура, классификация, номенклатура и биологическая роль).
Вариант 5
1. Напишите формулу незаменимых аминокислот с разветвленной углеродной цепочкой. К какому классу по классификации Ленинджера они относятся? Укажите их биологическую роль.
2. Напишите формулу аминоуксусной кислоты и α-амино-β-фенилпропионовой кислоты. Укажите их тривиальное название, классификацию и биологическую роль.
Вариант 6
1. Напишите формулу триптофана и серина. Укажите химическое название, классификацию и биологическую роль.
2. Напишите формулу α-амино-γ-метилтиомасляной кислоты и α-амино-изовалерьяновой кислоты. Укажите тривиальное название, биологическую роль, классификацию.
Вариант 7
1. Какие из перечисленных аминокислот (лизин, валин, глутами-новая кислота, треонин) являются гидрофобными неполярными? Напишите их формулы, укажите биологическую роль.
2. Аргинин (структура, классификация, биологическая роль).
Вариант 8
1. Из перечисленных ниже аминокислот укажите гидроксилсодержащие аминокислоты: валин, тирозин, аргинин, серин, аспарагин. Напишите, к какому классу (по всем трем классификациям) они относятся, укажите их биологическую роль.
2. α-амино-β-индолил-пропионовая кислота. Напишите ее формулу, тривиальное название, укажите биологическую роль.
Вариант 9
1. Напишите формулу аминокислоты, способной образовывать дисульфидные мостики в структуре белков. Укажите ее название, классификацию, биологическую роль.
2. Моноаминодикарбоновые кислоты и их амиды. Структура, класси-фикация и биологическая роль.
Вариант 10
1. Напишите формулу аминокислоты, не имеющей стереоизомеров. Укажите ее название, классификацию и биологическую роль.
2. Перечислите аминокислоты, которые относятся к классу неполярных, гидрофобных. Напишите формулы циклических, укажите их биологическую роль.
Вариант 11
1. Какие аминокислоты участвуют в образовании глутатиона? Напишите его формулу и формулы этих аминокислот, укажите их биологическую роль, классификацию.
2. Гистидин (структура, биологическая роль и классификация).
Вариант 12
1. Положительно заряженные аминокислоты, структура, классификация и биологическая роль.
2. Аминокислота – донор метильной группы. Напишите ее формулу, укажите название и классификацию.
Вариант 13
1. Отрицательно заряженные аминокислоты, структура, классификация и биологическая роль.
2. Из чего образуются в организме гистамин, триптамин и серото-нин? Напишите формулы этих аминокислот и биогенных аминов.
Вариант 14
1. Приведите примеры гетероциклических аминокислот, производ-ных пропионовой кислоты. Напишите их формулу, укажите тривиальное название, классификацию и биологическую роль.
2. Из каких аминокислот могут образовываться в организме трупные яды? Напишите формулы этих аминокислот и продуктов их декарбоксилирования.
Вариант 15
1. Пролин и гидроксипролин, структура, классификация и биоло-гическая роль.
2. Напишите формулы аминокислот, участвующих в процессах обезвреживания аммиака в организме человека и животных, укажите, к какому классу по классификации Ленинджера они относятся, их биологическая роль.
Вариант 16
1. Напишите формулу глутаминовой кислоты, валина и гистидина. К каким классам по классификации Ленинджера они относятся? Укажите их биологическую роль.
2. Какая аминокислота применяется в медицинской практике для подавления возбуждения ЦНС? Почему? Напишите формулы ее и биогенного амина, образующегося в организме из этой аминокислоты.
Вариант 17
1. Напишите формулы аминокислот, являющихся производными пропионовой кислоты и относящихся к классу полярных незаряженных. Укажите их название, биологическую роль.
2. Триптофан, структура, классификация и биологическая роль.
Вариант 18
1. Какие из перечисленных аминокислот относятся к классу положительно заряженных: лейцин, аргинин, глицин, лизин, фенилаланин? Напишите их формулу и укажите биологическую роль.
2. Тирозин, структура, классификация и биологическая роль.
Вариант 19
1. Перечислите незаменимые для человека аминокислоты. Напишите формулы циклических аминокислот из них, укажите их название, классификацию и биологическую роль.
2. Цистеин, структура, классификация и биологическая роль.
Вариант 20
1. Серосодержащая незаменимая аминокислота. Структура, классификация и биологическая роль.
2. Гомоциклические аминокислоты, структура, классификация и биологическая роль.
