Возбудители вирусных кровяных инфекций.Источники и пути заражения. Характерные клинические проявления. Профилактика распространения инфекций
Возбудители кровяных инфекций представлены главным образом вирусами, риккетсиями и гельминтами, реже - простейшими и бактериями. Сюда относятся все известные риккетсиозы, как эпидемические (сыпной тиф, окопная лихорадка), так и многочисленные эндемические клещевые риккетсиозы. Из вирусных инфекций к этому типу относятся многочисленные арбовирусные и аренавирусные инфекции. Гельминтозы среди кровяных инфекций представлены филяриидозами. Среди инфекций, вызываемых простейшими, наиболее распространенными болезнями являются малярия, а также лейшманиозы и трипаносомозы. К бактериальным инфекциям относятся: чума, туляремия, возвратный тиф и клещевые спирохетозы, бартонеллезы. Если учесть все эти заболевания, то число их достигает приблизительно 560.
Кровяные инфекции можно разбить на 3 группы: антропонозы, зоонозы синантропных животных и зоонозы диких животных. Последняя группа наиболее многочисленна по сравнению с двумя первыми, однако по распространенности среди людей первое место занимают антропонозы: в числе них паразитарные тифы, малярия, городская форма желтой лихорадки, лихорадка денге, наиболее распространенные лейшманиозы, а также гепатит В. Если попытаться и эту группу инфекций охарактеризовать одной фразой, то можно сказать, что паразиты-возбудители использовали пищевые связи кровососущих членистоногих, нападающих на животных и человека, приспособив к ним механизм перехода от зараженного организма в здоровый, который включает чередование пребывания паразита в организме теплокровного и членистоногого. Разнообразию кровососущих членистоногих и объектов их нападения соответствуют многочисленность и разнообразие инфекций этого типа.
Среди антропонозов выделяется небольшая группа паразитарных тифов, для возбудителей которых переносчиком (если пользоваться эпидемиологическими понятиями) шли вторым хозяином паразита (если исходить из паразитологических понятий) является вошь - единственный из известных кровососущих паразитов, имеющий только одного хозяина-человека. Моногостальность (наличие одного хозяина) этого паразита, постоянно живущего на человеке и не способного питаться кровью животных, является причиной того, что передаваемые им заболевания - сыпной и возвратный тифы - не связаны с определенным территориями.
Все остальные антропонозы связаны с летающими кровососущими насекомыми и в силу этого их ареал определяется прежде всего ареалами этих переносчиков. Но на самом деле он более узок, во-первых, потому, что не везде, где есть насекомые, живет человек, во-вторых, потому, что развитие паразита также требует определенных условий, например, возбудителе, желтой лихорадки не развивается в крайних северных районах распространения комара Aedes aegypti в силу недостаточно высокой температуры, необходимой для размножения вируса в организме комара. Сочетание этих факторов и является причиной разнообразия эндемичных очагов трансмиссивных антропонозов.
Особое место среди кровяных инфекций занимает гепатит В. Не касаясь истории этой болезни, отмечу, что в настоящее время эта болезнь распространяется препаратами крови (цельная кровь, плазма, сыворотка, форменные элементы крови), а также шприцами, иглами, зубоврачебными инструментами. При массовости соответствующих вмешательств этот механизм передачи поддерживает высокий уровень заболеваемости гепатитом.
Как говорилось и в отношении кишечных инфекций, зоонозы, относящиеся к кровяным инфекциям, не требуют участия человека для поддержания существования вида этих возбудителей, И здесь человек, заразившийся соответствующем зоонозом, является эпидемиологическим тупиком, если даже заболевания и имеют тенденцию к дальнейшему распространению от человека человеку, как иногда наблюдается при чуме (легочная форма). Такое временное распространение возбудителя «среди людей, иногда весьма значительное (например, но время эпидемий чумы в Европе в XIV столетии, охватившем миллионы людей), не упрочило существование чумного микроба кик биологического вида, так как имеется лишь одна гарантии этою - существование природных очагов чумы и в меньшей мере - существование очагов крысиной чумы в населенных пунктах. Влияние человека и здесь не прямое и заключается в формировании, помимо его воли, зоонозов домашних животных, а также в разрушении природных очагов заразных болезней.
Рассмотрение кровяных инфекций следует дополнить двумя замечаниями. Хозяевами возбудителей часто считают теплокровных животных, а переносчиками - членистоногих, и в этом невольно проявляется антропоцентризм. Между тем «с точки зрения» паразита клещ является главным хозяином, так как в нем проходит главная часть жизни паразита, а теплокровное животное скорее служит переносчиком, распространителем возбудителя в популяции клещей. С этой же точки зрения для малярийного плазмодия главным хозяином является комар, так как именно в его организме осуществляется половая стадия развития паразита, тогда как человек - всего лишь «распространитель» возбудителя.
Второе замечание касается непредвиденных последствий встречи возбудителя с особями и популяциями любого биологического вида (и человек не является исключением), с которым этот возбудитель обычно не встречается в силу экологической изоляции, Обезьяньи вирусы Марбург и Эбола, связанные с дикими грызунами аренавирусные инфекции, десятки арбовирусных инфекций, чума, мелиоидоз - вот лишь некоторые примеры зоонозов диких животных, вызывающих у людей тяжелейшие заболевания с высокой смертностью, но практически не влияющие на состояние популяций, адаптированных к возбудителю хозяев в природных очагах инфекции. Длительная циркуляция возбудителя в биоценозе неминуемо приводит в результате естественного отбора к изменению генофонда популяции основных хозяев со снижением смертности при заражении данным агентом. Одновременно происходит и изменение свойств популяции возбудителя со снижением его патогенности для хозяина. В общебиологическом плане этот ход эволюции отражает борьбу биологических видов за существование как частный случай рассмотренного феномена, а применительно к антропонозным инфекциям, вероятно, его следует расценивать как необычайно тяжелое клиническое течение таких массовых инфекций, как грипп и корь среди изолированных этнических групп, не адаптированных к встрече с этими возбудителями.
Итак, именно популяции являются единицей эволюции. Каждая популяция характеризуется определенным генофондом. Эволюция происходит при изменении частоты генов в ней, когда равновесие нарушается мутационным процессом, избирательным воспроизводством особей за счет естественного отбора и дрейфом генов в генетически изолированных популяциях. Изучение всех этих процессов имеет исключительно важное значение в раскрытии причин изменчивости возбудителей и, в конечном счете, возникновении эпизоотий и эпидемий.
Интерферон и другие противовирусные препараты. Индукторы интерферона. Устойчивость вирусов к химиопрепаратам. В последние годы наблюдается стремительный рост производства и продаж препаратов, противовирусного действия, рекомендованных для лечения гриппа и различных ОРВИ. Несмотря на широкую рекламную кампанию, заказанную фармакологическими фабриками, существует определенная недоказанность действия лекарств описываемой группы, тем не менее, регистрировались случаи успешной терапии такими средствами. Лечение вирусных инфекций (грипп и ОРВИ) основано на применении нескольких отличных друг от друга подходов. Каждый подход подразумевает использование препаратов определенного специфического действия.
Существует ли лучшее лекарство В связи с абсолютно разным механизмом воздействия препаратов направленных на противовирусную терапию, не существует отдельно взятого средства, которое является наилучшим для лечения. Каждый тип лекарства может оказывать разное действие у пациента. Терапия зависит от сроков заболевания, иммунного ответа заболевшего, типа вируса, наличия каких-либо аутоиммунных заболеваний (сахарный диабет, ревматоидный артрит и др.). Выбор отдельного противовирусного препарата зависит от вероятности вызова аллергических реакций. Современное лечение (предупреждение) гриппа и ОРВИ включает следующие мероприятия:
· проведение вакцинации в период прогнозирования вируса гриппа известного штамма (уменьшает вероятность развития);
· прием препаратов интерферона;
· прием противовирусных препаратов, подавляющих размножение вируса;
· прием иммуностимулирующих средств для усиления неспецифического иммунитета.
Проведение вакцинации нужно относить скорее к предупреждающим профилактическим мерам. Вакцинация актуальна только тогда, когда известны конкретные штаммы вируса гриппа, которые предположительно могут распространяться в определенном регионе и стране в ближайшее время. Как лечебный препарат вакцины не рассматриваются, так как механизм их действия основан на предварительном образовании антител к определенным вирусам. То есть любая вакцинация эффективна тогда, когда здоровый организм получают живую или инактивированную вакцину, в результате образуются антитела, блокирующие размножение попавшего в организм вируса. Препараты на основе интерферона, противовирусные и иммуностимулирующие средства активны в период течения заболевания. По каждому из типов лекарств нет единого научного мнения, доказанного исследованиями на широких слоях заболевшей аудитории. В основном производителями заложен гипотетический прогноз их действия относительно вируса гриппа и ОРВИ, иногда подкрепленный частными заказами лабораторных исследований их действия. Несмотря на отсутствие широких рандомизированных исследований, лечебное действие многих противовирусных лекарств подтверждается практикующими врачами. Эффективные препараты на основе интерферона Интерфероны являются специфическими белками, которые выделяются клетками, в результате ответной реакции на вторжение вируса. После попадания вируса в клетку и выделения интерферона запускается реакция, в ходе которой появляется невосприимчивость клеток к вирусу. Это приводит к остановке его размножения и распространению. Одними из известных препаратов группы интерферонов являются:
· циклоферон;
· кипферон;
· виферон.
Циклоферон относится к индукторам интерферона, обладает противовирусным и иммуностимулирующим действием. Отмечена и противовоспалительная способность. Одним из показаний для приема циклоферона является грипп и ОРВИ. Выпускается в виде таблеток, инъекций и линимента. Данное средство назначается взрослым и детям, которые достигли четырехлетнего возраста. Препарат запускает индукцию альфа- и бета интерферонов, в тканях человека, что приводит к невосприимчивости клеток к действию вируса. Также замедляется его размножение. Иммуностимулирующая деятельность средства корректирует иммунный статус больного, одновременно происходит активация клеток-киллеров, которые воздействуют на пораженные вирусом клетки. Параллельно циклоферон применяют при вирусных гепатитах, различных видов герпеса. Противопоказания: цирроз печени, беременность, период кормления грудью, аллергическая непереносимость. Побочные действия:
· в основном выражены аллергическими проявлениями, которые исчезают после прекращения приема препарата.
Эффективность препарата не доказана проведением широкомасштабных исследований, отдельные клинические испытания подтверждают эффект от терапии циклофероном. Следует учитывать, что прием этого вещества усиливает действие некоторых антибиотиков. Развития аутоиммунных болезней на фоне приема циклоферона не отмечалось. Кипферон позиционируется как противовирусный и иммуномодулирующий препарат, с противовоспалительным действием. Также отмечен антибактериальный эффект. Выпускается в виде интравагинальных и ректальных свечей. Показания включают терапию различных заболеваний вирусной и бактериальной этиологии таких как: грипп, ОРВИ, аденовирусная инфекция, кишечные инфекции различных видов. Отдельно применяют препарат при лечении гинекологических заболеваний. Действие кипферона основано на индукции интерферонов, в результате повышается неспецифическая иммунная реакция, приводящая к остановке размножения вирусов и их гибели. Противопоказания: индивидуальная непереносимость, в случае беременности или лактации прием согласовывают с врачом. Побочное действие на фоне терапии кипфероном не отмечено. Эффективность препарата, так же как и у циклоферона не доказана рандомизированными исследованиями. Практика врачей, назначающих кипферон, утверждает о действенности этого средства при терапии вирусных инфекций, включая грипп и ОРВИ. Виферон является комплексным противовирусным препаратом, который применяют для лечения гриппа, ОРВИ, герпетических инфекций, гепатитов. Часто, терапия вифероном проводится комплексно с другими средствами. Форма выпуска – свечи(суппозитории), мазь, гель. Препарат содержит человеческий интерферон альфа-2b, витамин С и Е. Основой для свечей служит масло-какао. Действие Виферона направлено на подавление вирусов, повышение собственного интерферона, отмечается повышение выработки антител и иммуномодулирующее действие. Производитель средства отмечает эффект в сочетании с витаминами, выраженный в нормализации уровня иммуноглобулина, отсутствии побочных эффектов. Противопоказания отсутствуют, если нет предрасположенности к аллергическим реакциям. Побочных явлений не обнаружено. Эффективность Виферона доказана курсом клинических исследований и испытаний в России. Исследования, которые соответствуют международным стандартам, не проводились. Практикующие педиатры и отдельные врачи доказывают эффект, появляющийся после терапии Вифероном. В некоторых случаях, при лечении заболеваний комплексным методом, удалось снижать курс антибактериальной терапии. Противовирусные средства прямого действия Данная группа препаратов, обладает прямым воздействием на вирус гриппа, нарушается его репликация, блокируется слияние вирусной оболочки в клетке. Также отмечается и индуктивное действие в отношении интерферона. Ингавирин это противовирусный препарат, на основе витаглутама, активен в отношении гриппа А и Б, аденовирусных инфекций. Параллельно является иммуномодулятором. Отмечается высокая противовоспалительная деятельность. Показаниями для приема ингавирина служатгрипп различных штаммов, парагрипп, респираторные инфекции. Выпускается в виде капсул. Дозировка и длительность лечения определяются врачом. Противопоказания: дети до 18 лет, беременность, гиперчувствительность. Побочные действия выражены в редких аллергических реакциях. Эффективность от терапии ингавирином гриппа и ОРВИ не доказана. Ранее проводились исследования на действие витоглутама у пациентов с онкологическими диагнозами. Ярко выраженного действия при лечении гриппа не наблюдается. Исключение составляют случаи небольшого сокращения периода болезни. Римантадин известен, как средство, которое на протяжении долгого времени применяется для профилактики и лечения гриппа. Является производным адамантана, для которого характерно замедление функции репродукции вируса после его проникновения в клетку. Активность римантадина обусловлена деятельностью против вируса гриппа А. Препарат получил широкую известность с 70-х годов прошлого века, при этом было проведено значительное количество исследований действия данного лекарства. Показания: профилактика и лечение гриппа А. Противопоказания: возраст детей до 7-ми лет, заболевание печени и почек, в том числе хронического характера, беременность. Побочные действия:(тошнота; рвота;боли в эпигастрии;головокружение). Отмечается повышение уровня билирубина. С осторожностью следует принимать людям пожилого возраста, в виду того, что у пациентов с артериальной гипертензией может развиться геморрагический инсульт. Эффективность средства доказана многими клиническими испытаниями. Большинство пациентов принимающих римантадин (при условии гриппа А) отмечают существенной облегчение течения заболевания и сокращение периода болезни. Тамифлю (осельтавмовира карбоксилат) показан при гриппе А и В и не эффективен при ОРВИ. Лекарственный препарат не является мерой профилактики, в виду его выраженной токсичности. Длительное лечение Тамифлю может привести к психическим расстройствам и нарушению функции почек. Выпускается в виде капсул и в форме порошка для суспензии. Основное действие состоит в подавлении репликации и росте вируса. Концентрация Тамифлю для ингибирования вируса гриппа В превосходит концентрацию для вируса А. Противопоказания: острая почечная недостаточность, аллергические реакции на препарат. В период беременности и лактации требуется дополнительная консультация врача. Побочные действия:
· головная боль, бессонница;
· тошнота и рвота;
· боль в животе, кашель;
· у детей: острый отит, синусит, пневмония.
Эффективность и безопасность. На сегодняшний день исследования действия препарата Тамифлю не завершены. Следует знать, что средство признано токсичным, в связи, с чем остановлены массовые закупки в ведущих странах мира. Среди отзывов врачей практикующих лечение гриппа Тамифлю, преобладает положительный характер. Многими клиниками доказана эффективность средства против некоторых штаммов гриппа, но из-за высокой вероятности побочных явлений терапия этим препаратом вызывает вопросы.
Арбидол является средством, которое подавляет вирусы гриппа А и В, применяется при лечении тяжелого респираторного синдрома и тяжелых кишечных инфекциях ротавирусного типа. Терапевтическая активность Арбидола объясняется в сокращении периода болезни и симптомов интоксикации. Вещество малотоксичное и не вызывает серьезных последствий во время лечения. Действующим веществом выступает умифеновир. Выпускается в виде капсул. Противопоказания: не применяется в возрасте до 3-х лет и в период беременности. Повышенная чувствительность к арбидолу. Побочные действия:
· аллергические реакции;
· головокружение.
Эффективность препарата не имеет четких доказательств, так как не проводились широкомасштабные исследования. Отдельные мнения врачей и пациентов распределены неоднозначно. Существуют как положительные, так и отрицательные моменты в результатах терапии. Иммуностимуляторы Тилорон синтетический индуктор интерферона. Вызывает его образование в организме, включая все подтипы. Выпускается в виде таблеток. Показаниями являются: грипп всех типов, ОРВИ, вирусные энцефаломиелиты. Противопоказания – беременность и период лактации. Нельзя проводить лечение тилороном детям до 7 лет. Побочные действия:
· аллергические реакции;
· озноб;
· головная боль.
Эффективность препарата имеет очевидное доказательство, в виду того, что это средство выпускается в течение 40 лет. Показано применение для профилактики гриппа и ОРВИ. Несмотря на это существует мнение специалистов ведущих клиник о токсичности Тилорона. Практикующие врачи несомненно видят терапевтический эффект терапии этим средством. Кагоцел также является индуктором синтеза интерферона. Применяется для лечения гриппа всех штаммов и ОРВИ. При этом рекомендуется начинать терапию Кагоцелом в первые 24 часа от начала болезни. Кагоцел содержит полифенол Госсипол, который весьма активен в отношении вирусов гриппа. Во время приема разовой дозы наблюдается максимальная концентрация интерферона в крови, что определяет его быстрое воздействие. Противопоказания: беременность, кормление грудью, нельзя принимать детям до 3-х лет. Побочные действия, в основном, выражены аллергическими реакциями. Эффективность терапии достаточно высока. Тем не менее, западные клиники пришли к выводу, что лечение Кагоцелом может приводить к нежелательным последствиям, из-за токсичности Госсипола. Отечественные исследователи не пришли к однозначному выводу, поэтому практика лечения Кагоцелом не является редкостью. Большое значение имеет то, что этот препарат действительно оказывает положительное действие, тем самым нивелирует вероятность возможных последствий. Цитовир 3 препарат комплексного действия, содержащий Тимоген, аскорбиновую кислоту и бендазол. Позиционируется как индуктор интерферона с действием аналогичным Кагоцелу и Тилорону. При этом предполагается, что бендазол усиливает выработку интерферона эндогенной природы. Выпускается в виде капсул, сиропа и порошка для растовра. Показания – лечение гриппа и ОРВИ на ранних стадиях. Противопоказания: прием детям до 1-го года (сироп), до 6-ти лет (капсулы),беременность, лактация Побочные действия:
· снижение АД;
· аллергические реакции.
Эффективность Цитовира 3 не имеет четкого представления, так как препарат не проходил рандомизированных исследований. Отзывы врачей и пациентов составляют ½ к ½. Не исключено ошибочное восприятие эффективности этого лекарства, вызванное подавлением вируса самостоятельным иммунным ответом. Терапия гриппа и ОРВИ лекарственными средствами Лавомакс и Реленза, должны учитывать что они являются аналогами рассмотренных веществ. Так, Лавомакс представляет собой заменитель Тилорона и относится к иммуностимуляторам. Реленза выступает в роли аналога Тамифлю, содержит схожее по действию вещество – занамивир, относится к противовирусным средствам. Лечение данными лекарствами выполняется по рекомендованным схемам, при этом противопоказания и побочные действия у них приблизительно такие же как и у брендовых средств. То есть предполагается замещение Тамифлю – Релензой, а Тилорона – Лавомаксом, без потери эффекта. Перамивир является новым лекарством, противовирусного действия. Эффект от его действия схож с Тамифлю. Требуется обратить внимание на то, что Перамивир не имеет существенной базы проведенных исследований, в связи с чем, лечение данным препаратом имеет высокую степень риска в области развития каких-либо последствий. Химиорезистентность у вирусов. Резистентность вирусов к терапии ( к лекарственным средствам ). Устойчивость вирусов к ацикловиру, ганцикловиру, зидовудину, невирапину, рибавирину. Устойчивость вирусов чаще развивается при многократном применении препаратов и передаётся последующим поколениям. Известно, что практически ко всем, заведомо немногочисленным противовирусным средствам, можно экспериментально получить устойчивые штаммы возбудителей. В основе изменения наследственных свойств вирусов лежат два различных процесса — мутация и селекция; для каждого из них важную роль играет внешняя среда как индуктор мутаций и как селективный фактор. Принимая во внимание тот факт, что спонтанные мутации вирусов позвоночных животных возникают с частотой 10-5-10-6, появление природных мутантов — достаточно редкое явление, и первоочередная роль в формировании резистентных штаммов принадлежит процессам селекции. Выделяют два основных пути преодоления устойчивости к химиопрепаратам: комбинированное применение препаратов с различными механизмами действия и использование ЛС, воздействующих на ранние этапы репродукции, что резко снижает вероятность проявления резистентности. В клинических условиях зарегистрированы случаи устойчивости к следующим препаратам. Ацикловир. Выделены устойчивые штаммы герпесвирусов, малопатогенные для лиц с нормальным иммунным статусом, но представляющие серьёзную угрозу для больных с иммунодефицитами, так как такие штаммы способны вызывать диссеминированные поражения, включая поражения ЦНС. Механизм резистентности обусловлен отсутствием или модификациями структуры тимидин киназы; реже устойчивость опосредуют мутации генов, кодирующих структуру ДНК-полимеразу, что делает её невосприимчивой к эффектам прочих ингибиторов фермента. Ганцикловир. Устойчивость обусловлена снижением уровня фоефорилирования ЛС в заражённых клетках в связи с изменениями структуры вирусной фосфотрансферазы и ДНК-полимеразы. Зидовудин. Наблюдают почти 100% резистентность штаммов ВИЧ, выделенных от пациентов, получавших препарат более 6 мес, что в некоторой степени парадоксально, так как известны случаи длительного выживания больных со СПИДом, получавших препарат более 15 мес. Устойчивость обусловлена мутациями генов, кодирующих структуру ревертазы, что приводит к снижению аффинитета фермента к ЛС, но не способности транскрибировать РНК вируса. Невирапин. Устойчивость развивается довольно быстро, иногда через несколько недель после начала химиотерапии; основные механизмы обусловлены точечными мутациями, вызывающими изменения структуры взаимодействующего с ЛС фрагмента молекулы обратной транскриптазы. Цитозинарабинозид и рибавирин. В отличие от прочих известных противовирусных препаратов, до настоящего времени не выявлены штаммы, резистентные к цитозинарабинозиду и рибавирин.
Микрофлора тела здорового человека. Значение микрофлоры тела в жизни человека.МИКРОФЛОРА ТЕЛА ЗДОРОВОГО ЧЕЛОВЕКА Организм человека в норме содержит сотни видов микроорганизмов; среди них доминируют бактерии. Вирусы и простейшие представлены значительно меньшим числом видов.
Термин «нормальная микрофлора» объединяет микроорганизмы, более или менее часто выделяемые из организма здорового человека. Провести четкую границу между сапрофитами и патогенными микробами, входящими в состав нормальной микрофлоры, часто невозможно.
Кровь и внутренние органы здорового человека и животных практически стерильны. Не содержат микробов и некоторые полости, соприкасающиеся с внешней средой - матка, мочевой пузырь. Быстро уничтожаются микробы в легких. Но в ротовой полости, в носу, в кишечнике, во влагалище имеется постоянная нормальная микрофлора, характерная для каждой области тела (аутохтонная). При этом человек служит источником поступления в окружающую среду множества микроорганизмов.
В течение внутриутробного периода организм развивается в стерильных условиях полости матки, и его первичное обсеменение происходит при прохождении через родовые пути и в первые сутки при контакте с окружающей средой. Затем в течение ряда лет после рождения формируется характерный для определенных биотопов его организма микробный «пейзаж». Среди нормальной микрофлоры выделяют резидентную (постоянную) облигатную микрофлору и транзиторную (непостоянную) микрофлору, не способную к длительному существованию в организме. Основные микробные биотопы Кожа
На кожных покровах микроорганизмы подвержены действию бактерицидных факторов сального секрета, повышающих кислотность. В подобных условиях живут преимущественно Staphylococcus epidermidis, микрококки, сарцины, аэробные и анаэробные дифтероиды. Соблюдение элементарных правил гигиены может уменьшить число бактерий на 90%.
Дыхательная система
В верхние дыхательные пути попадают пылевые частицы, нагруженные микроорганизмами, большая часть которых задерживается в носо- и ротоглотке. Здесь растут бактероиды, коринеморфные бактерии, гемофильные палочки, пептококки, лактобактерии, стафилококки, стрептококки, непатогенные нейссерии и др. Трахеи и бронхи обычно стерильны.
Мочеполовая система
Микробный биоценоз органов мочеполовой системы более скудны. Верхние отделы мочевыводящих путей обычно стерильны; в нижних отделах доминируютStaphylococcus epidermidis, негемолитические стрептококки, дифтероиды; часто выделяют грибы родов Candida. В наружных отделах Рис. 2. Нормофлора влагалища.доминируют Mycobacterium smegmatis. В микробиоценоз влагалища включены молочнокислые бактерии, энтерококки, стрептококки, стафилококки, коринебактерии, палочки Додерлайна. 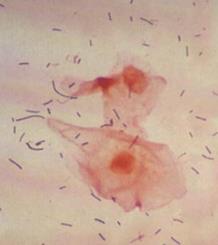 Полость рта
Полость рта
Ротовая полость является удобным местом для развития микроорганизмов. Влажность, обилие питательных веществ, оптимальная температура, слабо щелочная реакция среды являются благоприятными факторами для развития микроорганизмов. Поэтому микрофлора полости рта чрезвычайно обильна и разнообразна.
Среди бактерий доминируют стрептококки, составляющие 30-60% всей микрофлоры ротоглотки. Менее аэрируемые участки колонизируют анаэробы - актиномицеты, бактероиды, фузобактерии и вейлонеллы. В полости рта также обитают спирохеты,микоплазмы, грибы рода Candida и разнообразные простейшие.
Нормальная микрофлора ротовой полости может быть причиной воспалительных процессов и кариеса зубов, однако, при огромном количестве микробов в полости рта воспалительные процессы возникают сравнительно редко. Защитное значение имеют барьерная функция слизистой оболочки и эмали зубов, фагоцитоз. 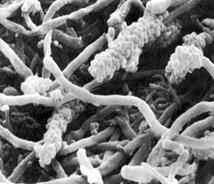 Рис.3.Трехдневный зубной налет(электронная фотография). Желудочно-кишечный тракт(ЖКТ)
Рис.3.Трехдневный зубной налет(электронная фотография). Желудочно-кишечный тракт(ЖКТ)
Наиболее активно бактерии заселяют ЖКТ; при этом колонизация осуществляется «по этажам».
В желудке здорового человека микробов практически нет, что вызвано действием желудочного сока. Тем не менее отдельные виды (например, Helicobacter pylori) адаптировались к обитанию на слизистой оболочке желудка. 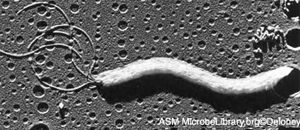 также относительно свободны от бактерий, что связано с неблагоприятным действием щелочного рН и пищеварительных ферментов. Тем не менее в этих отделах можно обнаружить кандиды, стрептококки и лактобациллы. Рис.4.Хеликобактер электронная фотография Верхние отделы тонкой кишки
также относительно свободны от бактерий, что связано с неблагоприятным действием щелочного рН и пищеварительных ферментов. Тем не менее в этих отделах можно обнаружить кандиды, стрептококки и лактобациллы. Рис.4.Хеликобактер электронная фотография Верхние отделы тонкой кишки
Нижние отделы тонкой и, особенно, толстая кишка - огромный резервуар бактерий; их содержание может достигать 1012 в 1 г фекалий (30% сухой массы кала).
Микрофлора кишечника представлена тремя основными группами.
К 1-й группе относятся грамположительные бесспоровые анаэробы - бифидобактерии и грамотрицательные бактероиды, составляющие 95% микробиоценоза. 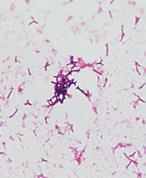
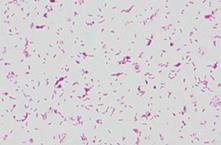 Рис. 5. Бифидобактерии (слева) и бактероиды (справа) кишечника (световая микроскопия).
Рис. 5. Бифидобактерии (слева) и бактероиды (справа) кишечника (световая микроскопия).
2-я группа(сопутствующая микрофлора) представлена в основном аэробами (лактобактерии, кокковая флора, Еscherichia coli) удельный вес ее невелик и не превышает 5%. Лактобактерии и нормальная E. coli являются синергистами бифидобактерий.
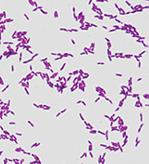
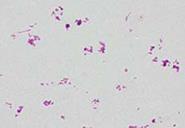

Рис. 6. Лактобактерии (слева), кокковая флора (в центре), кишечная палочка (справа) (световая микроскопия).
В 3-ю группу включают редко встречающуюся микрофлору условно-патогенную или факультативную). Ее удельный вес не превышает 0,01-0,001% от общего количества микробов. Представителями факультативной микрофлоры являются протей, синегнойная палочка, стафилококк, кандида, серрацина, цитро-, энтеро- и кампилобактерии.
Представители 2-й и 3-й групп в физиологических условиях являются симбионтами 1-й группы, прекрасно с ней сосуществуют, не нанося вреда, проявляя агрессивные свойства лишь при определенных условиях.
