Строение коллоидных частиц – мицелл
Отдельные частицы коллоидных растворов называют мицеллами. Мицеллы имеют сложное строение. Основой мицеллярной теории является наличие у мицелл двойного электрического слоя. Он может образоваться:
– либо за счёт избирательной адсорбции ионов на поверхности;
– либо в результате ионизации молекул твёрдой фазы.
Рассмотрим образование мицелл в коллоидном растворе иодида серебра, полученном методом химической конденсации по реакции обмена: AgNO3 + KJ = AgJ↓ + KNO3
В зависимости от соотношения исходных веществ может быть три случая:
а) при эквивалентом соотношении реагентов коллоидный раствор образоваться не может, стабилизация системы происходит за счет уменьшения площади поверхности, т.е. роста кристаллов AgJ и выпадения осадка.
б) рассмотрим образование мицеллы при небольшом избытке KJ. В этом случае уменьшение поверхностной энергии может идти за счёт адсорбции ионов из раствора. Согласно правилу Панета – Фаянса из раствора электролита на поверхности микрокристаллов адсорбируется тот ион, который входит в состав твёрдого тела и способен достраивать его кристаллическую решётку. В нашем случае в растворе имеются ионы К+ и J-. Достраивание кристаллической решётки агрегата идет за счёт ионов J–, входящих в состав кристалла. Иодид-ионы в количестве «n» адсорбируются на поверхности микрокристаллов (агрегате мицеллы), и поверхность приобретает отрицательный заряд: m[AgJ] · nJ- , поэтому их называют потенциалоообразующими. Образуется ядро мицеллы. К поверхности ядра притягиваются из раствора оставшиеся противоионы калия, К+ (но не все, а в количестве «n - x»).
Потенциалообразующие ионы J- и связанные противоионы К+ образуют вокруг ядра плотный адсорбционный слой. Он имеет заряд. Его потенциал называют дзета-потенциалом. Агрегат с адсорбционным слоем составляют гранулу: { m[AgJ] nJ- (n-х) К+ }х-
Поскольку в адсорбционном слое потенциалообразующих ионов больше, чем противоионов, то гранула имеет заряд, совпадающий по знаку с зарядом потенциалообразующих ионов.
В адсорбционный слой гранулы входят не все противоионы К+, а только часть, (n-x), а оставшиеся противоионы К+ (х) находятся дальше – в рыхлом диффузном слое. Почему? Противоионы испытывают действие двух противоположных сил:
1. притяжения к заряженной поверхности ядра;
2. теплового движения, стремящегося равномерно распределить их в объёме.
Поэтому плотность слоя противоионов убывает по мере удаления от заряженной поверхности гранулы.
двойной электрический слой, ДЭС
 агрегат
агрегат
 { m[AgJ] nJ- (n-х) К+ }х- хК+ ∙ l H2O
{ m[AgJ] nJ- (n-х) К+ }х- хК+ ∙ l H2O
ядро потенциало противоионы рыхлый гидратная
образующие диффузный оболочка
 ионы слой
ионы слой
плотный адсорбционный слой
 гранула
гранула
мицелла
Гранула с диффузным слоем образует мицеллу. Мицелла электронейтральна. В зависимости от исходных концентраций растворов, условий и других факторов числа m, n и х могут меняться. Снаружи мицелла окружена гидратной оболочкой. Избыток KJ адсорбировался на поверхности микрокристаллов нерастворимого иодида серебра и образовал двойной электрический слой (ДЭС). Этот защитный слой препятствует росту кристаллов и выпадению осадка. Поэтому избыток электролита, из которого формируется двойной электрический слой, является стабилизатором.
в) если имеется небольшой избыток другого электролита, AgNO3, то состав коллоидной мицеллы будет другим. Агрегат по-прежнему будут составлять молекулы иодида серебра, AgJ. Но после образования мелких кристалликов осадка AgJ – зародышей, в растворе остались лишь ионы Ag+ и NO3-. По правилу Панета-Фаянса адсорбироваться на поверхности могут только ионы Ag+, достраивающие ее кристаллическую решётку.
Ag+ - потенциалообразующие ионы. Образуется ядро - m[AgJ]nAg+ . Значит, противоионами будут ионы NO3-. Вместе с ионами Ag+ они образуют адсорбционный слой, а с агрегатом – положительно заряженную гранулу:
{ m[AgJ] nAg+ (n-х) NO3- }х+
 Оставшиеся х ионов NO3- входят в диффузный слой мицеллы. Они сольватированы
Оставшиеся х ионов NO3- входят в диффузный слой мицеллы. Они сольватированы
{ m[AgJ] nAg+ (n-х) NO3- }х+ хNO3- l H2O
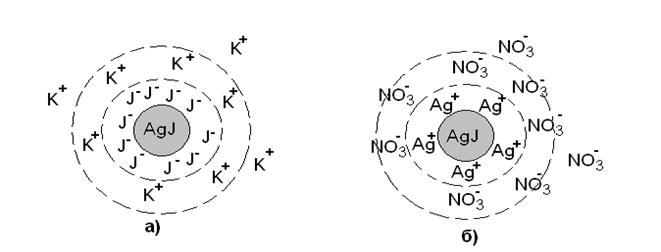
Рис.2.4 Схема строения коллоидной мицеллы золя иодида серебра
а) полученного при избытке KJ
б) полученного при избытке AgNO3
