Превращения азотсодержащих веществ
В природе происходит постоянный круговорот азота, в котором участвуют растения, животные, микроорганизмы. Азот входит в состав белков и продуктов их разложения (пептиды, аминокислоты, пуриновые и пиримидиновые основания), а также в состав мочевины и мочевой кислоты, азотсодержащего полисахарида хитина, гумусовых кислот. Аммонифицирующие микроорганизмы осуществляют разложение органических веществ, переводя азот органических соединений в минеральную форму (аммонийные соли, соли азотистой и азотной кислоты, молекулярный азот и аммиак), а также органические вещества своих клеток. Нитрифицирующие бактерии способны превращать аммиак в азотистую кислоту, а затем в азотную. Затем в процессе денитрификации происходит выделение свободного азота в атмосферу. Зеленые растения при синтезе белков способны использовать только азот минеральных солей - нитратов и нитритов (в меньшей степени аммонийных солей), свободный азот воздуха и связанный в органических соединениях азот им недоступен. Азот из атмосферного воздуха способны ассимилировать только специальные азотфиксирующие бактерии (рисунок Г.7)
Аммонификация
Аммонификация белка. Высокомолекулярные соединения, которыми являются белки, не могут непосредственно усваиваться микроорганизмами. Они должны быть расщеплены на составные части. Процесс минерализации белковых веществ микроорганизмами с выделением аммиака или образованием аммонийных солей называется аммонификациейбелка, или гниением, а микроорганизмы, вызывающие этот процесс – аммонифицирующими, или гнилостными микроорганизмами. Аммонификация белков начинается с их гидролиза под действием протеолитических экзоферментов микроорганизмов. Происходит последовательное образование пептонов, пептидов и аминокислот. Из полученных соединений наиболее доступными для микроорганизмов являются аминокислоты, которые растворимы в воде. В таком виде они поступают внутрь микробной клетки, где подвергаются воздействию эндоферментов, в частности дезаминированию под воздействием ферментов дезаминаз.
Существуют несколько типов дезаминирования (гидролитическое, окислительное, восстановительное и др.), которые приводят к образованию аммиака, оксикислот (гидрокислот), жирных кислот, кетокислот. Во всех случаях при любом типе дезаминирования среди конечных продуктов всегда обнаруживается аммиак:
+H2O
Гидролитическоедезаминирование: R-CHNH2-COOH → R-CHOH-COOH +NH3
гидрокислота
+H2
Восстановительноедезаминирование: R-CHNH2-COOH → R-CH2-COOH +NH3
жирная кислота
+O2
Окислительноедезаминирование: R-CHNH2-COOH → R-C=O-COOH +NH3
кетокислота
В аэробных условиях, кроме аммиака, образуется диоксид углерода, сероводород, в анаэробных - жирные и ароматические кислоты (бензойная и др.), спирты, индол, скатол, фенол, меркаптаны. В аэробных условиях происходит полное окисление жирных кислот с образованием СО2 и H2O.
Кроме дезаминирования внутри микробной клетки возможны и другие превращения аминокислот – 1) декарбоксилирование, в результате которого появляются первичные амины (предшественники трупных ядов); 2) переаминирование, приводящее к появлению новых аминокислот; 3) синтез белка.
Декарбоксилирование происходит под воздействием эндоферментов декарбоксилаз с образованием СО2 и первичных аминов:
R-CHNH2-COOH → R- CH2 - NH2 + СО2
Сероводород образуется из аминокислот, содержащих серу:
+H2O
SH-CH2CH-NH2-COOH → CH2OH-CHOH-COOH + H2S + NH3
цистеин глицериновая кислота
В анаэробных условиях не происходит полного окисления жирных кислот, и они накапливаются в среде. Из ароматических аминокислот в анаэробных условия образуются неприятно пахнущие вещества – индол, скатол, фенол.
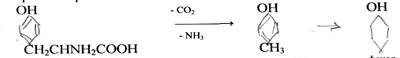
тирозин крезол фенол
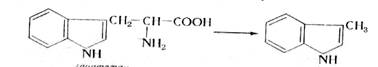
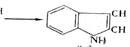
триптофан скатол индол
Из серусодержащих аминокислот образуются меркаптаны:
SH-CH2CH-NH2-COOH → SH-CH2-CH3OH + СО2 + NH3
цистеин этил меркаптан
Индол, скатол, крезол, меркаптаны являются ядовитыми веществами.
Первичные амины (диамины и птомаины) называются также биогенными аминами. Они являются токсическими соединениями, предшественниками трупных ядов.
Из аминокислоты лизина под воздействием фермента декарбоксилазыобразуется кадаверин (предшественник трупного яда нейрина):
NH2-(СH2)4-СH-NH2-COOH → NH2-(СH2)5-NH2 + СО2
Из аминокислоты орнитинапод воздействием декарбоксилазы образуется путресцин (предшественник трупного яда мускарина):
NH2-(СH2)3-СH-NH2-COOH → NH2-(СH2)4-NH2 + СО2
Из аминокислоты аргинина образуется агматин, фенилаланина – фенилэтиламин, тирозина – тирамин, гистидина – гистамин.
Аммонифицирующие микроорганизмы. Аммонификацию белков вызывают микроорганизмы, обладающие протеолитическими ферментами (протеазами).
К аэробным аммонификаторам относятся в основном спорообразующие палочки рода Bacillus: B.mesentericus (картофельная палочка); B.subtilis (сенная палочка); B.mycoides(земляная палочка); B.megaterium и др. Неспорообразующие аэробные аммонификаторы – это в основном пигментообразующие палочки рода Pseudomonas, например. P.fluorescens.
Факультативно-анаэробные аммонификаторы - это в основном представители семейства Enterobacteriaceae:Proteus vulgaris (вульгарный протей); Escherichia coli (кишечная палочка). Аммонифицирующие микроорганизмы встречаются среди актиномицетов, микроскопических грибов, например, грибы родов Penicillium, Mucor, Apergillus, Trichoderma и др.
Гнилостные анаэробные микроорганизмы – это спорообразующие бактерии рода Clostridium, являющееся возбудители раневых инфекций, такие как C.perfringens (возбудитель газовой гангрены), C.teteni (возбудитель столбняка), в такжеC.sporogenes, C.putrificum.
Аммонификация нуклеиновых кислот. Аммонификацию нуклеиновых кислот вызывают микроорганизмы, продуцирующие нуклеазы.Нуклеазы (внеклеточные ДНК-азы и РНК-азы) найдены у многих микроорганизмов – представителей родов Bacillus, Mycobacterium, Nocardia и др. (например, B.megatherium). При распаде нуклеиновых кислот и их производных (пуриновых и пиримидиновых оснований) тоже выделяется аммиак.
Аммонификация мочевины. Мочевина (карбамид) попадает во внешнюю среду в основном с мочой. Человек за сутки выделяет с мочой до 80 г мочевины. Азот в мочевине составляет 46%. За год люди и животные выделяют с мочой свыше 10 млн. т азота. Азот мочевины может усваиваться растениями только после ее разложения. Аммонификацию мочевины осуществляют микроорганизмы, продуцирующие фермент уреазу, под воздействием которого мочевина разлагается до углекислого аммония, который легко распадается на аммиак, углекислый газ и воду:
(NH2)2CO + H2O → (NH4)2СО3 → 2 NH3 + СО2 + H2O
Микроорганизмы, разлагающие мочевину, были открыты в 1862 г. Л.Пастером и названы уролитическими. Это аэробы бактерии, образующие споры. Среди них есть кокки (Micrococcus urea), сарцины (Planosarcina urea), бациллы (Bacillus probates, B.pasteurii). Эти микроорганизмы являются исключением среди кокковых форм. Кубики сарцин состоят из четырех-восьми кокков, имеют споры и покрыты многочисленными жгутиками.
Благодаря образованию углекислого аммония при развитии уробактерий происходит подщелачивание среды (до рН 9-10). Уробактерии относятся к наиболее щелочелюбивым микроорганизмам, оптимум их развития при рН 7,5-8,5. Уробактерии обитают в почве, в рубце жвачных животных, в сточных водах. За счет разложения мочевины почва и водоемы обогащаются доступными для растений формами азота.
Аммонификация мочевой кислоты. Одним из конечных продуктов белкового обмена животных (птиц, пресмыкающихся, насекомых) является мочевая кислота. В помете птиц (гуано) она составляет 25%. В моче млекопитающих концентрация мочевой кислоты незначительна. Разложение мочевой кислоты осуществляется рядом микроорганизмов (например, Clostridium acidiurici) с образованием мочевины и тартроновой кислоты (НООС-СНОН-СООН).
Аммонификация хитина. Хитин – очень стойкое соединение. Это сложный азотсодержащий полисахарид. Структурными элементами хитина являются остатки N-ацетилглюкозамина, соединенные 1,4-глико-зидными связями. Хитин является основным компонентом клеточной стенки многих грибов (например, базидиомицетов, аскомицетов), а также панцирных покровов насекомых, ракообразных, некоторых беспозвоночных. После отмирания этих микроорганизмов хитин попадает в почву, водоемы, где разлагается микроорганизмами, продуцирующими хитиназы. Хитиназы широко распространены у актиномицетов, мукоровых грибов, некоторых бактерий. При разложении хитина образуется аммиак, глюкоза и уксусная кислота.
Аммонификация гумусовых веществ. Значительная часть связанного азота в почве содержится в форме перегнойных (гумусовых) веществ. Их разложение происходит медленно и осуществляется различными группами почвенных бактерий.
Нитрификация
Нитрификация – процесс окисления аммиака до азотистой, а затем азотной кислоты. Процесс в природе происходит в две фазы, каждая из которых осуществляется специфическими группами бактерий. Первая фаза нитрификации– окисление аммонийных солей до солей азотистой кислоты (нитритов) осуществляется нитритнымибактериями – представителями родов Nitrosomonas, Nitrosocystis, Nitrosospira, Nitrosovibrio, Nitrosolobus:
2 NH3 + 3 О2 → 2 НNO2 + H2O + Эн. (148 ккал)
Вторая фаза нитрификации– окисление нитритов в нитраты осуществляется нитратными бактериями – представителями родов Nitrobacter, Nitrococcus, Nitrospira:
2 НNO2 + О2 → 2 НNO3 + Эн. (48 ккал)
Нитрифицирующие бактерии открыл в 1889 г. С.Н. Виноградский. В настоящее время они объединены в семейство Nitrobacteriaceae. Это грамотрицательные микроорганизмы, облигатные аэробы или микроаэрофилы. Большинство их являются облигатными автотрофами, которые при наличии органических веществ не размножаются. Лишь некоторые из них включают в состав своих клеток углерод отдельных органических соединений (глюкозы, аминокислот). Основным источником углерода для нитрифицирующих бактерий является СО2 воздуха, а энергия поступает в результате окисления аммиака.
Нитрификация происходит в почвах, озерах, морях, океанах. Она имеет как положительное значение, являясь важным этапом в круговороте азота в природе, так и отрицательное - может привести к обеднению почв азотом в результате вымывания нитратов. С целью регуляции этого процесса вносят препараты, ингибирующие нитрификацию.
Образовавшиеся при нитрификации нитраты подвергаются в почве дальнейшим превращениям: 1) они могут быть использованы высшими растениями; 2) могут вымываться в водоемы; 3) закрепляться в клетках микроорганизмов, которые используют нитраты в качестве источника азота; 4) восстанавливаться микроорганизмами до молекулярного азота и аммиака.
Денитрификация
Денитрификация – это восстановление, в результате которого азот переходит в менее окисленную форму, чем в нитратах. При денитрификации происходит восстановление нитратов до нитритов и далее до молекулярного азота:
NO3- → NO2- → NO → N2O → N2
Этот перенос приводит к потере определенного количества почвенного азота и возврату его в атмосферу. В зависимости от того, какие микроорганизмы принимают участие6 в процессе денитрификации, различают прямую и косвенную денитрификацию.
Прямая денитрификация осуществляется непосредственно микроорганизмами, способными восстанавливать нитраты, используя их в качестве акцептора водорода при окислении ими органических веществ. Способностью к прямой денитрификации обладают многие почвенные микроорганизмы. Наиболее активными среди них являются бактерии рода Micrococcus (M. deni-trificans), некоторые бациллы.
Микроорганизмы-денитрификаторы имеют две ферментные системы денитрификации: цитохромную (диссимиляционную) и флавопротеидную (ассимиляционную). Наличие этих систем обеспечивает два пути восстановления нитратов: ассимиляционный (неспецифический) и диссимиляционный (специфический).
Ассимиляционная денитрификация приводит к образованию аммиака, который ассимилируется организмом и включается в метаболизм. Нитраты здесь используются как источники азота. Диссимиляционная денитрификация осуществляется микроорганизмами для получения энергии и ее конечным продуктом является молекулярный азот.
4Н гидроксиламин Н2 Ассимиляционная
→ NН2OH → NH3 + Н2O денитрификация
Н2 Н2 ∕
NO3 → NO2 → NO
\ - Н2О Н2 Диссимиляционная
нитрат нитрит оксид → N2O → N2 + Н2O денитрификация
азота (II) оксид
азота (I)
Большинство денитрификаторов хемоорганотрофы. Использование в качестве конечного акцептора электронов нитратов позволяет им окислять органические субстраты до СО2 и воды. Однако есть один вид денитрификаторов, который способен усваивать СО2 воздуха. Это Thiobacillus denitrificans. В отсутствие органических соединений он окисляет серу до серной кислоты за счет кислорода нитратов и полученную энергию использует для синтеза органических соединений из СО2 воздуха.
Денитрифицирующие бактерии – факультативные анаэробы, переключающиеся на денитрификацию только в отсутствие кислорода. В аэробных условиях эти микроорганизмы окисляют органические вещества. В клетках денитрификаторов есть ферментная система, активизирующая кислород нитратов – нитратаза, и система, активизирующая молекулярный кислород. В анаэробных условиях функционирует первая ферментная система, в аэробных – вторая.
Косвенная денитрификация – чисто химический процесс, реакция восстановления, происходящая при взаимодействии нитратов с аминосоединениями, которые образуются в процессе жизнедеятельности различных микроорганизмов. В результате таких реакций тоже образуется молекулярный азот:
НNO2 + R-CHNH2COOH → R-CHOHCOOH + N2 + Н2O
Микроорганизмам в этой реакции принадлежит косвенная роль, они образуют исходные продукты реакции – нитриты и аминосоединения.
Косвенная денитрификация имеет место только в кислой среде и значение ее невелико, так как окультуренные почвы не кислые. Более распространена в природе прямая денитрификация. В целом же денитрификация - широко распространенный процесс, в результате которого в атмосферу ежегодно поступает свыше 300млн. т азота. Особенно активно денитрификация протекает в ризосфере растений, где имеются органические вещества.
Денитрификации способствуетслабая аэрация, высокая влажность, наличие достаточного количества органических соединений.
Денитрификацию не следует рассматривать как процесс, всегда приводящий к уменьшению азота в почве. Обычно в почве этот процесс до конца не доходит, так как растения усваивают образующиеся промежуточные продукты, возвращая их в круговорот. В настоящее время установлена даже положительная роль денитрификаторов в ризосфере растений, так как они способны кроме денитрификации одновременно осуществлять синтез веществ, стимулирующих рост растений.
Азотфиксация
Фиксация атмосферного азота в природе происходит физико-химическим и биологическим путем. Небиологический путь фиксации азота (грозовые разряды, работа двигателей внутреннего сгорания) дает всего 0,5% фиксированного азота. При электрических разрядах азот вступает в реакции с кислородом или водородом и попадает на землю в виде оксидов азота или аммиака. Основной путь пополнения дефицита азота в почве – процесс азотфиксации. Способность фиксировать молекулярный азот – уникальный процесс, присущий только прокариотам. За счет деятельности азотфиксаторов в почву ежегодно поступает 60-75% азота от общего его содержания в почве.
Способность микроорганизмов фиксировать азот была установлена С.Н. Виноградским и голландским ученым М. Бейеринком. Способность фиксировать молекулярный азот присуща многим систематическим группам бактерий (клостридии, сульфатредуцирующие бактерии, энтеробактерии, фотосинтезирующие спириллы, актиномицеты и многие другие группы прокариот). Существуют свободноживущие и симбиотические азотфиксаторы.
Свободноживущие азотфиксаторы. Представителями этих микроорганизмов являются Clostridium pasteurianum, выделенные в 1893 г. С.Н. Виноградским. Они широко распространены в природе, являются возбудителями маслянокислого брожения.
Бактерии рода Azotobacter выделены в 1901 г. М. Бейеринком. Это аэробные бактерии. Молодые клетки представляют собой грамотрицательные полиморфные палочки, но в зрелом возрасте могут иметь форму диплококков, покрыты толстой слизистой капсулой. Молодые клетки подвижны. При росте на безазотистых питательных средах азотобактеры образуют слизистые выпуклые колонии, окрашенные в темно-коричневый цвет (A.chroococcum), в желтый (A.vinelandii) и другие цвета. Источником углерода и энергии для азотобактера служат углеводы, спирты, органические кислоты. Источниками азота, кроме молекулярного, могут быть соли аммония, нитраты, нитриты, аминокислоты, мочевина. При культивировании на азотсодержащих средах азотобактер утрачивает азотфиксирующую способность.
Аэробные азотфиксирующие бактерии рода Beijerinkia имеют морфологическое сходство с азотобактером, но отличаются медленным ростом м высокой кислотоустойчивостью (развиваются при рН=3,0). К свободноживущим азотфиксаторам относятся также фотосинтезирующие бактерии, некоторые микобактерии, актиномицеты, синезеленые водоросли.
Симбиотические азотфиксаторы. Это клубеньковые бактерии, впервые обнаруженные в 1866 г. М.С.Ворониным на корнях люпина и ольхи в клубеньках. Клубеньковые бактерии чаще всего обнаруживаются там, где растут бобовые растения, хотя могут встречаться в почве и в свободном состоянии. Клубеньковые бактерии объединены в род Rhizobium (греч. rhizo – корень, bios – жизнь). Они проникают через корневые волоски в корневую систему растений и стимулируют деление тетраплоидных клеток корня, приводящее к образованию клубеньков. В клубеньках происходит интенсивное размножение бактерий. В молодых клубеньках большинство бактерий имеет форму палочек, с возрастом появляются клетки неправильной формы – бактероиды (L V X ), в которых происходит фиксация азота.
Клубеньковые бактерии характеризуются: специфичностью – способностью образовывать клубеньки только на корнях определенных видов бобовых растений; вирулентностью– способностью проникать через корневые волоски в корни растений и там образовывать клубеньки; активностью – интенсивностью фиксации азота. Активность клубеньковых бактерий связана с наличием в них гемоглобина, который называется леггемоглобин. Это единственный представитель гемоглобинов, обнаруженных в растительном мире. Образование его возможно только в симбиозе бактерий с растениями. Ни клубеньковые бактерии, ни бобовые растения сами по себе не способны к синтезу гемоглобина. Леггемоглобин выполняет функции регулятора парциального давления кислорода и транспорта электронов в азотфиксирующую систему.
Отношения между клубеньковыми бактериями и бобовыми растениями – пример мутуализма (симбиоза, при котором оба симбионта извлекают выгоду от совместного сожительства: растение получает азот, а бактерии используют корневые выделения).
Биологическая фиксация азота представляет собой ферментативный процесс восстановления молекулярного азота. Все азотфиксаторы обладают ферментной системой нирогеназой. Нитрогеназы всех известных азотфиксаторов состоят из двух белков: один белок содержит только атомы железа (малый компонент – азоферродоксин), другой – атомы молибдена и железа (большой компонент – молибдоферродоксин). В активации молекулы азота участвует молибден, а соединения железа используются как переносчик электронов. Нитрогеназа восстанавливает не только азот, но и другие соединения с тройной связью. Способность микроорганизмов фиксировать азот и обогащать им почву нашла применение в сельском хозяйстве. На основании использования клубеньковых бактерий и азотобактера получают удобрения нитрагин и азотобактерин.
Контрольные вопросы: 1. Какие микроорганизмы являются возбудителями спиртового брожения? 2. Какие существуют формы спиртового брожения, в каких условиях они протекают? 3. Что такое эффект Пастера? 4. Что такое эффект Крэбтри? 5. Какие существуют виды молочнокислого брожения? 6. Какие микроорганизмы вызывают молочнокислое брожение? 7. Какие микроорганизмы являются возбудителями пропионовокислого брожения? 8. Какие микроорганизмы вызывают маслянокислое брожение? 9. Какие микроорганизмы являются возбудителями ацетонобутанолового и ацетоноэтанолового брожений? 10. В каких условиях происходит уксуснокислое брожение? Какие микроорганизмы являются возбудителями этого процесса? 11. Какие плесневые грибы используют для получения органических кислот? 12. Как происходит расщепление микроорганизмами липидов? 13. Какие микроорганизмы участвуют в аэробном и анаэробном процессе распада клетчатки? 14. Какие микроорганизмы осуществляют аэробное и анаэробное разложение пектиновых веществ? 15. Какие микроорганизмы называются гнилостными? 16. Какое вещество получается при всех типах дезаминирования аминокислот? 17. Какие продукты получаются при аммонификации белков в аэробных и анаэробных условиях? 18. Какие микроорганизмы вызывают аммонификацию мочевины и в чем их особенность? 19. Какие микроорганизмы осуществляют первую и вторую фазы нитрификации? 20. В чем различие ассимиляционной и диссимиляционной денитрификации? 21. В каких условиях происходит денитрификация? 22. В чем состоит уникальность биологической азотфиксации? 23. Какие микроорганизмы относятся к свободноживущим аэробным азотфиксаторам? 24. Какие микроорганизмы относятся к свободноживущим анаэробным азотфиксаторам? 25. Какими свойствами характеризуются симбиотические азотфиксаторы?
