Оптимальні значення рН для деяких ферментів
(зa T.T. Березовим і Б.Ф. Коровкіним)
| Фермент | рН | Фермент | рН |
| Пепсин | 1,5 – 2,5 | Каталаза | 6,8 – 7,0 |
| Катепсин В | 4,5 – 5,0 | Уреаза | 7,0 – 7,2 |
| Амілаза із солоду | 4,9 – 5,2 | Панкреатична ліпаза | 7,0 – 8,5 |
| Сахароза кишкова | 5,8 – 6,2 | Трипсин | 7,5 – 8,5 |
| Амілаза слини | 6,8 – 7,0 | Аргіназа | 9,5 – 10,0 |
Більшість ферментів проявляє максимальну каталітичну активність при рН = 7 (рис. 3). Зміни рН уповільнюють або припиняють дію ферментів.
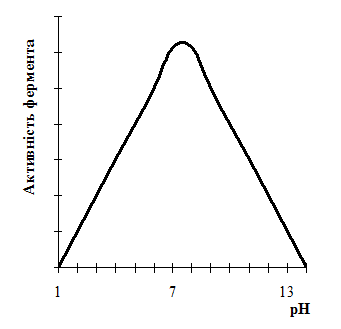
Рис. 3. Залежність активності ферментів від рН середовища
Вплив рН на активність ферментів пояснюється структурою їх молекул. Молекула ферменту має один або декілька активних центрів, в яких сконцентровані функціональні групи білків (рис. 5). Ступінь їх іонізації залежить від рН середовища. Більш того, рН середовища впливає на ступінь іонізації субстратів, фермент-субстратного комплексу і продуктів реакції, структуру молекули ферменту. Все це разом і визначає каталітичну здатність ферменту в тій або іншій реакції. Прикладом може бути фермент РНК-аза, яка розщеплює молекулу РНК на мононуклеотиди. Молекула РНК-ази, особливо її активний центр, містить високий відсоток лізину. Аміногрупа, розміщена в e-положенні, зазвичай вільна і визначає активність ферменту. Її іонізація можлива в кислому середовищі, тому і оптимальне значення рН для РНК-ази буде дорівнювати 5,4 – 5,6. У лужному середовищі фермент не активний, оскільки іонізація аміногрупи в цих умовах неможлива.
Специфічність дії ферментів. Кожний фермент діє на певний субстрат або групу речовин, схожих за своєю будовою. Специфічність дії ферментів пояснюється подібністю просторових конфігурацій активного центру ферменту і субстрату, їх хімічною спорідненістю, що призводить до утворення фермент-субстратного комплексу і здійснення каталітичного процесу. Без специфічності ферментів був би неможливий впорядкований ланцюг реакцій обміну речовин.
Розрізняють індивідуальну (абсолютну і стереохімічну) і групову (абсолютну і відносну) специфічність ферментів. Ферменти, які каталізують лише одну реакцію і діють на один точно визначений субстрат, мають абсолютну індивідуальну специфічність. Абсолютною специфічністю володіє уреаза, яка розщеплює сечовину на аміак і вуглекислий газ:
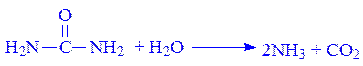
Довгий час вважали, що сечовина є єдиним субстратом уреази. Однак зовсім недавно було доведено, що кристалічна уреаза може діяти також на окремі сполуки – похідні сечовини, зокрема на оксисечовину. Правда реакція гідролізу оксисечовини відбувається у 100 разів повільніше:
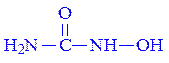
Стереохімічна абсолютна специфічність ферментів проявляється тоді, коли вони діють на оптично активні сполуки, або сполуки, для яких характерна цис- і транс-ізомерія. Прикладом стереохімічної специфічності є фумаратгідратаза. Вона каталізує приєднання води до фумарової кислоти, але не впливає на цис-ізомер – малеїнову кислоту:
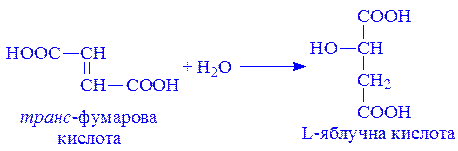
Групова абсолютна специфічність характерна для ферментів, які діють на різні субстрати, що мають однаковий тип зв’язку. Прикладом абсолютної групової специфічності може бути дія пепсину на різні білки (прості і складні) тваринного, рослинного і мікробного походження. До ферментів з груповою специфічністю належать також естерази, які каталізують гідролітичне розщеплення зв’язку складноефірного типу:
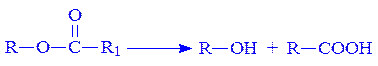
Відносну групову специфічність проявляють лужна і кисла фосфатази, які каталізують гідроліз моноефірів ортофосфорної кислоти. Зустрічається подвійна специфічність, наприклад, ксантиноксидаза, яка специфічно окислює пуринові основи і неспецифічно – альдегіди. Іноді подвійна специфічність позначається на механізмі реакції між субстратом і ферментом. Так, ізоцитратдегідрогеназа залежно від умов викликає або декарбоксилування, або окислення ізоцитрата.
Активатори і інгібітори ферментів. На активність ферментів впливає багато речовин. Деякі з них підвищують активність ферментів, інші – гальмують. Перші речовини називають активаторами, другі – інгібіторами, або паралізаторами. Нерідко одні і ті ж речовини для одних ферментів можуть бути активаторами, для інших – інгібіторами. Так, соляна кислота є активатором для пепсину і інгібітором для амілази слини. Активність ферменту зменшується у міру збільшення концентрації продуктів, що утворюються в результаті хімічних реакцій та каталізуються даним ферментом.
Розрізняють специфічні і неспецифічні активатори і інгібітори. Прикладом специфічного активатора для пепсину є соляна кислота, для трипсину – ентеропептидаза. Під їх впливом від молекули попередника (пепсиногена і трипсиногена) відщеплюється пептид, відкривається активний центр і формується молекула ферменту. Пептиди, що відщепилися, можна розглядати як специфічні інгібітори. До типових специфічних активаторів слід віднести жовчні кислоти, що активують ліпазу. Типовими специфічними інгібіторами є антиферменти – антипепсин, антитрипсин та ін. Багато лікарських речовин відносяться до специфічних інгібіторів, оскільки вони, з’єднуючись з ферментами мікроорганізмів, блокують їх (білий стрептоцид і ферменти стрептокока).
До неспецифічних активаторів відносяться різні неорганічні катіони (табл. 2), рідше – аніони: Na+, K+, Ca2+, Mg2+, СІ– та ін. Вплив катіонів на ферменти більш специфічний, ніж аніонів. Деякі іони для одних ферментів є активаторами, для інших – інгібіторами (наприклад, Ca2+ – активатор для лужної фосфатази і інгібітор для гліцил-лейцин-дипептидази). В активації або гальмуванні ферменту може брати участь один або декілька видів іонів.
Таблиця 2.
