Енергетичний баланс організму. Макроергічні сполуки
Обмін речовин в організмі тісно пов’язаний з обміном енергії. Постійне надходження та використання енергії є необхідною умовою існування живих організмів як відкритих систем. За рахунок надходження енергії забезпечується підтримання стабільного, впорядкованого стану живої системи, що запобігає дезорганізації, хаосу та її загибелі. Енергія необхідна організму для забезпечення таких процесів: виконання різної роботи (механічної, осмотичної, фізичної); руху, скорочення та розслаблення м'язів; синтезу та розщеплення різних сполук; транспорту речовин та іонів; підтримання гомеостазу; виконання специфічних функцій, що забезпечують процеси життєдіяльності.
У процесі еволюції в живих організмах сформувались механізми, які забезпечують сприймання або вилучення енергії, генерацію, акумулювання її та використання організмом. Різні форми енергії, що існують у живих системах – хімічна, електрична, світлова, теплова, можуть взаємоперетворюватись одна в одну.
Залежно від способу вилучення енергії всі живі організми поділяють на фото- і хемотрофи. Фототрофи у вигляді джерела енергії використовують енергію квантів світла. До фототрофів належать зелені рослини, водорості, деякі бактерії. Дані організми синтезують складні органічні сполуки з неорганічних (CO2 і H2O) за рахунок енергії сонячного випромінювання, тобто вони здатні до сприймання і перетворення енергії електромагнітних коливань потоку сонячного випромінювання на енергію хімічних зв'язків органічних сполук. За типом живлення дані організми належать до аутотрофних (від грец. aytos – сам, trofos – живлення). Хемотрофні організми у вигляді джерела енергії використовують енергію окислення органічних чи неорганічних сполук. У першому випадку їх відносять до органотрофів, а в другому – до літотрофів. За типом живлення хемотрофні організми є гетеротрофами (від грец. heteros – інший і trofos – живлення). Гетеротрофи не можуть синтезувати складні органічні сполуки з неорганічних і використовувати їх в готовому вигляді. До гетеротрофів належать організми людини, тварин та деякі мікроорганізми. Слід зазначити, що поділ живих організмів на гетеро- та аутотрофи дещо умовний. Досить часто один і той самий організм може мати клітини обох типів. Так, у вищих рослин клітини листків – аутотрофи, а клітини коренів – гетеротрофи.
Для гетеротрофних організмів основним джерелом енергії, яка необхідна для забезпечення процесів життєдіяльності, є енергія хімічних зв'язків між атомами складних органічних сполук – білків, вуглеводів, ліпідів. Такі органічні сполуки гетеротрофні організми одержують з навколишнього середовища як компоненти їжі (поживні речовини). Поживні речовини гетеротрофними організмами використовуються у вигляді джерела енергії та джерела вуглецю. Енергія, яка акумульована в хімічних зв'язках органічних сполук, може бути виділена при розриві їх у результаті гідролізу, фосфоролізу. Так, при гідролітичному розщепленні пептидних зв’язків виділяється 2600 кДж/моль енергії, при розщепленні хімічних зв'язків у молекулі глюкози – відповідно 2881 кДж/моль, тобто кожна органічна сполука, що входить до складу живої матерії, має певний запас потенціальної енергії, акумульованої в хімічних зв'язках. Це так звана загальна внутрішня енергія системи, або енергія зв'язку. Загальна потенціальна енергія сполуки, яка при згоранні її перетворюється на теплоту, називається ентальпією і позначається буквою Н.
Під час перетворення зв'язків рівень загальної потенціальної енергії змінюється. При цьому енергія, що міститься в хімічних зв'язках, розсіюється у вигляді теплоти частково, тобто вивільнення енергії проходить не одномоментно, а поступово і частина її використовується для виконання роботи. В зв'язку з цим у клітині різких температурних змін не спостерігається. Зміна ентальпії (DН) при розриві хімічних зв'язків має такий вираз:
DН = DF + рDV
де DF – зміна загальної енергії системи; р – тиск; DV – зміна об'єму.
Оскільки в біологічних системах зміною об'єму можна знехтувати, то DH » DF.
Частина загальної енергії системи, за рахунок якої може бути виконана певна робота, називається вільною енергією G0. Отже, за рахунок вільної енергії підтримується стабільний стан біологічної системи. Зміна рівня стандартної вільної енергії позначається DG0. Під цим розуміють зміну вільної енергії за нормальних умов: тиск 101,3 кПа, концентрація 1 M ітемпература 25 °C. Зміну рівня стандартної вільної енергії при рН = 7,0 позначають DG0'. Зміна стандартної вільної енергії хімічної реакції визначається як різниця між вільною енергією вихідних сполук та вільною енергією кінцевих продуктів реакції, тобто зміна вільної енергії системи при переході її з одного стану в інший є критерієм, який дає змогу стверджувати можливість хімічного перетворення згідно з законами термодинаміки.
Зміну вільної енергії системи можна визначити як ту частину зміни загальної енергії, яка може бути використана для виконання роботи системою, що прагне до рівноваги за нормальних умов. Так, зміна вільної енергії в ході реакції А ® В дорівнює:
DG0’ = D H + TDS,
звідки DH = DG0' + TDS, де DG0' – зміна стандартної вільної енергії системи; DH – зміна загальної енергії системи; T – абсолютна температура; DS– зміна ентропії.
Ентропія – це частина загальної енергії системи, яка не використовується для виконання роботи і розсіюється у вигляді теплоти. При будь-якому перетворенні енергії значення ентропії збільшується. Виділення теплоти з точки зору термодинаміки слід розглядати як марну втрату енергії. З наведеного вище рівняння видно, що зміна загальної енергії системи (DH) складається з суми зміни стандартної вільної енергії DG0', яка використовується організмом, та зміни тієї частини загальної енергії, яка розсіюється у вигляді теплоти (TDS). Залежно від знака члена (плюс чи мінус) рівняння (TDS) вільна енергія може бути більшою чи меншою від теплоти реакції. DG0' може мати як додатне, так і від'ємне значення. Його використовують для кількісної характеристики хімічних реакцій, що дає змогу виразити енергетичний стан клітини. Так, у ході реакції A ® В від'ємне значення DG0' свідчить про те, що продукти реакцій містять менше вільної енергії, ніж вихідні сполуки (DG0'В < DG0'A), тобто реакція проходить з виділенням енергії і є екзергонічною. В цьому випадку рівновага реакції зміщується в бік утворення продуктів реакції (самовільні процеси). Якщо DG0' мaє додатне значення, тобто енергоємність продуктів реакції більша, ніж вихідних сполук (DG0'В > DG0'A), реакція без додаткового надходження енергії не відбувається. Дані реакції є ендергонічними і проходять з поглинанням енергії, що надходить ззовні (світлова, теплова, електрична), чи від інших екзергонічних реакцій окислення. Отже, перетворення енергії в організмі підкоряється законам термодинаміки: енергія не зникає і не виникає, а перетворюється з одного виду на інший без зміни загального рівня енергії, тобто організм виграшу в енергії не має. При будь-якому перетворенні енергії відбувається зростання ентропії системи і навколишнього середовища. Ця тенденція зберігається доти, поки не настане стан рівноваги, при якому ентропія має максимальне значення для даних умов. Процес проходить спонтанно за умов збільшення суми ентропії системи (DSc) і навколишнього середовища (DSH.C.)
DSc + DSH.C. > 0.
Зміна ентропії кількісно пов'язана із зміною загальної енергії системи, яку можна виразити як функцію DG0'. Обмін енергії включає такі процеси, як виділення, перетворення, акумулювання та використання енергії організмом, тобто обмін речовин в організмі супроводжується постійним обміном енергії завдяки тісному взаємозв'язку анаболічних реакцій, характерних для асиміляції, та катаболічних реакцій, характерних для дисиміляції. Слід зазначити, що для енергетичних процесів, які здійснюються в живих організмах, властиві певні особливості, наприклад вивільнення, акумулювання та використання енергії. Так, виділення енергії, що міститься в хімічних зв'язках органічних сполук, здійснюється в процесі дисиміляції на певних етапах проміжного обміну. При цьому процес вивільнення енергії здійснюється не одномоментно, а поступово і включає три основні етапи: підготовчий, анаеробне та аеробне окислення.
Підготовчий етап – перетравлювання та всмоктування поживних речовин. На цьому етапі відбувається ферментативне розщеплення високомолекулярних біополімерів (білків, вуглеводів, ліпідів) до мономерних сполук. Так, білки розщеплюються до амінокислот, вуглеводи – до моносахаридів, ліпіди – до гліцерину та жирних кислот. На даному етапі виділяється незначна кількість енергії – менш як 1 %, яка переважно розсіюється у вигляді теплоти. Катаболічними реакціями, що забезпечують виділення енергії на даному етапі, є гідроліз і фосфороліз.
Наступний етап виділення енергії включає анаеробне окислення продуктів гідролітичного розщеплення біополімерів (амінокислот, моносахаридів, жирних кислот) до метаболітів, таких як ацетил-КоА, a-кетоглутарова та щавелевооцтова кислоти. На даному етапі виділяється близько 1/3 енергії, акумульованої в хімічних зв'язках органічних сполук.
Утворені метаболіти включаються далі в наступний етап виділення енергії – аеробне окислення до кінцевих продуктів. При цьому виділяється 2/3 енергії. Аеробне окислення метаболітів здійснюється у циклі Кребса, в якому поєднуються анаболічні та катаболічні реакції, тобто в даному циклі проходить інтеграція анаболічних реакцій, характерних для асиміляції, та катаболічних реакцій, характерних для дисиміляції. Субстрати, що утворюються в циклі Кребса, можуть бути використані як при розщепленні, так і підчас синтезу різних речовин. Як правило, завершальна фаза катаболізму стикується з початковою фазою анаболізму, тобто кінцеві продукти розщеплення можуть бути використані як вихідні продукти синтезу.
У процесі аеробного окислення в циклі Кребса нагромаджуються відновні еквіваленти у вигляді НАД×H2, НАДФ×H2, ФАД×H2, які є генераторами енергії і забезпечують синтез АТФ у процесі тканинного дихання.
Анаболічні реакції, як і катаболічні, складаються з кількох стадій. Синтез складних органічних сполук починається з простих метаболітів, що утворюються в процесі розкладання. При цьому спочатку синтезуються прості сполуки (мономери), які далі перетворюються під час складних ферментативних реакцій на важливі біополімери клітини – білки, вуглеводи, ліпіди. Синтез складних органічних сполук відбувається з використанням енергії АТФ. Тісний взаємозв'язок між анаболічними і катаболічними реакціями здійснюється на кількох рівнях:
1) на рівні джерел вуглецю (кінцеві продукти катаболізму часто є вихідними сполуками анаболічних реакцій);
2) на рівні відновних еквівалентів (при аеробному окисленні нагромаджуються відновні еквіваленти, які використовуються для відновлюючого синтезу складних органічних сполук);
3) на енергетичному рівні (при катаболізмі виділяється та нагромаджується (акумулюється) енергія, яка може бути використана для процесів синтезу).
Анаболічні та катаболічні реакції спряжені за рахунок так званих амфіболічних (об'єднуючих) шляхів метаболізму, одним з яких є цикл Кребса. Треба зазначити, що анаболічні та катаболічні реакції на окремих етапах не співпадають і каталізуються різними ферментними системами. Отже, реакції синтезу не завжди є оборотними реакціями розщеплення. Так, розщеплення та синтез вуглеводів відрізняються трьома суворо специфічними реакціями, які каталізуються різними ферментами. При цьому процеси синтезу часто проходять обхідними шляхами, спряженими з меншими енерговитратами. Використання специфічних шляхів розщеплення і синтезу різних сполук у живих організмах є досить доцільним з багатьох точок зору. Насамперед це дає змогу здійснювати процеси розщеплення і синтезу одночасно і незалежно один від одного.
В організмі існує тісний взаємозв'язок між процесами звільнення та використання енергії. Основна маса енергії, акумульованої в хімічних зв'язках органічних сполук, виділяється при катаболізмі на другому і третьому етапах (анаеробне та аеробне окислення). Однак виділена енергія не використовується безпосередньо для потреб організму, а попередньо перетворюється на доступну форму. Такою універсальною сполукою є ATФ, яка може бути в ролі донора, акцептора та трансформатора енергії. Однак енергія окислення органічних сполук на АТФ не передається, оскільки в клітині безпосередня передача енергії від низько- до високоенергетичних сполук не відбувається. Цей процес здійснюється за участю посередників – макроергічних сполук, які утворюються під час окислення субстратів, і нагромаджують енергію окислення в макроергічних зв'язках.
Макроергічні зв'язки – це зв'язки, при перетворенні яких рівень зміни вільної енергії становить понад 20 кДж/моль. Макроергічні зв'язки позначають знаком тільда (~). Якщо при перетворенні зв'язків рівень зміни вільної енергії становить 12 – 20 кДж/моль, такі сполуки є нормальними в енергетичному відношенні. Таку розмірність зміни рівня стандартної вільної енергії мають більшість органічних сполук. Слід мати на увазі, що поняття „макроергічні зв'язки” не треба плутати з поняттям „енергія зв'язку”. Поняття „енергія зв'язку” включає характеристику енергетичного рівня хімічного зв'язку з точки зору фізичної хімії, тобто величини енергії, необхідної для розриву зв'язку між атомами. Поняття макроергічні зв'язки полягає у врахуванні енергетичного ефекту в результаті перетворення зв'язку через хімічну реакцію. Отже, в розумінні „енергія зв'язку” обидва види зв'язку близькі між собою. Основна відмінність між ними полягає в тому, що при перетворенні макроергічних зв'язків виділяється значно більше енергії, ніж при перетворенні звичайних зв'язків. Так, енергія хімічного зв'язку між двома кінцевими залишками фосфату в молекулі макроергічної сполуки (АТФ) і енергія зв'язку між залишком фосфорної кислоти і глюкози в молекулі глюкозо-6-фосфату приблизно однакові, тобто для розриву зв'язків в першому і другому випадках необхідно витратити однакову кількість енергії. Однак при дослідженні енергетичного ефекту гідролітичного розриву даних зв'язків є суттєва відмінність. Для АТФ зміна рівня стандартної вільної енергії становить 37 – 42 кДж/моль, а для глюкозо-6-фосфату – 13,1 кДж/моль, тобто АТФ є макроергічною сполукою, а глюкозо-6-фосфат – нормальною в енергетичному відношенні.
Макроергічні сполуки, як правило, містять фосфатну групу в a-положенні, яка при розриві макроергічного зв'язку може переноситись на інші сполуки у вигляді радикалу – активного фосфорилу: –PО3Н2.
Залежно від того, між якими атомами виникають макроергічні зв'язки, розрізняють п'ять груп макроергічних сполук: нуклеозидфосфати (АТФ, ГТФ, УТФ); карбоксилфосфати (ацетилфосфат); ацилтіолові ефіри (ацетил KoA); фосфоамідні ефіри (кретинфосфат); енолфосфати (фосфоенолпіровиноградна кислота). У цих сполуках макроергічні зв'язки найчастіше виникають між атомами фосфору і сірки, фосфору і кисню, фосфору і вуглецю, фосфору і водню.
Отже, енергія, що виділяється при окисленні органічних сполук, акумулюється в макроергічних зв'язках, з яких вона разом з активними фосфорними групами передається на АДФ, внаслідок чого синтезується ATФ.
У загальному цей процес можна записати так:
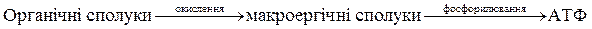 .
.
Макроергічні сполуки виконують роль посередників передачі енергії від низькоенергетичних сполук до АТФ. Постійний вміст АТФ у клітинах забезпечується фосфорилюванням АДФ як за рахунок енергії сонячного випромінювання (аутотрофні організми), так і за рахунок аеробного та анаеробного окислення біополімерів (гетеротрофні організми). Крім того синтез АТФ забезпечується за рахунок внутрішньоклітинних систем, що виконують резервну роль. Такою є система креатин-фосфат D креатин, яка може вступати в обмінну реакцію з нуклеозидфосфатами.
Біологічне окислення
Вивчення процесів окислення було започатковано M.В. Ломоносовим та А. Лавуазьє на основі дослідження продуктів згорання. А. Лавуазьє, співставляючи процеси горіння з процесами дихання в живих організмах, звернув увагу на подібність між ними.
При диханні, як і при згоранні, відбувається поглинання кисню і утворення CO2 і H2O. Енергетичний ефект окислення органічних сполук в організмі та згорання їх також виявились тотожними. Так, при окисленні глюкози до кінцевих продуктів і при згоранні її в колориметрі виділяється однакова кількість енергії 2881 кДж/моль. В зв’язку з цим А. Лавуазье висловив припущення, що сполуки в організмі окислюються в результаті їх повільного згорання. Не зрозумілим було ще те, чому „горіння” різних сполук в організмі відбувається при низькій температурі, без полум'я і за наявності води.
Перші спроби з'ясувати особливості та механізм окислення сполук в організмі (біологічного окислення) зробив Ф. Шенбайн, який висловив припущення, що біологічне окислення – це каталітичний процес, необхідною умовою перебігу якого є активація кисню.
На початку XX cт. O.H. Бах та K. Енглер одночасно і незалежно один від одного запропонували гіпотезу, згідно з якою біологічне окислення проходить за рахунок активування кисню і першим етапом даного процесу є утворення пероксидних сполук. Активування кисню здійснюється за рахунок енергії сполук, здатних до самоокислення, та ферментів оксидаз. Такими сполуками є каротини, терпени, полієнові вищі жирні кислоти, в молекулах яких є кратні подвійні зв'язки, внаслідок чого вони легко взаємодіють з молекулярним киснем, утворюючи пероксидні сполуки, які розщеплюються за участю ферментів пероксидаз і утворюють активний кисень. Останній окислює молекули інших органічних сполук, які з молекулярним киснем не реагують.
Оскільки окислення проходить через утворення пероксидних сполук, то теорія O.M. Баха дістала назву пероксидної теорії окислення.
Значний внесок у розуміння процесів біологічного окислення зробив російський біохімік В.І. Палладін. Вивчаючи окислення речовин у рослинах, він встановив, що воно може відбуватися і при відсутності кисню, якщо в реакційному середовищі єречовини, які здатні приєднувати водень. Такими речовинами виявились пігменти – хромогени. Приєднуючи водень від субстратів, які окислюються, вони відновлюються і стають безбарвними. Потім – віддають водень, тобто окислюються, знову набувають забарвлення, перетворюючись на хінони, причому, перетворення проходить за участю кисню повітря.
Слід зазначити, що В.І. Палладін надавав великого значення кисню як акцептора водню і цим самим показав важливу роль кисню в процесах біологічного окислення. Дослідження В.І. Палладіна були підтверджені працями Віланда. Він висловив думку, що дегідрування субстратів є основним процесом, який лежить в основі біологічного окислення, і що кисень взаємодіє вже з активованими атомами водню. Отже, була створена теорія окислення речовин шляхом їх дегідрування, яка дістала назву теорії Палладіна-Віланда.
Основою в підтвердженні даної теорії було відкриття і вивчення цілого ряду дегідрогеназ – ферментів, які каталізують відщеплення атомів водню від різних субстратів. Було доведено, що процеси окислення субстратів – це цілий ланцюг послідовних реакцій, які починаються з дегідрування субстратів і закінчуються перенесенням електронів на кисень та взаємодією останнього з протонами водню з утворенням води. Оскільки при такому окисленні постійно має місце поглинання кисню, то його ще називають тканинним диханням.
Отже, на основі вищенаведених теорій і досліджень створено сучасні уявлення про механізм біологічного окислення, в основі якого лежить пероксидна теорія Баха і теорія Палладіна-Віланда про дегідрування субстратів.
Суть біологічного окислення. Біологічне окислення, яке проходить в організмах людини і тварин, є досить складним процесом. У ньому беруть участь десятки і сотні різних ферментів, внаслідок чого потенціальна енергія, яка міститься в молекулах органічних речовин, вивільняється і використовується в найрізноманітніших процесах життєдіяльності організму.
Процес біологічного окислення проходить поетапно. У ньому беруть участь ферментні системи, які містять у вигляді: небілкової частини НАД+, НАДФ+; ФМН, ФАД, убіхінони і залізопорфіринові комплекси.
На першому етапі біологічного окислення здійснюється дегідрування субстратів – продуктів розщеплення білків, жирів і вуглеводів. Цей процес відбувається за участю ферментів дегідрогеназ (оксидоредуктаз), які містять коферменти НАД+ і НАДФ+. Вони є майже універсальними акцепторами водню для багатьох субстратів – спиртів, альдегідів, дикарбонових і кетокислот, амінів тощо. Віднімаючи від субстратів атоми водню (електрони і протони), вони самі відновлюються, а субстрати при цьому окислюються.
Прикладом дегідрогеназ може бути лактатдегідрогеназа, яка каталізує реакцію дегідрування молочної кислоти.
Далі, на наступному етапі, акцептором атомів водню є група флавінових ферментів, які у вигляді небілкової частини містять ФМН. Вони здійснюють перенесення атомів водню від відновлених НАД або НАДФ.
Наступним етапом є перенесення електронів і протонів від відновлених форм ФМН на убіхінони (коензим Q).
На наступному етапі з коензиму Q протони атомів водню переходять у навколишнє середовище, а електрони поступають на цитохромну систему. Цитохромна система складається з ряду оксидоредуктаз, небілковою частиною яких є залізопорфірини, близькі за своєю будовою до гему. Відомо понад 20 різних цитохромів. Вони позначаються латинськими буквами – а, в, с, d і т.д. В цитохромну систему входять цитохроми і фермент – цитохромоксидаза (аа3). Характерною особливістю цієї системи ферментів є те, що вони переносять електрони з відновленого коензиму Q на кисень, а останній, сполучаючись з іонізованими атомами водню, утворює воду.
Отже, на завершальному етапі дихання здійснюються два процеси – приєднання до кисню електронів і перетворення його на негативно заряджений іон (іонізація), а потім приєднання до іонізованого кисню протонів з утворенням молекули води. Молекулярний кисень O2 приєднує до себе 4 електрони і 4 протони, а оскільки через систему цитохромів переноситься лише 2 електрони, використовується ½ O2 (див. нижче).
У процесі перенесення електронів через систему дихального ланцюга проходить поступове вивільнення акумульованої в них енергії і до кисню вони переносяться вже енергетично бідними, тому утворення води в організмі не супроводжується вибухом, як у випадку утворення гримучого газу.
Отже, в ланцюгу окисно-відновних процесів створюється своєрідний електронний каскад. Послідовність розміщення основних компонентів дихального ланцюга визначається співвідношенням швидкості окислення і відновлення окремих компонентів системи, а також величиною редокс-потенціалів, що виникають між сусідніми компонентами. Перенесення електронів здійснюється завжди від меншого потенціалу до більшого. Для більшості органічних субстратів нормальні редокс-потенціали окисно-відновних систем дорівнюють – 0,6 В.
Окисно-відновна рівновага, окисно-відновний потенціал. Зміна вільної енергії, яка характеризує реакції окислення і відновлення, пропорційна здатності реактантів віддавати або приєднувати електрони. Відповідно, зміну вільної енергії окисно-відновного процесу можна характеризувати не тільки величиною DG, але і величиною окисно-відновного потенціалу системи (Е0). За звичай окисно-відновний потенціал системи (Е0) порівнюють з потенціалом водневого електрону, приймаючи останній за 0,00 В при рН = 0. Однак, для біологічних систем правильніше використовувати окисно-відновний потенціал при рН = 7 (Е0'); при такому рН потенціал водневого електрону дорівнює – 0,42 В. Окисно-відновні потенціали деяких систем, які представляють особливий інтерес для біохімії ссавців, наведені в таблиці 1. Використовуючи цю таблицю, можна передбачити, в якому напрямку піде потік електронів при спряженні однієї окисно-відновної системи з іншою.
Таблиця 1
Стандартні потенціали деяких окисно-відновних систем
| Система | Е’0, вольт |
| Кисень / вода | + 0,82 |
| Цитохром a: Fe3+ / Fe2+ | + 0,29 |
| Цитохром с: Fe3+ / Fe2+ | + 0,22 |
| Убіхінон: окислений / відновлений | + 0,10 |
| Цитохром b: Fe3+ / Fe2- | + 0,08 |
| Фумарат / сукцинат | + 0,03 |
| Флавопротеїн («жовтий фермент»): окислений / відновлений | – 0,12 |
| Оксалоацетат / малат | – 0,17 |
| Піруват / лактат | – 0,19 |
| Ацетоацетат / b-гідроксибутират | – 0,27 |
| Ліпоат: окислений / відновлений | – 0,29 |
| НАД+ / НАДН | – 0,32 |
| Н+ / Н2 | – 0,42 |
| Сукцинат / a-кетоглутарат | – 0,67 |
Ферменти і коферменти, які приймають участь в окисно-відновних процесах. Ферменти, які каталізують окисно-відновні процеси, називаються оксидоредуктазами. Їх ділять на 5 груп.
1) Оксидази. Істинні оксидази каталізують видалення водню із субстрату, використовують як акцептор тільки кисень. Вони обов’язково містять мідь, продуктом реакції є вода (виключення складають реакції, які каталізуються уриказою і монооксидазою, в результаті яких утворюється Н2О2 ):
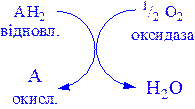
Цитохромоксидаза – гемопротеїн, широко розповсюджений в рослинних і тваринних тканинах. Вона служить кінцевим компонентом ланцюга дихальних переносників, локалізованих в мітохондріях, і каталізує реакцію, в результаті якої електрони, вивільняються із молекул субстрату при їх окисленні дегідрогеназами, переносяться на кінцевий акцептор – кисень. Даний фермент отруюється оксидом вуглецю, ціанідом сірководнем. Інколи цитохромоксидазу називають цитохромом аа3. Спочатку припускали, що цитохром а і цитохром а3 – це автономні гемопротеїни, оскільки кожний з них характеризується визначеним спектром, крім того, вони виявляють різну чутливість до дії оксиду вуглецю і ціаніду. Однак було доведено, що вони входять до складу комплексу, який одержав назву цитохром аа3. Він містить дві молекули гема, у кожній з який атом заліза може переходити зі стану Fe2+ у стан Fe3+ і назад у ході окислення і відновлення, а також два атоми Сu, кожний з яких взаємодіє з одним з гемів.
Фенолаза (тирозиназа, поліфенолоксидаза, катехолоксидаза) – це мідьвмісний фермент із широкою специфічністю. Він каталізує перетворення монофенолу (у присутності о-дифенолу) у о-хінон. Мідь виявлена в ряді інших ферментів, зокрема в уриказі, яка каталізує окислення сечової кислоти в алантоїн, і в моноамінооксидазі, яка окислює адреналін і тирамін у мітохондріях.
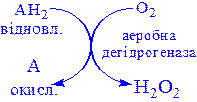
2) Аеробні дегідрогенази – ферменти, які каталізують видалення водню із субстрату; на відміну від оксидаз вони як акцептор водню можуть використовувати не тільки кисень, а і штучні акцептори, такі, як метиленовий синій. Ці дегідрогенази відносяться до флавопротеїнів, і продуктом реакції, яку вони каталізують є пероксид водню, а не вода:
 ,
,
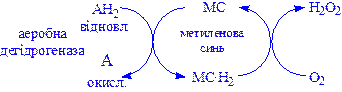
Аеробні дегідрогенази – флавопротеїни; містять простетичні групи – флавінмононуклеотид (ФМН) або флавінаденіндинуклеотид (ФАД).
До ферментів групи аеробних дегідрогеназ відноситься дегідрогеназа L-амінокислот (оксидаза L-амінокислот) ФМН-вмісний фермент, який знаходиться в нирках і володіє широкою специфічністю, каталізує окисне дезамінування природних L-амінокислот. Широко поширена ксантиндегідрогеназа (ксантиноксидаза); вона виявлена в молоці, у тонкому кишечнику, нирках і печінці.
Ксантиндегідрогеназа містить молібден; відіграє важливу роль у перетворенні пуринових основ у сечову кислоту в печінці і нирках. Особливе значення має для птахів, які екскретують сечову кислоту як головний кінцевий азотовмісний продукт метаболізму пуринів, а також катаболізму білків і амінокислот.
Альдегіддегідрогеназа – ФАД-вмісний фермент, що знаходиться в печінці. Це – металофлавопротеїн – містить молібден і негемове залізо, окислює альдегіди і N-гетероциклічні субстрати.
Глюкозооксидаза – ФАД-специфічний фермент, який одержують із грибів. Вона важлива тим, що використовується при визначенні глюкози.
Механізм окислення і відновлення, що здійснюється цими ферментами, дуже складний. Судячи з наявних даних, відбувається двостадійне відновлення ізоаллоксазонового кільця з проміжним утворенням семіхінона (вільного радикала):
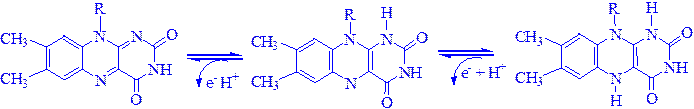
3) Анаеробні дегідрогенази – ферменти90
, які каталізують видалення водню із субстрату, але не здатні використовувати кисень як акцептор водню. До цього класу належить велике число ферментів. Вони виконують дві функції:
а) перенесення водню з одного субстрату на інший в спряженій окисно-відновній реакції:
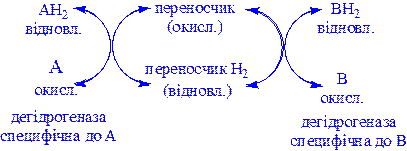
Ці дегідрогенази специфічні до субстратів, але часто використовують один і той же кофермент або переносник водню. Оскільки реакції, які розглядаються оборотні, то вони забезпечують у клітині вільне перенесення відновних еквівалентів. Реакції цього типу призводять до окислення одного субстрату за рахунок відновлення іншого, особливо важливі для здійснення окисних процесів за відсутності кисню.
б) функцію компонентів дихального ланцюга забезпечуючи транспорт електронів від субстрату на кисень:
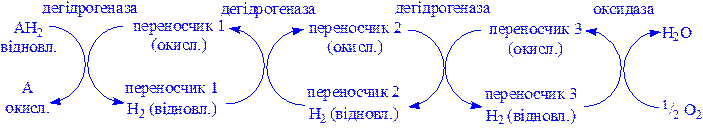
Поділяються на:
Дегідрогенази, залежні від нікотинамідних коферментів. До цієї категорії належить багато дегідрогеназ. Вони специфічні або до нікотинамідаденіндинуклеотиду (НАД+), або до нікотинамідаденіндинуклеотидфосфату (НАДФ+), які виконують роль коферментів (рис. 1). НАД+ і НАДФ+ утворюються в організмі людини з вітаміну В5. Для синтезу НАД+ чи НАДФ+ ферменти, які знаходяться в цитозолі більшості клітин, використовують тільки нікотинову кислоту, але не нікотинамід. Нікотинамідний фрагмент НАД+ утворюється з нікотинатного фрагмента, коли останній знаходиться в складі нуклеотиду; амідна група надходить від глутаміну (рис. 1).
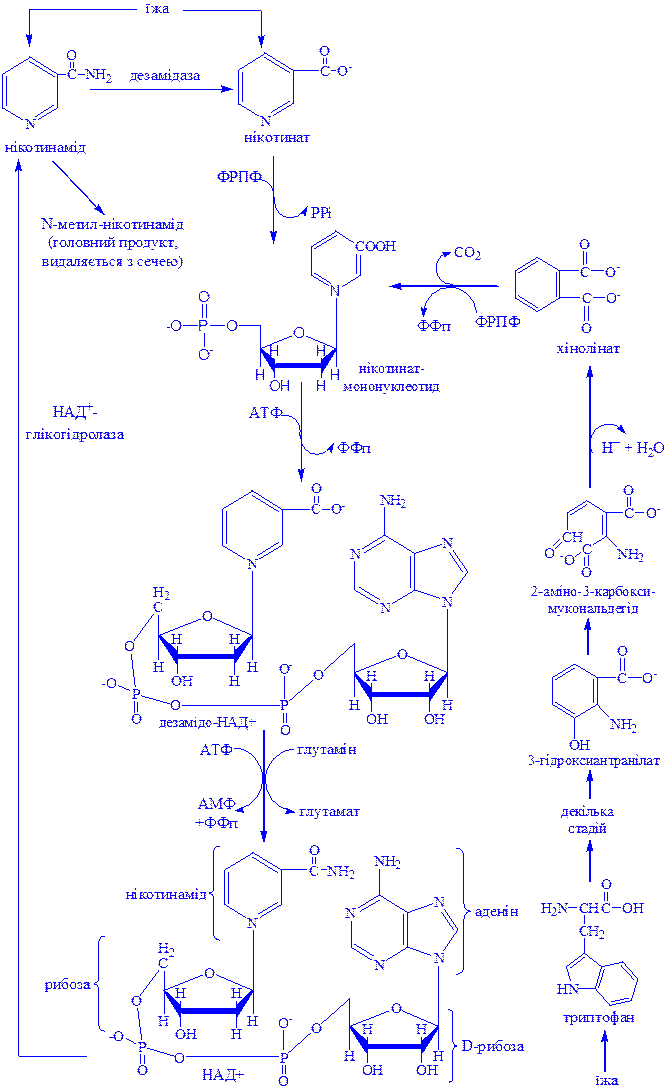
Рис 1. Синтез і розклад нікотинамідаденіндинуклеотиду (НАД).
Є дані про те, що в мітохондріях для синтезу НАД+ використовується нікотинамід. Коферменти відновлюються специфічними субстратами дегідрогеназ і окислюються адекватним акцептором електронів (рис. 2).
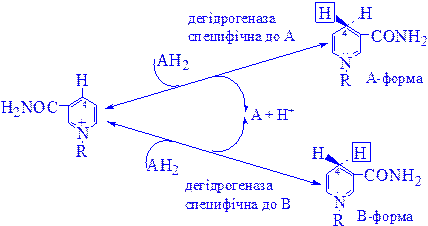
НАД+ + AH2 D НАДH + H+ + A
Рис 2. Механізм окислення і відновлення нікотинамідних коферментів.
У загальному випадку НАД-залежні дегідрогенази каталізують окисно-відновні реакції окисних шляхів метаболізму – гліколізу, циклу лимонної кислоти, дихального ланцюга мітохондрій. НАДФ-залежні дегідрогенази беруть участь у процесах відновного синтезу, зокрема у позамітохондріальному синтезі жирних кислот і стероїдів; вони також є коферментами дегідрогеназ пентозофосфатного шляху. Деякі дегідрогенази, які функціонують з нікотинамідними коферментами, містять іон цинку, зокрема алкогольдегідрогеназа печінки і гліцеральдегід-3-фосфатдегідрогеназа скелетних м'язів. Припускають, що іони цинку не беруть участь безпосередньо в процесах окислення і відновлення.
Рибофлавінзалежні дегідрогенази. Флавінові групи цих дегідрогеназ ті ж, що й в аеробних дегідрогеназ, ФМН і ФАД. Більшість рибофлавін-залежних анаеробних дегідрогеназ або бере участь у транспорті електронів по дихальному ланцюзі, або поставляє електрони для цього ланцюга. НАДФ-дегідрогеназа – компонент дихального ланцюга, яка переносить електрони від НАДН до більш електропозитивних компонентів. Інші дегідрогенази, наприклад сукцинатдегідрогеназа, ацил-СоА-дегідрогеназа і мітохондріальна гліцерол-3-фосфат-дегідрогеназа переносять відновні еквіваленти від субстрату безпосередньо на дихальний ланцюг. Ще одна функція флавін-залежних дегідрогеназ – каталіз дигідроліпоїл-дегідрогеназою дегідрування відновленого ліпоату (інтермедіату при окисному декарбоксилуванні пірувату й a-кетоглутарату). У цьому випадку внаслідок низького значення окисно-відновного потенціалу системи ліпоату переносником водню від відновленого ліпоату до НАД+ є флавопротеїн (ФАД). Електрон-переносний флавопротеїн є проміжним переносником електронів між ацил-СоА-дегідрогеназою і дихальним ланцюгом.
в) Цитохроми. За винятком розглянутої вище цитохромоксидази, цитохроми класифікуються як анаеробні дегідрогенази. Їх ідентифікація і вивчення полегшуються тією обставиною, що у відновленому стані вони мають характерні смуги в спектрі поглинання, які зникають при окисленні. У дихальному ланцюзі вони служать переносниками електронів від флавопротеїнів до цитохромоксидази. Цитохроми є залізовмісними гемопротеїнами, у яких атом заліза переходить зі стану Fe2+ у Fe3+ і назад у процесі окислення і відновлення. До складу дихального ланцюга входять цитохроми b, с1, с, а і а3 (цитохромоксидаза). З них розчинним є тільки цитохром с. Крім дихального ланцюга цитохроми містяться в ендоплазматичному ретикулумі (цитохроми Р450 і b5), у рослинних клітинах, бактеріях і дріжджах.
Відновлення нікотинаміду субстратом (АН2) по положенню 4 відбувається стереоспецифічно. Один з атомів водню переноситься від субстрату в положення 4 у виді ядра водню з двома електронами (гідрид-іон, Н- ): він може приєднатися або в А-, або у В-положенні в залежності від специфічності дегідрогенази, яка каталізує дану реакції. Інший водень, який відщеплюється від субстрату, залишається вільним у виді іона водню.
4) Гідроксипероксидази – ферменти, які використовують як акцептор перекис водню або органічні перекиси. До цієї категорії відносяться два типи ферментів: пероксидази, які знаходяться в складі молока, в рослинах, лейкоцитах, тромбоцитах, еритроцитах і т.д., і каталаза, яка функціонує в тканинах тварин і рослин.
Пероксидаза. Спочатку пероксидази вважалися рослинними ферментами, пізніше вони були виявлені також у молоці, лейкоцитах, тромбоцитах, а також у тканинах, у яких відбувається метаболізм ейкозаноїдів. Простетичною групою є протогем, який на відміну від гемових груп більшості гемопротеїнів дуже слабко зв'язаний з апоферментом. У реакції, яку каталізує пероксидаза, перекис водню відновлюється за рахунок сполук, що виступають як донори електронів, таких, як аскорбат, хінони чи цитохром с. Реакція, яку каталізує пероксидаза, має складний характер; сумарна реакція виглядає в такий спосіб:
Н2О2 + АН2 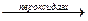 2Н2О + А
2Н2О + А
В еритроцитах глутатіонпероксидаза, яка містить як простетичну групу – селен, каталізує розклад Н2О2 і гідроперекисів ліпідів відновленим глутатіоном і в такий спосіб захищає ліпіди мембран і гемоглобін від окислення перекисами.
Каталаза. Гемопротеїн, який містить чотири гемові групи. Поряд з пероксидазною активністю каталаза здатна використовувати одну молекулу Н2О2 як донор електронів, а іншу – як окислювач, тобто акцептор електронів. In vivo у більшості випадків каталаза розкладає пероксид водню:
2Н2О2 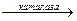 2Н2О + О2
2Н2О + О2
Каталаза міститься у крові, кістковому мозку, мембранах слизових оболонок, нирках і печінці. Її функція – розкладання перекису водню, що утворюється при дії аеробних дегідрогеназ. У багатьох тканинах, включаючи і печінку, виявлені мікротільця, пероксисоми, які багаті аеробними дегідрогеназами і каталазою. Очевидно, біологічно вигідно групувати як ферменти, що призводять до утворення Н2О2, так і ферменти, що розкладають його в одному місці:
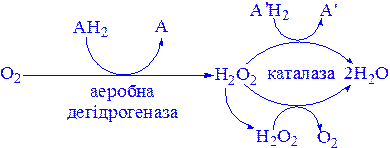
До ферментів, що забезпечують утворення Н2О2, крім пероксисомних ферментів відносяться також мітохондріальні і мікросомні системи транспорту електронів.
5) Оксигенази – ферменти, які каталізують пряме введення кисню в молекулу субстрату.
Оксигенази не належать до ферментів, що каталізують реакції, які збагачують клітину енергією; вони беруть участь у синтезі і розкладі багатьох типів метаболітів. Ферменти цієї групи каталізують включення кисню в молекулу субстрату.
Воно відбувається в дві стадії: 1) кисень зв'язується з активним центром ферменту; 2) відбувається реакція, у результаті якої зв'язаний кисень відновлюється чи переноситься на субстрат. Оксигенази діляться на дві підгрупи.
а) Діоксігенази (кисень-трансферази, істинні оксигенази). Ці ферменти каталізують включення в молекулу субстрату обох атомів молекули кисню:
А + О2 ® АО2.
Приклад – залізовмісні ферменти гомогентизатдіоксігеназа і 3-гідроксиантранілат-діоксігеназа із супернатантної фракції гомогенату печінки, а також гемвмісні ферменти, зокрема L-триптофандіоксігеназа (триптофанпіролаза) з печінки.
б) Монооксигенази (оксидази зі змішаною функцією, гідроксилази). Ці ферменти каталізують включення в субстрат тільки одного з атомів молекули кисню. Інший атом кисню відновлюється до води; для цього необхідний додатковий донор електронів (косубстрат):
А–Н + О2 + ZH2 ® А–ОН + Н2О + Z
Мікросомні цитохром Р450-вмісні монооксигеназні системи. До цієї групи належать ферменти, які беруть участь у метаболізмі багатьох лікарських речовин шляхом їх гідроксилювання. Вони знаходяться в мікросомах печінки разом з цитохромом Р450 і цитохромом b5. Відновниками цих цитохромів є НАДН і НАДФН (рис. 3); цитохроми окислюються субстратами в результаті серії ферментативних реакцій, які складають так званий гідроксилазний цикл (рис. 4):
Лік–Н + О2 + 2Fe2+(P450) + Н+ 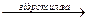 Лік–ОН + Н2О + 2Fe3+
Лік–ОН + Н2О + 2Fe3+
(Лік – лікарська речовина).
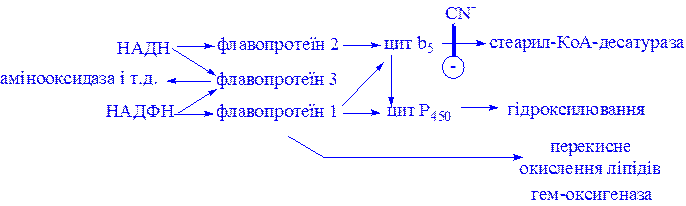
Рис 3. Ланцюг транспорту електронів в мікросомах.
Ціанід (CN-) гальмує стадію, вказану на рисунку.
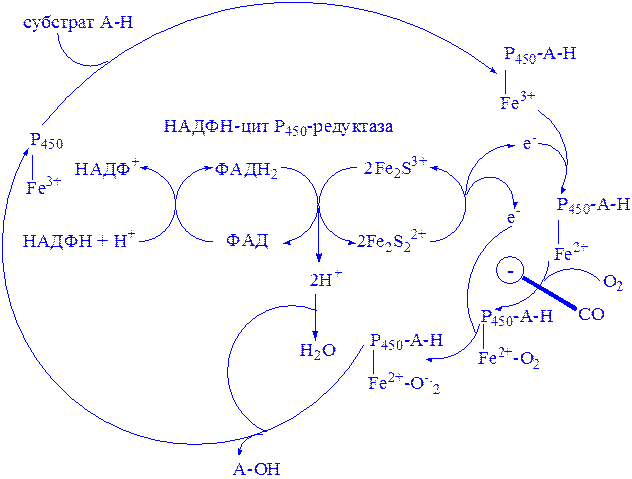
Рис 4. Цитохром Р450-гідроксилазний цикл у мікросомах.
До лікарських речовин, метаболізм яких відбувається за участю розглянутих систем, відносяться: бенз[a]пірен, амінопірин, анілін, морфін і бензофетамін. Багато лікарських речовин, наприклад фенобарбітал, здатний індукувати синтез мікросомних ферментів і цитохрому Р450.
Мітохондріальні цитохром Р450-вмісні монооксигеназні системи. Ці системи знаходяться в стероїдогенних тканинах – у корі наднирників, у сім’яниках, яєчниках і плаценті; вони беруть участь у біосинтезі стероїдних гормонів з холестеролу (гідроксилювання по С22 і С20 при відщепленні бічного ланцюга і по положеннях 11b і 18). Ферменти ниркової системи каталізують гідроксилювання 25-гідроксихолекальциферолу по положеннях 1a і 24; у печінці відбувається гідроксилювання холестеролу по положенню 26 при біосинтезі жовчних кислот. У корі наднирників вміст мітохондріального цитохрома Р450 у шість разів вище, ніж вміст цитохромів дихального ланцюга. Монооксигеназна система складається з трьох компонентів, локалізованих у внутрішній мітохондріальній мембрані на границі з матриксом: НАДФ-специфічного ФАД-вмісного флавопротеїну, Fе2S2-білка (адренодоксину) і цитохрома Р450 (рис. 5).
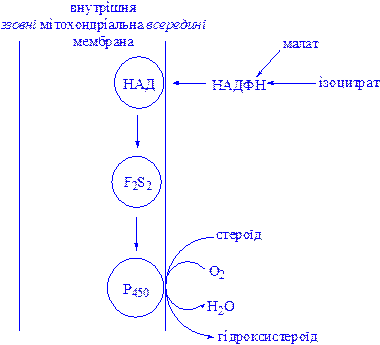
Рис 5. Мітохондріальна цитохром Р450-монооксигеназна система.
Наведена система типова для гідроксилаз стероїдів у корі наднирників. Мікросомна цитохром Р450-гідроксилаза печінки не має потреби в присутності залізо-сірчаного білка Fe2S2. Оксид вуглецю (СО) гальмує зазначену на рисунку стадію.
Fe2S2 – залізо-сірчаний білок (адренодоксин). Оскільки НАДФ(H) не може проникати в мітохондріальну мембрану, джерелами відновних еквівалентів є такі субстрати, як малат і ізоцитрат, для яких усередині мітохондрій є специфічні НАДФ-залежні дегідрогенази.
Метаболізм супероксид-радикала. Кисень є потенційно токсичною речовиною. Донедавна його токсичність пов'язували з утворенням Н2О2. Однак останнім часом, приймаючи на увагу, по-перше, ту обставину, що кисень у тканинах легко відновлюється в супероксидний аніон-радикал (O2-.), і, по-друге, наявність в аеробних організмів супероксиддисмутази (СОД) (її немає в облігатних анаеробів), було висунуто припущення про те, що токсичність кисню обумовлена його перетворенням у супероксид. Однак прямих даних про токсичність супероксид-радикала поки не отримано.
Супероксид утворюється в ході одноелектронного окислення молекулярним киснем відновленого флавіну, наприклад флавіну в складі ксантиндегідрогенази. Він утворюється також при одноелектронному окисленні молекулярним киснем відновленого компонента дихального ланцюга:
Enz–H2 + O2 ® Enz–H + O2-. + H+.
Супероксид може відновлювати окислений цитохром с:
О2-. + Цит с (Fе3+) ® О2 + Цит с (Fе2+).
Він відщеплюється також специфічним ферментом – супероксиддисмутазою:
О2-. + О2-. + 2Н+ 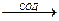 Н2О2 + О2
Н2О2 + О2
У цій реакції супероксид виступає одночасно як окислювач, так відновник. Хімічна дія супероксиду в тканинах підсилюється в результаті ініціювання ланцюгової реакції утворення вільних радикалів. Було висловлено припущення, що О2-., зв'язаний з цитохромом Р450, є інтермедіатом при активації кисню в процесі реакцій гідроксилювання (рис 4).
Функцією супероксиддисмутази є, очевидно, захист аеробних організмів від ушкоджуючої дії супероксиду. Фермент виявляється в декількох внутрішньоклітинних кампартментах. Цитозольний фермент складається з двох подібних субодиниць, які містять по одному іонові Сu2+ і Zn2+; мітохондріальний фермент, так само як і фермент, виявлений у бактерій, містить іон Мn2+. Ця обставина служить ще одним доказом на користь гіпотези про походження мітохондрій із прокаріот, що вступили в симбіоз із протоеукаріотами. Дисмутаза присутня у всіх основних тканинах аеробів. Перебування тварин в атмосфері 100%-ного кисню викликає адаптивне підвищення вмісту дисмутази, особливо в легенях; тривале перебування в такій атмосфері призводить до ушкодження легень і летальному результату. Антиоксиданти, наприклад a-токоферол (вітамін Е), здатні вловлювати вільні радикали, такі, як О2-., знижуючи тим самим токсичність кисню.
