Гормоны поджелудочной железы
Поджелудочная железа относится к железам со смешанной секрецией. Внешнесекреторная функция заключается в синтезе ряда ключевых ферментов пищеварения (амилазы, липазы, трипсина и др.). Внутриклеточную функцию выполняют панкреатические островки (островки Лангерганса), состоящие из клеток разного типа
(А-, В-, D-, F-клетки). А-клетки (или a-клетки) являются местом выработки гормона глюкана, В-клетки (b-клетки) – инсулина, D-клетки (d-клетки) – соматостатина, F-клетки – панкреатического пептида.
Инсулин. Молекула инсулина состоит из 51 аминокислотного остатка и представляет собой объединение двух полипептидных цепей: А-цепи, содержащей 21 аминокислотный остаток, В-цепи из 30. Обе цепи связаны дисульфидными связями. Полипептидный остов молекулы инсулина образует более сложные вторичную и третичную структуры.
В физиологической регуляции синтеза инсулина доминирующую роль играет концентрация глюкозы в крови, повышение содержания глюкозы в крови вызывает увеличение секреции инсулина, а снижение – замедление секреции. На секрецию инсулина оказывают влияние, кроме того, электролиты (особенно ионы кальция), аминокислоты, глюкагон и секретин.
Инсулин синтезируется из проинсулина и может существовать в нескольких формах, различающихся по биологическим, иммунологическим и физико-химическим свойствам.
Биологический эффект инсулина связан с влиянием на углеводный, белковый, липидный обмен, обмен нуклеиновых кислот. Инсулин стимулирует проникновение и утилизацию глюкозы в тканях, прежде всего «инсулинзависимых»; воздействует на различные пути метаболизма глюкозы – окисление, использование на биосинтез гликогена и гликозаминогликанов, синтез жирных кислот, нуклеотидов и др.
Инсулин индуцирует и повышает активность ключевых ферментов тканевого метаболизма глюкозы – гексокиназы и глюкокиназы, стимулирующих фосфорилирование глюкозы и, следовательно, использование глюкозы в процессах клеточного метаболизма.
Инсулин стимулирует биосинтез гликогена и задерживает его распад. Под действием гормона происходит активизация ключевого фермента глюкогенеза – гликогенсинтетазы, одновременно при действии инсулина происходит снижение активности основного фермента фосфорилитического распада гликогена – гликогенфосфорилазы.
Для ключевых ферментов гликолиза 6-фосфофруктокиназы и пируваткиназы инсулин является стимулятором. Под влиянием инсулина повышается синтез и активность глюкозо-6-фосфатдегидрогеназы, транскетолазы и других ферментов пентозного цикла превращения глюкозы.
Важную роль инсулин играет в регуляции обмена липидов, являясь одним из основных липогенетических гормонов. Инсулин стимулирует биосинтез жирных кислот в клетках жирового депо. Кроме того, инсулин способствует биосинтезу нейтрального жира в жировых клетках благодаря активному расщеплению глюкозы с образованием глицерофосфата. Гормон также стимулирует накопление жира в жировых депо, так как является антагонистом различных липолитических гормонов – адреналина, СТГ, АКТГ, глюкагона и др.
Инсулин является анаболитическим гормоном в отношении обмена белков и нуклеиновых кислот; в тканях стимулирует биосинтез нуклеотидов и нуклеиновых кислот.
Повышение образования нуклеотидов связано с активизацией окисления глюкозы пентозофосфатном цикле и обеспечением данного процесса рибозо-5-фосфатом, с другой – непосредственным усилением биосинтеза пуриновых азотистых оснований. Инсулин в тканях также повышает активность РНК-полимеразы и ДНК-полимеразы, стимулируя биосинтез ДНК и всех типов РНК.
Инсулин усиливает транспорт аминокислот через клеточные мембраны, повышает биосинтез различных аминоацил-тРНК-синтетаз - ферментов, активирующих аминокислоты, вступающие на путь синтеза белка. Кроме того, гормон усиливает процессы трансляции, благодаря индукции синтеза специфического белка – фактора трансляции, который является белком, способствующим объединению рибосом в полисомы.
При недостаточном синтезе инсулина развивается специфическое заболева-
ние – сахарный диабет, для которого характерно нарушение метаболитических процессов: гипергликемия (увеличение уровня глюкозы в крови), гликозурия (выделение глюкозы с мочой), кетонурия (избыточный синтез кетоновых тел) и др. У больных наблюдается постоянная жажда и чувство голода, быстрая утомляемость и другие симптомы, связанные с глубокими нарушениями в метаболизме углеводов, липидов, аминокислот, белков, НК, водно-солевого и энергетического обмена. Клинические симптомы при данном заболевании могут быть обусловлены не только отсутствием синтеза инсулина; могут иметь место и молекулярные дефекты: нарушение структуры инсулина или ферментативного превращения проинсулина в инсулин, или возможна потеря рецепторами клеток-мишеней способности соединяться с молекулой инсулина.
Глюкагон. Глюкагон представляет собой одноцепочечный полипептид, состоящий из 29 аминокислот с молекулярной массой 3,5 кД.
Биологические эффекты глюкагона весьма многообразны. Он является сильным гипергликемическим фактором, оказывающим свое влияние в печени и не действующим на мышцы и другие ткани. Глюкагон, влияя на активность фосфорилазы и гликогенсинтетазы, оказывает двойное действие: ускоряет распад гликогена и ингибирует его синтез, в результате чего гликоген превращается в печени в глюкозу.
Глюкагон стимулирует также продукцию глюкозы из аминокислот путем индукции цАМФ-зависимого синтеза ключевых ферментов глюконеогенеза.
Глюкагон обладает также выраженной липолитической активностью, что также обусловлено цАМФ-зависимой активизацией липазы в клетках жировой ткани с освобождением свободных жирных кислот и глицерина.
В печени глюкагон тормозит синтез жирных кислот и холестерина из ацетил-КоА и стимулирует кетогенез, активирует печеночную липазу.
В почках глюкагон увеличивает клубочковую фильтрацию и ускоряет ток крови, что приводит к повышению экскреции Na+, K+, Cl-, неорганических фосфатов и мочевой кислоты.
Биосинтез и секреция глюкагона контролируются главным образом концентрацией глюкозы по принципу обратной связи. Таким же свойством обладают аминокислоты и свободные жирные кислоты. На секрецию глюкагона оказывают влияние также инсулин и инсулиноподобные факторы роста.
Гормоны надпочечников
Надпочечники состоят из двух индивидуальных в морфологическом и функциональном отношениях частей – мозгового и коркового вещества. Гормоны этих двух структур различаются по химической природе и действию, но могут оказывать взаимное влияние на функцию мозгового и коркового вещества надпочечников.
Гормоны мозгового слоя надпочечников. В надпочечниках синтезируются два главных гормона: адреналин и норадреналин, а также гормон изопропиладреналин. Адреналин и норадреналин являются производными двухатомного фенола пирокатехина, поэтому они называются катехоламинами.
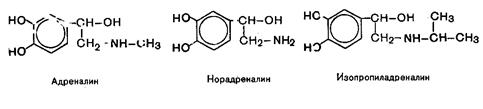
Биосинтез этих катехоламинов осуществляется из аминокислоты тирозина.
Физиологические эффекты адреналина и норадреналина сложны и многообразны; влияя на метаболитические процессы, катехоламины участвуют в поддержании гомеостаза организма в условиях изменившейся среды, в условиях стресса. Сильнее всего они оказывают влияние на сердечно-сосудистую систему, а также на гладкую мускулатуру и функциональную активность нервной системы. Гормоны оказывают сильное действие на углеводный обмен. Они вызывают усиление гликогенолиза, гипергликемию и способствуют накоплению молочной кислоты. Гипергликемический эффект обусловлен активацией распада гликогена в печени под действием фермента фосфорилазы.
Адреналин и норадреналин оказывают выраженное влияние на жировой обмен, приводя к липолизу, мобилизации жирных кислот и повышению их уровня в крови.
Гормоны коркового слоя надпочечников. Из коркового вещества надпочечников выделено около 50 различных соединений (кортикоиды или кортикостероиды).
В зависимости от характера биологического действия гормоны коркового вещества надпочечников условно делят на глюкокортикоиды (кортикостероиды, оказывающие влияние на обмен углеводов, белков, жиров и нуклеиновых кислот) и минралкортикоиды (кортикостероиды, оказывающие преимущественное влияние на обмен солей и воды).
В основе структуры гормонов коркового слоя, как и в основе строения других стероидных гормонов, лежит конденсированная кольцевая система циклопентанпергидрофенантрена. Непосредственным предшественником кортикостероидов является холестерин(ол).
Глюкокортикоиды (кортизол, кортикостерон и др.) оказывают воздействие на многие физиологические процессы в клетках. Они регулируют обмен углеводов, белков и липидов. В мышечной, лимфатической, соединительной и жировой тканях глюкокортикоиды вызывают снижение проницаемости клеточных мембран и торможение поглощения глюкозы и аминокислот, проявляя катаболитическое действие. В печени оказывают противоположное действие. Они ускоряют регенерацию печеночной паренхимы, вызывают гипертрофию печени, стимулируя биосинтез мРНК, индуцирующих новообразование альбумина и других белков плазмы, а также ряда ферментов.
Глюкокортикоиды повышают концентрацию глюкозы в крови, вследствие увеличения глюконеогенеза в печени и почках и уменьшения поглощения и утилизации глюкозы некоторыми тканями.
Длительный избыток кортизола может привести к развитию стероидного диабета.
Глюкокортикоиды оказывают существенное регулирующее действие на систему кроветворения. При введении этих гормонов уменьшается количество лимфоцитов и эозинофилов в крови, стимулируется эритропоэз. Глюкокортикоиды вызывают инволюцию лимфоидной ткани, оказывая депрессивное действие на иммунные процессы.
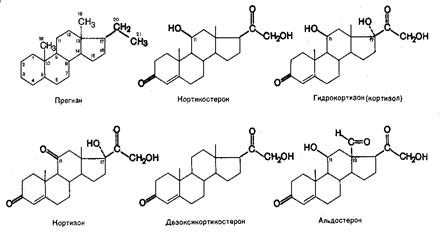
На водный и электронный обмен оказывают свое влияние минералкортикоиды (дезоксикортикокостерон и альдостерон). Самым активным минералкортикоидом является альдостерон, получивший свое название на основании наличия в его молекуле альдегидной группы у 13-го углеродного атома вместо метильной группы, как у всех остальных кортикостероидов.
Альдостерон вызывает задержку в организме ионов Na+ и K+ , аммония. Под его влиянием увеличивается реабсорбция Na+ в дистальных отделах канальцев почек. Альдостерон усиливает выделение кальция и магния.
При недостаточном поступлении кортикостероидов, например, при гипофункции коркового слоя надпочечников снижается кальцевая реабсорбция Na+, это приводит к увеличению экскреции Na+ , Cl и воды, с последующим увеличением объема плазмы. Уменьшение объема внеклеточной жидкости, сгущение крови, увеличение ее вязкости приводят к уменьшению эффективности работы сердца и к гипотонии; развивается метаболитический ацидоз.
Гормоны коркового вещества надпочечников широко используются в клинической практике в качестве лекарственных препаратов. Кортикостероиды обладают антивоспалительной, антиаллергической и антииммунной активностью, что делает их эффективными средствами при лечении целого ряда заболеваний, причиной которых является воспалительный процесс и измененная реакция иммунной системы организма: ревматоидного артрита, пузырчатки, бронхиальной астмы, дерматозов и др.
Половые гормоны
Половые гормоны вырабатываются преимущественно в половых железах; некоторое количество образуется в плаценте и корковом веществе надпочечников. Женские половые гормоны секретируются в основном в яичниках, а мужские – в семенниках. Однако в небольших количествах как семенники, так и яичники вырабатывают и выделяют в кровь также гормоны противоположного пола.
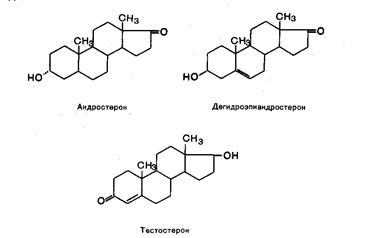
Мужские половые гормоны (андрогены). Андрогены (от греч. andros - мужчина) – группа стероидных гормонов, в основе строения которых лежит ядро андростана.
Наиболее активным андрогеном является тестостерон. Другие (андростендиол и андростерон) обладают в 6-10 раз меньшей активностью, а дегидроэпиандростерон, эпитестостерон – в 25-50 раз менее активны, чем тестостерон.
Регуляция биосинтеза андрогенов в семенниках осуществляется гонадотропными гормонами гипофиза (ЛГ и ФСГ). Выработка андрогенов в мужских половых железах существенно зависит от возраста, физиологического состояния, времени суток и других факторов.
Биологическая роль андрогенов в мужском организме связана с дифференцировкой и функционированием репродуктивной системы. В отличие от эстрогенов андрогенные гормоны уже в эмбриональном периоде оказывают существенное влияние на дифференцировку мужских половых желез, а также других тканей. Во взрослом организме андрогены регулируют развитие мужских вторичных половых признаков, сперматогенез в семенниках и т.д.
Андрогены оказывают существенное влияние на обмен веществ. Они обладают мощным анаболитическим действием, которое в первую очередь связано со стимуляцией синтеза белка в костной, хрящевой, мышечной тканях.
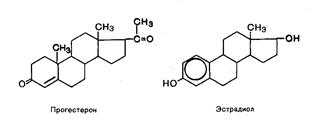
Женские половые гормоны. Основным местом синтеза женских половых гормонов являются яичники и желтое тело; доказано также и образование этих гормонов в надпочечниках, семенниках и плаценте. Женские половые гормоны делятся на две группы: эстрогены и прогестины.
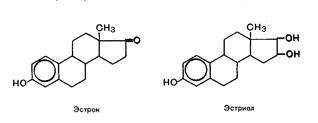
К эстрогенам относятся эстрадиол, эстрол (фолликулин) и эстриол. Основным эстрогенным гормоном является эстрадиол. Предшественником гормонов является холестерин.
Ведущую роль в регуляции синтеза эстрогенов и прогестерона играют гонадотропные гормоны гипофиза (фоллитропин и лютропин).
Действие эстрогенов и прогестинов, синтез которых начинается после наступления половой зрелости, направлено на развитие органов женской половой сферы и обеспечение репродуктивной функции организма женщины. В этот период гормоны вызывают развитие вторичных половых признаков и создают оптимальные условия, обеспечивающие возможность оплодотворения яйцеклетки после овуляции. Прогестерон выполняет в организме ряд специфических функций: подготавливает слизистую оболочку матки к успешной имплантации яйцеклетки в случае ее оплодотворения, а при наступлении беременности основная роль – сохранение беременности; оказывает тормозящее влияние на овуляцию и стимулирует развитие ткани молочной железы. Эстрогены оказывают анаболическое действие на организм, стимулируя синтез белка.
Гормоны вилочковой железы
Тимус осуществляет синтез и секрецию гормонов, которые влияют на скорость развития и созревания определенных популяций лимфоидных клеток. Вилочковая железа обуславливает иммунокомпетентность лимфоидных клеток и определяет спектр иммунологической активности организма. Тимус секретирует группу пептидов (тимозин, тимопоэтин I и II и др.), каждый из которых влияет на один или несколько имуннологических процессов.
При отсутствии тимуса при рождении или его неадекватном функционировании происходит нарушение нормального иммунологического статуса либо он вообще отсутствует.
Гормоны насекомых
У насекомых гормоны образуются в нейросекреторных клетках мозга, продолговатого ганглия и узлов брюшной нервной цепочки, а также в эндокринных железах, к которым относятся прилежащие железы. Зерна нейросекрета перемещаются вдоль аксонов нейросекреторных клеток к их окончаниям и могут накапливаться в специальных депо (например, в кардиальных телах). Эндокринные железы секретируют свои гормоны непосредственно в гемолимфу.
Гормоны насекомых участвуют в регуляции обмена веществ, линьки и метаморфоза, развития яичников и придаточных желез полового аппарата, влияют на движения кишки, мальпигиевых сосудов и яйцеводов. Эндокринная система управляет ходом развития и размножения насекомых.
У насекомых открыт целый спектр гормонов разного действия, но не все они идентифицированы.
Нейросекрет клеток, расположенных в интерцеребральной части мозга, содержит активационный гормон (АГ). АГ стимулирует синтез РНК, влияет на проницаемость мембран и мембранный потенциал клеток проторакальной железы. Воздействуя на проторакальные железы, АГ побуждает их к синтезу экдизона – гормона, обусловливающего наступление и прохождение линьки, а также склеротизацию покровов. Основными мишенями для экдизона служат клетки гиподермы и имагиальных дисков, точнее, хромосомы этих клеток. Экдизон обуславливает наступление и прохождение линочного процесса, однако его характер и результат зависят от ювенильного гормона (ЮГ), продуцируемого прилежащими телами. Выявлено три вида терпеноида, условно названных ЮГ-I, ЮГ-II, ЮГ-III. ЮГ предотвращает превращение личинки в куколку и во взрослое насекомое (имаго), т.е. тормозит метаморфоз. Именно поэтому этот гормон называют неотенином (гормоном молодых), или гормоном статус-кво.
Вопросы и задачи
1. Какие вещества называются гормонами?
2. Приведите классификацию гормонов.
3. Где синтезируется вазопрессин?
4. Какие гормоны обеспечивают следующие процессы:
а) стимулирует распад гликогена в печени; б) стимулирует процессы роста и развития; в) стимулирует проникновение и утилизацию глюкозы в тканях?
5. При недостатке какого гормона возникает сахарный диабет?
6. В каких органах вырабатываются половые гормоны?
7. Какую долю в массе тироксина (785 Да) составляет йод (атомная масса 130)?
Рекомендуемая литература
1. Биохимия. Краткий курс с упражнениями и задачами / Под ред. чл.-корр. РАН, проф. Е.С. Северина, проф. Н.Л. Николаева. – М.: ГЭОТАР-МЕД, 2001. – 448 с.
2. Биохимия / В.Г.Щербаков, В.Г. Лобанов, Т.Н. Прудникова и др.; Под ред. В.Г. Щербакова. – СПб.: ГИОРД, 2003. – 440 с.
3. Березов Т.Т., Коровкин Б.Ф. Биологическая химия: Учебник.– М.: Медицина, 1998. – 704 с.
4. Жеребцов Н.А., Попова Т.Н., Артюхов В.Г. Биохимия.– Воронеж: Изд-во Воронеж. гос. ун-та, 2002. – 696 с.
5. Камилов Ф.Х., Давлетов Э.Г. Биохимия гормонов и механизм гормональной регуляции обмена веществ.– Уфа: Гилем, 1998. – 268 с.
6. Киршенблат Я.Б. Общая эндокринология: Учеб. пособие для университетов.– М.: Высшая школа, 1971. – 384 с.
7. Комов В.П. Биохимия. – М.: Дрофа, 2004.– 640 с.
8. Чиркин А.А. Практикум по биохимии: Учеб. пособие. – Мн.: Новое издание, 2002. – 512 с.
ГЛАВА 8. МОЛЕКУЛЯРНЫЕ МЕХАНИЗМЫ
ГОРМОНАЛЬНОГО СИГНАЛА
Несмотря на огромное разнообразие гормонов и гормоноподобных веществ, в основе биологического действия большинства гормонов лежат сходные механизмы, передающие информацию от одних клеток к другим.
Направленность и тонкая регуляция процесса передачи информации обеспечиваются, прежде всего, наличием на поверхности клеток рецепторных молекул, узнающих гормональный сигнал. Этот сигнал рецепторы трансформируют в изменения концентраций внутриклеточных посредников (мессенджеров), уровень которых определяется активностью ферментов, катализирующих их синтез и распад.
Каждый гормон имеет свой специфический рецептор в клетках-мишенях, и действие любого гормона начинается с его рецепции, связывания с клеткой. Реализация биологического эффекта гормона зависит не только от концентрации этого гормона в плазме, но и от состояния специфического рецептора в клетках-мишенях.
Рецепторы гормонов располагаются как внутри клеток-мишеней, так и на мембранах. Стероидные гормоны благодаря своей гидрофобности хорошо преодолевают клеточные и другие мембраны, и их рецепторы расположены внутри клеток.
Гормоны белковой природы являются гидрофильными и поэтому не способны пассивно проникать через клеточные мембраны. Рецепторы для них расположены на плазматических мембранах.
