Дистрофия миокарда физического перенапряжения с нарушениями сократительной функции сердца (ДМФП)
Высокие адаптационные резервы спортивного сердца и, как правило, ограниченный характер дистрофии миокарда способствуют тому, что нарушения сократительной способности сердца у спортсменов в течение долгого времени могут отсутствовать или оставаться скрытыми.

Рис. 13. ЭКГ в покое в трех однополюсных отведениях от конечностей после установки стимулятора по требованию. Зарегистрирован момент включения стимулятора после импульса из парацентра
Для их выявления необходимы специальные исследования, и прежде всего пробы с физическими нагрузками. На первых этапах дизадаптации удается выявить лишь снижение максимальной интенсивности функционирования структур.
Клинически скрытые признаки нарушения сократительной способности сердца могут проявляться неадекватной реакцией на физическую нагрузку с преимущественной компенсацией возрастающего МОК за счет прироста ЧСС. К ранним признакам нарушений сократительной способности сердца следует отнести и замедление процессов восстановления после физических нагрузок.
Seals и соавт. (1988) исследовали функцию левого желудочка у здоровых лиц, выполнявших длительную (около 3 ч) работу на тредмиле мощностью, составившей 70% от МПК. Выявлено, что нагрузки изнурительного характера способны привести к дисфункции левого желудочка и депрессии его сократительной функции. Авторы отмечают, что при кратковременных нагрузках подобные нарушения не выявлялись.
При нагрузочном тесте в условиях лаборатории при ДМФП удается выявить заметные отклонения в адаптации. Выделяют три типа срочной адаптационной реакции:
1)физиологически экономичный тип– повышение МОК происходит за счет синхронного прироста ЧСС и УО или прирост УО опережает увеличение ЧСС;
2)физиологически неэкономичный тип– повышение МОК происходит преимущественно за счет увеличения ЧСС;
3)патологический (условно патологический) тип – не происходит достаточного увеличения МОК, несмотря на выраженный прирост ЧСС, возможно снижение УО и МОК в конце выполнения нагрузки.
Последний тип расценивают как ДМФП, протекающую с нарушением сократительной способности миокарда.
Смешанный вариант клинического течения
Перечисленные клинические варианты течения ДМФП могут встречаться в различных сочетаниях — от изолированного нарушения процесса реполяризации без нарушений функции сердечнососудистой системы до сочетанного выявления существенных морфологических изменений по данным ЭхоКГ, нарушений электрических явлений в сердце и аритмий в покое с нарушениями функции сердечно-сосудистой системы при физических нагрузках.
Лечение и профилактика
Учитывая широкую распространенность ДМФП и опасность развития патологической гипертрофии и миодистрофического кардиосклероза, а иногда серьезных осложнений, вопросы лечения и профилактики ДМФП чрезвычайно актуальны. На основе современных представлений о патогенезе ДМФП следует рассматривать два основных направления в лечении и профилактике:
1)врачебно-педагогическое;
2)медикаментозное.
К врачебно-педагогическим мероприятиям следует прежде всего отнести регулярные врачебно-педагогические наблюдения и обследования, позволяющие выявить нарушения адаптации к физическим нагрузкам на ранних стадиях и существенно облегчающие индивидуализацию спортивной тренировки. В случае выявления тех или иных признаков ДМФП взаимодействие врача и тренера позволяет снизить или даже на время полностью прекратить тренировки, устранить факторы риска, способствующие нарушениям адаптации сердца. Уже только этих мероприятий порой бывает достаточно, чтобы добиться нормализации функционального состояния сердечно-сосудистой системы.
Однако ожидаемый эффект достигается быстрее и оказывается более стойким, если используется сочетание врачебно-педагогических и медикаментозных средств лечения ДМФП.Терапевтические мероприятия следует выбирать с учетом многообразия патогенетических механизмов развития ДМФП и учитывать важную роль ОХИ при этом патологическом состоянии.
Активное выявление и лечение ОХИ любой локализации обеспечивает эффективность профилактики и лечения ДМФП.
Медикаментозная терапия подтверждается работами многих авторов (Ю.И. Каросене и др., 1976; К.С. Чернявский и др., 1980; Л.А. Бутченко и др., 1980; С.А. Душанин, В.В. Шигалевский,1988; Э.В. Земцовский,1995).
Многообразие патогенетических механизмов, участвующих в развитии ДМФП, требует врачебно-педагогического воздействия на несколько звеньев патогенетической цепи. Учитывая роль эмоционального и физического стрессов в развитии ДМФП, целесообразно использовать средства для нормализации психоэмоционального статуса. При гиперадренергическом типе ДМФП показано использование β-адреноблокаторов для защиты кардиомиоцитов от повреждающего действия липидов, и прежде всего перекисного окисления липидов (ПОЛ). Рекомендуют использовать мембранопротекторы, к которым относятся ингибиторы ПОЛ – ионол (Ф.З. Меерсон, М.Г. Пшенникова,1988).
При участии в формировании ДМФП нарушений ионного равновесия следует активно использовать препараты калия (хлорид калия, панангин), а также блокаторы кальция (верапамил). И.М. Шестаков и соавт. (1990) получили убедительные данные, подтверждающие участие кальциевого механизма в формировании ДМФП, и эффективность антагонистов кальция в терапии скрытой недостаточности сократительной способности миокарда, развивающейся при этом.
Авторы получили при применении финоптина у спортсменов с третьим патологическим типом срочной адаптационной реакции на возрастающую физическую нагрузку отчетливые и статистически значимые приращения производительности сердца и экономизации функции. Важно, что УО возрастал тем значительнее, чем он был меньше до медикаментозной коррекции.
Важной задачей лечения ДМФП является стимуляция восстановительных процессов и синтеза нуклеиновых кислот. Существенную роль в этом, как показали клинические наблюдения и экспериментальные данные, играют рибоксин и оротат калия, а также незаменимые аминокислоты.
Рекомендуются препараты, стимулирующие репаративные процессы (восстановления природной структуры ДНК, поврежденной под воздействием физических факторов) (метилурацил, карнитин, оротат калия и др.).
Рядом авторов (В.В. Шигалевский и др., 1980) разработаны программы реабилитации спортсменов с ДМФП, специальные двигательные режимы, способствующие восстановлению спортивной работоспособности. В целом при ранней диагностике и патогенетическом обоснованном лечении эффект достигается в 67–50% случаев. Сроки лечения до полной нормализации ЭКГ и восстановления функционального состояния сердечно-сосудистой системы различны и зависят от своевременной диагностики, правильного лечения и точного выполнения спортсменом предписаний врача.
По данным К.С. Чернявского и соавт. (1980), в 61% случаев эффект достигается за 30 дней, в 13% – за 60 дней, в 20% – в течение 3—5 мес. и в 5,5% – за 1–2 года. По данным этих авторов, у 22% спортсменов, излечившихся от ДМФП, при начале спортивных тренировок отрицательные изменения ЭКГ возникали вновь.
Представляет значительный интерес предлагаемое Г.Л. Апанасенко и соавт. (1984) лечение ДМФП методом гипербарической оксигенации. Авторы исходят из того, что у спортсменов с ДМФП уменьшается доставка кислорода к миокарду за счет снижения эффективности субэндокардиальной перфузии (прохождения крови через миокард).
Происходящее при интенсивных физических нагрузках повышение энергозатрат в 20 раз и более чаще вызывает нарушения адекватного снабжения организма кислородом, в том числе и клеток миокарда.
Возникает необходимость увеличения содержания кислорода в крови, чего невозможно достигнуть при нормальном насыщении гемоглобина кислородом. Как известно, насыщение гемоглобина О2 составляет 96—97% и даже доведение уровня насыщения до 100%, что возможно лишь при вдыхании чистого кислорода, очень незначительно увеличивает его количество в крови. Очевидна необходимость увеличения содержания кислорода в плазме, в которой он находится в растворенном состоянии (в норме 0,3%). Это возможно только при гипербарической оксигенации.
Из медикаментозных средств для профилактики ДМФП на сборах и в период интенсивных тренировочных нагрузок с хорошим эффектом используют антиоксиданты. Из антиоксидантов рекомендуется использовать а-токоферол (100 мг), аскорбиновую кислоту (50 мг в день), дибунол (1 г через день в течение 10 дней). Их применение обосновывается тем, что при интенсивной физической нагрузке происходит активация ПОЛ. При чрезмерной нагрузке оно нарушает структуру и функции биологических мембран, что может быть одним из механизмов развития ДМФП. Антиоксиданты как ингибиторы ПОЛ подавляют этот процесс (Ф.З. Меерсон и др.,1983).
Основываясь на данных о роли простагландидов в развитии ДМФП, И.Е. Смирнов и соавт. (1991) предлагают использовать для профилактики повреждений миокарда комплекс мер, направленных на образование кардиопротективных простагландидов.
Авторы рекомендуют диету с высоким содержанием полиненасыщенных жирных кислот и эссенциальных фосфолипидов.
В качестве профилактики ДМФП следует также использовать питание, содержащее повышенное количество протеинов, включая незаменимые аминокислоты. Профилактика ДМФП прежде всего заключается в том, чтобы тренировочный процесс всегда был строго индивидуализирован, физическая нагрузка соответствовала возможности спортсмена. Необходимы также тщательное врачебное наблюдение и систематический ЭКГ-контроль.
Все спортсмены, перенесшие ДМФП, при возобновлении тренировок должны длительное время находиться под строгим врачебным наблюдением.
Исход и прогноз
Основываясь на изложенных выше теоретических положениях, данных патолого-анатомических исследований и результатах экспериментов можно утверждать, что ДМФП может иметь два варианта исхода — восстановление структуры и функции миокарда либо развитие миодистрофического кардиосклероза. Основными условиями для обратного развития дистрофических изменений являются: ранняя диагностика, устранение этиологического фактора, т.е. чрезмерных физических и эмоциональных нагрузок и проведение комплексных терапевтических и реабилитационных мероприятий. При несоблюдении этих условий возникает реальная опасность перехода ДМФП в миодистрофический кардиосклероз.
При этом степень выраженности нарушений сократительной способности миокарда определяется обширностью зоны повреждения. Необходимо учитывать также и то обстоятельство, что даже при тяжелых поражениях миокарда и миогенной дилатации сердца спортсмены способны иногда демонстрировать поразительную физическую работоспособность, особенно в тех случаях, когда речь идет о специальных упражнениях в избранном виде спорта.
Вместе с тем ДМФП может также достаточно быстро привести к миодистрофическому кардиосклерозу и выраженной сердечной недостаточности. А.А. Кедров (1963) описывал случай острой дистрофии миокарда у спортсменки 24 лет после участия в ответственных соревнованиях. Перед финишем спортсменка почувствовала сильное сердцебиение, перебои, «страх смерти». После этих соревнований ушла из спорта. Несмотря на это, в течение нескольких лет наблюдения жаловалась на сердцебиение и перебои, выявлялась одышка в покое и отеки на ногах к вечеру, лечилась от сердечной недостаточности.
Есть все основания полагать, что в основе развития сердечной недостаточности лежала острая дистрофия миокарда вследствие физического перенапряжения с исходом в миодистрофический кардиосклероз.
Прогноз ДМФП следует рассматривать в трех аспектах – прогноз жизни, здоровья и спортивный прогноз.
Прогноз жизни при ДМФП вполне благоприятен. Следует помнить, однако, о риске внезапной смерти у спортсменов во время или вскоре после тренировок или соревнований. Непосредственной причиной внезапной смерти в подобных случаях чаще является фибрилляция желудочков, развивающаяся вследствие электрической нестабильности миокарда. Причиной последней может стать гипертрофия миокарда и локальная гипоксия на фоне дистрофических изменений сердца.
Прогноз здоровья при ДМФП в значительной мере зависит от своевременной диагностики ДМФП на ранних стадиях устранения воздействия этиологического фактора, какими являются чрезмерные физические и эмоциональные нагрузки, а также от эффективности комплекса терапевтических и реабилитационных мероприятий. Принятие соответствующих мер при выявлении ДМФП приводит к
полному восстановлению измененной ЭКГ, исчезновению аритмий и других возможных проявлений ДМФП.
Доказано, что даже при компенсаторно-гипертрофическом типе ДМФП прекращение тренировок приводит к уменьшению степени выраженности гипертрофии. Вместе с тем сроки достижения полной нормализации ЭКГ могут колебаться от нескольких недель до 2—3 лет.
Спортивный прогноз. Вопрос о возможности возобновления тренировок должен решаться после нормализации ЭКГ и исчезновения других проявлений ДМФП. Начинать тренировки можно, только постепенно увеличивая нагрузки под постоянным врачебным контролем. В значительной части случаев постепенное увеличение тренировочных нагрузок в сочетании с медикаментозной терапией и мерами физической реабилитации позволяет добиться стойкого сохранения высокой спортивной работоспособности без повторных проявлений нарушения адаптации к физическим нагрузкам.
Однако не исключен и другой вариант реакции сердечно-сосудистой системы на повторное включение в спортивные тренировки — в ответ на возобновление тренировок вновь появляются патологические изменения. В подобных случаях следует считать, что спортивные тренировки противопоказаны. Это не только не исключает достаточно высокий уровень двигательной активности бывшего спортсмена, но и делает физические тренировки (с исключением соревновательных элементов и стремления улучшить спортивный результат) необходимыми.
Встречается и третий вариант реакции сердечно-сосудистой системы на прекращение спортивных тренировок после выявления ДМФП — отсутствие положительной динамики. В подобных случаях в миокарде возникают необратимые изменения дистрофического характера на фоне патологической гипертрофии миокарда.При таком исходеследует рекомендовать лишь оздоровительную физкультуру.
Прогноз здоровья и спортивный прогноз в значительной мере зависят от патогенетического типа ДМФП и стадии заболевания. С прогностической точки зрения наиболее неблагоприятен компенсаторно-гипертрофический тип ДМФП. Напротив, дисэлектролитный и гипоадренергический типы в течение длительного времени не сопровождаются нарушениями сократительной функции миокарда и при принятии вовремя необходимых мер легко подвергаются обратному развитию.
Практические занятия
Семинар. Вопросы:
–этиология ДМФП;
–патогенез ДМФП;
–формы ДМФП;
–клиническое течение ДМФП;
–лечение ДМФП;
–прогноз ДМФП: прогноз жизни, прогноз здоровья и спортивный прогноз;
Демонстрация ЭКГ.
Литература
1.Бондарев С.Л. Аритмический вариант клинического течения дистрофии миокарда у спортсменов: Автореф. дисс. канд.мед.наук.–СПб., 1995. – 24 с.
2.Граевская Н.Д. Влияние спорта на сердечно-сосудистую систему. – М.: Медицина,1975. – С. 278.
3.Земцовский Э.В. Дистрофия миокарда у спортсменов//Спортивная кардиология. – СПб.: Гиппократ, 1995. – С. 254–324.
Кардиомиопатия
Под названием «кардиомиопатия» в настоящее время объединяют большое количество заболеваний сердечной мышцы. К их числу относится идиопатическая кардиомиопатия, при которой расширение сердца является следствием фиброза, дегенерации и гипертрофии сердечной мышцы неизвестного происхождения. Заболевание бывает распространено среди мужчин среднего возраста. Образующуюся при этом декомпенсацию обычно рассматривают как ишемическое заболевание сердца (кардиосклероз). Часты легочные и системные эмболии, тромбозы, желудочковые экстрасистолии, отклонение S-Т и Т на ЭКГ, фибрилляция предсердий, блокада ножки пучка Гиса. По-видимому, алкоголь также способствует развитию кардиомиопатии. Послеродовая кардиомиопатия проявляется у новорожденных. Гипертрофические формы идиопатических заболеваний сердечной мышцы приводят к развитию гипертрофического субаортального стеноза, гипертрофической обструктивной кардиомиопатии. Эти заболевания достоверно распознаются только при катетеризации сердца. Клинические симптомы: одышка, стенокардия, потеря сознания, слабость левого желудочка, расщепление второго тона, систолический шум выбрасывания на верхушке сердца. На ЭКГ — признаки гипертрофии левого желудочка и глубокая широкая волна Q, которую часто считают признаком бывшего инфаркта.
Кардиомиопатии часто являются семейными заболеваниями, к этой группе относят случаи идиопатической дилатации сердца, вызывающей сердечную декомпенсацию неизвестной природы в молодом возрасте. Диагноз ставится после исключения других заболеваний.
Согласно классификации Goodwin (1982), КМП подразделяются на 3 основные группы –застойную, гипертрофическую и обструктивную. Обструктивная и застойная КМП встречается у спортсменов крайне редко.
Э.В. Земцовский наблюдал лишь одного спортсмена, у которого это заболевание было диагностировано клинически и впоследствии подтверждено на аутопсии. Речь шла о 30-летнем спортсмене-велосипедисте, злоупотреблявшем алкоголем.Огромное сердце было обнаружено у него при клиническом, а позднее при ЭхоКГ-исследовании левого желудочка –93 мм, больной обратился к врачу с жалобами на приступы сердцебиения.
При ЭКГ-исследовании были выявлены пароксизмы фибрилляции предсердий и частая желудочковая экстрасистолия.
Есть основания полагать, что в данном случае поражение сердца было вызвано сочетанным воздействием этанола и больших физических нагрузок.
Гипертрофическая КМП (ГКМП), как одна из наиболее частых причин прекращения спортивных тренировок и даже внезапной смерти, является самостоятельным заболеванием. В. Магоn (1993) на основании большого собственного материала (около 100 наблюдений) приходит к заключению, что среди всех причин внезапной смерти спортсменов КМП составляет примерно 50% случаев.
Большинство исследователей связывают заболевание с генетической аномалией, передающейся по аутосомно-доминантному типу. Предполагают, что генетический дефект приводит к нарушению дифференцировки сократительного миокарда и появлению гигантских и хаотически расположенных миофибрилл; у 30% больных выявляется злоупотребление пивом.
Выделяют 4 наиболее часто встречающихся анатомических варианта локализации гипертрофии (B.C. Моисеев и др.,1993):
1)гипертрофия базальных отделов межжелудочковой перегородки (10,2%);
2)тотальная гипертрофия межжелудочковой перегородки (27,5%);
3)тотальная гипертрофия перегородки и свободной стенки левого желудочка – симметричная гипертрофия (43,5%);
4)гипертрофия верхушки сердца с возможным распространением на свободную стенку (18,8%).
Критерием заболевания является развитие гипертрофии с утолщением стенки левого желудочка до 15 мм и более, а критерием асимметричности гипертрофии является превышение отношения толщины гипертрофированного и негипертрофированного сегментов левого желудочка 1,3–1,4 мм. При этом гипертрофия межжелудочковой перегородки более выражена, а диастолическая функция желудочков снижена.
По данным SanjaySharma (2002), у молодых спортсменов толщина стенки левого желудочка редко превышает 12 мм. Систематические тренировки приводят к увеличению толщины стенки левого желудочка, затрудняя дифференциальную диагностику между спортивным сердцем и ГКМП. Точный диагноз очень важен, так как ГКМП является причиной каждого третьего случая внезапной смерти среди молодых спортсменов. Для уточнения физиологических границ гипертрофии левого желудочка Lewisham (Лондон) провел обследование 720 атлетов в возрасте 14–18 лет и 250 здоровых молодых людей, не занимающихся спортом. Среди спортсменов среднее значение толщины стенки левого желудочка (ТСЛЖ) достигло 9,6 мм, в группе контроля –8,5 мм. Из 720 атлетов только у 38 человек (5%) значение толщины стенки левого желудочка превышало допустимые верхние границы нормы. У девушек-спортсменок ТСЛЖ не превышала 11 мм. У всех атлетов с ТСЛЖ выше нормы отмечалось увеличение полости левого желудочка до 54,4 мм (у незанимающихся – 45–46 мм). По мнению английских исследователей, ГКМП должна быть заподозрена при значении ТМЛЖ более 12 мм (11 мм у девушек).
R. Maron (1993) отмечает также, что наряду с гипертрофией, на аутопсии обнаруживаются фиброзные и рубцовые изменения миокарда, однако обструкция путей оттока из левого желудочка имеет место лишь в 25% случаев (рис. 14).
Интересно, что вероятность взаимосвязи КМП и физических перегрузок большинством исследователей не рассматривается. Вместе с тем гигантские миофибриллы обнаруживаются не только у больных с КМП, но и у здоровых лиц, а наряду с семейной формой гипертрофической КМП часто встречаются наблюдения, при которых не удается обнаружить признаков наследственной передачи заболевания. Это позволяет (Э.В. Земцовский, 1995) высказать предположение о важной роли физических перегрузок, психоэмоционального стресса и других факторов риска, сопряженных со спортивными тренировками и соревнованиями в развитии гипертрофии миокарда как в асимметрическом варианте, так и особенно при симметричной гипертрофии перегородки и свободной стенки левого желудочка.
Не отвергая семейный характер гипертрофической КМП, большинство спортивных кардиологов склонны считать, что в подавляющем большинстве случаев выявления выраженной гипертрофии миокарда у спортсменов речь идет не о первичной, а о вторичной КМП. Последняя, согласно принятой терминологии, соответствует дистрофии
миокарда вследствие хронического физического перенапряжения. Ведущим звеном в патогенезе ДМФП в подобных случаях является компенсаторная гипертрофия миокарда, вызванная чрезмерными физическими нагрузками и (или) генетически детерминированной низкой мощностью систем ресинтеза АТФ и систем, ответственных за расслабление миокарда (Ф.З. Меерсон,1985).
И все же первичная гипертрофическая КМП встречается в спортивно-медицинской практике. И.Б. Гитель (1991), И.Б. Гитель и Л.Н. Марков (1993) за 10 лет работы в 1-м Московском врачебно-физкультурном диспансере при обследовании нескольких десятков тысяч спортсменов высокого класса диагностировали гипертрофическую КМП у 13 пациентов.
Диагноз КМП устанавливается по данным клинического и инструментального исследования. Важнейшим инструментальным методом исследования в подобных случаях является эхокардиография. Однако дифференциальная диагностика между гипертрофической
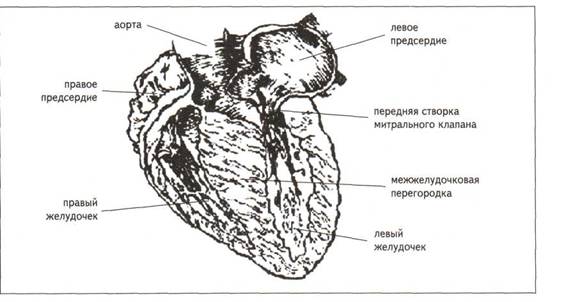
Рис. 14. Разрез сердца от верхушки к основанию при ГКМП. Верхняя часть перегородки утолщена и вплотную приближена к передней створке митрального клапана (А.Г. Чучалин,1996)
КМП и ДМФП компенсаторно-гипертрофического типа может быть успешно проведена путем оценки динамики состояния и выраженности гипертрофии миокарда после прекращения спортивных тренировок. При гипертрофической КМП прекращение тренировок не сопровождается какой-нибудь существенно положительной динамикой ЭКГ и уменьшением выраженности гипертрофии миокарда. Напротив, при ДМФП компенсаторно-гипертрофического типа прекращение тренировок приводит к нормализации ЭКГ и обратному развитию признаков гипертрофии миокарда.
Таким образом, в спортивно-медицинской практике у лиц молодого возраста первичная КМП встречается крайне редко, но, учитывая опасность развития электрической нестабильности миокарда и внезапной смерти, своевременное распознавание этого заболевания крайне важно. Учитывая семейный характер ГКМП, следует уже на этапе отбора для занятий спортом выявлять лиц с повышенным риском развития этого заболевания. Диагностика гипертрофической КМП у действующих спортсменов должна строиться на анализе клинических данных (снижение спортивных результатов, жалобы на головокружения, систолический шум изгнания при аускультации) и результатах инструментального исследования, прежде всего на данных ЭхоКГ.
Практические занятия
–Понятие о кардиомиопатиях;
–Причины;
–Течение;
–Вопросы медицинско-спортивной экспертизы;
–Связь кардиомиопатий с внезапной смертью спортсменов.
Литература
1. Земцовский Э.В. Кардиомиопатий//Спортивная кардиология. – СПб.: Гиппократ,1995. – С. 376-378.
2. Макарова Г.А. Проблема риска внезапной смерти при занятиях физической культурой и спортом//Вестник спортивной медицины России. – 1992. -№1. – С.18–21.
