Антибактерицидная (Анти-БАС) активность
Диагностический признак
• Факультативные анаэробы, предпочитают аэробные условия
1. Адгезия:
тейхоевые кислоты, капсульный полисахарид, белок А
2. Ферменты:
· плазмокоагулаза –
· лецитиназа фибринолизин
· ДНК-аза
· гиалуронидаза
· каталаза
· липазы
· бета-лактамазы –(устойчивость к
антибиотикам)
Факторы агрессии: белок А- антифагоцитарное
действие (связывает Ig по Fc-фрагменту); каталаза- антифагоцитарное действие
(инактивация перекисных соединений фагоцитов); антилизоцимная (ALA) и
Антибактерицидная (Анти-БАС) активность
Альфа-токсин (мембранотоксин) – гемолитическое, кардиотропное, нейротропное,
дермонекротическое действие;
Эксфолиативный токсин (мембранотоксин) – разрушает соединительнотканные клетки
(пузырчатка новорожденных, импетиго и пр., синдром ошпаренной кожи)
Токсин синдрома токсического шока (ТСТШ) - активация продукции цитокинов
моноцитами и макрофагами (функции суперантигена)
Энтеротоксины (A,B,C,D,E,F)
Антигенные свойства проявляют:
• Пептидогликан, тейхоевые кислоты, микрокапсула, белок А
• Экзотоксины и некоторые ферменты
Стафилококковые инфекции являются токсикоинфекциями (кроме поражений ЖКТ) – в
развитии клинических проявлений имеет значение как размножение возбудителя и
действие на окружающие ткани его факторов патогенности, так и циркулирующие в
кровотоке его экзотоксины
Иммунитет при стафилококковых инфекциях:
1. Направленность: антибактериальный и антитоксический
2. Выраженность и продолжительность: нестойкий, ненапряженный
3. Ведущая роль принадлежит IgA (защита входных ворот)
Источник инфекции:
1. Больные
2. Реконвалесценты
3. Здоровые бактерионосители (постоянные(резидентные) и транзиторные)
Пути и механизмы заражения:
1. Аэрогенный (преимущественно воздушно-капельный)
2. Контактный (бытовой, контактно-интсрументальный в лечебных учреждениях)
3. Алиментарный
Бактериологический метод:
• Патологический материал зависит от клинических проявлений и исследуется с
учетом количества возбудителя
• Элективная среда – солевой агар (6-10% хлорида натрия)
• Основные видовые дифференцирующие признаки:
1. Гемолитическая активность
2. Плазмокоагулирующая активность
3. Лецитиназная активность
• При определении источника инфекции – фаготипирование (чувствительность к
типовым стафилококковым бактериофагам)
Вакцины (для терапии больных с хроническими стафилококковыми инфекциями и
предоперационной вакцинации групп риска)
• Химическая стафилококковая («антифагин»): компоненты оболочки золотистого
стафилококка, включая белок А
• Убитая стафилококковая (корпускулярная): смесь клинически значимых
штаммов золотистого стафилококка
• Вакцина ВП-4: содержит экстрагированные антигены золотистого стафилококка,
протея, клебсиеллы пневмонии, кишечной палочки адсорбированные на
гидроокиси аллюминия
• Комплексная стафило-протейно-синегнойная: анатоксины золотистого
стафилококка и синегнойной палочки + экстрагированные антигены золотистого
стафилококка и протея
Анатоксины (для иммунизации доноров, для предоперационной вакцинации групп риска) • Стафилококковый адсорбированный (альфа-токсин)
Иммуноглобулины (для лечения больных)
• Стафилококковый иммуноглобулин (донорский)
Бактериофаги (для лечения очаговых стафилококковых инфекций)
9. Проблема госпитальной стафилококковой инфекции в педиатрии. Значение носительства стафилококков у работников в детских учреждениях. Принципы санации носителей. Методы эпидемиологического анализа госпитальных стафилококковых инфекций.
Путь этим вопросом займётся какой-нибудь педиатр
10. Стрептококки, их классификация (Ленсфильд). Общая характеристика стрептококков, факторы патогенности. Роль стрептококков группы А и В в патологии человека. Микробиологическая диагностика стрептококковых заболеваний.
Стрептококи
Сем. Streptococcaceae
Род Streptococcus
Виды
Str. pyogenes,
Str. viridans,
Str. pneumoniae,
в полости рта:
Str. mutans,
Str. mitis
Гр+ кокки, иногда овальные; в мазках – цепи разной
длины;
неподвижны
спор нет
гиалуроновая капсула
Альфа-гемолиз – «зеленящий»; неполный гемолиз
По полисахаридному Ag стрептококки
Распределены по группам (17 групп: A,B,C,D и т.д.) Внутри группы стрептококки
Ревматизма
А: основные патогены для человека (90% всех стрептококковых инфекций): рожистое воспаление, стрептодермия, отиты, гломерулонефриты, артриты и пр.; скарлатина
• В: послеродовые инфекции, урогенитальные инфекции у женщин, сепсис и менингиты новорожденных, эрозивные стоматиты
• С: поражение дыхательных путей, мочеполовой системы
• D: поражение желчных путей, мочеполовой системы, эндокардиты
• Н,К: эндокардиты
Скарлатина – антропонозная инфекция; болеют дети младшего возраста;
возбудитель вегетирует на слизистой зева; передается воздушно-капельным путем;
в эпидемиологии имеет значение бактерионосительство скарлатинозных
стрептококков.
Клинические проявления скарлатины:
1. Ангина
2. Интоксикация
3. Сыпь ярко-красного цвета
Иммунитет при скарлатине антитоксический стойкий
Бактериологический метод: патологический материал зависит от клинических
проявлений и исследуется с учетом количества возбудителя
• Дифференцирующие признаки:
Обладать токсигенностью.
У C. diphtheriae выделяют О- и К-Ag
О-Ag коринебактерий преимущественно представлены межвидовыми Ag
Поверхностные термолабильные К-Ag обеспечивают видовую специфичность и
проявляют выраженную иммуногенность (около 58 биоваров).
Микроскопический – обнаружение в мазках из зева или из чистой культуры
типичных дифтерийных палочек;
2. Бактериологический – посев патологического материала (мазки из зева и носа,
фибриновые пленки) на теллуритовый кровяной агар с последующей
идентификацией на жидких средах Гисса и определением токсигенности в реакции
преципитации в агаре (см. рис.9);
3. Серологический – реакция непрямой гемагглютинации (РНГА) с парными
сыворотками; РНГА может использоваться для оценки антитоксического
иммунитета (диагностический титр 1:40)
При лечении дифтерии обязательно используется антитоксическая сыворотка
(лошадиная ) или антитоксический иммуноглобулин (донорский)
Создание искусственного иммунитета обеспечивается: вакцинами АКДС, АКДС-М,
АДС, АДС-М у детей и подростков; у взрослых – дифтерийным анатоксином.
2. Микобактерии, классификация, характеристика биологических свойств возбудителя туберкулеза, виды микобактерий, факторы патогенности. Иммунитет, его особенности, методы микробиологической диагностики, специфическая профилактика туберкулеза.
Род Mycobacterium
Виды: M.tuberculosis
M.bovis
M.africanum
Грамположительные, неподвижные,
полиморфные (от длинных до кокковидных форм), прямые или изогнутые
палочковидные бактерии. Длиной от 1 до 10 мкм и шириной от 0,2 до 0,6 мкм.
Строгие аэробы
Требовательны к питательным средам: необходимы аминокислоты,
витамины и пр. (среда Ливенштейна-Йенсена содержит глицерин,
картофельный крахмал, аминокислоты, яичный желток, малахитовый
зеленый для задержки роста сопутствующей микрофлоры)
Растут медленно (2-3 недели)
Колонии кремового цвета, сухие, морщинистые, трудно снимаются с агара
(см. рис.3)
Патогенность связана с химическим составом клетки
Корд-фактор препятствует фагоцитозу, нарушает функцию митохондрий, тормозит
миграцию лимфоцитов, способствует формированию «жгутов» и «кос»
Жирные кислоты, воск Д и пр. компоненты обладают токсическими свойствами
В антигенном отношении однороден
Носители антигенных свойств: липиды (выполняют функцию адъювантов),
полисахариды, корд-фактор
Основной носитель антигенных свойств: белок – туберкулин; вызывает в
организме иммунный ответ (гиперчувствительность замедленного типа - ГЗТ);
используется в качестве диагностического препарата (туберкулиновая проба
Манту)
Туберкулёз
Микроскопический – микроскопия мокроты, окрашенной по Цилю-Нильсену (см.
рис.2); люминисцентная микроскопия.
2. Бактериологический – посев мокроты на элективные среды (Левенштейна-
Йенсена) с последующей идентификаций выделенных микобактерий. Особенности
бактериологического метода при диагностики туберкулеза: длительность
исследования; предварительная обработка мокроты серной кислотой с целью
подавления сопутствующей микрофлоры; определение чувствительности к
химиотерапевтическим препаратам и антибиотикам только методом серийных
разведений;
3. Биологический – заражение морских свинок материалом от больного; через 5-10
суток развивается лимфаденит, через 3-4 недели – положительная туберкулиновая
проба; через 1-2 месяца – генерализованный процесс приводит к гибели животного
4. Иммунологический – выявление антигенов микобактерий из патологического
материала: иммунофлюоресценция (ИФ), иммуноферментный анализ (ИФА).
5. Аллергический – выявление ГЗТ с целью отбора контингента на ревакцинацию; с
целью выявления заболевших и инфицированных. Суть метода: введенный
внутрикожно очищенный туберкулин вызывает ГЗТ; размер папулы и гиперемии
зависит от выраженности защитных реакций, что позволяет судить о выраженности
противотуберкулезного иммунитета и возможного заболевания (см. рис.4)
6. Генетический – полимеразная цепная реакция (ПЦР)
ИММУНИТЕТ ПРИ ТУБЕРКУЛЕЗЕ
• Клеточный - гиперчувствительность замедленного типа (ГЗТ)
• Нестерильный
• Основа иммунной защиты - незавершенный фагоцитоз
• Антитела - «свидетели» инфекционного процесса
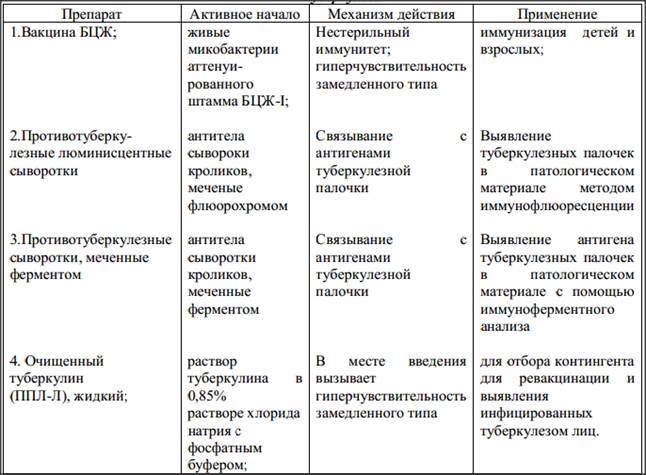
Плановая массовая иммунизация живой вакциной БЦЖ на 5-й день с момента рождения; механизм заключается в формировании нестерильного иммунитета
Ревакцинация – 7 – 12 – 17 – 22 и 27-30 лет (лица, отрицательно реагирующие на
пробу Манту)
3. Микобактерии лепры, биологические свойства, факторы патогенности, лабораторная диагностика.
Микобактерии лепры
M. leprae
Род Mycobacterium
Гр+ палочки, образуют плотные шаровидные скопления (лепрозные шары). Кислотоустойчивы
На искусственных не культивируются
Те же, что и у других микобактерий.
Термостабильный полисахаридный и термолабильный белковый, который высокоспецифичен для микобактерий лепры.
Бактериоскопический с окраской по Цилю-нильсону. Бактериологический
Профилактики нет. Лечение проводят в лепрозориях. Применяют антибиотики.
4. Трепонема сифилиса, классификация, характеристика биологических свойств, факторы патогенности, патогенез сифилиса, иммунитет, лабораторная диагностика.
Трепонема сифилиса
- сем. Spirochaetaceae
род Treponema
вид: Tr. pallidum («бледная трепанема»)
Морфология: протоплазматический цилиндр, 6-20 мкм, покрыт ЦПМ и тонкой клеточной
стенкой (пептидогликан, полисахариды, липиды), 8-12 завитков, в цитоплазме – 1 или
несколько фибрилл, прикрепленных к полярным дискам (см.рис11,12,13)
• Подвижен: вращательные, маятникообразные, поступательные, волновые движения
• Плохо фиксирует красители (используется окраска по Романовскому)
• Анаэроб
В организме образует цисты и L-формы
Плохо культивируется на искусственных питательных средах
• Для культивирования используют кроликов (заражение в яичко)
•
Выраженная антифагоцитарная активность
• ЛПС - оказывает повреждающее действие на ткани
• Способность образовывать цисты и L-формы в пораженных тканях (что способствует
«уходу»от защитных механизмов организма)
Белковые антигены – высокая иммуногенность, быстрая индукция антител
• Полисахаридные антигены – низкая иммуногенность
• Липидные антигены – сходны с компонентами мембран клеток организма человека (данное
явление используется в реакции Вассермана – постановка реакции с двумя антигенами:
кардиолипидным (неспецифическим) и собственно антигеном трепанемы)
Микроскопический метод: микроскопия отделяемого язвы или элементов сыпи
• Световая микроскопия (окраска по Романовскому)
• Темнопольная
• Фазово-контрастная
• Серебрение (по Морозову)
2. Бактериологический метод: не применяется из-за трудностей культивирования возбудителя
на искусственных питательных средах
3. Серологический метод:
• Реакция Вассермана (РСК) с двумя антигенами (кардиолипидным и
трепонемным);
• РНГА
• ИФА, ИФ (обнаружениеIgMи IgG)
• Осадочные пробы (экспресс-диагностика) на стекле – концентрированный
кардиолипидный антиген+сыворотка больного; при положительной реакции
(образование осадка) проводится полное исследование сыворотки (РСК,РНГА, ИФА и
тд.)
ИММУНИТЕТ ПРИ СИФИЛИСЕ
• Нестерильный
• Формы иммунитета: клеточный (ГЗТ) и гуморальный
• Основной защитный механизм – фагоцитоз
• Антитела появляются через 3-4 недели после заражения
ИММУНОПРОФЛАКТИКА СИФИЛИСА НЕ РАЗРАБОТАНА
5. Гонококки, их классификация, общая характеристика. Факторы патогенности, патогенез. Лабораторная диагностика острой и хронической гонореи, методы провокации. Бленорея новорожденных. Специфическая терапия и меры профилактики.
Гонококки
сем. Neisseriaceae
род Neisseria
вид: N. gonorrhoeae
Грамотрицательные диплококки
Микроаэрофилы – требуют 5 – 10% углекислого газа при культивировании
• Требовательны к питательным средам: в состав должны входить сыворотка или кровь
• На плотных средах дают мелкие прозрачные блестящие колонии
Пили – адгезия (к эпителию матки, маточных труб, кишечника, слизистой полости рта,
конъюнктиве)
• Капсула – антифагоцитарные и иммуногенные свойства
• Каталаза – антифагоцитарные свойства фагоцитоз при гонорее незавершенный (гонорея -
«болезнь фагоцитов»)
• Эндотоксин
Микроскопический метод: при острой гонорее - обнаруживаются гонококки внутри
фагоцитов!(см. рис.8)
при хронической гонорее – отсутствует данный признак!
• Бактериологический метод: наиболее достоверный, так как часто встречаются хронические
и латентные формы течения.
Для провокации (обострения)процесса с целью диагностики и лечения используется
гоновакцина (взвесь убитых гонококков)
• Иммунофлюоресценция: выявление гонококков в патологическом материале
• Генетический метод: ПЦР
Иммунные реакции не защищают от повторного заражения и от суперинфекции.
6. Хламидии, классификация. Характеристика биологических свойств, факторы патогенности, виды хламидий, формы существования и жизненный цикл. Заболевания, вызываемые хламидиями. Лабораторная диагностика.
Хламидии сем. Chlamidiaceae
род Chlamidia
виды: Ch. Psittaci
Ch. Trachomatis
Ch. pneumoniae
1. Мелкие кокковидные бактерии, по строению оболочки напоминают грамотрицательные
бактерии (см. рис.1)
2. Облигатные внутриклеточные паразиты: хламидии не способны синтезировать
высокоэнергетические соединения («энергетические паразиты»).
3. Способны к образованию L-форм
Культивирование на клеточных культурах (McCoy, L-929, куриные эмбрионы), так как
хламидии не могут расти на искусственных питательных средах
Аг клеточной поверхности, подавляющие защитные реакции организма
2. Эндотокины – ЛПС
3. Экзотоксины ( в эксперименте в/в введение вызывает гибель мышей)
4. Поверхностные белки, способствующие адгезии
1. Поверхностный родоспецифический антиген (ЛПС)
2. Главный белок наружной мембраны – проявляет свойства поринов, включает родо-, видо-,
типо- и сероварспецифические детерминаты
3. Ch. trachomatis по антигенным свойствам делиться на 15 сероваров
Трахома (хронический хламидийный конъюнктивит
Хламидийная пневмония:
источник – человек
Орнитоз (пситтакоз) Cl.psittaci:
Культивирование на клеточных культурах (McCoy, L-929, куриные эмбрионы), так как
хламидии не могут расти на искусственных питательных средах
• Определение телец включений в окрашенных мазках (низкая чувствительность)
• Выявление Аг хламидий (иммунофлюоресценция (ИФ), иммунная хроматография (ИХГ),
иммуноферментный анализ (ИФА)
• ПЦР
• Серологический метод – выявление Ig M (мало информативен, так как хламидийная инфекция
протекает, преимущественно хронически)
Иммунитет гуморальный и клеточный
• Высокие титры антител выявляются при острых формах хламидийной инфекции: пневмониях
• Иммунные механизмы не защищают от повторного заражения и от суперинфекции
Иммунопрофилактика и иммунотерапия не разработаны
7. Микоплазмы, классификация, характеристика биологических свойств, факторы патогенности, патогенные для человека виды. Заболевания, вызываемые микоплазмами. Методы микробиологической диагностики.
Семейство – Mycoplasmataceae
род I Mycoplasma
5 видов, патогенных для человека:
M. pneumoniae,
M. hominis,
M. genitalium,
M. incognitus,
M. fermentas
Факультативные анаэробы
• Полиморфны (кокковидные, ветвящиеся, крупные многоядерные формы, псевдомицелий)-
обусловлено отсутствием ригидной клеточной стенки (пептидогликана) (см. рис.4)
• Размножение бинарным делением
• Способны к почкованию и сегментации
• Размер – 0.2 – 0.7 мкм
• Основной элемент клеточной мембраны –холестерин (утилизируют из тканей и питательных
сред)
Требовательны к питательным средам - в состав сред обязательно входят: нативная
сыворотка, холестерин, аминокислоты, углеводы, витамины, соли (триптический перевар
сердца крупного рогатого скота); для уреаплазмы – добавление мочевины
• Возможно выделение на куриных эмбрионах
• На средах содержащих кровь, некоторые виды дают α- и β-гемолиз
• На твердых средах микоплазмы образуют характерные мелкие колонии (0.2-1, 5 мм) типа
«яичницы глазуньи», появляющиеся на 5-7 сутки, уреаплазмы – могут не иметь характерной
картины «яичницы глазуньи» (см. рис.5,6)
• На жидких средах дают очень незначительное помутнение или опалесценцию
Адгезины – входят в состав поверхностных антигенов
• Экзотоксины – нейротоксин (мишень действия – астроциты)
• Эндотоксины – вызывают пирогенный эффект, лейкопению, тромбогеморрагические
поражения, коллапс и отёк легких (не тождественен эндотоксину грамотрицательных
бактерий)
• Гемолизин (некоторые виды)
• Ферменты агрессии:
фосфолипаза А, аминопептидазы – гидролизируют фосфолипиды клеточной стенки;
нейраминидаза – нарушение архитиктоники клеточных мембран и межклеточные
взаимодействия;
протеазы и эндопептидазы – дегрануляция клеток, расщепление АТ;
РНКазы, ДНКазы
Основные антигены представлены липидами, полисахаридами и белками
• Изменчива
• Антигенная мимикрия (вызывает выработку аутоантител)
I.микоплазменной инфекции:
а) Поражение МПС:
• уретриты
• простатиты
• цервициты
• воспалительные поражения тазовых органов • невынашивание беременности
• преждевременные роды
• внутриутробное заражение плода
б) Пневмонии
в) Поражения суставов
г) Поражения центральной и периферической нервной системы
II. уреаплазменной инфекции
Поражение МПС
Бактериологический метод – сроки появления колоний 5 - 7 суток. с последующей
идентификацией по биохимическим свойствам
2. Иммунофлюоресценция(выявление возбудителя в патологическом материале,
идентификация при росте на питательных средах) и ИФА (выявление возбудителя в
патологическом материале; обнаружение IgM и IgG)
3. Серологический метод :РСК (парные сыворотки)
4. Генетический метод: гибридизация ДНК, ПЦР
8. Внутрибольничные и госпитальные инфекции. Причины и условия возникновения госпитальных инфекций. Этиология и патогенез. Характеристика госпитальных штаммов. Эпидемиология. Методы диагностики, методы эпидемиологического анализа госпитальных инфекций.
Внутрибольничные инфекции: Любое, клинически распознаваемое инфекционное заболевание, поражающее больного в результате госпитализации или посещения лечебного учреждения с целью лечения, а также персонал, независимо от того, проявлялось ли оно при нахождении в стационаре.
Практическое значение внутрибольничных инфекций:
1. Удлинение сроков лечения
2. Увеличение доли инвалидизации
3. Рост смертности
4. Экономический ущерб: оплата больничных листов, оплата инвалидности, оплата лечебных процедур и лекарственных средств и пр.
Причины и условия возникновения ВБИ:
1. Нарушение правил асептики или недостаточность асептических мероприятий:
а) неграмотность, небрежность, нехватка медицинского персонала;
б) старые помещения, старое оборудование
в) неадекватные методы стерилизации сложного медицинского оборудования
г) вентиляция
2. Высокая вероятность контакта больных и персонала: скученность пациентов, нехватка
персонала
3. Массовая госпитализация: до 25% населения госпитализируется 1 раз в год
4. Инвазивные методы обследования и лечения: создание искусственных «входных ворот»;
до 30% манипуляций не обоснована
5. Снижение резистентности организма пациентов
6.Циркуляция госпитальных штаммов: высоковирулентных и полирезистентных
Условия селекции:
а) снижение резистентности организма
б) нерациональная антибиотикотерапия; использование антисептиков, дезинфектантов
Основа селекции:
а) гетерогенность микробной популяции
б) R-плазмиды
Источники ВБИ
1. Больные
2. Медицинский персонал
3. Внешняя среда стационара (лечебно-диагностического учреждения)
4. Посетители
Механизмы и пути распространения ВБИ
1. Аэрогенный: воздушно-капельный, воздушно-пылевой
2. Фекально-оральный: водный, пищевой, контактно-бытовой
3. Контактный: непосредственный контакт
4. Артифициальный (искусственный) – в основе его лежит преодоление микроорганизмами
естественных защитных барьеров:
• Контактно-инструментальный
• Инъекционный, инфузионный
• Трансфузионный
• Имплантационный
• Посткатетеризационный
• Ингаляционный
Этиология ВБИ:
Все известные инфекционные агенты: бактерии, вирусы
*** респираторные (грипп, ветрянка и пр.)
*** кишечные (особенно у детей младшего возраста)
Условно-патогенные микроорганизмы: представители нормальной микрофлоры
Госпитальные инфекции: Входят в структуру ВБИ
Этиология: условно-патогенные микроорганизмы – высоковирулентные и полирезистентные
(энтеробактерии, НГОБы, стафило- и стрептококки, дифтероиды и облигатные анаэробы)
Эпидемиология: чаще всего механизм распространения – артифициальный
Клинические проявления госпитальных инфекций
• гнойно-септические (гнойно-воспалительные) процессы (85%)
• диареи, особенно в детских стационарах
• пневмонии • мочевая инфекция
• сепсис
Принципы диагностики госпитальных инфекций:
I. Факт госпитальной инфекции: наличие не менее 3 пациентов в очаге
II. Выделение и идентификация возбудителя
III. Выявление источников инфекции:
1) обследование персонала; обследование объектов среды стационара, инструментов
2) фаготипирование, бактерцинотипирование
IV. Выявление маркеров госпитализма: резистентности к антибиотикам (выявление бета-
лактамаз); плазмидный профиль, ДНК- гомология
Принципы профилактики госпитальных инфекций
• Рациональная антибиотикотерапия
• Мониторинг резистентной микрофлоры в лечебном учреждении
• Целесообразность инвазивных манипуляций
• Строгое соблюдение правил асептики
• Санация носителей (сотрудников и пациентов перед операцией)
• Вакцинация пациентов перед плановыми операциями
9. Внутриутробные инфекции, их этиология. Источники и пути инфицирования плода. Поражения плода на разных стадиях его внутриутробного развития (гаметопатия, фетопатия ранняя и поздняя). Методы диагностики. Меры профилактики внутриутробных инфекций.
· Внутриутробные инфекции (ВУИ) — это различные инфекционные заболевания эмбриона, плода и новорождённого, заражение которыми происходит внутриутробно и в процессе родов Группа ВУИ, вызываемая вирусами: краснуха, ЦМВ, герпесвирусы, вирусный гепатит и др.
· Заболевания, вызываемые бактериями: сифилис, листериоз, туберкулёз, ЗППП
· Паразитарные инфекции: токсоплазмоз
· Грибковые инфекции, в том числе ятрогенного генеза
· Микст-инфекции (сочетанные).
Источником инфекции является мать. Но так же есть и ятрогенные причины инфицирования во время медицинских манипуляций.
· Трансплацентарный (гематогенный) путь — от матери к плоду через плаценту. Чаще передаются вирусные ВУИ, так как вирус легко проникает через гемато-плацентарный барьер (как и токсоплазма).
· Восходящий — когда инфекция из половых путей попадает в полость матки и затем может инфицировать плод. Чаще это бактериальные инфекции, ЗППП, хламидиоз, грибы, микоплазмы, энтерококки.
· Нисходящий путь — из маточных труб в полость матки
· Контактный (интранатальный) путь — заражение во время прохождения через родовые пути.
Гаметопатии — поражение гамет родителей
Различают ранние фетопатии (возникают в раннем фетальном периоде эмбриогенеза — до 28-недельного срока беременности) и поздние фетопатии (после 28 недель беременности и до начала родов).
Прямые методы
Прямые методы исследования направлены на выявление возбудителя или его антигена в организме больного ребёнка.
· Микроскопический (бактериоскопический) метод.
· Культуральный метод (посев биологических жидкостей и выделений больного на специальные среды) наиболее точен, но его редко используют из-за дороговизны и длительности исследования (от 3 до 20 дней).
· Молекулярно-биологический метод. Наибольшее распространение получила полимеразная цепная реакция (ПЦР), позволяющая обнаружить минимальное количество ДНК возбудителя. Результаты оценивают в сопоставлении с данными других лабораторных методов и клиническими проявлениями. Для решения вопроса об активности процесса и эффективности лечения используют сочетание ПЦР и серологического метода, а также параллельно исследуют сыворотку крови ребёнка и матери в динамике (нарастание титра антител при методе парных сывороток).
· С помощью иммуноферментного анализа (ИФА) и реакции иммунофлюоресценции (РИФ) выявляют специфические антигены.
Диагностический признак
• Факультативные анаэробы, предпочитают аэробные условия
1. Адгезия:
тейхоевые кислоты, капсульный полисахарид, белок А
2. Ферменты:
· плазмокоагулаза –
· лецитиназа фибринолизин
· ДНК-аза
· гиалуронидаза
· каталаза
· липазы
· бета-лактамазы –(устойчивость к
антибиотикам)
Факторы агрессии: белок А- антифагоцитарное
действие (связывает Ig по Fc-фрагменту); каталаза- антифагоцитарное действие
(инактивация перекисных соединений фагоцитов); антилизоцимная (ALA) и
антибактерицидная (Анти-БАС) активность
Альфа-токсин (мембранотоксин) – гемолитическое, кардиотропное, нейротропное,
дермонекротическое действие;
Эксфолиативный токсин (мембранотоксин) – разрушает соединительнотканные клетки
(пузырчатка новорожденных, импетиго и пр., синдром ошпаренной кожи)
Токсин синдрома токсического шока (ТСТШ) - активация продукции цитокинов
моноцитами и макрофагами (функции суперантигена)
Энтеротоксины (A,B,C,D,E,F)
Антигенные свойства проявляют:
• Пептидогликан, тейхоевые кислоты, микрокапсула, белок А
• Экзотоксины и некоторые ферменты
Стафилококковые инфекции являются токсикоинфекциями (кроме поражений ЖКТ) – в
развитии клинических проявлений имеет значение как размножение возбудителя и
действие на окружающие ткани его факторов патогенности, так и циркулирующие в
кровотоке его экзотоксины
Иммунитет при стафилококковых инфекциях:
1. Направленность: антибактериальный и антитоксический
2. Выраженность и продолжительность: нестойкий, ненапряженный
3. Ведущая роль принадлежит IgA (защита входных ворот)
Источник инфекции:
1. Больные
2. Реконвалесценты
3. Здоровые бактерионосители (постоянные(резидентные) и транзиторные)
Пути и механизмы заражения:
1. Аэрогенный (преимущественно воздушно-капельный)
2. Контактный (бытовой, контактно-интсрументальный в лечебных учреждениях)
3. Алиментарный
Бактериологический метод:
• Патологический материал зависит от клинических проявлений и исследуется с
учетом количества возбудителя
• Элективная среда – солевой агар (6-10% хлорида натрия)
• Основные видовые дифференцирующие признаки:
1. Гемолитическая активность
2. Плазмокоагулирующая активность
3. Лецитиназная активность
• При определении источника инфекции – фаготипирование (чувствительность к
типовым стафилококковым бактериофагам)
Вакцины (для терапии больных с хроническими стафилококковыми инфекциями и
предоперационной вакцинации групп риска)
• Химическая стафилококковая («антифагин»): компоненты оболочки золотистого
стафилококка, включая белок А
• Убитая стафилококковая (корпускулярная): смесь клинически значимых
штаммов золотистого стафилококка
• Вакцина ВП-4: содержит экстрагированные антигены золотистого стафилококка,
протея, клебсиеллы пневмонии, кишечной палочки адсорбированные на
гидроокиси аллюминия
• Комплексная стафило-протейно-синегнойная: анатоксины золотистого
стафилококка и синегнойной палочки + экстрагированные антигены золотистого
стафилококка и протея
Анатоксины (для иммунизации доноров, для предоперационной вакцинации групп риска) • Стафилококковый адсорбированный (альфа-токсин)
Иммуноглобулины (для лечения больных)
• Стафилококковый иммуноглобулин (донорский)
Бактериофаги (для лечения очаговых стафилококковых инфекций)
9. Проблема госпитальной стафилококковой инфекции в педиатрии. Значение носительства стафилококков у работников в детских учреждениях. Принципы санации носителей. Методы эпидемиологического анализа госпитальных стафилококковых инфекций.
