Бронхиальная астма. Пинципы базисной терапии.
Программа лечения больных бронхиальной астмой:
1. Обучение больных, в результате которого они должны стать соратниками врачей
2. Оценка и мониторинг тяжести бронхиальной астмы с помощью объективных показателей, отражающих легочную функцию
3. Избегание контакта или контролирование влияния факторов, являющихся пусковыми механизмами развития приступов бронхиальной астмы
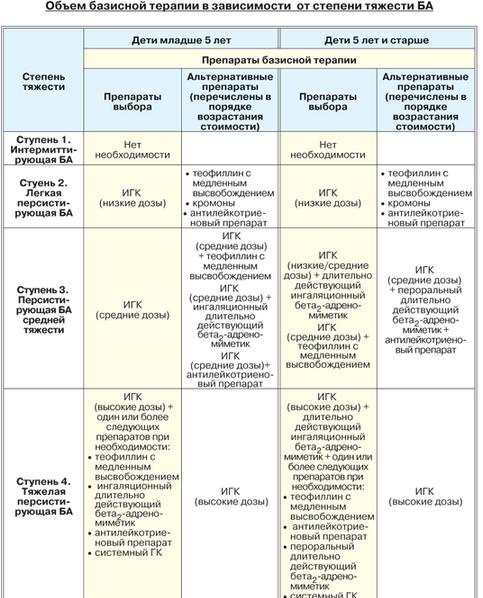
4. Разработка плана медикаментозной терапии для постоянного лечения
5. Разработка плана мероприятий в период обострения
6. Обеспечение регулярного наблюдения за больным.
Задачи успешного лечения заключаются в:
1. достижении и установлении контроля над симптомами;
2. предотвращении обострений астмы;
3. поддержании функции легких максимально близко к нормальному уровню;
4. поддержании нормального уровня физической активности, включая занятия спортом;
5. избежании побочных эффектов от препаратов, применяемых для лечения астмы;
6. предотвращении развития необратимой обструкции;
7. предотвращении смерти от астмы.
Приведенные задачи терапии отражают новое понимание астмы как заболевания и принципов ее лечения. С учетом того, что астма - это хроническое воспалительное заболевание, было показано, что любую астму, кроме легкой интермиттирующей, можно более эффективно контролировать лечением, направленным на подавление и обратимость воспаления, чем лечение только острого бронхоспазма и связанных с ним симптомов.
Противоастматические препараты сегодня разделяют на две группы:
1. Средства, обеспечивающие длительный контроль астмы (то есть профилактические),
2. Средства, использующиеся для купирования приступов (то есть симптоматические).
К препаратам первой группы относят противовоспалительные средства (ингаляционные и системные кортикостероиды, кромогликат натрия и недокромил), длительно действующие бронходилататоры (b-адреномиметики и теофиллины) и антагонисты лейкотриенов,
К препаратам второй группы - коротко действующие b-адреномиметики, антихолинергические средства (ипратропиума бромид).
Первые могут предотвратить развитие воспаления в бронхах, они также оказывают профилактическое и супрессивное действие. Противовоспалительные препараты и, в частности, ингаляционные кортикостероиды в настоящее время являются наиболее эффективными препаратами, контролирующими течение заболевания.
Препараты, использующиеся для неотложной помощи, быстро купируют бронхоспазм и сопутствующие ему симптомы. Однако они не устраняют воспаления и гиперреактивности бронхов.
Рассмотрим препараты, применяемые для контроля над бронхиальной астмой.
Профилактические средства необходимо принимать ежедневно в течение длительного времени с целью стойкого контроля над астмой. Постоянным морфологическим признаком этого заболевания является эозинофильное воспаление слизистой оболочки дыхательных путей, поэтому наиболее эффективными считают средства, уменьшающие воспалительную реакцию и гиперреактивность бронхов.
Сегодня известно, что многие противоастматические препараты (в том числе b-адреномиметики и теофиллины) обладают определенной противовоспалительной активностью, однако наиболее выраженный противовоспалительный эффект дают ингаляционные кортикостероиды, которые сегодня считают основой лечения среднетяжелой и тяжелой астмы.
Негормональные противовоспалительные препараты
Кромогликат натрия и недокромил натрия подавляют выброс медиаторов тучными клетками и хемотаксис эозинофилов. Оба препарата обладают сопоставимой противовоспалительной активностью, однако по эффективности уступают ингаляционным кортикостероидам, поэтому их обычно применяют для лечения астмы легкого течения.
Имеются сведения о том, что применение недокромила позволяет несколько снизить потребность в ингаляционных кортикостероидах. Преимуществом недокромила является возможность применения два, а не четыре раза в день. Важным достоинством обоих препаратов является безопасность.
Рекомендуемые дозы ингаляционных негормональных противовоспалительных препаратов, применяемых для лечения бронхиальной астмы (дозы, используемые у взрослых):
Кромогликат натрия - низкая доза: 6 мг/сутки в 3 приема, средняя доза: 9-12 мг/сутки в 3 приема, высокая доза: 16 мг/сутки в 3 приема,
Недокромил натрия - низкая доза: 8-12 мг/сутки в 2-3 приема, средняя доза: 18-24 мг/сутки в 2-3 приема, высокая доза: 16 мг/сутки в 4 приема.
Примечание: Наиболее важный критерий определения подходящей дозы - суждение врача об ответе на проводимую терапию.
По материалам Expert Panel Report 2: Guidelines for the Diagnosis and Management of Asthma. National Institutes of Health pub no 97-4051. Bethesda, MD, 1997.
Дополнительная информация:
1. Необходимо провести 4-6-недельный курс лечения кромогликатом натрия, чтобы подтвердить его эффективность у данного больного.
2. Перед применением кромогликата натрия в капсулах, особенно в период обострения, рекомендуется вдохнуть бронхорасширяющий препарат, чтобы лекарство лучше проникало в глубь бронхиального дерева.
3. При сопутствующей терапии гормонами добавление кромогликата натрия может позволить уменьшить их поддерживающую дозу. Темп снижения дозы ингаляционных кортикостероидов не должен превышать 10% в неделю. Увеличение дозы гормонов может потребоваться при усилении симптомов заболевания, сопутствующей инфекции, антигенном воздействии, стрессе.
Антагонисты лейкотриенов
Являются относительно новыми профилактическими противоастматическими средствами.
Лейкотриены - биохимические медиаторы, которые высвобождаются тучными клетками, эозинофилами и базофилами и вызывают сокращение гладких мышц бронхов, повышают проницаемость сосудов и секрецию слизи и активируют воспалительные клетки в дыхательных путях.
К препаратам этой группы относятся антагонисты лейкотриеновых рецепторов (зафирлукаст - Аколат, монтелукаст - Сингуляр) и ингибиторы 5-липоксигеназы (зилеутон).
Имеющиеся данные свидетельствуют о том, что антагонисты лейкотриенов улучшают функцию легких, уменьшают симптомы астмы и потребность в ингаляционных b2-адреномиметиках. Большинство исследований антагонистов лейкотриенов проводились у больных астмой легкого или среднетяжелого течения, а достигнутый эффект был умеренным. Антагонисты лейкотриенов можно считать альтернативой ингаляционным кортикостероидам в низких дозах у больных астмой легкой тяжести, хотя необходимы дальнейшие исследования с целью установления их роли в лечении астмы.
Ингаляционные глюкокортикостероиды
Глюкортикостероиды (ГК) в настоящее время являются наиболее эффективными противовоспалительными препаратами для лечения астмы. Широкий спектр воздействия препаратов этой группы на процессы воспаления определяет эффективность кортикостероидов, как средств превентивной терапии.
Клинические эффекты кортикостероидов включают в себя снижение активности симптомов, улучшение пиковой скорости выдоха и показателей спирометрии, уменьшение бронхиальной гиперреактивности, предотвращение обострений и, возможно, предотвращение ремоделирования бронхиальной стенки.
Первый ингаляционный ГК был синтезирован в начале 70-х годов. Это был беклометазона дипропионат. Синтезировали его одновременно две фирмы "Glaxo" (Великобритания) и "Shering-Plough" (США). Однако зарегистрировала его раньше "Glaxo" под названием бекотид, поэтому эта фирма и считается создателем ингаляционных ГК. С тех пор было создано много ингаляционных ГК.
В настоящее время наибольшее применение в клинике имеют следующие препараты ингаляционных кортикостероидов:
беклометазона дипропионат,
флунисолид,
флютиказона пропионат,
будесонид,
триамцинолона ацетонид.
Для того чтобы оказать действие, ГК должен проникнуть внутрь клетки, для этого он должен быть липофильным. Чем больше коэффициент липофильности, тем лучше он проникает в клетки. Затем он должен связаться с ГК-рецепторами, для чего препарат должен обладать большой селективностью.
Таким образом, к ингаляционным ГК в настоящее время предъявляют следующие требования:
липофильность,
селективность,
аффинность (сродство к рецепторам),
низкая биодоступность,
разрушение в печени всосавшейся части препарата при первом прохождении.
Ингаляционные кортикостероиды отличаются друг от друга по активности и фармакокинетическим свойствам.
По данным экспериментальных исследований, наиболее высокой активностью обладает флютиказона пропионат (Фликсотид), за ним следуют будесонид (Пульмикорт), беклометазона дипропионат (Альдецин, Бекотид, Бекломет) и флунисолид (Ингакорт). Флютиказона пропионат обладает также максимальным сродством к рецепторам.
Вероятность системных эффектов ингаляционных кортикостероидов определяется их активностью и биодоступностью: при применении дозированных аэрозолей без спейсера около 80% дозы проглатывается и поступает в желудочно-кишечный тракт. Благодаря активной биотрансформации в печени (эффект первого прохождения) ингаляционные кортикостероиды обладают очень низкой биодоступностью (беклометазона дипропионат - 20%, флунисолид - 21%, будесонид - 11%, флютиказона пропионат - 1%), что снижает риск системных нежелательных эффектов.
Ограничение применения ингаляционных ГК: структурные изменения легочной ткани, грибковые инфекции легких, туберкулез, иммунодефицит.
Использование кортикостероидов в любой форме всегда вызывает опасение возможности развития системных эффектов.