I. Нарушение инициирования глотательного рефлекса
Таблица 1. Причины развития нейрогенной дисфагии.
I. Нарушение инициирования глотательного рефлекса
- Повреждение центра глотания
- Парез/паралич языка
- Повреждение чувствительных волокон IX и X нервов
- Ротоглоточная анестезия
- Понижение слюноотделения
II. Дисфункция мышц глотки, верхнего отдела пищевода, надподъязычных мышц
1. Мышечная слабость
- Бульбарный паралич (инсульты, полинейропатии, амиотрофический боковой склероз)
- Нервно-мышечное поражение (миастения)
- Повреждение мышц (полимиозит, дерматомиозит, миопатии)
2. Одновременное начало сокращений/нарушение глотательного угнетения
- Поражение экстрапирамидных путей
- Ппсевдобульбарный паралич
III. Дисфункция гладких мышц пищевода
1. Паралич тела пищевода
- Склеродермия и родственные коллагенозы
- Метаболическая нейромиопатия (амилоид, алкоголь, диабет)
2. Одновременное начало сокращений и нарушение глотательного угнетения
в теле пищевода и/или нижнем пищеводном сфинктере
- Диффузный спазм пищевода
- Ахалазия
В организме человека существуют резервные возможности для обеспечения глотания, которые позволяют одной структуре компенсировать недостаточность прилегающей. Например, мягкое нёбо перекручивается вниз, чтобы сблизиться с паретичным или атрофированным языком и препятствовать преждевременному просачиванию болюса в глотку, или при слабости мягкого нёба возможно компенсаторное утолщение валика Пассавана [Bucholzetal., 1985]. При прогрессировании нейромышечных нарушений или под воздействием алкоголя или медикаментов (антидепрессанты, седативные препараты) происходит декомпенсация, и возникают очевидные симптомы дисфагии [Jones & Donner, 1988].
Нейрогенная дисфагия может проявляться самыми разными дефектами, но у большинства больных обнаруживается сочетание нескольких проблем, обусловливающих трудности проглатывания [И.А. Авдюнина с соавт., 2000; Veis & Logemann, 1985]. Компоновка симптоматики нарушенного глотания индивидуальна у каждого больного и может включать: слабость оральной мускулатуры с изменением стереотипа еды; оральную апраксию; ограничение движений языка; невозможность склеивания и формирования пищевого болюса; гипосаливацию или слюнотечение; снижение чувствительности рецепторов глотки и отсроченный запуск глотательного рефлекса; задержку пищи в ротовой полости и/или глотке; регургитацию в нос; дисфонию; попёрхивание; стридор; снижение кашлевого рефлекса (Veis & Logemann, 1985; Buchholz, 1987; Horner, Massey, & Brazer, 1988; Bakheit, 2001]. Здесь, наверное, следует отметить, что постоянное сплёвывание слюны, например, после стволового инсульта, которое часто расценивают как гиперсаливацию, обычно вызвано не избыточным количеством секретов, а невозможностью их проглотить. У больных паркинсонизмом слюнотечение также не является следствием избыточной саливации, а обусловлено брадикинезией орофарингеальной мускулатуры [Bakheit, 2001]. А вот регургитация желудочно-кишечных секретов может вызвать гиперсаливацию, известную как «водяная отрыжка» [Schulze-Delrieu & Miller, 1997].
На сегодняшний момент неизвестны дефекты акта глотания, патогномоничные конкретно для какого-то неврологического заболевания. Тяжесть лежащей в основе дисфагии болезни, её особенности и преморбидные характеристики глотания у каждого данного больного весьма вариабельны. Нет также существенной зависимости выраженности дисфагии от характера патологического процесса в нервной системе. Некоторые больные испытывают лёгкий дискомфорт, тогда как другие полностью лишены возможности глотать, и у них развиваются серьёзные осложнения. В Таблице 2 представлены осложнения, свойственные дисфагии.
Таблица 2. Осложнения дисфагии
Аспирация, трахеобронхит, пневмония, ателектаз и/или эмпиема
Нарушения дыхания, длительная искусственная вентиляция легких
Истощение и дегидратация
Носовая регургитация, синуситы
Полиорганная патология
Длительное пребывание в ОРИТ
Увеличение затрат на лекарственные препараты и расходные материалы
Ухудшение качества жизни
Депрессия
Летальный исход
Подробнее остановимся на нескольких осложнениях, требующих особого внимания. Аспирация (лат. aspiratio дуновение, дыхание) – проникновение инородных тел в дыхательные пути в результате их засасывания потоком вдыхаемого воздуха [ЭСМТ, 1982] ниже уровня истинных голосовых связок [Perlman & Schulze-Delrieu, 1997]. Некоторые авторы выделяют проход орофарингеального содержимого через гортань дистальнее истинных голосовых складок (в некоторых случаях несвязанный с дыханием) и пассаж материала внутрь лёгких (часто сопутствующее вдоху): пенетрацию и аспирацию, соответственно [Groher & Gonzalez, 1992; Kramer, 1989], тогда как другие или уравнивают термины, или используют во всех обстоятельствах термин «аспирация» [Feinbergetal., 1990]. Perlman & Schulze-Delrieu [1997] называют пенетрацией вступление орофарингеального содержимого в гортань выше истинных голосовых складок.Аспирация считается тяжёлой, если больной аспирирует больше 30% проглоченного жидкого болюса, умеренной – при объёме 30-10%, лёгкой – при объёме менее 10%. Неврологические дефициты, разрушая нормальный респираторный паттерн, ведут к несогласованности дыхания и глотания, обрекая больных на аспирацию [Selleyetal., 1989]. Частота аспирации, например, при инсульте достигает 50% и более [Horner, Massey& Brazer, 1988; Veis & Logemann, 1995]. Клинически аспирация проявляется кашлем, одышкой, болью в груди, свистящим дыханием, лихорадкой, тошнотой или рвотой [П.Э. Парсонз и Д.Э Хеффнер, 2004]. Аспирация может возникать до, во время и/или после глотания. В Таблице 3 отображены причины аспирации в разные периоды глотания.
Таблица 3. Причины аспирации
До глотка:
Слабые движения языка
Нарушение нёбно-язычного затвора
Задержка инициации глотательного рефлекса
Во время глотка:
Ослабленное поднятие гортани
Ослабленное смыкание голосовых связок
Ослабленная перистальтика глотки
После глотка:
Неэффективное очищение глотки
Крикофарингеальная дисфункция
Рефлюкс или регургитация из желудка и/или пищевода
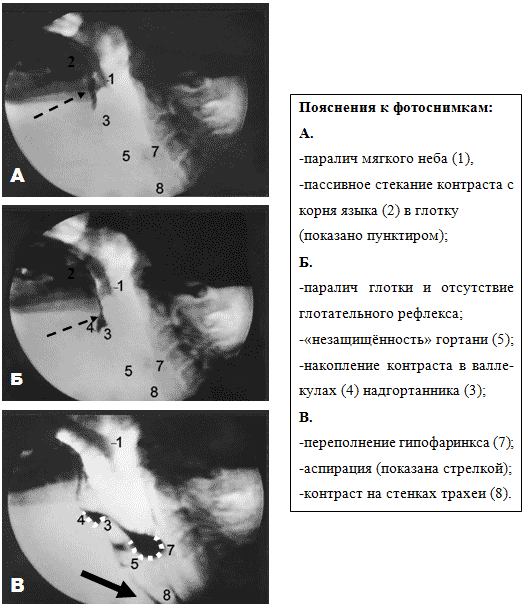
Фото 1. Кадры видеорентгеноскопии глотания жидкого болюса больной дифтерийной полинейропатией(совместное наблюдение с Н.В. Докучаевой)
До начала глотания аспирация возникает, если есть преждевременное просачивание пищи изо рта, когда гортань открыта и незащищена (Фото 1, А). Во время глотания аспирацию часто обусловливает нарушение защиты гортани. Дисфония, особенно, «влажно-хриплая» почти в 90% случаев свидетельствует об аспирации [Linden& Siebens, 1983]. После глотания, например, фарингеальный парез может привести к нарастающей задержке жидкости в грушевидных карманах с последующим переливом в преддверие гортани и аспирацией (Фото 1, В). Подход к оценке и управлению этими нарушениями должен быть основан на понимании лежащего в основе их повреждения. Терапия меняется, если врач знает, когда и почему больной аспирирует.
Компрометация ларингеального кашлевого рефлекса во многих случаях не только способствует аспирации, но и усугубляет её. Снижение кашлевого рефлексау неврологическихбольных играет важную роль в развитии осложнений, поскольку создаёт условия для неожиданной в 40% случаев [Splaingard, 1988] - «молчаливой» или «немой» (без кашля или удушья) аспирации [И.А. Авдюнина и Н.В. Докучаева, 1998; И.А. Авдюнина с соавт., 2000; Jones & Donner, 1988; Horner, Brazer & Massey, 1993; Holas, DePippo, Reding, 1994]. Кашлевой рефлекс, может пострадать из-за нарушения чувствительности и/или двигательного ответа на инвазивный материал, обусловленные самой болезнью (повреждение или адаптация центра). Местные чувствительные рецепторы становятся невосприимчивыми и в ответ на длительную ларингеальную стимуляцию, как при хронической аспирации или рефлюксе/регургитации желудочного содержимого. Кроме того, при повреждении мышц, обеспечивающих кашлевой рефлекс (диафрагмы и гортани), как происходит у больных с чисто двигательными расстройствами (при болезни мотонейрона или миопатии), кашель становится невозможным. Кашель фактически неэффективен при тетрапарезе. Эндотрахеальная интубация, трахеостомия, снижение уровня бодрствования, медикаменты (снотворные и местные анестетики) и множество других факторов могут повреждать ларингеальный кашлевой рефлекс [Bishop, Weymuller, & Fink, 1984; Horner & Massey, 1988; Horner, Massey, Riski et al., 1988; Alberts et al., 1992]. Рефлекторный кашель на пенетрацию в гортань орофарингеального болюса может быть сниженным у пожилых людей, способствуя тяжести обеденной аспирации [Feinberg, Knebl, Tully, & Segall, 1990]. Типичные для гериартрических больных мышечная слабость и неврологические расстройства создают дополнительные условия для аспирации в этой возрастной группе. Поэтому при постоянном старении нашей популяции, будет увеличиваться число лёгочных осложнений и смертей от дисфагии [Blitzer, 1990].
Выделяют несколько видов лёгочной патологии, которые могут возникнуть при нейрогенной дисфагии. Они зависят от свойств и объёма аспирированного материала, способности человека очищать воздушные пути. Объём аспирированной жидкости (50-300 мл) обеспечивает повреждение лёгких [Jamesetal., 1984]. Но даже маленькие твёрдые частицы (такие как, пилюли, фруктовые косточки) могут быть фатальными, если они застревают в голосовой щели и не могут быть удалены. При острой обструкции воздушных путей аспирированными твёрдыми веществами развивается острая дыхательная недостаточность, афония, цианоз, потеря сознания, и человек умирает от асфиксии в течение минут. Это известная причина смерти больных, за которыми ухаживают на дому, и людей, поспешно заглатывающих большие куски пищи («кофейный синдром») [Curtis & Langmore, 1997]. Аспирация желудочного содержимого приводит к химическому повреждению лёгочной ткани, так называемому «аспирационному пневмониту». При рН аспирата ≤ 2,5 и его объёме > 0,4 мл/кг - прогноз наихудший, но присутствие твёрдых частиц пищи, вызовет выраженную лёгочную дисфункцию и при рН > 5,0 [Парсонз и Хеффнер, 2004]. Большинство пневмоний при нейрогенной дисфагии (часто от анаэробных организмов) является результатом аспирации заражённого орального секрета или остатков органических веществ [Russin & Adler, 1989]. Поскольку даже здоровые люди могут аспирировать небольшие количества ротового секрета, по-видимому, имеет значение не слюна сама по себе, которая бактериостатична, а выраженная контаминация слюны бактериями [Gibbons & Houte, 1975] или колонизация дёсен анаэробными организмами. Для беззубых больных, например, нехарактерны классические анаэробные инфекции нижних дыхательных путей [Schachter, 1981]. В результате массивной аспирации анаэробных организмов в лёгких возможно образование долевого или сегментарного инфильтрата, а при снижении иммунной защиты - абсцесса или эмпиемы, долго протекающих вяло (невысокая температура; ночные поты; выраженная утомляемость и недомогание; потеря веса). Это созвездие симптомов подчас ошибочно трактуется как проявление злокачественного онкологического процесса. Пневмония обычно развивается в течение первых 24-48 часов после аспирации (первичная пневмония). Хотя она диагностируется только в 23-30% случаев, с ней связывают утяжеление состояния больного и рост летальности. У многих пациентов пневмония появляется только через 2-7 дней после аспирации (вторичная пневмония). В основе её лежит нарушение механизмов защиты лёгких вследствие обструкции дыхательных путей и/или воспалительного ответа лёгочной ткани на аспирацию. Риск развития вторичной аспирационной пневмонии возрастает у больных, находящихся в стационаре более 5 суток или на ИВЛ [Парсонз и Хеффнер, 2004]. Хроническая аспирация небольших количеств пищи ведёт к лёгочному фиброзу, обусловленному гранулематозным процессом, или вялотекущей пневмонии, на фоне которой возможно формирование абсцесса лёгкого. Все аспирационные синдромы наиболее часто вовлекают зависимые сегменты лёгкого. В горизонтальном положении на спине, аспирация обычно происходит в верхние сегменты нижних долей, задние сегменты верхних долей и реже в задние и медиальные основные сегменты нижних долей [Curtis & Langmore, 1997]. Повторяющиеся и объёмные аспирации подавляют защитные механизмы воздушных путей и обусловливают развитие дыхательной недостаточности.
Другим грозным осложнением нейрогенной дисфагии является алиментарная дистрофия с дегидратацией. При поступлении в стационар от 30 до 60% больных имеют в той или иной степени выраженную недостаточность питания, при этом у 10-25% из них диагностируется тяжёлая степень алиментарного истощения [Sobotka, 2004]. Дисфункция глотания, мешающая больному нормально питаться, недооцениваются многими неврологическими больными и их родственниками, но, к сожалению, она часто игнорируются и медицинским персоналом (Фото 2). В процессе больничного лечения нарушения трофологического статуса «дисфагичных» больных усугубляются из-за небрежности медицинского персонала в распознавании недостаточности питания, их неосведомлённости или некомпетентности, а главным образом, вследствие непонимания дурного влияния алиментарного истощения на развитие инфекционных осложнений, результаты лечения и исход заболевания.

Фото 2. Описание своих страданий больной миопатией с тяжёлой дисфагией (собственное наблюдение).
Этому способствуют также особенности неврологических больных: пожилой возраст; нарушения сознания; гиперкинезы, замедление темпа движений, нарушение координации и/или длительная обездвиженность; зрительное невнимание и/или выпадение полей зрения; проблемы общения и нарушения речи (не просят есть и пить); снижение аппетита и чувства жажды; депрессия и зависимость от окружающих. Нейрогенная дисфагия приводит к тяжёлым изменениям трофологического статуса с водно-электролитными нарушениями, гемоконцентрацией, гиповолемией и полиорганной недостаточностью, которые усугубляются на фоне лихорадочного состояния, инфекции лёгких, гипергликемии и применения, например, диуретиков.В Таблице 4 представлены виды недостаточности питания при нейрогенной дисфагии.
Таблица 4. Недостаточность питания при нейрогенной дисфагии.
Смешанный тип
Обычно результатом ограничения приёма пищи при дисфагии, существующего в течение длительного времени и ведущего к потере подкожного жира и мышечной массы, становится дефицит калорий и соматического пула белка, но с сохранением висцерального пула (маразматический тип, Фото 3).

Фото 3. Маразматический тип недостаточности питания (собственное наблюдение).
При неадекватно низком потреблении белка с пищей и нормальном калорическом балансе развивается истощение квашиоркор (Фото 10). При этом в организме больного сохраняются запасы жира, но потеря обоих пулов белка обусловливает развитие отёков. Для ситуации острого метаболического стресса (травмы, хирургические операции, тяжёлые инфекционные процессы) характерен именно квашиоркор. Отягощение течения нейрогенной дисфагии с маразматическим типом алиментарной дистрофии острым инфекционным процессом является причиной смешанного типа недостаточности питания (присоединение пневмонии, например, при амиотрофическом боковом склерозе). Нарушения питания, снижая иммунореактивность неврологических больных, способствуют обострениям хронического воспалительного процесса в лёгких, развитию острых синуситов и отитов, образованию пролежней, увеличению длительности пребывания в стационаре и росту летальности [Ч.П. Ворлоу с соавт., 1998]. Нарушение глотания, возникшее при инсульте, приводя к респираторным осложнениям и недостаточности питания, является основной причиной смертности [Veis & Logemann, 1985; Horneretal., 1988]. Восстановление функции глотания при инсульте обусловливает улучшение нутриционных параметров и нормализацию трофологического статуса [Gariballaetal., 1998].
Общение за столом является важнейшим атрибутом повседневной жизни современного человека. Без него немыслимо проведение, как досуга, так и деловых мероприятий. Дисфагия драматично влияет на качество жизни неврологических больных. Она превращает удовольствие от еды в переживание и мучение. Она делает пациентов зависимыми при кормлении от других людей или от искусственного питания. Она может принять вид постоянной угрозы неожиданной обструкции воздушных путей или респираторных инфекций от аспирации. Дисфагия приводит к изменению психического состояния, депрессии и социальной дезадаптации.
Диагностика причины и уровня расстройства акта глотания при заболеваниях нервной системы с определением терапевтической тактики сложный и многоступенчатый процесс. Условно в нём можно было бы выделить четыре основных этапа. Первой задачей при осмотре «дисфагичных» больных является исключение потенциальных не нейрогенных причин дисфункции глотания. Затем надлежит понять индивидуальный механизм дисфагии конкретного больного, используя «прикроватную оценку» и результаты дополнительных методов исследования, и определить специфическую стратегию безопасного и эффективного приёма пищи через рот или необходимость протезирования акта глотания. Следующее: очень важно предупредить или не пропустить признаки возможных осложнений нарушенного глотания. А уже потом на основании объективных данных осмотров и инструментальных обследований, продумать программу лечебных и реабилитационных мероприятий.
Анамнез может обеспечить постановку правильного диагноза более чем у 80% больных [Schatzki, 1959]. Главные вопросы, которые следует выяснить у больного и его родственников:
· «Какой вид пищи вызывает проблемы?»;
· «В какой момент глотания возникают трудности?»;
· «Есть ли изжога?»;
· «Дисфункция глотания прогрессирует, стабильна или по какой-то причине вариабельна?»;
· «Есть ли ещё какие-то заболевания, течение которых может сопровождаться дисфагией (коллагенозы, опухоли и т.д.)?»;
· «Проводились ли какие-либо хирургические вмешательства в тех областях, где располагаются структуры, обеспечивающие акт глотания (голова, шея, грудная клетка)?»;
· «Изменился ли голос?»;
· «Есть ли кашель или удушье во время еды?»;
· «Изменился ли сон (храп, кашель)?;
· «Нет ли температуры, ознобов, ночных потов?»;
· «Как больной приспосабливается к нарушениям глотания?».
· «Является ли дисфагия источником изоляции и депрессии?»;
Очень важную информацию даёт знание о консистенции пищи, приводящей к дисфагии. Нейрогенную (орофарингеальную) дисфагию вызывают, как правило, жидкие болюсы. Затруднения, возникающие при употреблении только твёрдой пищи, указывают на наличие механической дисфагии. При дальнейшем уменьшении просвета застрявший пищевой комок уже нельзя протолкнуть через суженный участок выпитой вслед жидкостью. При ахалазии и диффузном спазме пищевода к дисфагии с самого начала заболевания одинаково приводит употребление как твёрдой, так и жидкой пищи. Натуживание, выпивание залпом нескольких стаканов жидкости, сублингвальный приём нитроглицерина облегчают ахалазию кардии, что воспринимается больными как "провал пищи в желудок" [В. Нечаев и А. Трухманов,1992]. Склеродермия, характеризуется затруднением пассажа в желудок твёрдой пищи вне зависимости от положения тела и жидкости в положении лёжа, и изжогой, вследствие развития желудочно-пищеводного рефлюкса и эзофагита. В результате прогрессирующего при склеродермии патологического изменения стенок пищевода образуется стриктура, и дисфагия становится стойкой. При выраженном рефлюксе страдают глотка и слизистая оболочка полости рта, может быть ларингит, дисфония (охриплость) по утрам и лёгочная аспирация, чреватая пневмонией, фиброзом лёгких или хроническими приступами астмы [Р.К. Гойял, 1996]. Дисфункция глотания (проблемы с жеванием, формированием пищевого комка и началом глотания), возникающая перед глотком свидетельствует о нарушении ротовой фазы, сразу же после глотания (регургитация пищи в нос, кашель, удушье) – глоточной, а дисфагия через несколько секунд после глотка (ощущение препятствия прохождению пищи за грудиной) – пищеводной [Schulze-Delrieu & Miller, 1997]. Если хрипота предшествует дисфагии, то первичное поражение обычно локализуется в гортани. Появление хрипоты вслед дисфагии указывает на вовлечение возвратного гортанного нерва при распространении рака пищевода. Сочетание симптомов поражения гортани с дисфагией наблюдается при различных нервно-мышечных нарушениях. Для них характерно также медленное прогрессирование и пожизненное существование дисфагии (мышечная дистрофия, амиотрофический боковой склероз и т.д.), либо острое её появление после какого-то события (инсульт, операция на голове или шее и т.д.) [Schulze-Delrieu & Miller]. Быстро прогрессирующая в течение нескольких месяцев дисфагия и/или выраженное снижение массы тела, не пропорциональное тяжести дисфагии, заставляют думать о раке пищевода. Непродолжительная преходящая дисфагия может быть обусловлена каким-либо воспалительным процессом. При пищеводной дисфагии обычны жалобы на «зависание» пищи за грудиной: локализация дисфагии обычно коррелирует с местом обструкции пищевода. Однако восприятие больными локализация дисфагии в области шеи, как правило, не имеет диагностической ценности, поскольку эти ощущения возможны при поражении глотки, шейного отдела и даже более низко расположенных участков пищевода. Бульканье при прохождении воздуха через глотку, наполненную слизью, характерно для параличей глотки и гортани. Поэтому даже у больных, находящихся в бессознательном состоянии, они довольно легко распознаются [Л.М. Попова, 1983]. Регургитация в нос и трахеобронхиальная аспирация при глотании являются признаками паралича мышц глотки или наличия трахеопищеводного свища. Трахеобронхиальная аспирация, не связанная с глотанием, может быть вторичной при ахалазии, дивертикуле Ценкера или желудочно-пищеводном рефлюксе. Боль при глотании (одинофагия) указывает на острый или хронический воспалительный процесс в глотке или пищеводе. Боль в области грудной клетки, сочетающаяся с дисфагией, развивается при диффузном спазме пищевода и связанных с ним двигательных нарушениях. При патологии дистального отдела пищевода могут быть жалобы на икоту. Больные пытаются приспосабливаться и компенсировать возникшие проблемы с глотанием, меняя консистенцию и температуру пищи, запрокидывая голову или помогая пальцами продвинуть еду к зеву, наклоняя или поворачивая голову, надавливая на одну сторону шеи, подпрыгивая после глотка. Из-за того, что приём пищи сопряжён с болью, кашлем и т.д., больные тревожатся и смущаются, воздерживаются от еды в присутствии других людей, впадают в депрессию, становятся равнодушными к еде. Иногда жалобы, напоминающие симптомы нейрогенной дисфагии, на самом деле имеют психогенную основу [Buchholzetal., 1994]. Их выраженность может драматично колебаться, и возникают они, как правило, у относительно молодых людей, у которых нет дисфонии или какого-либо другого объективного неврологического дефицита. Больные с психогенной дисфагией утверждают, что не способны есть и пить, делают это с неохотой, долго перемещают болюс во рту и, даже когда разоблачается (например, при видеорентгеноскопии) их способность глотать успешно, продолжают жаловаться на затруднения глотания. Однако важность тщательного поиска альтернативного диагноза, даже при отсутствии доказательств неврологического заболевания, не может быть преувеличена. Симптомы, наиболее характерные для нейрогенной дисфагии, представлены в Таблице 5.
Таблица 5. Клинические симптомы, указывающие на нейрогенную дисфагию.
· Трудности в проглатывании жидкости
· Слюнотечение или частое сплёвывание слюны
· Прилипание пищи в горле и/или глотке
· Удушье и кашель при приёме пищи и жидкости, проглатывании слюны
· Ослабление (или отсутствие) произвольного или непроизвольного кашля
· Влажный или булькающий голос
· Дискомфорт в глотке и рецидивирующие бронхолёгочные инфекции
· Носовая регургитация
· Необходимость повторных глотков, чтобы освободить глотку
· Потеря веса, изменение трофологического статуса
Осмотр «дисфагичного» больного должен состоять из неврологической (включая исследование функции тройничных, лицевых, языкоглоточных, блуждающих и подъязычных черепных нервов), психологической, логопедической и отоневрологической оценки (обязательно непрямая ларингоскопия) [Buchhols, 1994], наблюдения больного во время глотания различных видов и объёмов жидкости и пищи, исследования дыхательной системы и анализа трофологического статуса [Detsky, 1987]. Как скрининг-тесты для отбора больных с аспирацией, требующих полной инструментальной оценки дисфагии, используется глотание фиксированных болюсов с разными объёмами (3, 5, 10, 15 и 20 мл) и с определённой вязкостью (жидкость, газированная вода и пудинг) и наблюдение кашля или удушья при питье 50 мл воды [DePippo, 1992]. В Таблице 6 перечислены необходимые «пункты», которые следует включать в схему клинического обследования при нейрогенной дисфагии.
Таблица 6. Клиническое обследование больного с дисфагией
· Когнитивные, речевые и поведенческие особенности
· Инспекция рта (зубы, состояние слизистой оболочки и т.д.)
· Стереотип поведения во время приёма пищи
· (медлительность, застывание и т.п.)
· Функция губ и жевательной мускулатуры, объём движений нижней челюсти
· Вытекание жидкости или пищи изо рта
· Оценка скорости формирования пищевого болюса и проглатывания жидкости
· Функция мягкого нёба и глоточный рефлекс
· Объём движений и сила языка
· Фиксация дополнительных глотательных движений
· Степень очищения ротовой полости после глотка
· Объём движений подъязычной кости
· Голос и его изменения после глотания
· Регистрация попёрхивания, кашля или удушья во время или после глотка
· Аускультация трахеи во время глотка
· Непрямая ларингоскопия (консультация отоневролога)
· Оценка кашлевого толчка
· Перкуссия и аускультация лёгких
· Оценка трофологического статуса и гидратации: кожа и слизистые; вес; диурез; потеря подкожного жира (трицепсы); мышечная атрофия (дельтовидные, четырёхглавые мышцы)
· Исследование шеи (лимфатические узлы, щитовидная железа, позвоночник)
Здесь необходимо специально остановиться на диагностической ценности глоточного (рвотного) рефлекса, который, по мнению многих врачей, является надёжным показателем, даже«индикатором» дисфункции глотания. На самом деле, корреляция между рвотным рефлексом и безопасным глотанием настолько слабая, что нормальный глоточный рефлекс может сосуществовать с тяжёлой нейрогенной дисфагией, тогда как при сохранном глотании у многих здоровых людей он либо отсутствует, либо снижен [Ellul & Barer, 1993; Davies, Kidd, Stone, & MacMahon, 1995; Ч.П. Ворлоу с соавт., 1998].
Клиническую оценку дополняют рентгеноскопия акта глотания с барием; гибкая носовая эндоскопия и глоточно-пищеводная манометрия, позволяющие проанализировать уровень и выраженность поражения, безопасность и эффективность глотания, и утвердится в диагнозе. Кроме того, у больных с дисфагией используются электромиография мышц, участвующих в глотании (надподъязычных, жевательных мышц, языка и др.), ультразвуковая оценка глотания, эзофагогастроскопия, рентгенологическое исследование грудной клетки, компьютерная (или магниторезонансная) томография шеи и органов грудной клетки.
«Глотательный тракт» простирается от губ до кардии, поэтому только рентгенологическое исследование с глотком бария даёт возможность в целом рассмотреть как его анатомическое строение, так и выявить дисфункцию механизмов, обеспечивающих акт глотания, на любой физиологической стадии прохождения болюса. Это особенно полезно в тех случаях, когда непонятно, что главным образом вовлечено в патологический процесс - глотка или пищевод. Поскольку глотание происходит за короткий промежуток времени (особенно его фарингеальная фаза), то во время простого рентгеноскопического исследования невозможно детально проанализировать происходящие события. Поэтому золотым стандартом для изучения (особенно орофарингеальной) дисфагии,считаетсявидеорентгеноскопия. Метод основывается на видеозаписи рентгеноскопической картины проглатывания контрастного болюса (Фото 1, 4). Больной обследуется в боковой и прямой проекциях.

Фото 4. Кадры видеорентгеноскопической записи: А. в боковой и Б. в прямой проекциях (совместное наблюдение с Н.В. Докучаевой).
Начинать рекомендуется с боковой проекции, так как именно такой взгляд на процесс глотания даёт большую часть информации. Осматривается поверхность, ограниченная спереди губами, сзади - задней стенкой глотки, вверху - твёрдым нёбом, внизу - 7-м шейным позвонком (Фото 4 А.). Прямая проекция необходима, так как позволяет диагностировать асимметричность поражения при параличах глотки и гортани, выраженность стаза в валлекулах надгортанника и грушевидных карманах и не пропустить, например, дивертикул. Применяются три консистенции рентгеноконтрастного материала: начинают с жидкого бария, затем дают бариевую пасту и заканчивают исследование кусочком хлеба (или 1/4 домашнего печенья), покрытого бариевой пастой для оценки жевания и адекватности формирования пищевого болюса. Для получения повторяемости результатов больной делает два глотка каждого материала в контролируемых малых количествах (1/3 чайной ложки жидкости и 1/3 чайной ложки пасты). Ограничение количества контраста (так называемый «модифицированный бариевый глоток») при видеорентгеноскопическом исследовании акта глотания предложено Veis & Logemann [1985]. Частота аспирации, например, при инсульте свидетельствует в пользу использования именно модифицированного, а не рутинного, бариевого глотка. Даже если больной аспирирует, только очень маленькое количество контрастного материала попадёт в нижние дыхательные пути. Кроме того, при использовании больших объёмов бария, структуры ротовой полости и глотки частично облитерируются рентгеноконтрастным веществом, что затрудняет интерпретацию двигательных событий [Veis & Logemann, 1985; Logemann, 1997]. Таким образом, модифицированный бариевый глоток облегчает оценку физиологии глотания оральной и фарингеальной фаз с минимальным риском аспирации.Если больной аспирирует, исследование заканчивается, как только причина аспирации определена. Протокол исследования трансформируется в каждом конкретном случае, в зависимости от истории болезни, данных клинического обследования и полученных находок. Для идентификации нарушений глотания и для измерения времени прохождения болюса каждая видеозапись анализируется с обычной скоростью, при замедленном просмотре и кадр за кадром.Видеорентгеноскопический метод с высокой степенью достоверности позволяет сделать заключение, насколько глотание безопасно и эффективно. Понятие«безопасное глотание» означает, что во время еды никакие инородные вещества не проникают в нижние дыхательные пути, а понятие «эффективное глотание»подразумевает, что после глотка во рту, глотке или пищеводе не задерживается никаких остатков пищи [Clave, 2001].
Видеорентгеноскопия выявляет признаки дисфункции на различных этапах акта глотания. Остановимся подробнее на проявлениях орофарингеальной дисфагии, характерной для неврологических больных. В процессе исследования хорошо видны нарушения жевания, обусловленные слабостью или дискоординацией жевательных мышц или смещением нижней челюсти. При этом следует помнить о стоматологических проблемах, которые влияют на способность жевать и формировать пищевой комок. При болезнях Паркинсона или Альцгеймера больным свойственно пожёвывать, а не разжёвывать пищу [Perlman, Lu & Jones, 1997]. Растягивание времени формирования болюса характерно как для больных с деменцией, у которых это может быть формой ротовой или вкусовой агнозии, когда больной не ощущает положение болюса во рту или не производит необходимые движения языком или челюстью, так и для больных с апраксией глотания. В последнем случае больные могут глотать болюс любого объёма и вязкости без его подготовки [Perlman, Lu & Jones, 1997]. Кроме того, ротовая фаза удлиняется из-за ксеростомии, обусловленной гипофункцией слюнных желёз или приёмом препаратов, снижающих слюноотделение. При слабом (вследствие пареза или дискоординации) языке болюс распространяется по всей ротовой полости, заваливается под язык и/или застревает на твёрдом нёбе. Слабость губ усиливает трудности удержания и формирования болюса. Поражение лицевого нерва с параличом щёчных мышц (m.m. buccinators) сопровождается складированием пищи за щеками, о котором больной не подозревает. Слабость губ, языка, щёк приводит к удлинению ротовой фазы при проглатывании твёрдого болюса и её укорочению при глотании жидкости. В последнем случае происходит преждевременное стекание контраста в глотку, характеризующее несостоятельность ротовых структур. В отличие от потери болюса, замедленная инициация глотка (отсроченное время или латентность ответа [Langmore, 2001])обусловлена несвоевременным срабатыванием триггера глотательного рефлекса вследствие гипестезии корня языка и, возможно, глотки и плохого центрального контроля. При видеорентгеноскопии преждевременная потеря болюса проявляется отделением порции несформированного болюса и стеканием его с корня языка, как правило, в валлекулы надгортанника, тогда как при отсроченной инициации глотательного рефлекса болюс формируется и доставляется языком в глотку, а вот глоток своевременно не возбуждается. Считается существенным запаздывание инициации глотка на секунду и более. Удлинение отсрочки повышает вероятность аспирации болюса [Perlmanetal., 1994]. Раскачивание и обилие колебательных движений языка наблюдается у больных с психогенной дисфагией, когда они жалуются на свою неспособность глотать и сопротивляются инициации глотания. В этих случаях видеорентгеноскопическое исследование обнаруживает странное, напряжённое, сложное поведение с оральной или язычной активностью, не продвигающей болюс, но и не сопровождаемое утечкой орального содержимого в глотку. При инициировании глотательного рефлекса (часто отсроченном из-за «ротовой» борьбы) реализуется нормальная фарингеальная фаза [Barofskyetal., 1994]. В отличие от психогенного беспокойства языка миоклония проявляется быстрыми непроизвольными повторяющимися подёргиваниями мышц вовлечённых структур, как в покое, так и при движениях. Ориентиром начала фарингеальной фазы является поднятие подъязычной кости. Именно это движение имеет решающее значение в перемещении гортани вверх и вперёд. В норме подъязычная кость двигается в среднем на 9-12 мм вперёд и на 11-12 мм вверх. [Jacobetal., 1989]. Ограничение подвижности подъязычной кости увеличивает риск аспирации в 3,7 раза [Perlmanetal., 1994]. Слабость надподъязычных мышц ведёт к малоподвижности надгортанника и скоплению контраста в его валлекулах (Фото 1,4). Остатку также способствует уменьшение давления на надгортанник корнем языка. Если умеренный стаз в валлекулах в два раза увеличивает вероятность аспирации, то дальнейшее накопление создаёт ещё большую угрозу попадания инородных веществ в нижние дыхательные пути [Perlmanetal., 1994]. При видеорентгеноскопии хорошо визуализируется первый этап двигательного фарингеального паттерна: разделение носоглотки и р<
