Анатомо-физиологические основы жизненно важных функций организма
Часть I
ОБЩИЕ ВОПРОСЫ НЕОТЛОЖНЫХ СОСТОЯНИЙ
В данной части учебника рассматриваются анатомо-физиологические основы жизненно важных функций организма, реакция его на травму, водно-электролитный обмен в норме и при различных видах патологии, кислотно-щелочное состояние и варианты его нарушений.
ГЛАВА 1.
АНАТОМО-ФИЗИОЛОГИЧЕСКИЕ ОСНОВЫ ЖИЗНЕННО ВАЖНЫХ ФУНКЦИЙ ОРГАНИЗМА
Диапазон заболеваний, при которых могут возникнуть неотложные состояния, весьма велик, однако при всем многообразии этиологических факторов их патогенез неизменно включает такие патофизиологические сдвиги, как гипоксия, расстройства гемодинамики и особенно микроциркуляции, печеночная и почечная недостаточности, нарушение водно-солевого обмена и кислотно-щелочного состояния, гемостаза и др.
Исходя из этого бесспорного положения, для правильного понятия патогенеза неотложных состояний необходимо знать анатомо-физиологические основы жизненно важных функций организма.
ДЫХАТЕЛЬНАЯ СИСТЕМА
Основной функцией легкихявляется обмен О2 и СО, между внешней средой и организмом. Это достигается сочетанием вентиляции, диффузии газов через альвеолярно-капиллярную мембрану и легочного кровообращения (В. Д. Малышев, 1989).
Примечание.
Помимо основной функции газообмена, легкие играют большую роль в эндо- и экзогенной защите, обеспечивают детоксикацию, ингибицию, депонирование многих биологически активных веществ (В. А. Гончарова, Н. В. Сыромятникова, 1975), участвуют в белковом, жировом, углеводном обмене, выполняют фибринолитическую и антикоагулянтную, кондиционирующую и выделительную функции, регулируют водный баланс (А. П. Зильбер, 1977), синтезируют поверхностно-активные вещества (И. А. Козлов, М. А. Выжигина, М. Л., Бархи, 1983).
Процесс дыхания условно можно подразделить на три этапа.
Первый этап(внешнее дыхание) включает в себя доставку кислорода из внешней среды в альвеолы.
Вторым этапомдыхания является диффузия О2, через альвеолярно-капиллярную мембрану ацинуса и транспортировка его к тканям; движение СО, осуществляется в обратном порядке.
Третий этапдыхания (тканевое дыхание) заключается в утилизации кислорода при биологическом окислении субстратов и образовании, в конечном итоге, энергии в клетках.
Примечание.
Регуляция дыхания осуществляется центральной и периферической нервной системой.
В кровеносных сосудах находятся хеморецепторы, реагирующие на концентрацию продуктов обмена, парциальное напряжение кислорода и углекислого газа и реакцию внутренней среды организма (рН).
Через них осуществляется регуляция объема вентиляции, частоты, глубины, длительности вдоха и выдоха, силы сокращений дыхательных мышц.
Первый этап.Адекватность первого этапа зависит от многих факторов, начиная с функции верхних дыхательных путей: очищение, согревание, увлажнение воздуха.
Эффективность очищения вдыхаемого воздуха зависит от количества и качественного состояния макрофагов, содержащихся в слизистых оболочках; они фагоцитируют и переваривают минеральные и бактериальные частицы.
Внутренняя поверхность верхних дыхательных путей выстлана реснитчатым псевдомногослойным эпителием.
Его основная функция — эвакуация мокроты из верхних дыхательных путей; в норме из трахеи и бронхов за сутки удаляется до 100 мл мокроты, при некоторых видах патологии до 100 мл/час.
Для нормальной функции верхних дыхательных путей важное значение имеет состояние кашлевого рефлекса.
При его нарушении не происходит своевременного освобождения верхних дыхательных путей от патологического секрета.
Кашель состоит из трех фаз:
— голосовая щель раскрыта, дыхательный объем (ДО) достигает жизненной емкости легких (ЖЕЛ);
— голосовая щель закрыта, альвеолярные ходы раскрываются, альвеолы и дыхательные пути образуют герметичную систему;
— сокращение диафрагмы резко повышает давление, воздух выходит, открываются альвеолярные ходы, и «запертый» в альвеолах воздух устремляется в бронхи, унося слизь и патологический секрет.
Различают верхние (полость носа, рта, глотки и гортани) и нижние (трахея, бронхи) дыхательные пути.
Емкость верхних дыхательных путей называется анатомическим мертвым пространством, оно приблизительно равно 150 см1 или 2,2 см3 на 1 кг массы.
Воздух, заполняющий анатомическое мертвое пространство, в газообмене не участвует. Вентиляция легких зависит от дыхательного обмена и частоты дыханий в 1 мин.
Основные параметры вентиляции легких представлены в табл. 1.15
Таблица 1. Нормальные величины функциональных проб легких (Comroe J. et al., 1961).
| Показатель | Параметры |
| Дыхательный объем | 0,5 л |
| Резервный объем вдоха | 1,5-2 л |
| Остаточный объем | 1,0-1,5 л |
| Общая емкость легких | 3,8-5,8 л |
| Резервный объем выдоха | 1,5-2,0 л |
| Минутный объем дыхания | 9,0 л/мин. |
| Жизненная емкость легких | 2,8-4,3 л |
Примечание.
Данные приведены для здорового человека (поверхность тела 1,7 м2) в покое лежа при дыхании воздухом.
Величина вдоха определяется разницей между силой сокращения дыхательных мышц и эластичностью легких.
Эластичность легких зависит от поверхностного натяжения жидкости, покрывающей альвеолы и эластичности самой легочной ткани.
Вентилируемость легких во время вдоха (по значимости): нижний отдел, передний, задний, верхушка.
Работа дыхания увеличивается при заболеваниях легких, сопровождающихся повышением эластичного и неэластичного сопротивлений.
Этот факт необходимо учитывать при проведении искусственной вентиляции легких (ИВЛ).
Примечание
Современная диагностическая аппаратура (приборы типа Custo-vit) позволяют в течение 10—15 мин. определить в автоматическом режиме работы все данные спирограммы, оценить проходимость бронхов на всех уровнях, скорость потока воздуха и вязкость мокроты.
Кроме этого, прибор дает заключение о наличии в легких рестрикции или обструкции.
Вторым этапомдыхания является диффузия кислорода через АЦИНУСи транспортировка его к тканям; движение углекислого газа осуществляется в обратном порядке.
Ацинус является структурной единицей легких.
Он состоит из дыхательной бронхиолы и альвеол.
Диффузия кислорода осуществляется за счет парциальной разности его содержания в альвеолярном воздухе и венозной крови, после чего незначительная часть О2, растворяется в плазме, а большая часть связывается с гемоглобином, содержащимся в эритроцитах, и в таком виде транспортируется к органам и тканям (см. ниже:
Примечание
Функция альвеолярно-капиллярной мембраны не ограничивается только диффузией газов. Она влияет на химический состав крови, участвует в процессах регуляции свертывающей системы крови и др.
Внутренняя поверхность альвеол покрыта сложным белковым поверхностно-активным веществом — СУРФАКТАНТОМ.
Сурфактантный комплекс препятствует спадению терминальных бронхиол, играет важную роль в регуляции водного баланса, осуществляет противоотечную функцию, оказывает защитное действие за счет противоокислительной активности.
Предполагается участие сурфактанта в процессах диффузий О2, и СО2 через альвеолярно-капиллярный барьер за счет регулирующего влияния на динамику перикапиллярной, интерстициальной и альвеолярной жидкости (В. Б. Скобельский, 1996).
Сурфактант очень чувствителен к различным эндо- и экзогенным факторам: снижение кровообращения, вентиляции, уменьшение парциального напряжения кислорода в артериальной крови (раО2) вызывают уменьшение его количества, в результате чего нарушается стабильность поверхности альвеол, что может осложниться возникновением ателектазов.
Третий этапдыхания заключается в утилизации кислорода в цикле трикарбоновых кислот (цикл Кребса) для биологического окисления белков, жиров и углеводов, с целью выработки энергии.
Молекулярной основой клеточного дыхания является окисление углерода до углекислого газа и перенос атома водорода на атом кислорода с последующим образованием молекулы воды.
Данный путь получения энергии (аэробный) в организме является ведущим и наиболее эффективным.
Так, если из 1 молекулы глюкозы при анаэробном окислении образуется только 2 молекулы АТФ, то при аэробном окислении из нее образуется 36 молекул АТФ.
В нормальных условиях 96-98% всей энергии, вырабатываемой в организме, образуется в условиях аэробного окисления и только 2-4% приходится на анаэробное.
Отсюда ясна исключительная роль адекватного снабжения организма кислородом.
Сосудистое русло легких состоит из 2-х систем: легочной и бронхиальной.
Давление в легочной артерии в среднем равно 17-23 мм рт. ст.
Общая поверхность стенок капилляров составляет 30-60 м2, а при физической нагрузке увеличивается до 90 м2.
Диастолическое давление в левом желудочке равно 0,2 мм рт. ст.
Нормальный кровоток в системе легочной артерии зависит от величины венозного возврата крови в сердце, сократительной способности миокарда, функционирования клапанов, тонуса артериол и прекапиллярных сфинктеров.
В зависимости от конкретных условий, емкость малого круга может значительно меняться, т. к. он относится к системе сосудов с низким давлением.
СЕРДЕЧНО-СОСУДИСТАЯ СИСТЕМА
Взаимосвязь между внешней средой и различными анатомо-физиологическими структурами организма обеспечивает сердечнососудистая система (ССС).
Кровь
Основные показатели крови: плотность 1,055—1,065, вязкость в 5—6 раз больше, чем у воды, объем приблизительно равен 8% массы тела (5—6 л).
Гематокрит: мужчины — 0,45—0,48, женщины — 0,42—0,45.
Основная функция эритроцитов — транспорт кислорода к тканям; лейкоцитов — фагоцитоз, иммунные процессы, пирогенные реакции; тромбоцитов — процессы свертывания.
Плазма крови представляет собой коллоидно-электролитно-белковый раствор, в котором взвешены форменные элементы.
Она имеет большое значение в осуществлении гемо- и гидродинамики.
Плазма составляет большую часть ОЦК.
Содержащийся в ней белок обеспечивает значительную часть коллоидно-осмотического давления крови.
Белки плазмы, особенно альбумины, связывают лекарственные вещества, токсины и транспортируют их к местам разрушения.
Для крови характерно увеличение вязкости в зависимости от градиента скорости.
В свою очередь, от вязкости зависит еще одно свойство крови — текучесть, величина, обратная вязкости.
Вязкость возрастает при сахарном диабете (на 20%), при коматозных состояниях, коронарной недостаточности, дегидратации, шоке и т. д.
При этом основной причиной снижения текучести является увеличение гематокрита и возрастание концентрации глобулинов и фибриногена.
Уменьшение вязкости наблюдается при гипертермии, лечении антикоагулянтами, декстранами.
Кроме этого, текучесть крови зависит от физико-химических свойств форменных элементов (их концентрации, взаимодействия между собой и сосудистой стенкой).
Таблица 3. Парциальное давление дыхательных газов на различных участках их транспортировки у здоровых людей в покое
(Сиггаард-Андерсен, 1960).
| Давление газа, в мм рт. ст. | Вдыхаемый воздух | Альвеолярный воздух | Артериальная кровь | Капиллярная кровь | Венозная кровь |
| рО2 рСО2 | 0,3 | 100>40 40<46 |
Примечание
При обычных условиях различные газы смешиваются друг с другом в любых соотношениях.
При этом каждый газ, входящий в состав смеси, характеризуется своим парциальным давлением.
Оно представляет собой то давление, которое производило бы имеющееся в смеси количество данного газа, если бы оно одно занимало при той же температуре весь объем, занимаемый смесью.
Установленный Дальтоном закон парциальных давлений гласит: «Давление смеси газов, химически не взаимодействующих друг с другом, равно сумме парциальных давлений газов, составляющих смесь».
В условиях покоя организм потребляет 250 мл О2, в 1 мин., а при значительной физической нагрузке эта величина может возрасти до 2500 мл/мин.
Каков механизм доставки О2 к тканям?
Кислород в крови находится в двух видах — физически растворенный в плазме и химически связанный с гемоглобином (НЬ).
Для определения клинической значимости каждого из этих двух видов существования О2 требуется провести несложные расчеты.
Нормальный минутный объем сердца (МОС) равен 5 л/мин., из этой величины примерно 60% (3 л) приходится на плазму.
Коэффициент растворимости кислорода в плазме при t = 38°С и при 760 мм рт. ст. равен 0,024 мл/мл, следовательно, в 3 л плазмы может быть растворено (3000 х 0,024) 72 мл кислорода.
В крови парциальное давление О2 во много раз меньше и составляет 80—90 мм рт. ст., а так как известно, что любой газ растворяется в жидкостях пропорционально своему парциальному давлению, то несложно рассчитать, что в 3 л циркулирующей в организме плазмы крови будет находиться не 72, а 8 мл растворенного кислорода, что составляет приблизительно всего 3% от минимальной потребности организма, равной 250 мл/мин.
Полученная нами расчетная величина полностью совпадает с данными, выявленными Cuenter С. А. (1977).
Эта величина (3%) настолько мала, что ею в дальнейшем можно пренебречь и не обсуждать значение физически растворенного О2 для жизнедеятельности организма.
Исходя из вышеизложенного, становится ясным, что единственным реальным переносчиком кислорода в организме может быть только гемоглобин.
Его молекула состоит из четырех полипептидных цепей, каждая из которых связана с гемом (сложное небелковое соединение, содержащее в своем составе железо).
При присоединении кислорода к гемоглобину последний превращается в оксигемоглобин.
Объем переносимого кислорода зависит, в свою очередь, от суммарного количества циркулирующего гемоглобина и его кислородной емкости, что, в конечном итоге, определяет кислородную емкость крови — это то количество кислорода, которое одномоментно находится в связанном виде с НЬ в артериальной крови.
Кислородная емкость 1 г гемоглобина при условии 100% насыщения крови кислородом составляет 1,34 мл, следовательно, должная величина кислородной емкости крови будет равна Нb • 1,34, или при Нb, равном 150 г/л, 150 г умножаем на 1,34 мл и получается, что в одном литре крови будет находиться 201 мл связанного кислорода, или 20,1% по объему. Это и есть величина кислородной емкости крови.
Приведенные цифры носят академический характер.
На самом деле в нормальных условиях кислородная емкость артериальной крови составляет 18-19, а венозной крови — 12—14% по объему.
Разница между этими величинами носит название артериовенозной разницы по кислороду (А—В).
В норме эта величина равна 5—6% по объему.
Исходя из приведенных цифр, можно легко рассчитать, что организм в нормальных условиях утилизирует только 25% имеющегося в артериальной крови кислорода.
Оставшиеся невостребованными 75% служат для обеспечения так называемого «запаса прочности» организма по кислороду.
Уровень насыщения гемоглобина кислородом (sO2) зависит не только от суммарного количества гемоглобина, но и от парциального давления кислорода в крови (рО2), рН внутренней среды и температуры тела.
Графическая зависимость между sO2 и рО2 носит характер S-образной кривой и отражает степень насыщения гемоглобина кислородом; иначе она называется кривой диссоциации оксигемоглобина (КДО)
S-образный характер КДО имеет важное физиологическое значение.
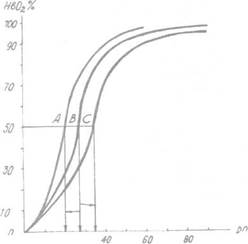
Рис. 1. Смещение кривой диссоциации гемоглобина.
А — влево; В — норма; С— вправо.
Такой характер кривой обеспечивает возможность адекватного насыщения крови при изменениях рО2 в довольно широких пределах.
Так, при снижении рО2 во вдыхаемом воздухе до 60—70 мм рт. ст. (это соответствует подъему на высоту 3—3,5 км над уровнем моря), кривая КДО смещается влево, и значительных признаков гипоксемии у человека не наблюдается.
С другой стороны, даже при значительном увеличении рО2 выше 80 мм рт. ст. (например, в условиях эксперимента в барокамере создали РaО2, равное 600 мм рт. ст.), sO2 достигает своего верхнего физиологического предела, но не превышает его.
Другое дело, что при таком высоком давлении возрастет примерно на 11% содержание физически растворенного в плазме кислорода (с 1,6 до 1,8 мл/л), но это имеет весьма косвенное отношение к КДО.
Численно сродство гемоглобина к кислороду принято выражать величиной Р50.
Она равна такому парциальному напряжению кислорода, при котором весь гемоглобин, имеющийся в артериальной системе организма (при рН 7,4 и 37°С), на 50% насыщается кислородом.
В норме Р50 равно 30 мм рт. ст. (см. рис. 1).
Смещение кривой насыщения НЬ вправо означает уменьшение способности гемоглобина связывать кислород и, следовательно, сопровождается повышением P50.
Напротив, смещение кривой влево свидетельствует о повышенном сродстве гемоглобина к кислороду, и величина Р50 будет снижена.
Помимо вышеуказанных факторов, КДО зависит и от рН.
На тканевом уровне, чем дальше от легких, тем рН тканей становится меньше (один из компонентов закисления — накопление избытка углекислого газа), а это уменьшает сродство гемоглобина к кислороду; благодаря этому артериальная кровь легко отдает его тканям на уровне системы микроциркуляции.
Обратным током кровь, ставшая к этому моменту уже венозной, попадает в сеть легочных капилляров, где рН значительно выше, чем в венозной сети.
В результате этого сродство гемоглобина к кислороду восстанавливается, и процесс переноса кислорода возобновляется.
Характер КДО зависит и от температуры тела.
Чем она выше, тем меньше будет сродство гемоглобина к кислороду и наоборот.
Знание этого фактора дает объяснение одной из причин возникновения признаков острой дыхательной недостаточности у больных с высокой температурой.
Кроме вышеуказанных факторов, на транспортную функцию кислорода существенную роль оказывает и внутриклеточный органический фосфат — 2,3-дифосфоглицерат (2,3-ДФГ).
Он непосредственно образуется в эритроцитах, находится в молекуле гемоглобина и влияет на ее сродство ккислороду.
Повышение уровня 2,3-ДФГ в эритроцитах уменьшает сродство гемоглобина к кислороду, а понижение концентрации 2,3-ДФГ приводит к увеличению его сродства к O2.
Ряд патологических синдромов может сопровождаться выраженными изменениями уровня 2,3-ДФГ как в сторону его увеличения, так и снижения.
При наличии легочных заболеваний, сопровождающихся развитием хронической гипоксии, содержание 2, 3-ДФГ повышается и, соответственно, уменьшается сродство Нb к О2, что вызывает улучшение снабжения тканей кислородом.
При кетоацидотической коме наблюдается обратный процесс.
Осложняющий ее течение декомпенсированный метаболический ацидоз нарушает образование 2,3-ДФГ в эритроцитах, вследствие чего сродство гемоглобина к кислороду возрастает, и нарушаются условия его отдачи на тканевом уровне.
В консервированной крови, особенно с длительным сроком хранения, уровень 2, 3-ДФГ снижается, поэтому при ее переливании нарушается отдача кислорода тканям.
Следовательно,смещение КДО является важнейшим физиологическим процессом, обеспечивающим транспорт кислорода в организме.
К факторам, приводящим к возрастанию сродства Нb к О2 и смещению КДО влево при падении Р50, относятся:
— увеличение рН;
— уменьшение рСО2;
— уменьшение концентрации 2,3-ДФГ и неорганического фосфата;
— снижение температуры тела;
— алкалоз.
С другой стороны, уменьшение рН, увеличение рСО2, концентрации 2,3-ДФГ и неорганического фосфата, а также повышение температуры и ацидоз приводят к уменьшению сродства Нb к О2 и смещению КДО вправо при возрастании Р50.
Потребление кислорода, кроме функционального состояния гемоглобина, в определенной мере отражает компенсаторную роль гемодинамики.
Увеличение минутного объема кровообращения (МОК) может компенсировать недостаток кислорода в крови.
Транспорт углекислого газа (СО2)
Конечным продуктом аэробного гликолиза является углекислый газ.
Он образуется в клетках и реагирует с водой, в результате чего получается угольная кислота, которая, в свою очередь, диссоциирует на ионы водорода и НСО3-.
Эта реакция происходит во всех водных секторах и эритроцитах.
Катализирует ее карбоангидраза.
Далее углекислота диффундирует через клеточные мембраны и попадает в венозную кровь.
В состоянии покоя за 1 мин. в тканях образуется и выделяется легкими примерно 180 мл СО2.
Данную величину легко рассчитать.
Ввиду того, что дыхательный коэффициент (ДК — отношение количества выведенной углекислоты к количеству поглощенного кислорода) в норме составляет 0,85, при поглощении организмом за одну мин. 250 мл О2 должно будет выделиться 210 мл СО2.
Каковы механизмы выведения углекислого газа из организма?
Часть углекислого газа физически растворена в плазме крови.
Хотя растворимость СО2 в плазме в 40 раз выше растворимости О2, тем не менее, небольшая артериовенозная разница по парциальному напряжению углекислого газа между венозной и артериальной кровью делает возможным перенос физически растворенного газа не более 6—7% от его суммарного количества.
Примерно 3—10% углекислого газа из тканей к легким транспортируется в виде карбаминовой формы.
Что это такое?
Рядом исследований было доказано, что СО2 может присоединяться к гемоглобину посредством карбаминовой связи, образуя карбогемоглобин (синоним — карбаминогемоглобин).
Данное соединение химически очень нестойко и в системе легочных капилляров легко диссоциирует с отщеплением СО2.
Основное количество углекислого газа (более 80%) транспортируется из тканей к легким в форме бикарбоната, важнейшая роль в этом механизме принадлежит гемоглобину и его способности к процессам оксигенации и деоксигенации.
Оксигенированный гемоглобин (НbО2) является более сильной кислотой, чем деоксигенированный, благодаря этому обеспечивается связывание СО2 в тканевых капиллярах и освобождение его в легочных.
Показатели газов крови
Для знания точного содержания газов нужно одновременно исследовать артериальную, венозную и капиллярную кровь.
Однако если у больного нет существенных нарушений газообмена, о состоянии газов вполне адекватно можно судить по динамике их содержания в «артериализированной» капиллярной крови.
Для ее получения необходимо предварительно согреть или хорошо в течение 5 мин. отмассировать мочку уха или палец кисти.
Исследование рО2 и рСО2 проводят при помощи анализаторов микрометодом Аструпа.
Каждый такой прибор оборудован микро-ЭВМ, и все расчеты содержания кислорода в крови осуществляются в автоматическом режиме по нижеприведенным формулам.
СаО2 = Нb (г%)х 1,39х SaO2/100 + 0,0031х раО2
CvO2 = Нb (г%)х 1,39х SvO2/100 + 0,0031х PvO2
где: СаО2 — содержание О2 в артериальной крови,
CvO2 — содержание О2 в смешанной венозной крови,
SaO, — насыщение кислородом артериальной крови,
SvO, — насыщение кислородом смешанной венозной крови,
рО2 —- парциальное напряжение кислорода в артериальной крови,
PvO2 — парциальное напряжение кислорода в смешанной венозной крови,
1,39 — константа Гюффнера,
0,0031 — коэффициент растворимости кислорода.
Таблица 4. Показатели газов крови у здорового человека (Сиггаард-Андерсен, 1960).
| Показатель | Артериальная кровь | Смешанная кровь |
| р.О,, мм рт. ст. SaO2,% рСО2,мм рт. ст. | 80-100 96-98 35-45 | 37-42 60-70 42-48 |
Примечание. Приведенные данные касаются лиц молодого и среднего возраста. С возрастом происходит снижение рСО2 и SaOr
Сердце
Основные электрофизиологические характеристики сердца: возбудимость, сократимость, проводимость, автоматизм.
Функция сердца, как насоса, зависит от состояния эндокарда, миокарда, перикарда, состояния клапанного механизма, ЧСС и ритма.
Основной путь выработки энергии для сердца — аэробный.
Одно из важнейших свойств сердца — возбудимость, которая обусловлена периодическим изменением трансмембранного потенциала.
Сумма этих изменений в виде биотоков регистрируется на ЭКГ.
Ведущий показатель адекватной работы сердца — ударный объем (УО; синоним — систолический объем, норма: 60—80 мл) и производная от него величина: минутный объем сердца (МОС); равен УО • ЧСС, норма 5-6 л).
Сосуды
Привязка кровотока к органам и тканям осуществляется при помощи пяти видов кровеносных сосудов:
1. Сосуды-буферы, или артерии.
2. Сосуды-емкости, или вены.
3. Сосуды распределения (сопротивления) — это артериолы и венулы.
4. Сосуды обмена — капилляры.
5. Сосуды-шунты.
Структурной единицей системы микроциркуляции является КАПИЛЛЯРОН, состоящий из артериолы, венулы, капилляров и артерио-венозного анастомоза.
Тонус артериол в головном мозге и сердце регулируется через хеморецепторы, реагирующие на рН, РаСО2, а в других органах и системах еще и симпатической нервной системой.
Движущая сила обмена веществ на уровне капилляров — гидродинамическое (ГД) и коллоидно-осмотическое давление (КОД).
Лимфатическая система обеспечивает постоянство плазмы крови и межклеточной жидкости. Объем лимфы приблизительно 2 л, скорость лимфотока 0,5-1,0 мл/сек.
Дополнительная информация по данному вопросу изложена в разделе 8.1. ЭТИОЛОГИЯ И ПАТОГЕНЕЗ ШОКОВЫХ СОСТОЯНИЙ.
ПЕЧЕНЬ
Печень занимает одно из центральных мест в метаболизме организма: регулирует энергетический баланс (вырабатывает 1/7 количества энергии), водно-солевое и кислотно-щелочное состояние, свертывание крови, теплообмен и детоксикацию, образование белка, конъюгацию билирубина и образование желчи.
Структурной единицей печени является ГЕПАТОЦИТ.
Он представляет из себя образование, состоящее из бассейна терминальной артериолы и воротной венулы, терминальных желчных протоков и ветвей лимфатических капилляров.
Гепатоциты периферических отделов печеночных долек накапливают различные вещества, в т. ч. и высокоэргические соединения, участвуют в детоксикации; гепатоциты центральных отделов печеночных долек осуществляют метаболизм билирубина и экскрецию в желчные капилляры ряда веществ эндо- и экзогенного происхождения (БМЭ, 1982).
ПОЧЕЧНАЯ СИСТЕМА
В системе поддержания постоянства объема и состава жидкостей организма основным эффекторным органом является почка.
Структурная единица почек — НЕФРОН.
Образуя первичную мочу из плазмы крови, почки избирательно возвращают в кровоток необходимые компоненты и выводят с вторичной мочой избыток воды, солей, ионы водорода и органические метаболиты, накопление которых вызывает интоксикацию.
Количество и состав мочи, в отличие от других жидкостей организма, может колебаться в значительных пределах.
Процесс образования мочи представляет собой несколько взаимосвязанных между собой процессов: ультрафильтрацию, реабсорбцию, секрецию и экскрецию.
Продуктом ультрафильтрации является первичная моча, состав которой отличается от состава плазмы крови, в основном, содержанием белка: в ультрафильтрате его в 1000 раз меньше, чем в плазме.
На этапе реабсорбции приблизительно 99% первичной мочи всасывается.
Окончательный состав мочи формируется благодаря секреции Н+ и К+.
Фильтрационная функция почек уменьшается, а в последующем может прекратиться при снижении системного артериального давления до 80 и менее мм рт. ст.
Среднесуточный объем мочи — 1,5 л, плотность — 1,014-1,021.
Кроме почек, определенную роль в выделительной функции организма играют легкие, кишечник и кожа.
Через легкие за сутки с дыханием выделяется 0,4—0,6 л воды.
Приблизительно столько же выделяется и через кожные покровы.
При повышении температуры тела на 1°С происходит увеличение потери воды за сутки через легкие в объеме 0,5 л и на столько же возрастает потеря через кожу.
С калом за сутки выделяется 150—200 мл воды.
ЖЕЛУДОЧНО-КИШЕЧНЫЙ ТРАКТ
В течение суток организм выделяет в просвет кишечника примерно 8—10 л пищеварительных соков (слюна — 1,5 л, желудочный сок — 2,5 л, желчь — 0,5 л, секрет поджелудочной железы — 0,7 л, тонкокишечный сок — 3,0 л) и все обратно всасывает.
При патологии ЖКТ (рвота, понос) теряется большое количество пищеварительных соков и различных микроэлементов.
Регуляция всего сокообращения осуществляется через периферические рецепторные звенья, гипоталамус, нейрогипофиз, надпочечники и выделительные органы.
К центральным механизмам сокорегуляции относится жажда, осморегуляция, обмен натрия.
Жажда возникает в результате обезвоживания клеток и повышения осмотического давления плазмы.
ВОДНО-ЭЛЕКТРОЛИТНЫЙ ОБМЕН
Объем, концентрация электролитов и рН жидкостей являются основными характеристиками внутренней среды, определяющими условия нормальной деятельности функциональных систем.
Организм на 60—65% (40—45 л) состоит из воды.
Ее суммарное количество зависит от пола, возраста, массы.
Вода в организме находится в связанном состоянии.
Она участвует в процессах гидратации и образует ряд комплексных систем, которые входят в состав клеток и жидкостей.
Выделяют 3 сектора воды:
• внутрисосудистый — 5%,
• интерстициальный — 15%,
• внутриклеточный — 40%.
Первые два сектора (внутрисосудистый и интерстициальный) образуют внеклеточное пространство.
Организм с большой точностью регулирует постоянство осмотической концентрации, уровня электролитов и взаимосвязи водных секторов.
Химические вещества
Одни химические вещества — электролиты — диссоциируют на ионы, другие — неэлектролиты — ионов не образуют (мочевина, креатинин).
Ионы несут на себе положительный или отрицательный заряд, в целом же вся внутренняя среда организма электронейтральна.
Катионы и анионы обеспечивают один из компонентов осмотического давления тела — биоэлектрический потенциал мембран, катализируют обмен веществ, являются кофакторами ферментов, определяют рН, участвуют в энергетическом обмене и процессах гемокоагуляции.
Одним из наиболее стабильных параметров внутренней среды является осмотическое давление.
Оно зависит от концентрации осмотически активных частиц в растворе и определяется их количеством, независимо от массы, заряда и размера.
Во внутриклеточном секторе осмотическое давление определяется концентрацией калия, фосфата и белка, во внеклеточном — содержанием Na+, Cl- и белка.
Осмотическое давление тем больше, чем больше этих частиц.
Клеточные мембраны полупроницаемы, они свободно пропускают воду, но не пропускают другие молекулы, поэтому вода всегда идет туда, где концентрация молекул больше.
В норме обмен ионами, водой и субстратами окисления подчинен процессу получения энергии и выведению метаболитов.
Дополнительная информация по данному вопросу изложена в главе 3. ВОДНО-ЭЛЕКТРОЛИТНЫЙ ОБМЕН.
КИСЛОТНО-ЩЕЛОЧНОЕ СОСТОЯНИЕ
Нормальная функция клетки зависит от постоянства объема, состава и рН жидкости.
Регуляторные механизмы, контролирующие нормальный объем, осмотическую концентрацию, ионный состав и Н+, взаимосвязаны.
Поддержание постоянства КЩС внутренней среды осуществляется через систему буферов, легкие, почки и другие органы.
Принцип саморегуляции организмом КЩС заключается в том, что при избыточном закислении внутренней среды происходит усиленное выведение ионов водорода, а при ощелачивании — их задержка.
Дополнительная информация по данному вопросу изложена в главе 4. КИСЛОТНО-ЩЕЛОЧНОЕ СОСТОЯНИЕ.
Литература
3. Неотложные состояния: патофизиология, клиника, лечение. Терновой К. С, Бутылин Ю. П., Бобылев Ю. И. — К.: Здоровье, 1984. - С. 7-79.
4. Рябов Г. А. Синдромы критических состояний. — М.: Медицина, 1994. - 368 с, ил.
Заключение.
Расстройства водно-электролитного обмена, КЩС, энергетического обмена, функций дыхания, кровообращения, почек, печени являются взаимосвязанными этиопатогенетическими факторами остро возникающих заболеваний.
Одним из ключевых вопросов неотложной терапии является знание механизмов, клинических проявлений и принципов коррекции расстройств водно-электролитного обмена и КЩС.
ОБМЕН ВОДЫ В ОРГАНИЗМЕ
Для нормального течения обменных процессов внутри организма, как в условиях нормы, так и при патологии, необходим должный общий объем водной среды.
Общий объем воды у новорожденного составляет 80% массы тела, у взрослого человека — 50—60%, колебания зависят от типа телосложения, пола и возраста.
Из этой величины 40% приходится на внутриклеточный(интрацеллюлярный) и 20% на внеклеточный(экстрацеллюлярный) объемы.
Внутриклеточная жидкостьявляется составной органической частью протоплазмы.
По сравнению с внеклеточным сектором, внутри клетки отмечаются более высокий уровень белка и калия и менее низкий уровень натрия.
Такая разность концентрации ионов создается функционированием калиево-натриевого насоса, обеспечивающего биоэлектрический потенциал, необходимый для возбудимости нервно-мышечных структур.
Вода, поступившая из плазмы внутрь клетки, включается во все биохимические процессы и выделяется из нее в виде обменной воды; на весь этот цикл уходит 9—10 суток.
У детей грудного возраста данный цикл, в силу более интенсивных окислительно-восстановительных процессов, составляет 5 суток.
Вода внеклеточного объемараспределяется по трем водным секторам: внутрисосудистый, интерстициальный и трансцеллюлярный.
1. Внутрисосудистый секторсостоит из плазменного объема и воды, связанной в эритроцитах.
Кроме обычного обмена вновь поступающей в эритроциты воды на обменную воду (см. выше), часть воды из эритроцитов может выделяться при дегидратации, а при гипергидратации происходит обратный процесс.
Если учесть, что масса эритроцитов составляет до 30 мг/кг массы тела, то объем воды, связанной в эритроцитах будет примерно равным 2100 мл.
Принимая во внимание длительность обменных процессов водой между эритроцитами и плазмой, объем воды, связанный в эритроцитах, следует учитывать как необменный.
Объем плазмы у взрослого человека составляет 3,5—5% массы тела.
Данный сектор отличается высоким содержанием белка, что определяет соответствующее онкотическое давление и является наиболее мобильным в обменных процессах.
При лечении шоковых состояний любой этиологии этот сектор требует самого пристального внимания.
Наши рекомендации
