Биосинтез глицерина и ВЖК в тканях
Биосинтез глицерина в тканях тесно связан с метаболизмом глюкозы, которая в результате катаболизма проходит стадии образования триоз. Глицеральдегид–3–фосфат в цитоплазме под влиянием глицерол–дегидрогеназы (НАДН2) превращается в глицерол–3–фосфат, занимающий центральное место в биосинтезе простых и сложных жиров. Глицерол–3–фосфат, ацилируясь, превращается в фосфатидную кислоту, из которой образуются нейтральные и сложные жиры (ФЛ).
Биосинтез ВЖК в тканях происходит в эндоплазматической сети. Исходным материалом синтеза ВЖК в тканях является ацетил-КоА, который в цитозоль поступает из митохондрий, где образуется при окислении метаболитов белков, углеводного и липидного обменов. Также может образовываться из цитрата, который в силу ряда причин (при гиподинамии, избыточном питании), когда значительно снижается интенсивность окислительных процессов в ЦТК (в митохондриях) выходит в цитозоль, тем самым стимулируя синтез ВЖК. Цитрат в цитозоле под влиянием лиазы распадается на АцКоА и ЩУК. АцКоА участвует в биосинтезе ВЖК, а ЩУК при участии малатдегидрогеназы (НАДН2) восстанавливается до малата, который возвращается в митохондрии, где вновь окисляется до ЩУК. Тем самым завершается внутренний челночный цикл.
Условием для биосинтеза ВЖК в тканях:
- наличие ацетил-КоА;
- наличие НАДФН2, поступающего для реакции синтеза из пентозного цикла;
- наличие специальных белков-переносчиков (НS–АПБ-ацил переносящие белки);
- наличие энергии в форме АТФ; СО2; Н2О;
- наличие ферментов синтеза ВЖК.
Процесс биосинтеза ВЖК циклический. Каждый цикл включает 6 этапов. Ацетил-КоА используется только на 1 этапе, как “затравка синтеза” с образованием 3-х углеродного соединения малонил-КоА.
1 этап – образование малонил-КоА:
СН3-СОSKoA (это ацетил-КоА)® (АцКоА-карбоксилаза (биотин), +СО2, +Н2О, АТФ®АДФ+Фн) СOOН-СН2-СОSKoA (это малонил-КоА).
2 этап – перенос ацетила и малонила на специальные белки под действием соответствующих трансфераз:
СOOН-СН2-СОSKoA (это малонил-КоА) ® (малонилтрансфераза, +HS-АПБ, -HS-KoA) СOOН-СН2-СОSАПБ (это малонил-АПБ);
СН3-СОSKoA (это Ац-КоА)®(ацилтрансфераза, +HS-АПБ, -HS-KoA) СН3-СОSАПБ (это ацетил-АПБ).
3 этап – конденсация малонила и ацетила под влиянием синтетазы (конденсирующий фермент):
СOOН-СН2-СОSАПБ (это малонил-АПБ) + СН3-СОSАПБ (это ацетил-АПБ)®(конденсирующий фермент, -СО2, -HS-АПБ) СН3-С(О)-СН2-СОSАПБ (это ацетоацетил-АПБ).
4 этап – восстановление b-кетоацетила-АПБ при участии редуктазы (НАДФН2):
СН3-С(О)-СН2-СОSАПБ (это ацетоацетил-АПБ)® (редуктаза, НАДФН2®НАДФ) СН3-СН(ОН)-СН2-СОSАПБ (это b-гидроксибутирил-АПБ).
5 этап – дегидратация b-гидроксибутирила-АПБ:
СН3-СН(ОН)-СН2-СОSАПБ (это b-гидроксибутирил-АПБ)®(дегидратаза, -Н2О) СН3-СН=СН-СОSАПБ (это кротонил-АПБ или еноилацетил-АПБ).
6 этап – восстановление еноилацетила-АПБ при участии редуктазы (НАДФН2):
СН3-СН=СН-СОSАПБ (это кротонил-АПБ)®(редуктаза, НАДФН2®НАДФ) СН3-СН2-СН2-СОSАПБ (это бутирил-АПБ).
Т.о., в результате первого цикла синтеза ВЖК образуется 4-х углеродный фрагмент. Далее, в зависимости от того какую ВЖК в клетке нужно синтезировать, будут последовательно и циклично присоединяться молекулы малонил-КоА. Завершается синтез любой ВЖК реакцией гидролиза с участием фермента деацилазы: R-СН2-СН2-COSАПБ ®(деацилаза, +Н2О, -HS-АПБ) R-СН2-СН2-COОН (это ВЖК).
Для расчета количества молекул АТФ, необходимых для синтеза ВЖК, а также количества синтеза и количества молекул малонил-КоА можно воспользоваться формулой: n/2-1, где n – количество углеродных атомов ВЖК.
Таким образом, в организме можно синтезировать все предельные ВЖК и непредельные ВЖК, имеющие 1 двойную связь.
Биосинтез холестерина (ХС)
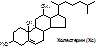
Основа - циклопентанпергидрофенантрен
Биосинтез ХС в клетках печени, тонкого кишечника и кожи осуществляется из АцКоА, который освобождается в результате распада белков, липидов и углеводов. Эндогенный ХС синтезируется преимущественно в печени (85%), в небольшой степени в тонком кишечнике (10%) и коже (5%).
Всего в организме взрослого здорового человека массой 70 кг за сутки образуется 2,8-3,5 г ХС. С пищей за сутки в организм поступает около 0,3 г ХС. Источником ХС для организма человека являются липиды пищи и эндогенный холестерин. Печень участвует в распределении ХС между клетками органов и тканей через транспортные ЛП крови. На экспорт ХС синтезируется только печенью и тонкой кишкой.
Холестерин является обязательным компонентом клеток. Наиболее богата ХС плазматическая мембрана гепатоцитов, где на его долю приходится 30% всех мембранных липидов. В миелине уровень ХС составляет 20%. В свободном виде и в виде эфиров он содержится в ЛП крови, входит в состав жировых включений цитоплазмы.
В организме человека ХС выполняет следующие функции:
1. структурная – ХС является структурным компонентом биомембран клеток. Принимает участие в регуляции их проницаемости, регулирует активность ферментов, работу рецепторов и переносчиков биомембран;
2. метаболическая – связана с тем, что ХС является предшественником стероидных гормонов (андрогены, эстрогены, минерало- и глюкокортикоиды), витамина D3 и желчных кислот.
Процесс биосинтеза ХС сложный и многоступенчатый и включает 35 реакций. Детали синтеза ХС практического врача не интересуют, поскольку многочисленные попытки управлять этим процессом в терапевтических целях оказались безуспешными, но знать схему биосинтеза надо. Источником БС ХС является ацетил-КоА, который образуется в результате катаболизма белков, углеводов и липидов.
2 ацетил-КоА (2 углеродных атома) ®(ацетил-КоА-тиолаза) ацетоацетил-КоА (4С) ®(гидроксиметилглутарил-КоА-синтетаза, +АцКоА) b-гидрокси-b-метилглутарил-КоА (6С) ®(редуктаза) 5 мевалоновая кислота (6С) ®(конденсация) сквален (30С) ®(циклизация) ланостерин (30С) ®(происходит деметилирование и перемещение двойной связи в кольце, -3СН3) холестерин (27С)
Освободившийся в результате распада клеток, ХС с помощью ЛПВП транспортируется в печень, где при участии цитохрома Р450 окисляется с образованием желчных кислот. примерно 80% окисленного ХС выводится с желчными кислотами через кишечник в виде капостеринов.
Патология липидного обмена
На этапе поступления с пищей. Обильная жирная пища на фоне гиподинамии ведёт к развитию алиментарного ожирения. Нарушение обмена может быть связано с недостаточным поступлением жира в организм с пищей, что приводит к развитию дерматитов, склероза сосудов из-за недостатка в незаменимых ВЖК. Полное исключение липидов из пищи ведет к авитаминозам (А, D, Е, К). Недостаточное поступление с пищей липотропных веществ ведет к нарушению синтеза ФЛ – структурных компонентов клеток – и в конечном итоге к развитию жировой инфильтрации печени, тканей (ФЛ®ТГ). Липотропными веществами являются: холин, инозит, серин – обязательные структурные компоненты ФЛ, а также витамин В6 (ПФ) - кофермент декарбоксилазы серина, метионин – донор метильных групп при биосинтезе фосфатидилхолина, фолиевая к-та и витамин В12 – коферменты метил-ТФ.
На этапе пищеварения. При поражении печени, желчных путей, желчного пузыря, когда в результате воспалительных процессов нарушается синтез или выведение в кишечник желчных кислот, когда нарушается биосинтез ЛП крови. Наиболее часто эти нарушения связаны с нарушением экскреция желчных кислот, что ведет к скоплению желчи в желчном пузыре, насыщении ее ХС. В этих условиях могут образовываться холестериновые камни. Застой желчи, воспалительные заболевания в печени и желчном пузыре способствуют осаждению ХС. Центрами образования холестериновых камней служат слущивающиеся клетки эпителия, на которые осаждается эпителий. Развитие желчекаменной болезни приводит к нарушению оттока желчи в кишечник и нарушению перевариванию липидов. В крови наблюдается гиперхолестеринэмия.
Поражение поджелудочной железы, слизистой тонкой кишки ведёт к нарушению переваривания жира. Развивается стеаторея, когда содержание жира в тканях увеличивается и составляет более 50%, кал становится ахоличный (преобретает серовато-белый цвет). Причины – нарушение образования или выведения желчных кислот. Нарушается функция поджелудочной железы (образование липаз, фосфолипаз, холестераз), воспаление слизистой в тонкой кишке, нарушается всасывание.
Липидный обмен нарушается при сахарном диабете. Накопление недоокисленных веществ ведёт к развитию кетоза. В случае недостаточной выработки инсулина интенсивному окислению подвергаются липиды клеток, что сопровождается избыточным Ацетил КоА, а это усиливает синтез ХС (гиперхолестеринэмия).
На этапе обмена ХС. Самым распространённым заболеванием является атеросклероз, которое характеризуется отложением ХС в стенке сосудов и тканей. Вокруг ХС формируются бляшки, развивается соединительная ткань (склероз), развивается кальцификация сосудов, тромбозы, нарушается кровоснабжение тканей. Болезнь развивается тогда, когда между клетками тканей и ЛП крови нарушается гомеостаз, развивается гиперлипопротеинэмия. Как правило, в крови растёт содержание фракций ЛПОНП и ЛПНП, которые снабжают клетку ХС. Снижение содержания ЛПВП – назначение которых удалять избыточный ХС. В клетки сосудов проникают все ЛП за исключением хиломикронов. Поскольку в их состав входят ФЛ, ТГ и белки, они быстро распадаются и удаляются из клетки. ХС выходит в межклеточное пространство. Он является чужеродным, поэтому его окружают марофаги. Все вещества, фагоцитирующие ЛП крови, разрушают ферменты лизосом за исключением ХС. Накапливаясь в большом количестве, откладывается в межклеточном пространстве, инкапсулируясь соединительной тканью, он ведёт к развитию склероза, к образованию атеросклеротических бляшек. Развитию его способствует курение, употребление алкоголя, сахарный диабет, обильная жирная пища и гипертоническая болезнь, т.е. все заболевания, которые ведут к повреждению стенок сосудов токсинами.
Гормоны
Гормоны - мобильные посредники в регуляторной системе. Термин «гормон» - от латинского «побуждать к действию».
Гормоны - это вещества, синтезирующиеся специальными железами, транспортируемые кровью и воздействующие на различные органы.
Гормоны характеризуются:
- синтезируются железами внутренней секреции;
- действуют дистантно;
- строгая специфичность действия;
- высокая биологическая активность (концентрация 10-12-10-15 моль/л).
В настоящее время установлено, что гормоны образуются во всех тканях.
Выделяют гормоны:
- с эндокринным эффектом - гормоны, синтезируемые ЖВС и поступающие в кровь;
- с паракринным эффектом - гормоны образуются в одном месте и действуют рядом;
- гормоны с аутокринным эффектом - действуют на ту ткань, где и образуются.
Для каждого гормона существует ткань-мишень. По первым представлениям, ткань-мишень - это та ткань, в которой гормоны вызывают физиологические или биохимические изменения. Например, тиреотропный гормон действует на щитовидную железу, следовательно, ткань-мишень - щитовидная железа; для инсулина - печень, мышечная ткань, жировая ткань.
По современным же представлениям, ткань-мишень - это ткань, в которой имеются рецепторы к данному гормону.
Концентрация гормонов значительно ниже, чем других БАВ, поэтому клетка-мишень должна отличить гормоны от других соединений, что осуществляется с помощью рецепторов - молекул узнавания. Связывание гормона с рецептором основано на комплиментарности какого-то участка мембраны. G+R®GR®G+R Комплекс «гормон-рецептор» может быть более активен, чем просто гормон.
Свойства рецепторов: связывают гормоны, генерируют сигналы (усиливают сигналы гормона).
Гормоны - это межклеточные регуляторы рецепторного действия (включая и гормоны и нейромедиаторы).
Классификация гормонов
Существует несколько видов классификации.
По месту образования гормонов:
1. гормоны гипоталамуса;
2. гормоны гипофиза;
3. гормоны щитовидной железы;
4. гормоны поджелудочной железы;
5. гормоны паращитовидных желез;
6. гормоны надпочечников;
7. гормоны половых желез;
8. гормоны местного действия.
По химическому строению:
1. белково-пептидные гормоны: гормоны гипоталамуса, гипофиза, поджелудочной железы, паращитовидных желез;
2. производные аминокислот: адреналин, норадреналин, тироксин, трийодтиронин;
3. стероиды: в их основе лежит структура циклопентанпергидрофенантрена, образуются из холестерина (половые гормоны, коры надпочечников).
По механизму действия (по расположению рецепторов):
1. гормоны, действующие через внутриклеточный рецептор - липофильные гормоны - стероиды и тиреоидные гормоны;
2. гормоны, действующие через рецепторы, находящиеся на поверхности клетки - гидрофильные гормоны. Они действуют через внутриклеточный посредник - мессенджер.
Гормон - первый посредник, а цАМФ, ионы Са2+, фосфатидилинозиды - вторые (чаще цАМФ, которая образуется из АДФ) посредники. [рис. цАМФ]
Механизм действия гормонов
Липофильные гормоны.
Гормон диффундирует через плазматическую мембрану и связывается внутренними рецепторами, образуется комплекс «гормон-рецептор», который активируется и действует на ДНК. G+R®GR®GR*®ДНК. В ДНК выделяют гормон-чувствительный элемент (ГЧЭ). Под его влиянием изменяется транскрипция, что влияет на деградацию мРНК. Гормоны влияют на процессинг белка. Гормоны действуют непосредственно на ДНК, активируют ферменты, стимулируя их синтез.
Гидрофильные гормоны.
Самый распространенный второй посредник - цАМФ-аденилатциклазная система. Она состоит из 2 частей: собственно аденилатциклазный компонент и протеинкиназный компонент.
В плазматической мембране находятся рецепторы 2 типов: Rs - стимулирующий и Ri - ингибирующий. Внутри мембран находится G-белок (Gs, Gi) (читается джи-белок). G-белок распадается на a и bg субъединицы, которые могут взаимодействовать между собой. a-субъединица и ГТФ действуют на аденилатциклазу, превращая ее в активную форму. Эта активная аденилатциклаза находится на внутренней поверхности ЦПМ. Под влиянием АЦ АТФ превращается в цАМФ+ФФн. Разрушается цАМФ с помощью фермента - фосфодиэстеразы.
После образования АЦ включается протеинциклазный компонент. цАМФ + протеинкиназа (фермент, вызывающий фосфорилирование других белков) ®активированая протеинкиназа. Протеинкиназа – тетрамер, содержащий 2 субъединицы R (регуляторная субъединица) и 2 субъединицы C (каталитическая субъединица). R2C2+4цАМФ«R2(4цАМФ) +2C (активная протеинкиназа). Активная протеинкиназа вызывает фосфорилирование белков.
Белок+ АТФ®(над стрелкой 2С) фосфопротеин (серин-фосфат, треонин-фосфат) +АДФ.
В результате образования фосфорилированных белков могут быть:
1. усиленный распад гликогена: фосфорилаза В®фосфорилаза А;
2. изменение транспорта ионов;
3. изменение метаболизма углеводов, липидов;
4. регулируется генная транскрипция.
Таким образом, фосфорилирование белков является важнейшим регуляторным механизмом.
Ионы Са2+.
Образуют соединение с белком - кальмодулин. Комплекс Са2+-кальмодулин активирует ферменты (аденилатциклазу, фосфодиэстеразу, Са2+-зависимую протеинкиназу). Есть группа гормонов, для которой второй посредник неизвестен - инсулин, гормон роста, пролактин.
