Глава vi трансфузионная терапия при нарушении питания
Любая травма (ранение, переломы костей, ожоги, радиационное поражение, хирургическое вмешательство) способствует выбросу в кровь кортикостероидов и адреналина. Эти вещества нарушают гомеостаз, вызывая гипергликемию, ацидоз, гиперкоагуляцию, гипераммоние-мию, гиперкалиемию, гипонатриемию [Лабори А., 1970]. Следовательно, неизбежно наступает усиление основного обмена.
Стрессовая ситуация в большей или меньшей степени характерна как для экстренной, так и для плановой хирургической патологии. Активация основного обмена усиливает распад углеводов и белков. Этому способствуют освобожденные под влиянием кислых продуктов литические ферменты, а также утилизация белков на энергетические потребности [Рябов Г. А., 1979; KrufM., PetrasekJ, 1978].
Так возникает катаболическая направленность обмена, протекающего по Moore, в виде четырех последовательных фаз: I — фаза повреждения, или адренокортико-идная, длительностью 2—4 дня, характеризующаяся выраженным катаболизмом; II—ф а за гормонального разрешения (или точка поворота), характеризуется улучшением состояния и исчезновением гормональных сдвигов (продолжается от 3 до 7 дней); III — фаза мышечной силы с преобладанием анаболизма и положительным азотистым балансом, длительностью от 2 до 5 нед; IV — фаза накопления жира, продолжающаяся несколько месяцев.
Установлено, что запаса углеводов в условиях голода хватает на 13 ч, а белков и аминокислот — только на 4—6 ч. Следовательно, после этого периода организм пострадавшего переходит на потребление собственных белков и жиров. Так, в первые 3—5 ч шокового состояния пострадавший может потерять до 100 г тканевого белка, а при глубоких обширных ожогах на покрытие азотистых и энергетических затрат ежесуточно расходуется до 500 г мышечной ткани и 250 г жира. Потеря мышечной ткани после больших операций на органах брюшной полости составляет 300—450 г. Если учесть, что в белке содержится 16% азота, т.е. 1 г азота соответствует 6,25 г белка (а в мышечной ткани белка содержится 25%), то суточные потери азота будут составлять при шоке около 80—128 г, при ожогах — около 20 г, при операциях на брюшной полости — 12 — 18г.
Наши исследования показали, что после резекции желудка больные в первые дни теряли в среднем до 17 г азота, что соответствует 106,25 г белка, или 425 г мышечной ткани [Васильев П. С. и др., 1980]. Следует учитывать, что повышение температуры тела на 1°С увеличивает обмен на 13%.
Большие потери белка отрицательно сказываются на заживлении ран, сопротивляемости организма неблагоприятным фактором и способствуют возникновению осложнений [СуджанА. В., 1973].
При тяжелых оперативных вмешательствах потери азота настолько велики, что их не удается полностью компенсировать даже при энтеральном питании [Луком-ский Г. И. и др., 1977]. Еще более тяжело они сказываются на состоянии больных и пострадавших при вынужденном голодании (травма и операции на органах желудочно-кишечного тракта).
Р. М. Гланц и Ф. Ф. Усиков (1979) различают три периода голодания человека: 1) период усилений основного ^обмена и временного повышения энергетических затрат с наибольшими суточными потерями массы тела; 2) период неуклонного постепенного понижения основного обмена и .уменьшения суточных энергетических затрат организма, „дюгда происходят мобилизация жира из жировых депо и 'Транспортировка его в печень, где он и окисляется; 3) период ^возрастания распада резервного белка, когда происходит ^неэкономное расходование пластического белка, в том числе Уу. жизненно важных органов.
|; Практически с 1-го дня голодания как для пластических Уцелей, так и для энергетического обеспечения организм ^человека утилизирует структурный белок мышц, органов, ^ферменты и гормоны. Это приводит к нарушению регуляции ^обмена веществ. Уже в 1-е сутки резко снижается синтез |альбумина в печени и других органах, что ведет к понижению [КОД и водоудерживающей функции плазмы крови. Развивается белково-волемические нарушения [Лукомский Г. И. и др., 1976]. При полном или частичном белковом голодании печень может потерять до 40% белков. В то же время в ней [ накапливается жир, ухудшая ее функциональное состояние. : В связи с белковой недостаточностью и утилизацией ' ферментов наступает дискоординация деятельности ферментных систем [Кошелев Н. Ф., 1975]. Быстро уменьшается ; активность ферментных систем, осуществляющих переами-нирование, дезаминирование и синтез аминокислот. В пече-[ ни снижается синтез мочевины, в связи с чем количество ее I почти вдвое уменьшается. Одновременно увеличивается количество аминокислот и значительно меняется аминокислотный спектр сыворотки крови [Климан-ский В. А. и др., 1979]. Понижается интенсивность окислительных процессов, в связи с чем происходит неполная утилизация распадающихся белков и жиров, изменяется кислотно-щелочное состояние. Нарушается координация | других видов обмена веществ, развиваются морфологиче-1 ские изменения в виде атрофии слизистой оболочки тонкой кишки почти до полного исчезновения ворсинок с нарушением всасывания углеводов и жиров, что приводит к появлению поноса. Продолжительная белковая недостаточность ведет к морфологическим, биохимическим и функциональным нарушениям регуляции желез внутренней секреции и других специфических функций.
Из сказанного ясно, какое важное значение в лечении больного имеет питание. Бесспорно, самым лучшим является энтеральное питание, но, как мы уже отмечали, при тяжелых стрессовых ситуациях оно недостаточно. В таком случае возникает необходимость в парентеральном питании (ПП).
Задача и цели ПП вытекают из описанного выше патогенеза голодающего организма человека, а также из патогенеза стрессовой ситуации, в которой оказался пострадавший или больной, перенесший хирургическое вмешательство. Они сводятся к применению средств ПП для пластических целей, энергетического обеспечения и стимуляции их усвоения. В более широком понимании в задачи ПП входят заместительное питание или введение цельных белков (альбумин, протеин, нативная плазма, концентрат нативной плазмы) в сосудистое русло при гипопротеинемии и устранение белково-волемических расстройств.
До недавнего времени при вынужденном голодании и необходимости вспомогательного ПП клиницисты ограничивались введением углеводов (глюкоза, реже этиловый спирт) и некоторых электролитов (натрий, калий, хлор). Достижения современной биохимии и физиологии питания вооружили клиницистов белковыми препаратами, средствами энергетического обеспечения, обосновали необходимость введения электролитов, микроэлементов, витаминов и стимуляторов усвоения средств ПП. Все это позволило изучить проблему ПП на научной основе и в то же время существенно усложнило задачи клинициста, оказывающего непосредственную помощь больному.
Краткая характеристика препаратов ПП. Основными компонентами питания являются белки, углеводы и жиры;
необходимы также электролиты, микроэлементы, витамины и стимуляторы усвоения средств питания. Ведущее место в ПП занимают белковые препараты, которые являются источниками азота. Активное внутривенное белковое питание может быть осуществлено с помощью белковых гидролизатов и сбалансированных аминокислотных смесей. С заместительной целью (восполнение цельных белков в сосудистом русле) применяются альбумин, протеин, плазма.
Препараты азотистого питания должны содержать 8 незаменимых аминокислот: изолейцин, лейцин, лизин, метионин, фенилаланин, треонин, триптофан, валин.
Отечественная промышленность выпускает три препарата гидролизатов белка.
Гидролизат казеина, разработанный в Центральном ордена Ленина институте переливания крови ^(ЦОЛИПК) и получаемый в результате кислотного гидролиза казеина, содержит 0,70—0,95% общего азота, 35—45% которого приходится на азот аминокислот. В составе его
•имеются все незаменимые аминокислоты. Кроме того, к ^препарату добавлены 0,55% хлорида натрия, 0,04% хлорида ; калия, 0,05% хлорида кальция и 0,0005% хлорида магния. t Гидролизин Л-103 получен кислотным гидроли-^зом белков крови крупного рогатого скота. Содержание ^общего и аминного азота в нем, как и во всех отечественных 1гидролизатах, примерно одинаково. К препарату добавлены ^2% глюкозы, 0,8 — 0,9% хлорида натрия и 0,02% хлорида ""кальция. Лимитирующей аминокислотой в нем является | изолейцин.
f Аминопептид — препарат, получаемый методом ^ферментативного гидролиза, не отличающийся принципи-^ально по составу от предыдущих гидролизатов. Лимитиру-^ющей аминокислотой в нем также является изолейцин. I Учреждениями службы крови и лабораториями выпуска-Нются аминокровин и другие гидролизаты. Кроме |того, начат промышленный выпуск усовершенствованных t гидролизата казеина и гидролизина. За рубежом также j производятся гидролизаты белка: аминозол (Швеция),
* минон (Финляндия), амиген (США), изовак (Франция), i ..миноплазмаль (ФРГ), альвезин (ГДР) и др.
В отделе парентерального питания ЦНИИГПК под руководством проф. П. С. Васильева разработан и апробирован в ряде ведущих клиник страны новый отечественный j аминокислотный препарат полиамин. Он представляет | собой 8% раствор смеси 13 чистых аминокислот (в их числе все незаменимые) с добавлением 50 г сорбита с содержанием азота 11,3 г/л.
Из зарубежных аминокислотных смесей широко применяются мориамин S-2, по питательной ценности близкий к полиамину, и ряд других препаратов.
Анаболический эффект препаратов белкового ПП в значительной мере зависит от обеспечения организма небелковыми энергетическими веществами. Введение источников энергии одновременно с пластическими азотистыми веществами в условиях голодания при нарушении окислительно-восстановительных и других метаболических процессов предупреждает утилизацию собственных белков организма и вводимых аминокислот по пути глюконеогене-за, т.е. «сгорания» для энергетического обеспечения. Следовательно, средства энергетического обеспечения лают азотсберегающий эффект, причем углеводы — больший, с;
жировые эмульсии — несколько меньший. К источникам энергетического обеспечения относятся углеводы, спирты г, жировые эмульсии.
Углеводы. В клинической практике применяют моносахариды (глюкоза, фруктоза). По эффективности и влиянию на организм человека наиболее распространенным препаратом остается глюкоза, применяемая для ПП в ви де 5; 10; 20; 30; 40 и 70% растворов с соответствующим количеством инсулина (1 ЕД на 3—5 г сухого вещества глюкозы).
С п и р т ы. К применяемым при ПП спиртам относятся этанол, полиолы (сорбит и ксилит), диолы (1,2-пропандиол и 1,3-бутандиол). Однако они не используются из-за худшем по сравнению с моносахаридами усвояемости, побочного токсического действия (этанол), малой изученности (диолы).
Жировые эмульсии. Высокая калорийность жира (1 г — 9 ккал) позволяет в небольшом объеме жидкости вводить значительное количество калорий. Преимущество жировых эмульсий состоит и в том, что их можно вводить в любые, в том числе периферические, вены. Наряду с азотсберегающим эффектом жировые эмульсии необходимы организму человека для синтеза фосфолипидов играющих важную роль в белковом и липидном обмене.
Практическое применение в ПП получили 10—20^' жировая эмульсия интралипид (Швеция) и липофундиь (Финляндия). Ведутся работы по получению отечественных жировых эмульсий.
Минеральные в е щ е с т в а и микроэлементы. Наряду с белками, углеводами и жирами при ПП большое значение имеют минеральные вещества: калий, натрий, кальций, фосфор, железо, магний, хлор и сера. К микроэлементам относят марганец, цинк, кобальт, молибден, йод, фтор, никель и др.
Минеральные вещества принимают участие в важнейших метаболических и физиологических процессах (реакции энергетического обмена, мышечного сокращения, окислительно-восстановительные процессы), входят в структуру клеток, в том числе крови, и мембран, участвуют в осмотических* процессах и т.п. Микроэлементы находятся в ферментных системах, гормонах и т.д.
Если ПП назначают на короткий срок (3—7 сут), в его состав целесообразно включать препараты калия, натрия, кальция, магния, хлора, фосфора и цинка. Последний содержится в ряде ферментов и способствует ускорению заживления ран. При длительном ПП целесообразно использовать все перечисленные электролиты и микроэлементы.
Витамины. Известно, что водорастворимые витамины (группы В, С и др.) участвуют в построении различных коферментов, а жирорастворимые витамины (A, D, Е, К) — в контроле функционального состояния мембран и субклеточных структур. Отсюда ясна их роль в переаминировании, декарбоксилировании и других процессах, активирующих белковый и углеводный обмен. Особенно важно применение витаминов при ПП больных с явлениями белковой недостаточности, когда выражен их большой дефицит, а метаболизм вводимых веществ требует активации анаболических процессов за счет ферментов, в состав которых входят витамины группы В, и усиления окислительно-восстановительных процессов с участием аскорбиновой кислоты.
Стимуляторы эффективности ПП. Для усиления эффекта ПП, кроме витаминов, применяются анаболические гормоны (неробол, ретаболил), андрогены, гормон роста, инсулин, некоторые пиримидиновые производные (пентоксил, метилурацил). Анаболические стерои-ды, как и андрогены, стимулируют молекулярные механизмы биосинтеза белка. Механизм действия анаболических стероидов направлен на увеличение синтеза белка из аминокислот с уменьшением их выхода в мочевину и на снижение катаболизма. Аналогично влияют и андрогены. Последние увеличивают активность ферментов в белковом обмене. Все это способствует задержке азота и накоплению белка в мышцах, усилению роста и прибавке массы тела, благоприятно влияет на репаративные процессы.
Инсулин содействует сохранению и накоплению энергетических и пластических материалов в клетке, повышая синтез основных составных ее частей — белков, гликогена и жиров. Он стимулирует синтез ключевых ферментов гликолиза, создавая тем самым предпосылки для энергетического обеспечения синтеза белка. Одновременно индуцируется образование гликогенсинтетазы, усиливающей продукцию гликогена, тормозится липолиз и стимулируется липогенез. Инсулин является сильным супрессором транса-миназ, что исключает участие аминокислот в энергетических процессах и создает возможность максимально использовать гх для биосинтеза белка.
Используемая при ПП глюкоза сама является возбудителем секреции инсулина. Существует определенный параллелизм между интенсивностью поступления глюкозы и ответной реакцией лангергансовых островков. Секрецию инсулина индуцируют и некоторые аминокислоты (аргинин, лейцин). Наличие такой связи между концентрацией глюкозы в крови и секрецией инсулина делает ненужным дополнительное введение его. Однако при стрессовых ситуациях этот механизм может нарушаться. Такие состояния сопровождаются значительным выбросом катехоламинов и резким снижением толерантности к глюкозе. В этих условиях, а также при использовании концентрированных растворов глюкозы показано введение инсулина.
Пиримидиновые производные усиливают репаративные процессы в ране, повышают антитоксическую и белоксинте-зирующую функцию печени и ограничивают катаболическую реакцию, усиливая анаболический эффект ПП.
Важную роль в усвоении средств ПП играют макро- и микроциркуляция, полноценный транспорт компонентов по сосудистому руслу и через клеточные мембраны. В этом отношении большое значение придается поддержанию объема циркулирующего альбумина.
Показания. В настоящее время показания к ПП весьма многообразны. Коротко их можно сформулировать так:
ПП применяют, если больной не может, не должен или не хочет питаться через рот.
Перечень патологических состояний, при которых используют ПП, достаточно велик. Это травмы и операции на желудочно-кишечном тракте, черепно-мозговая травма, ожоги. Хорошие результаты ПП дает при перитонитах, панкреатите, энтероколите и других заболеваниях органов брюшной полости. К ПП прибегают при некоторых психических заболеваниях. Другими словами, в тех случаях когда невозможен энтеральный путь подведения питательных веществ, можно и должно применять ПП.
Для успешного ПП важно иметь представление о суточной потребности (табл. 10). При этом необходимо соблюдать следующие условия: 1) предварительно устранить гемодинамические расстройства и восполнить внутри-сосудистый дефицит глобулярного и, главное, плазменного объема', 2) ликвидировать грубые расстройства водно-солевого обмена и кислотно-щелочного состояния; 3) восстановить функции жизненно важных органов и систем (дыхание, сердечная деятельность).
ПП может быть полным, когда в ор анизм пострадавшего или больного вводят все питате тъные вещества, неполным, когда используют только основ-
Таблица 10. Суточная потребность в калориях и белке при ряде патологических состояний [Герасимова Л. И., 1974]
| С ист on mir больно! о | OdiOBHO | 1 обмен | Потребность в fit-JIKf (J/CVT) больного f M.iccoil ir.iii 70 кг |
| % нормы | KK.l.'l /CVT | ||
| Норма | 1 800 | ||
| Температура тела °С 38 | |||
| 2 150 | |||
| Послеоперационный период: | |||
| операции в верхней половине брюшной полости тяжелые операции | 115 130 | 2 100 2350 | 110 140 |
| Постравматические состоя | |||
| ния: | |||
| тяжелые ожоги | |||
| сотрясение мозга ушиб мозга | 185 300 | 3300 5400 | |
| столбняк |
ные питательные вещества (белки или белки и углеводы, или белки, углеводы и жиры), и вспомогательным, когда питание через рот недостаточно и его нужно дополнить отдельными веществами (белки, белки и углеводы в неполной дозировке).
Расчет потребности в средствах ПП и методика его ведения. Наиболее важное значение имеет азотистый, т.е. белковый компонент, поэтому расчеты начинают с определения индивидуальной потребности в азотистых веществах. Эта потребность зависит от величины эндогенного катаболизма (НЭ), т. е количества азота мочи, выделившегося при безазотистой диете, и степени использования азота вводимого препарата, определяемой по формуле Митчелла:
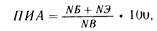
где ПИЛ — показатель использования азота, или показатель усвоения азота, или показатель истинного использования белка, %; НЭ — эндогенный катаболизм; НБ азотистый баланс, или разность введенного и выведенного азота за сутки; НВ — азот, выведенный за сутки.
К более простым методам относится расчет, при котором исходят из средней суточной потребности больного и здорового человека. Установлено, что в течение суток здоровый взрослый человек нуждается в среднем в 0,7—1 ;
условного белка на 1 кг массы тела, дети — 2,5 г на 1 ю массы тела. Потребность больных при легких и средне ii тяжести операциях соответствует потребности здорового человека. При более тяжелых операциях она увеличивается до 1,5—2 г на 1 кг массы тела.
Зная эти данные и содержание азота в препарате. нетрудно вычислить потребность больного в количестве препарата. Например, взрослому человеку с массой тело 70 кг, имеющему повреждение органов брюшной полости вследствие травмы или операции, при суточной потребности 1,5 г условного белка на 1 кг массы тела требуется 1,5х70=105 г белка. Если предполагается инфузия полиамина (1,13 г азота в 100мл), то, умножив 1,13 г на 6,25 (коэффициент пересчета азота в белок), получим 7,125 г условного белка в 1W мл. Тогда количество полиамина составит
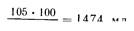
7,125 ' " ' "'"""
Аналогично производится расчет гидролизата казеина с примерным содержанием общего азота 0,8 г в 100 мл, что соответствует 5 г условного белка:
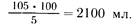
Известен расчет по количеству мочевины. Учитывая, что в среднем 80% общего азота мочи составляет азот мочевины, можно подсчитать потерю азота с мочой (через почки выделяется 85%, с потом и через кишечник — 15% всего азота). Известно, что 1 г мочевины содержит 0,466 г азота. Зная суточное количество мочевины в моче, можно вычислить потерю азота: количество мочевины мочи в сутки, умноженное на 0,466, равно количеству азота мочевины. Например, больной выделил за сутки 30 г мочевины, тогда 30 • 0,466= 14 г азота, но это только 80% общего азота мочи, а 100% будет составлять (14 • 100):80=17,5 азота. В переводе на условный белок это составит 17,5 • 6,25 =109,4 г. С учетом приведенных выше расчетов полиамина потребуется (109,4 • 100):7,125= 1530 мл, а гидролизата казеина — соответственно 2183 мл.
Следует отметить, что в гидролизатах для пластических целей быстро утилизуется только азот аминокислот, т.е. 45—50% от общего азота препарата, что значительно снижает эффективность ПП гидролизатами по сравнению с аминокислотными смесями. Так, расчеты показывают, что в 100 мл гидролизата казеина содержание условного белка из аминокислот 2,5 г, в полиамине — выше 7 г, что почти в 3 раза больше. Следовательно, для пластических целей полиамина надо вводить почти в 3 раза меньше.
Таким образом, для расчетов нужно знать количество азота или условного белка в препарате. Хотя последние два метода не отличаются идеальной точностью и, кроме массы тела, не отражают других индивидуальных особенностей больного, которые могут повлиять на потребности в препарате, в практике ПП их легче использовать для расчета, можно применять в любом лечебном учреждении.
Основываясь на формуле Митчелла, Р. М. Гланц и ф. Ф. Усиков (1973, 1979) предложили формулу для определения количества трансфуз ионной азотистой среды:
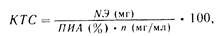
где К ТС — количество трансфузионной среды, мл; п — содержание азота, мг в 1 мл препарата.
Поскольку определение эндогенного азота практически очень сложно, авторы разработали метод определения эндогенного катаболизма с учетом величины основного обмена.
N3--Q ' К,
где О — величина основного обмена больного в килокалориях;А' — коэффициент пересчета основного обмена в эндогенный катаболизм; НЭ — эндогенный катаболизм (азота), мг.
Коэффициенты пересчета получены авторами для конкретных трансфуз ионных программ (гидролизат-+-витамины + инсулин; гидролизат -+- витамины + инсулин 4- анабо-лический стероид), что ограничивает их применение при использовании других сред парентерального питания.
Максимальное и целенаправленное усвоение азотистых веществ возможно при условии достаточного энергетического обеспечения. Потребность здорового человека в энергетических веществах составляет в среднем 25—30 ккал на 1 кг массы тела в сутки, пострадавших и больных после операции — 35—40 ккал и более. Так, больному с массой тела 70кг нужно ввести 70х40=2800 ккал в сутки. Зная калорийность препарата и потребность в калориях, нетрудно рассчитать количество сухого вещества и выбрать концентрацию его раствора, которая оказалась бы применимой по действию на организм больного и по количеству вводимое, жидкости.
Другой способ расчета потребности в энергетические веществах заключается в использовании отношения калории к количеству потребляемого азота в граммах. Оно должш составлять 150—200:1. Тогда в приведенном примере больному с массой тела 70 кг и потребностью в 1,5 г услов ного белка на 1 кг нужно ввести 105 г белка, что соответствует 16,8 г азота. Следовательно, соотношение калорий и азота 2800:16,8=170 ккал на 1 г азота, что соответствует допустимым пределам.
Мы уже отмечали, что в настоящее время наилучшие средством энергетического обеспечения признана глюкоза Это объясняется большой потребностью в ней тканей и хорошей усвояемостью (минимальная суточная потребность около 180 г; при травмах и регенеративных процессах она может возрастать вдвое). Глюкоза является исходные компонентом синтеза РНК и способствует интенсивному включению аминокислот в тканевые белки.
Введение глюкозы со скоростью выше 0,5г/кгхч повышает ее содержание в крови до 8,2—9,9 ммоль/л, что является почечным порогом, выше которого наступает глюкозурия и осмотический диурез. Кроме того, в 1—2-й день послеоперационного периода и при других стрессах в адренокортикоидной фазе катаболизма нарушается усвоение глюкозы и уменьшается чувствительность ее к инсулину. В эти дни даже при введении 0,25 г на 1 кг массы тела в час может возникнуть глюкозурия. Нередко комбинируют глюкозу с фруктозой, спиртами (этанолом, полиолы). В виде гипертонических растворов (10; 20; 30; 50 и 70%) ее применяют при введении только в центральные вены во избежание возникновения флебитов.
Наши исследования показали, что введение 30% раствора глюкозы с инсулином не вызывает осложнений. У ряда пожилых больных в адренокортикоидной фазе при превышении почечного порога и возникновении глюкозурии мы в первые 2 дня после операционного периода концентрацию глюкозы снижали до 10—20%.
Общее количество глюкозы, вводимое разными исследователями, составляет от 100 до 750 г сухого вещества. количество глюкозы, обеспечивающее менее. 20% общей калорийности (около 100 г сухого вещества), вводить нельзя, так как наступает усиление катаболизма, изменения метаболизма азотистых веществ в направлении глюконеогенеза и может возникнуть кетоз. Оптимальным является покрытие
г-; 50% энергетического обеспечения за счет глюкозы. При
Применении Д0% раствора глюкозы эта величина составляет .1—1,5л.
Кроме глюкозы, применяют жировые эмульсии; они не вызывают полиурии, 'не наступает их потеря с мочой и калом. Временная гиперлипемия, возникающая после введения эмульсии, быстро исчезает. Необходимость введения жировых эмульсий, их азотсберегающий эффект, участие в стимуляции обменных процессов в настоящее время доказаны. Липиды являются составными частями клетки, входят в состав биологических мембран, поэтому потеря их при ^голодании отрицательно сказывается на обменных про-• цессах.
Необходимо энергетическое обеспечение жировыми эмульсиями от 30 до 40% общей калорийности, что достигается применением 10—20% жировых эмульсий в объеме 0,5—1 л.
Известно, что соотношение основных компонентов питания (белки, углеводы, жиры) у здоровых людей колеблется в различных территориальных регионах. Наиболее распространено следующее распределение по калорийности: белки— 10—15%, углеводы— около 50%, жиры— 35—40% общей калорийности. Примерно те же соотношения целесообразны при ПП.
Составление программы ПП можно показать на примере трансфузионной терапии после резекции желудка. Белковый компонент ПП назначается по 1 г условного белка на 1 кг массы тела. Больному с массой тела 70 кг полиамина, содержащего, как мы рассчитали выше, 7,125 г условного белка в 100 мл, потребляется:
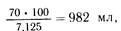
т.е. около 1 л. Однако 1 л полиамина содержит 11,3 г азота.Умножив 11,3 на 200 (отношение азота к количеству небелковых калорий), получим 2260 ккал, из которых 50% должны составлять углеводы (глюкоза), от 10 до 15% — белки и от 35 до 40% — жировые эмульсии. Следовательно, глюкоза должна обеспечить 2260:2= 1130 ккал. Известно, что 1 г глюкозы— это 4,1 ккал. Разделив 1130 на 4,1, получим количество сухого вещества глюкозы — 275,6 г. Если применить 30% раствор, то объем глюкозы будет оавен:
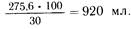
В 1 л полиамина условного белка содержится 11,3 х 6,25 =70,6 г, что составит 70,6х5,3 =374 ккал (5,3 ккал содержит 1 г белка), а 374 ккал по отношению к 2260 составляют 12,1%. Следовательно, на долю жировых эмульсий остается 50—12,1 =37,9%, т. е.
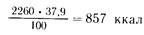
1 г жира обеспечивает 9 ккал, поэтому чистого жира потребуется 857:9=95 г. Следовательно, 10% жировой эмульсии необходимо 950 мл, т.е. около 1 л, а 20% — 500 мл.
Остается рассчитать общее количество жидкости:
полиамина 1 л, 30% раствора глюкозы 920 мл и 10 % жировой эмульсии 1 л, всего 2 л 920 мл, что является оптимальным количеством. Для непродолжительного ПП (3 сут) можно ограничиться предложенной программой неполного ПП.
Кроме указанных расчетов, проводятся расчеты на основе массы и площади поверхности тела (табл. 11).
Таблица 11. Суточные дозы и оптимальная скорость введения некоторых препаратов ПП [Глущенко Э. В., 1974]
| Суточн | ая доча | Оптималы | ая скорость | |
| введения | ||||
| На.жание препарат;] | ||||
| [ 11,4 1 КГ | i на 1 м'' | Г/ ( КГ • Ч) | г/(м2 • ч) | |
| массы теча | поверхности | |||
| тела | ||||
| Глюкоза Фруктоза | 2-6 | 100—300 40 | 0.5 0.4 | 20 17 |
| Спирт этиловый | 0,1 | |||
| Белок (условный) Аминокислоты Общий азот Жиры | 1-2 0,16 0-1,5 | 40—80 30 7 70 | 0,1 0,15 0,02 0,2 | 4 6 0 8 |
Кроме перечисленных компонентов, для полного ПП необходимы минеральные вещества, витамины и стимуляторы эффективности ПП.
Учитывая, что водно-электролитный баланс подробно описан в литературе по хирургии, мы ограничимся приведением потребностей в указанных средствах и прописи препаратов (табл. 12, 13).
Многие исследователи не без основания считают, что в подключичную вену, куда вводятся компоненты ПП, нецелесообразно вводить другие лекарственные средства.
Таблица 12. Потребность в компонентах полного ПП больных и пострадавших [Schenkin A., Wretlind A., 1978]
| Потребность на | 1 кг массы тела взрослого человека в сутки | |
| Компоненты ПП ————————————г-д.ти здоровых | для больных в со- | для тяжело боль |
| и больных в со | ных и пострадав | |
| стоянии умеренной | 'тяжести и постра | ших |
| тяжести | давших | |
| Вода, мл 30 | 100-150 | |
| Энергетическое обеспечение, ккал 30 | 35—40 | 50—60 |
| Азот аминокислот, мг 90 | Г) 9 Л Ч U,^——V.J | 0 л п ^ U.^t——u,l> |
| 1 люкоза, г 2. | ||
| w ч п г о /1\ир, г z | ч <J | Ч 4 о— ^ |
| Натрий, ммоль 1—1,4 | 9 3 ^ <J | 3—4 |
| Калий, ммоль 0,7—0,9 | Ч 4 J—— Ч | |
| Кальций, ммоль 0,11 | 0,15 | 0,2 |
| Магний, ммоль 0,04 | П i к п 90 U, 1 0——u.ZU | п ч (\ л U,0——V,' |
| Железо, мкмоль 0,25—1,0 | ||
| ЛЛарганец, мкмоль 0,1 | Г) Ч u,o | 0,6 |
| Цинк, мкмоль 0,7 | 0,7—1,5 | 1,5—3,0 |
| Медь, мкмоль 0,07 | 0,3—0,4 | 0,4—1,0 |
| Хром, мкмоль 0,015 | ||
| Селен, мкмоль 0,006 | ||
| Молибден, мкмоль 0,003 | ||
| Хлор, ммоль 1,3—1,9 | 9 Ч L——0 | |
| Фосфор, ммоль 0,15 | 0,4 | 0,6—1,0 |
| Фтор, мкмоль 0,7 | 0,7—1,5 | |
| Йод, мкмоль 0,015 | — |
Введение средств ПП надо начинать с 30% раствора глюкозы, к которому добавлен инсулин из расчета 1 ЕД на 5 г сухого вещества глюкозы. Если содержание сахара в крови превышает «почечный порог» (99 ммоль/л) и наблюдается глюкозурия, то дозу инсулина увеличивают до 1 ЕД на 4 г или даже на 3 г сухого вещества глюкозы. После введения 200—300 мл раствора глюкозы в одноразовую систему через прокол резиновой трубки перед канюлей, соединяющей систему с подключичным катетером, начинают вводить аминокислотный препарат или гидролизат. В дальнейшем аминокислотную смесь или гидролизат вводят вместе с глюкозой. К раствору глюкозы добавляют электролиты и витамины.
Таблица 13. Потребность в витаминах при полном ПП больных и пострадавших [Schenkin A., Wretlind A., 1978]
| Витамины —————————————г для :<дировы\ и больных в состоянии умеренной | для больных в состоянии сред- | )c.'iuro человека для тяжелобольных |
| Тиамин, мг 0,02 Рибофлавин, мг 0,03 Никотянамид, мг 0,2 | 0,04 0,06 0,4 | 0,3 0,3 2 |
| Пиридоксин, мг 0,03 Фолиевая кислота, мкг 3 | 0,06 | 0,4 |
| Цианкобаламин, мкг 0,03 Пантотеновая кисло | 6 0,06 | 6—9 0,06 |
| та, мг 0,2 Биотин, мкг 5 | 0,4 | 0,4 |
| Аскорбиновая кисло | ||
| та, мг 0,5 Ретинол, мкг 10 Эргокальциферол, мкг 0,04 | 2 10 0,04 | 25 20 0,1 |
Скорость введения аминокислотных смесей и гидролиза-тов находится в обратной зависимости от усвоения препарата, т.е. чем выше скорость, тем меньше его усвояемость. Аминокислотные смеси и гидролизаты целесообразно вводить со скоростью не больше 40 капель в минуту. Скорость введения глюкозы — 0,5 г сухого вещества на 1 кг массы тела в час. Практически больному с массой тела 70 кг 30% раствор глюкозы можно вводить со скоростью 40 капель в минуту.
Жировые эмульсии вводят вместе с аминокислотными смесями или гидролизатами. Их нельзя вводить вместе с электролитами, так как последние способствуют укрупнению жировых частиц, что создает опасность жировой эмболии. Если азотистый препарат содержит много электролитов, то жировые эмульсии надо вводить отдельно. В 1-й день следует вводить половину или четвертую часть дозы жировой эмульсии для проверки на реактогенность, а начиная со 2-го дня — всю суточную дозу. Вначале скорость вливания должна быть 10 капель в минуту. Через полчаса ее можно увеличить до 15 капель в минуту. При этой скорости меньше опасность аллергических, пирогенных и токсических реакций. При отсутствии реакции скорость можно увеличить до 20—30 капель в минуту. На каждые 500 мл жировой эмульсии вводят 5000 ЕД гепарина.
Для стимуляции эффекта ПП, кроме витаминов и инсулина, надо применять анаболические стероиды (5% раствор ретаболила по 2 мл внутримышечно 1 раз в 3—5 дней).
На примере приведенного выше расчета для больного с массой тела 70 кг, перенесшего резекцию желудка, составим график введения препаратов с указанием их прописей (табл. 14). При введении препаратов ПП необходимо постоянно следить за капельницей, так как при неравномерном уменьшении количества препарата во флаконах (особенно /это касается препаратов, которые вводят с различной скоростью, например полиамина и интралипида) число капель в минуту меняется.
Методыконтроля эффективности ПП. Такие методы многочисленны и все еще трудоемки. Их можно разделить на клинические и лабораторные. К первым относятся: 1) определенные массы тела (взвешивание); 2) исследование гемо-динамики (частота сердечных сокращений, артериальное и центральное венозное давление); 3) определение почасового диуреза; 4) оценка общего состояния больного в процессе ПП.
Лабораторная диагностика предусматривает определение следующих показателей: 1) коллоидно-осмотического давления (ежедневно); 2) гематокрита (ежедневно); 3) инкремента мочевины ежедневно (разница мочевины крови до и через 40 минут после введения; чем меньше разница, тем выше анаболическая эффективность белкового препарата);
4) гемоглобина (1 раз в 2—3 дня); 5) ОЦК и его компонентов (1 раз в 2—3 дня); 6) кислотно-щелочного состояния (ежедневно); 7) мочевины мочи (суточное количество) ежедневно.
Для контроля за функциональным состоянием органов и систем необходимы также определение содержания билиру-бина, трансаминаз, состояния свертывающей системы и другие общепринятые лабораторные исследования.
Большинство перечисленных методов контроля можно применять в хорошо оснащенных стационарах.
Для оценки возможной гипергидратации или дегидратации можно использовать следующую формулу:
