Гилберт Г. Дэниеле, Джозеф Б. Мартин (Gilbert H. Daniels, Joseph В. Martin)
Гипофиз, по праву называемый главной железой, продуцирует шесть основных гормонов и, кроме того, служит хранилищем еще двух. Гормон роста (ГР) регулирует рост и оказывает существенное влияние на межуточный обмен (см. гл. 322). Пролактин (ПРЛ) необходим для лактации. Лютеинизирующий (Л Г) и фолликулостимулирующий (ФСГ) гормоны контролируют активность половых желез у мужчин и женщин. Тиреотропный гормон (ТТГ, тиреотропин) регулирует функцию щитовидной железы. Адренокортикотропный гормон (АКТГ) определяет глюкокортикоидную функцию коры надпочечников. Все эти гормоны синтезируются в передней доле гипофиза. Антидиуретический гормон (аргинин-вазопрессин, АВП) и окситоцин продуцируются нейронами гипоталамуса и запасаются в задней доле гипофиза (см. гл. 323). АВП контролирует задержку воды в почках; окситоцин необходим для отделения молока во время лактации (рис. 321-1).
Между передней долей гипофиза и тремя его железами-мишенями — гонадами, корой надпочечников и щитовидной железой существуют важнейшие обратные связи. При недостаточности или удалении гонад возрастают концентрации ЛГ и ФСГ. Это состояние известно как первичный гипогонадизм. При удалении или разрушении коры надпочечников возникает первичная надпочечниковая недостаточность (или аддисонова болезнь) и в сыворотке крови повышается концентрация АКТГ. Недостаточность щитовидной железы (первичный гипотиреоз) характеризуется повышенной концентрацией ТТГ.
При разрушении или удалении гипофиза исчезновение тропных гормонов приводит к вторичным гипогонадизму, надпочечниковой недостаточности и гипотиреозу. Выпадают также 4)ункции гормона роста и пролактина. Антидиуретическая и окситоцпновые функции при разрушении гипофиза не меняются, если только не затронуты места их образования в гипоталамусе.
Гипофиз в свою очередь находится под контролем гипоталамуса, который вырабатывает ряд химических посредников (гормонов). Эти гормоны синтезируются в гипоталамусе и поступают в систему портальных сосудов и по ним через ножку гипофиза — в его переднюю долю (см. рис. 321-1). При перерезке ножки гипофиза секреция ГР, ЛГ, ФСГ, ТТГ и АКТГ снижалась. Это позволило сделать вывод, что для секреции этих гормонов необходимо стимулирующее влияние гипоталамуса. В отличие от этого уровень пролактина после перерезки ножки гипофиза возрастает, свидетельствуя о том, что в норме гипоталамус оказывает на секрецию пролактина тоническое ингибирующее влияние. Повышенная секреция пролактина указывает также на то, что перерезка ножки не приводит к атрофии гипофиза. Если такая перерезка производится не слишком высоко, секреция АВП и окситоцина продолжается главным образом из аксонов, заканчивающихся в срединном возвышении гипоталамуса. При удалении гипоталамуса снижаются уровни ГР, ЛГ, ФСГ, ТТГ, АКТГ, АВП и окситоцина, но содержание пролактина в плазме увеличивается (см. рис. 321-1).
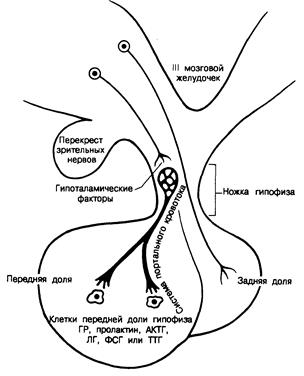
Рис. 321-1. Связь между гипоталамусом и гипофизом (см. в тексте).
В большинстве случаев гипоталамический контроль секреции гипофизарных гормонов осуществляется пептидами (табл. 321-1). Рилизинг-гормон гормона роста (ГРГ) оказывает преобладающее влияние на секрецию ГР; кроме того, на секрецию ГР ингибиторное действие оказывает соматостатин. Хотя уровни ЛГ и ФСГ в физиологических условиях колеблются независимо друг от друга, основную роль в регуляции их секреции играет один и тот же рилизинг-гормон [рилизинг-гормон лютеинизирующего гормона (ЛГРГ), называемый также гонадотропин-рилизинг-гормоном (ГнРГ)]. Тиреотропин-рилизинг-гормон (ТРГ) контролирует секрецию ТТГ и может влиять на секрецию пролактина, а кортикотропин-рилизинг-гормон (КРГ) контролирует секрецию АКТГ. Кроме того, в качестве пролактинингибирующего фактора (ПИФ) выступает дофамин.
Опухоли гипофиза могут приводить как к повышению, так и к снижению продукции его гормонов или механически сдавливать соседние структуры. Наиболее часто опухоли гипофиза продуцируют пролактин и ГР — два гормона, для которых не существует простых ингибирующих петель обратной связи с органами-мишенями. Избыток пролактина ведет к галакторее и/или гипогонадизму, а избыток ГР — к гигантизму и акромегалии. АКТГ-секретирующие опухоли обусловливают болезнь Кушинга, ТТГ-секретирующие служат редкой причиной гипертиреоза. Парадоксально, но опухоли, продуцирующие гонадотропины, чаще всего приводят к гипогонадизму. Большие гипофизарные опухоли, сдавливая нормальную железистую ткань или ножку гипофиза, могут вызывать частичный или полный гипопитуитаризм и сопровождаются нарушениями зрительных полей вследствие сдавления перекреста зрительных нервов и другими неврологическими нарушениями, связанными с инвазией опухоли в кавернозные синусы или мозговые структуры.
Поражения гипоталамуса могут вызывать гипопитуитаризм с повышенной секрецией пролактина. Недостаточность АВП, приводящая к несахарному диабету, всегда указывает на поражение гипоталамуса или высокое повреждение ножки гипофиза. При повреждении гипоталамуса могут отмечаться также нарушения чувства жажды, температурной регуляции, аппетита и артериального давления. Крупные новообразования в гипоталамусе вызывают нарушения зрительных полей, закупорку III мозгового желудочка и могут проникать в соседнюю мозговую ткань.
Таблица 321-1. Гипофизарные и гипофизотропные гормоны
| Гипофизарный гормон | Гипофизотропные гормоны | |
| название | структура | |
| Тиреотропин (ТТГ) | Тиреотропин-рилизинг-гормон (ТРГ) | Трипептид |
| Адренокортикотропин (АКТГ) | Кортикотропин-рилизинг-гормон (КРГ) | 41 аминокислота |
| Лютеинизирующий гормон (ЛГ) | Рилизинг-гормон лютеинизирующего гормона (ЛГРГ) | Декапептид |
| Фолликулостимулирующий гормон (ФСГ) | ЛГРГ | Декапептид |
| Гормон роста (ГР) | Рилизинг-гормон гормона роста (ГРГ) Рилизингибирующий гормон гормона роста' (соматостатин, СРИФ) | 44 аминокислоты 14 аминокислот |
| Пролактин | Рилизингибирующий фактор пролактина (ПИФ) Пролактин-рилизинг фактор (ПРФ)2 | Дофамин Пептид ? Вазоактивный интестинальный полипептид (ВИП) |
1 Соматостатин ингибирует также стимулируемую ТРГ секрецию ТТГ.
2 Секрецию пролактина стимулирует и ТРГ.
Анатомия и эмбриология
Питуитарная железа (гипофиз) расположена в турецком седле основной кости в основании черепа и состоит из передней (аденогипофиз) и задней (нейрогипофиз) долей. Промежуточная доля у человека рудиментарна. В норме масса гипофиза составляет 0,5—0,91
От мозга гипофиз отделяет диафрагма турецкого седла, являющаяся выростом твердой мозговой оболочки, а от сфеноидального синуса спереди и снизу — тонкий слой кости. Латеральные стенки турецкого седла примыкают к кавернозным синусам, где проходят внутренние сонные артерии, а также III, IV, V и VI пары черепных нервов. Несколько кпереди от ножки гипофиза тотчас над диафрагмой турецкого седла расположен перекрест зрительных нервов. Поэтому опухоли гипофиза могут сопровождаться нарушением полей зрения, параличом черепных нервов или прорастанием в сфеноидальные синусы (рис. 321 -2 и 321 -3).
Гипоталамус занимает пространство, спереди ограниченное перекрестом зрительных нервов, а сзади включающее сосковидные тельца. Сверху гипоталамус отделяется от мозгового бугра (таламуса) бороздой III желудочка. Округлое нижнее основание гипоталамуса образует серый бугор. Центральная часть основания (называемая воронкой, или срединным возвышением) образует дно III желудочка (см. рис. 321-3) и продолжается вниз, образуя ножку гипофиза. Рилизинг-факторы синтезируются в нейронах, лежащих по краям III желудочка, волокна которых оканчиваются в срединном возвышении по соседству с капиллярами портальной системы.
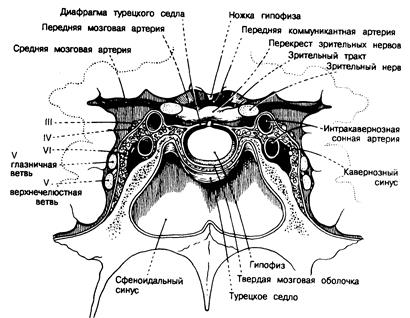
Рис. 321-2. Соотношения между гипофизом, черепными нервами и кавернозными синусами. Вид снизу. (Из J. А. Тагеп, — In: R. С. Schneider et al. (eds). Correlative Neurosm-serv 3d ed, Springfield, 111., Charles C. Thomas, 1982.)
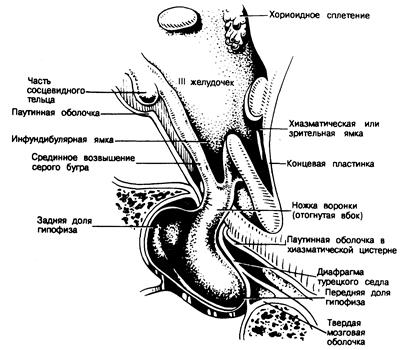
Рис. 321-3. Сагиттальный разрез через гипоталамо-гипофизарный комплекс человека Показаны анатомические соотношения между перекрестом зрительных нервов и ножкой гинойиза (Из Reichlin in: Post et al.) '
Клеточные тела супраоптических и паравентрикулярных ядер гипоталамуса продуцируют вазопрессин и окситоцин, которые по аксонам нервов супраоптикогипофизарного и паравентрикулогинофизарного трактов попадают в заднюю долю гипофиза.
Связь гипоталамуса с передней долей гипофиза имеет химическую, а не физическую природу. Образуемые гипоталамическими нейронами рилизинг-факторы попадают в переднюю долю гипофиза через портальную систему и стимулируют или ингибируют продукцию гипофизарных гормонов. Некоторые нейроны, содержащие вазопрессин, оканчиваются и в срединном возвышении, причем вазопрессин может стимулировать секрецию АКТГ и ГР.
Кровоток через переднюю долю гипофиза (0,8 мл/г в 1 мин) выше, чем через любой другой орган тела. Передняя доля снабжается кровью кружным путем через гипоталамус. Две ветви внутренних сонных артерий — верхние гипофизарные артерии (ВГА) разделяются в субарахноидальном пространстве вокруг ножки гипофиза и образуют капиллярную сеть в срединном возвышении. Эндотелий этих капилляров фенестрирован и легко пропускает гипоталамические рилизинг-гормоны. Перенос веществ из капилляров в срединное возвышение также происходит беспрепятственно, поскольку оно расположено вне гематоэнцефалического барьера. Затем капилляры сливаются, образуя 6—10 прямых вен, которые и называют гипоталамо-гипофизарной портальной системой. Эти вены играют основную роль в снабжении передней доли гипофиза кровью и питательными веществами, равно как и информацией из гипоталамуса. Небольшая часть артериальной крови приносится в переднюю долю гипофиза трабекулярными ветвями ВГА. Задняя доля гипофиза получает всю кровь из нижних гипофизарных артерий.
Передняя доля гипофиза образуется преимущественно из латеральной стенки кармана Ратке — эмбрионального выпячивания задней стенки ротовой полости зародыша. Пролиферируя, карман Ратке сливается с распространяющимся книзу дивертикулом дна III желудочка, который образует заднюю долю гипофиза.
Карман Ратке закрывается растущими долями гипофиза, и впоследствии от него остается в железе тонкая щель (щель Ратке). Это небольшое пространство может сохраняться в виде кисты, выстланной кубическим или цилиндрическим эпителием. Поскольку в процессе своего роста гипофиз поворачивается, такие кисты располагаются обычно над ним. Рост и пролиферация этих кист может привести к образованию краниофарингиом — опухолей, занимающих, как правило, супраселлярное положение. Развивающаяся основная кость отделяет гипофиз от ротовой полости. Внутри или ниже основной кости могут сохраняться остатки гипофиза, называемые глоточными гипофизами. Эти остатки могут продуцировать гипофизарные гормоны и иногда перерождаются в опухоли.
Клетки передней доли гипофиза, подразделяющиеся на пять типов, секретируют шесть разных гормонов: лактотрофы — пролактин, соматотрофы — ГР, гонадотрофы — ЛГ и ФСГ, тиреотрофы — ТТГ и кортикотрофы — АКТГ.
Пролактин
Физиология. В норме на долю лактотрофов приходится 10—25% клеток гипофиза, а во время беременности их число достигает 70%. Ген пролактина, располагающийся на 6-й хромосоме, кодирует молекулу предшественника, большую по размерам, чем выделяющийся в кровь гормон. Преобладающая форма окончательного гормона содержит 198 аминокислотных остатков (мол. масса 23 000) в одной цепи, имеющей три дисульфидных мостика. В крови здоровых людей и в большем количестве у больных с аденомами гипофиза могут присутствовать и формы пролактина с более высокой мол. массой, вплоть до 100 000 («большой» и «большой-большой» пролактин). Эти формы обнаруживаются при иммунологическом определении пролактина, но не обладают нормальной биологической активностью.
Пролактин необходим для лактации. У человека его рецепторы локализуются в молочных железах и гонадах, но у животных они найдены во многих тканях. У грызунов пролактин способствует развитию рака молочной железы, но у человека такая зависимость не установлена (см.гл. 295).
Возрастающая при беременности продукция плацентарных эстрогенов стимулирует рост и размножение лактотрофов гипофиза и приводит к повышению секреции пролактина. Во время нормальной беременности размеры гипофиза увеличиваются вдвое, а после родов возвращаются к исходным. Секреция пролактина во время беременности подготавливает молочные железы к послеродовой лактации. Эстрогены ингибируют действие пролактина на молочные железы, так что до послеродового снижения уровня эстрогенов лактация не начинается.
У плода, начиная примерно с 25-недельного возраста, уровень пролактина увеличивается, вероятно, в результате переноса к плоду материнских эстрогенов, стимулирующих фетальный гипофиз. После рождения содержание пролактина быстро уменьшается, достигая минимума к 2—4-недельному возрасту. В амниотической жидкости содержится большое количество пролактина, но откуда он попадает сюда и какова его функциональная роль здесь — неизвестно.
В нормальных условиях секреция пролактина передней долей гипофиза «сдерживается» гипоталамусом. При разрушении гипоталамуса или перерезке ножки гипофиза секреция пролактина увеличивается, и его концентрация в сыворотке крови возрастает. Роль гипоталамического ингибирующего фактора играет, по-видимому, дофамин, хотя описаны ингибирующие факторы и пептидной природы. Главным местом синтеза дофамина в гипоталамусе является дугообразное ядро. Дофамин спускается по аксонам к нервным окончаниям в срединном возвышении, где и высвобождается (тубероинфундибулярная дофаминовая система). Затем он проникает в портальную систему и достигает передней доли гипофиза, ингибируя секрецию пролактина. Внутривенное введение дофамина (2 мкг/мин на 1 кг массы тела) или пероральный прием его предшественников (например, леводопа) или агонистов (например, бромкриптин) ингибирует секрецию пролактина. Увеличение уровня пролактина в крови, по-видимому, стимулирует гипоталамическую продукцию дофамина, что в свою очередь частично снижает секрецию пролактина через «короткую» петлю механизма обратной связи.
Возрастание секреции пролактина во время кормления грудью требует, очевидно, действия пролактин-рилизинг-фактора, который пока еще окончательно не идентифицирован. Им может быть вазоактивный интестинальный пептид (ВИП), так как он является мощным стимулятором секреции пролактина. Индуцируемое грудным кормлением повышение секреции пролактина блокируется антагонистами серотонина, такими как метизергид, что свидетельствуете влиянии серотонина на секрецию пролактина. Мощным стимулятором секреции пролактина является и ТРГ. Действительно, наименьшая доза ТРГ, способная стимулировать секрецию ТТГ, одновременно стимулирует и секрецию пролактина. Однако в большинстве физиологических ситуаций секреция ТТГ и пролактина контролируется независимо друг от друга: лактация не приводит к повышению секреции ТТГ, а первичный гипотиреоз редко сопровождается избыточной продукцией пролактина.
Концентрация пролактина повышается во время сна. Этот феномен предполагает существование в гипоталамусе входа для влияний высших центров. Секрецию пролактина, индуцируемую стрессом, можно заблокировать антагонистами опиатов, такими как налоксон, и она опосредуется, вероятно, эндогенными опиоидами. Действительно, морфин стимулирует секрецию пролактина, что может объяснять аменорею, встречающуюся у наркоманок, но на базальную секрецию пролактина антагонисты опиатов не влияют.
Гиперпролактинемия. Клинические проявлния. Избыток пролактина (гиперпролактинемия) сопровождается гипогонадизмом и/или галактореей и может быть важным признаком наличия аденомы гипофиза или поражения гипоталамуса. У 10_40% женщин с аменореей отмечается гиперпролактинемия, а у 30% женщин с аменореей и галактореей имеются пролактинсекретирующие опухоли гипофиза.
Гипогонадизм, связанный с гиперпролактинемией, обусловлен, по-видимому, ингибированием гипоталамической секреции ЛГРГ, что приводит к снижению секреции ЛГ и ФСГ. Этот функциональный гипогонадизм можно рассматривать отчасти как физиологический (адаптивный) механизм, так как кормление грудью сопровождается снижением фертильности и более поздним возобновлением менструаций. В целом, чем выше уровень пролактина в плазме, тем больше вероятность аменореи. При менее выраженной гиперпролактинемии у женщин отмечается нерегулярность менструаций или бесплодие из-за укороченной лютеальной фазы цикла. Недостаточность эстрогенов, сопровождающая гиперпролактинемию, может привести к остеопорозу.
У мужчин избыток пролактина вызывает импотенцию и бесплодие. По данным ряда исследований, гиперпролактинемия обнаруживается у 8% мужчин с импотенцией и у 5% бесплодных мужчин. При повышении уровня пролактина содержание ФСГ и ЛГ у мужчин снижается, концентрация тестостерона у них также часто снижается.
Галакторея, определяемая как выделение молока вне связи с послеродовым периодом, наблюдается у 30—90% женщин с гиперпролактинемией (см. гл. 332). Различия в частоте встречаемости этого признака отчасти объясняют разницей в тщательности опроса больных. Галакторея может встречаться и в отсутствие гиперпролактинемии, особенно у рожавших женщин. Тем не менее галакторея зачастую служит важным указанием на избыток пролактина. При сочетании галактореи с аменореей гиперпролактинемия имеется у 75% женщин. У мужчин гиперпролактинемия редко вызывает гинекомастию или галакторею (см. гл. 332).
Дифференциальная диагностика. Избыток пролактина может быть связан со следующими причинами: 1) автономной продукцией гормона (аденомы гипофиза); 2) уменьшением уровня дофамина или его ингибирующего действия (например, из-за патологии гипоталамуса или приема средств, блокирующих синтез, секрецию или действие дофамина); 3) наличием стимулов, преодолевающих нормальное дофаминергическое ингибирование (например, эстрогены или, возможно, гипотиреоз); 4) снижением клиренса пролактина (почечная недостаточность). Разграничить физиологические, фармакологические и патологические причины гиперпролактинемии с помощью какого-либо единственного супрессивного теста невозможно (табл. 321-2).
У женщин концентрация пролактина (менее 20 нг/мл) несколько выше, чем у мужчин (менее 15 нг/мл). Во время беременности концентрация пролактина начинает возрастать со 11 триместра и достигает максимума к моменту родов. Максимальные цифры колеблются от 100 до 300 нг/мл, но обычно ниже 200 нг/мл. Тест на беременность необходимо проводить у всех женщин с гиперпролактинемией и аменореей, равно как и только аменореей. После родов средняя концентрация пролактина снижается, но при каждом кормлении ребенка возрастает. Постепенно за несколько месяцев уменьшается как базальная, так и стимулируемая актом кормления концентрация пролактина; через 4—6 мес после родов базальный уровень его нормализуется и больше не возрастает при кормлении грудью, несмотря на его продолжение.
Больных с гиперпролактинемией следует тщательно расспрашивать о принимаемых лекарствах. Частой причиной гиперпролактинемии являются средства, блокирующие действие дофамина (например, фенотиазины, бутирофеноны, метоклопрамид) или снижающие его уровень (например, метилдофа и резерпин). Прием таких средств редко сопровождается возрастанием концентрации пролактина выше 100 нг/мл, если нет почечной недостаточности. Хотя высокие дозы эстрогенов вызывают гиперпролактинемию, прием пероральных контрацептивов, содержащих низкие дозы эстрогенов, не сопровождается повышением уровня пролактина
Таблица 321-2. Причины гиперпролактинемии
I. Физиологические состояния (беременность, ранние сроки кормления грудью, стресс, сон, раздражение сосков молочной железы)
II. Фармакологические средства
Антагонисты дофаминовых рецепторов (фенотиазины, бутирофеноны, тиоксантены, метоклопрамид)
Средства, снижающие уровень дофамина (метилдофа, резерпин)
Эстрогены
Опиаты
III. Патологические состояния
Опухоли гипофиза [пролактиномы; аденомы, секретирующие ГР и пролактин; аденомы, секретирующие АКТГ и пролактин (синдром Нельсона и болезнь Кушинга); нефункционирующие хромофобные аденомы со сдавлением ножки гипофиза]
Поражения гипоталамуса и ножки гипофиза (гранулематозные заболевания, особенно саркоидоз; краниофарингиомы и другие опухоли; облучение черепа: перерезка ножки гипофиза; синдром «пустого» турецкого седла; сосудистая патология, включая аневризмы)
Первичный гипотиреоз
Хроническая почечная недостаточность
Цирроз печени
Травма грудной стенки (включая операционную и опоясывающий герпес)
Конечная стадия почечной недостаточности приводит к гиперпролактинемии у 70— 90% женщин и 25—60% мужчин. Это обусловливает гипогонадизм у части больных с почечной недостаточностью. Повышение уровня пролактина в таких случаях может определяться не только снижением его клиренса, но и увеличением секреции. Повышение концентрации пролактина в сыворотке крови при циррозе печени объяснить трудно.
Причиной умеренного повышения концентрации пролактина в сыворотке может быть тяжелый первичный гипотиреоз. Это происходит либо за счет повышения уровня ТРГ, либо за счет снижения дофаминергического тонуса. Поскольку при первичном гипотиреозе может наблюдаться и увеличение турецкого седла, имитирующее аденому гипофиза, тиреоидную функцию следует проверять у всех больных с повышенным уровнем пролактина в сыворотке крови. Изредка обратимое повышение концентрации пролактина в сыворотке отмечается при первичной недостаточности надпочечников.
Если гиперпролактинемия развилась не на фоне беременности, послеродового состояния или приема соответствующих лекарств, если больной не страдает циррозом печени, гипотиреозом или почечной недостаточностью, то остается предполагать патологию гипофиза или гипоталамуса. Эктопическая продукция пролактина внегипофизарными опухолями практически не встречается. Патология гипоталамуса или ножки гипофиза сопровождается умеренным повышением уровня пролактина (обычно ниже 150 нг/мл). Гиперпролактинемия имеется у 20—50% больных с опухолями гипоталамуса.
Пролактинсекретирующие аденомы гипофиза (пролактиномы) представляют собой либо маленькие опухоли, локализующиеся в паренхиме железы (так называемые микроаденомы), либо крупные опухоли, вызывающие увеличение размеров гипофиза (макроаденомы). Крупные нефункционирующие аденомы гипофиза также могут вызывать умеренное повышение уровня пролактина вследствие сдавления ножки гипофиза и создания препятствия для поступления дофамина в железу. Повышенный уровень пролактина обычно наблюдается и у больных акромегалией (у 25—45%), а также при синдроме Нельсона (опухоль гипофиза после адреналэктомии у больных с болезнью Кушинга). При нелеченой болезни Кушинга гиперпролактинемия встречается реже.
Результаты лабораторных исследований. У всех больных с гипогонадизмом или галактореей необходимо определять уровень пролактина в сыворотке крови. Если базальная концентрация пролактина повышена и доказано, что это небольшое ее увеличение (например, ниже 30 нг/мл) не связано со стрессом, целесообразно проводить дальнейшие исследования. Хотя какого-то одного теста для дифференциации причин гиперпролактинемии не существует, все же уровень пролактина в сыворотке выше 300 нг/мл свидетельствует в пользу аденомы гипофиза; содержание пролактина в сыворотке выше 100 нг/мл в отсутствие беременности также обусловливается обычно аденомой гипофиза. Введение агонистов дофамина, таких как бромкриптин, снижает уровень пролактина независимо от причины его повышения и поэтому не может служить дифференциально диагностическим тестом (рис. 321 -4). Стимуляционные тесты также не позволяют дифференцировать причины гиперпролактинемии. Например, у большинства больных с пролактиномами повышение уровня пролактина в ответ на ТРГ минимально или вообще отсутствует, тогда как в норме это повышение превышает 200%, а для больных с патологией гипоталамуса или принимающих дофаминблокирующие средства характерна промежуточная величина (обычно наблюдается удвоение уровня пролактина в сыворотке). К сожалению, реакция на ТРГ слишком непостоянна, чтобы быть полезным тестом в каждом отдельном случае.
Всем больным с необъяснимой гиперпролактинемией необходимо производить контрастную компьютерную томографию (КТ) гипоталамуса и гипофиза или магнитную резонансографию (МРГ) этой области. При КТ-сканировании легко визуализируются макроаденомы гипофиза, но микроаденомы (менее 10 мм) увидеть сложнее. Если рентгенологических изменений нет, то состояние квалифицируют как «идиопатическую гиперпролактинемию», не исключая при этом возможности существования маленькой микроаденомы. Томография турецкого седла — также ненадежный скрининг-тест на небольшие аденомы гипофиза, так как часто дает ложноположительные и ложноотрицательные результаты.
Микропролактиномы не сопровождаются гипопитуитаризмом (не считая гипогонадизма). При выявлении у больного с гипопитуитаризмом и гиперпролактинемией небольшого нарушения в гипофизе следует подозревать саркоидоз или другую патологию с вовлечением ножки гипофиза, а не микропролактиному. У больных с макропролактиномами или гипоталамическими нарушениями необходимо оценивать функцию гипофиза и проверять поля зрения.
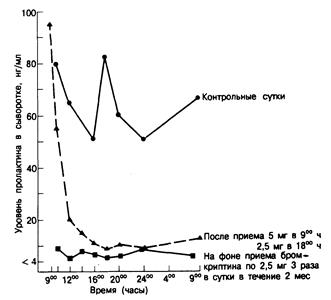
Рис. 321 -4. Изменение концентрации пролактина в сыворотке крови у женщин с «идиопатической» гиперпролактинемией» после первичного приема бромкриптина в дозе 5 мг и на фоне поддерживающей терапии — по 7,5 мг в сутки. (По G. H. Besser, М. О. Thorner, Postgrad. Med. J, 1976,52:66.)
Пролактиномы. Патологические изменения. Пролактиномы —это наиболее частый вид функционирующих аденом гипофиза. Небольшие микроаденомы, о существовании которых при жизни больного и не подозревали, обнаруживают в 15—25% всех аутопсий; в 40% этих маленьких опухолей методами иммунологического окрашивания выявляют пролактин, но как часто они действительно секретировали данный гормон — неизвестно. Примерно 70% макроаденом, ранее считавшихся не4)ункционирующими, на самом деле являются пролактиномами. Пролактинсекретирующие карциномы гипофиза встречаются редко.
Размеры пролактиномы коррелируют с уровнем секреции гормона; в целом, чем крупнее опухоль, тем выше уровень пролактина. Большие опухоли гипофиза с умеренным повышением уровня пролактина (50—100 нг/мл) — это не истинные пролактиномы. Они и проявляются своеобразно. Микропролактиномы сопровождаются только гиперпролактинемией и гипогонадизмом, тогда как макропролактиномы могут изменять уровень и других гипофизарных гормонов и сопровождаться головной болью, изменением полей зрения и другими признаками структурных нарушений.
Клинические проявления. Микропролактиномы встречаются чаще, чем макропролактиномы, причем 90% больных с микропролактиномами — женщины, тогда как 60% больных с макропролактиномами — мужчины. Нерегулярность менструаций, аменорея и галакторея способствуют ранней диагностике опухоли, а это, вероятно, объясняет преимущественное выявление микроаденом именно у женщин. У большинства мужчин с пролактиномами тоже отмечаются половые нарушения, но первой жалобой они бывают лишь в 15% случаев или меньше. Однако, хотя более позднее обращение мужчин за медицинской помощью объясняет, по-видимому, больший размер опухолей у них, нельзя исключить и более агрессивный рост опухоли у мужчин.
Эстрогены способствуют росту лактотрофов, но роль пероральных контрацептивов в патогенезе пролактином не установлена. У многих женщин с пролактиномами галакторея впервые развивается на фоне приема контрацептивов или аменорея впервые развивается после их отмены. У некоторых из таких больных нерегулярность менструаций, обусловленная пролактиномой, совпадает по времени с применением пероральных контрацептивов. Хотя аменорея после отмены этих препаратов встречается редко (примерно в 2% случаев), примерно у 30% больных с такой аменореей (после отмены пилюль) имеются пролактиномы. Развитие галактореи у женщин в период приема пероральных контрацептивов оправдывает определение у них уровня пролактина. Примерно у 5—7% больных с пролактиномой никогда не было менструаций (первичная аменорея), что делает эту опухоль важной курабельной причиной первичной аменореи. Пролактиномы могут расти во время беременности, и у 15% больных с пролактиномой диагноз впервые устанавливается в послеродовой период.
Желающие забеременеть женщины с пролактиномами требуют особого внимания. При медикаментозном лечении больных с микропролактиномами 95—98% срока беременности протекает без осложнений; в остальное время могут появиться головная боль или нарушения полей зрения из-за увеличения опухоли, что редко требует специальной терапии. Бессимптомное увеличение микропролактином, судя по результатам рентгенологических исследований, встречается примерно у 5% больных. При макропролактиномах рост опухоли в период беременности чаще дает осложнения. Симптомы увеличения размеров опухоли встречаются примерно у 15% таких больных, хотя в отдельных группах эта цифра достигала 35%. У большинства больных симптомы роста опухоли появляются в I триместре беременности.
Влияние беременности на секрецию пролактина у больных с пролактиномой проявляется по-разному. У некоторых больных, даже несмотря на рост опухоли, уровень пролактина в дальнейшем не увеличивается. Концентрацию последнего у женщин с пролактиномами следует периодически определять на всем протяжении беременности. При заметном повышении уровня пролактина (более 300—400 нг/мл) во время беременности он обычно остается выше исходного и после родов, причем увеличивается вероятность роста опухоли. У больных со стабильной или снижающейся концентрацией пролактина во время беременности уровень гормона после родов может быть ниже, чем до беременности. У таких больных во время беременности может происходить инфаркт или инволюция аденом.
Лечение больных с пролактиномами требует учета естественной эволюции заболевания. Хотя крупные аденомы гипофиза вырастают из маленьких опухолей, большинство микроаденом не прогрессирует до макроопухолей. Сведения о естественной эволюции не леченых микропролактином неполны; у 90—95% больных уровень пролактина в сыворотке за 7-летний срок наблюдения остается стабильным или снижается. У большинства больных с «идиопатической гиперпролактинемией» предположительно имеются маленькие микропролактиномы. У 30% таких больных уровень пролактина в сыворотке за 5-летний срок нормализуется без всякого лечения. При базальном уровне пролактина менее 40 нг/мл нормализация его содержания за этот срок отмечается у 60% больных.
Лечение. Не все больные с микропролактиномами нуждаются в лечении. Женщинам с микропролактиномами лечение необходимо, если они хотят забеременеть, если у них снижается либидо или беспокоит галакторея, если они хотят, чтобы менструации у них стали регулярными или имеется риск остеопороза. Мужчин с микропролактиномами следует лечить при снижении потенции или либидо, а также в случае предъявления жалоб на бесплодие. При наличии макропролактином лечение требуется в большинстве случаев.
Антагонисты дофамина снижают концентрацию пролактина практически у всех больных с гиперпролактинемией (см. рис. 321-4). Овуляторные циклы и фертильность восстанавливаются у 90% женщин пременопаузального возраста, что подчеркивает прямую связь между гиперпролактинемией и аменореей. В США в настоящее время единственным разрешенным препаратом, эффективно снижающим уровень пролактина, является бромкриптин — производное алкалоидов спорыньи, обладающее свойствами агониста дофамина. Бромкриптин следует назначать дважды в день с пищей во избежание раздражения желудочно-кишечного тракта. Лечение нужно начинать с дозы 1,25 мг, принимаемой лежа, чтобы свести к минимуму побочные эффекты (тошнота, рвота, слабость, отек слизистой оболочки носа и постуральная гипотензия). Дозы постепенно повышают до 2,5 мг дважды в день (в среднем). Однако у некоторых больных с макропролактиномами для нормализации уровня пролактина в сыворотке может потребоваться 15 мг бромкриптина в сутки. Хотя этот препарат и дорогостоящ, он эффективен при всех формах гиперпролактинемии, а часто снимает и галакторею, не связанную с гиперпролактинемией. Один раз в день можно вводить перголид — длительно действующий агонист дофамина, но в США он не применяется. Хотя перголид и бромкриптин дают сходные побочные эффекты, отдельные больные переносят только один из этих препаратов.
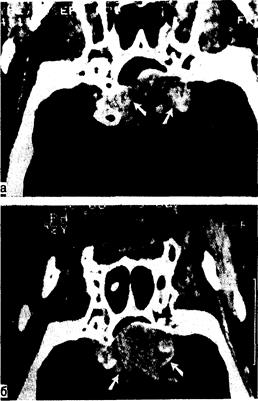
Рис. 321-5. Фронтальная КТ-сканограмма мужчины с крупной пролактинсекретирующей макроаденомой (верхний край опухоли показан стрелками). а — до лечения; б — через 1 год после начала лечения бромокриптином. (По Molitch et al.).
У больных с микропролактиномами с одним из вышеперечисленных показаний к лечению бромкриптин является средством выбора. Почти у всех, кто переносит этот препарат, концентрации пролактина нормализуются обычно через несколько дней после начала приема полной лечебной дозы (см. рис. 321-4). Менструации восстанавливаются, как правило, в течение 2 мес, однако иногда нарушения сохраняются на срок до 1 года. Поскольку беременность может наступить и в отсутствие нормальных менструаций, до установления их регулярности рекомендуется пользоваться барьерными контрацептивами. В этом случае при наступлении беременности бромкриптин можно отменить уже в первом безменструальном периоде. Однако применение бромкриптина во время беременности не сопряжено с увеличением риска врожденных пороков или выкидыша. Эффект бромкриптина обычно нестабилен, но у 15—17%о больных с микропролактиномами нормальная концентрация пролактина сохраняется и после отмены препарата.
У больных с макропролактиномами бромкриптин обычно снижает уровень пролактина в сыворотке и может уменьшать массу опухоли. Концентрация тестостерона у мужчин начинает увеличиваться через 3 мес, а через 6—8 мес может достигать нормы. У некоторых больных нормализуется и число сперматозоидов.
Одна из групп больных с крупными пролактиномами, супраселлярно распространенными (средний уровень пролактина 1441 нг/мл у женщин и 3451 нг/мл у мужчин) представляет особый интерес. Хотя у 96% больных уровень пролактина снизился на 10% от исходного, у большинства не произошло его нормализации, несмотря на дозы бромкриптина от 7,5 до 20 мг/сут. Нарушения полей зрения уменьшились у 90% больных (рис. 321 -5). Таким образом, бромкриптин может служить средством выбора у больных с небольшими макропролактиномами. Однако у больных с более крупными опухолями, у которых сохраняются нарушения полей зрения или симптомы гиперпролактинемии, а также у женщин с крупными опухолями, желающими забеременеть, бромкриптин в качестве единственного средства лечения не рекомендуется. У таких больных рост опухоли может возобновиться после отмены бромкриптина, будь то из-за небрежности, беременности или возникновения заболеваний, при которых его применение противопоказано. Крупные нефункционирующ
