Глава 190. острый инфаркт миокарда
Ричард К. Пастернак, Евгений Браунвальд, Джозеф С. Алперт (Richard С. Pasternak, Eugene Braunwald, Joseph S. Alpert)
Инфаркт миокарда это одно из наиболее часто встречающихся заболеваний в странах Запада. В США ежегодно регистрируется примерно 1,5 млн человек, перенесших инфаркт миокарда. При остром инфаркте миокарда умирает примерно 35 % заболевших, причем чуть более половины из них до того, как попадают в стационар. Еще 15-20% больных, перенесших острую стадию инфаркта миокарда, умирают в течение первого года. Риск повышенной смертности среди лиц, перенесших инфаркт миокарда, даже через 10 лет в 3,5 раза выше, чем у лиц такого же возраста, но без инфаркта миокарда в анамнезе.
Клиническая картина
Чаще всего больные с острым инфарктом миокарда жалуются на боль. У некоторых больных она бывает настолько сильной, что они описывают ее как наиболее выраженную из болей, которые им когда-либо доводилось испытывать (гл. 4). Тяжела я, сжимающая, разрывающая боль обычно возникает в глубине грудной клетки и по характеру напоминает обычные приступы стенокардии, однако более интенсивная и продолжительная. В типичных случаях боль ощущается в центральной части грудной клетки и/или в области эпигастрия. Примерно у 30 % больных она иррадиирует в верхние конечности, реже в область живота, спины, захватывая нижнюю челюсть и шею. Боль может иррадиировать даже в область затылка, но никогда не иррадиирует ниже пупка. Случаи, когда боль локализуется ниже мечевидного отростка, или когда больные сами отрицают связь боли с сердечным приступом, являются причинами постановки неправильного диагноза.
Часто боли сопровождаются слабостью, потливостью, тошнотой, рвотой, головокружением, возбуждением. Неприятные ощущения появляются обычно в состоянии покоя, чаще утром. Если боль начинается во время физической нагрузки, то в отличие от приступа стенокардии, она, как правило, не исчезает после ее прекращения.
Однако присутствует боль далеко не всегда. Примерно у 15—20 %, а по-видимому, даже и у большего процента больных острый инфаркт миокарда протекает безболезненно, и такие больные могут вообще не обращаться за медицинской помощью. Чаще безболевой инфаркт миокарда регистрируют у больных сахарным диабетом, а также у лиц преклонного возраста. У пожилых больных инфаркт миокарда проявляется внезапно возникшей одышкой, которая может перейти в отек легких. В других случаях инфаркт миокарда, как болевой, так и безболевой, характеризуется внезапной потерей сознания, ощущением резкой слабости, возникновением аритмий или просто необъяснимым резким понижением артериального давления.
Физикальное обследование
Во многих случаях у больных доминирует реакция на боль в грудной клетке. Они беспокойны, возбуждены, пытаются снять боль, двигаясь в постели, корчась и вытягиваясь, пытаются вызвать одышку или даже рвоту. Иначе ведут себя больные во время приступа стенокардии. Они стремятся занять неподвижное положение из-за боязни возобновления болей. Часто наблюдаются бледность, потливость и похолодание конечностей. Загрудинные боли, продолжающиеся более 30 мин, и наблюдаемая при этом потливость свидетельствуют о высокой вероятности острого инфаркта миокарда. Несмотря на то что у многих больных пульс и артериальное давление остаются в пределах нормы, примерно у 25 % больных с передним инфарктом миокарда наблюдают проявления гиперреактивности симпатической нервной системы (тахикардия и/или гипертония), а почти у 50 % больных с нижним инфарктом миокарда наблюдают признаки повышенного тонуса симпатической нервной системы (брадикардия и/или гипотония) .
Прекардиальная область обычно не изменена. Пальпация верхушечного толчка может быть затруднена. Почти у 25 % больных с передним инфарктом миокарда в течение первых дней болезни в периапикальной области выявляется измененная систолическая пульсация, которая вскоре может исчезнуть. Другие физикальные признаки дисфункции левого желудочка, которые могут встречаться при остром инфаркте миокарда, в порядке убывания по частоте встречаемости располагаются следующим образом: IV (S4) или III (S3) сердечные тоны, приглушенность тонов сердца и, редко, парадоксальное расщепление II тона (гл. 177).
Преходящий систолический шум на верхушке сердца, возникающий преимущественно как следствие вторичной недостаточности левого предсердно-желудочкового клапана (митральной недостаточности) из-за дисфункции сосочковых мышц, имеет средне- или позднесистолический характер. При выслушивании у многих больных с трансмуральным инфарктом миокарда временами прослушивается шум трения перикарда. У больных с инфарктом правого желудочка часто возникает пульсация растянутых яремных вен, отмечается уменьшение объема пульса на каротидных артериях, несмотря на нормальный сердечный выброс. В 1-ю неделю острого инфаркта миокарда возможен .подъем температуры тела до 38 °С, но, если температура тела превышает 38 °С, следует искать другие причины ее повышения. Величина артериального давления варьирует в широких пределах. У большинства больных с трансмуральным инфарктом миокарда систолическое артериальное давление снижается на 10—15 мм рт. ст. от исходного уровня.
Лабораторные исследования
Для подтверждения диагноза инфаркта миокарда служат следующие лабораторные показатели: 1) неспецифнческие показатели тканевого некроза и воспалительной реакции; 2) данные электрокардиограммы; 3) результаты изменения уровня ферментов сыворотки крови.
Проявлением неспецифической реактивности организма в ответ на повреждение миокарда является полиморфно-клеточный лейкоцитоз, который возникает в течение нескольких часов после появления ангинозной боли, сохраняется в течение 3—7 сут и часто достигает значений 12—15•109/л. СОЭ повышается не так быстро, как число лейкоцитов в крови, достигает пика в течение 1-й недели и иногда остается повышенной 1—2 нед.
Электрокардиографические проявления острого инфаркта миокарда подробно описаны в гл. 178. Хотя не всегда имеется четкая связь между изменениями на ЭКГ и степенью повреждения миокарда, однако появление патологического зубца Q или исчезновение зубца R обычно позволяет с большой вероятностью диагностировать трансмуральный инфаркт миокарда. О наличии нетрансмурального инфаркта миокарда говорят в тех случаях, когда на ЭКГ выявляются лишь транзиторные изменения сегмента ST и стойкие изменения зубца Т. Однако эти изменения весьма вариабельны и неспецифичны и поэтому не могут служить основой для диагностики острого инфаркта миокарда. В этой связи рациональная номенклатура для диагностики острого инфаркта миокарда должна лишь разграничивать последний на трансмуральный и нетрансмуральный в зависимости от наличия изменений зубца Q или волн ST—Т.
Сывороточные ферменты
Некротизированная во время острого инфаркта миокарда сердечная мышца выделяет в кровь большое количество ферментов. Скорость выброса различных специфических ферментов неодинакова. Изменение уровня ферментов в крови во времени имеет большую диагностическую ценность. Динамика концентрации ферментов, наиболее часто используемых для диагностики острого инфаркта миокарда, показана на рис. 190-1. Уровень двух ферментов, сывороточной глутаматоксалоацетаттрансаминазы (СГОТ) и креатинфосфокиназы (КФК) возрастает и снижается очень быстро, в то время как уровень лактатдегидрогеназы (ЛДГ) нарастает медленнее и дольше остается повышенным. Недостаток определения СГОТ заключается в том, что этот фермент содержится также в скелетных мышцах, в клетках печени, эритроцитах и может высвобождаться из этих экстракардиальных источников. Поэтому в настоящее время определение СГОТ для диагностики острого инфаркта миокарда используют реже, чем раньше, вследствие неспецифичности этого фермента и того, что динамика его концентрации занимает промежуточное положение между динамикой концентрации КФК и динамикой концентрации ЛДГ, в связи с чем информация об уровне СГОТ становится в большинстве случаев излишней. Определение содержания MB изофермента КФК имеет преимущества перед определением концентрации СГОТ, поскольку этот изофермент практически не определяется в экстракардиальной ткани и поэтому более специфичен, чем СГОТ. Поскольку подъем концентрации КФК или СГОТ определяется в течение короткого времени, он может оставаться незамеченным в тех случаях, когда образцы крови берут более чем через 48 ч после развития инфаркта миокарда. Определение MB—КФК имеет практический смысл в тех случаях, когда есть подозрение на повреждение скелетных мышц или ткани мозга, поскольку в них содержатся значительные количества этого фермента, но не его изофермента. Специфичность MB-изофермента для определения повреждения миокарда зависит от используемой методики. Наиболее специфичен радиоиммуноанализ, однако на практике тем не менее чаще используют электрофорез в геле, обладающий меньшей специфичностью и поэтому чаще дающий ложноположительные результаты. При остром инфаркте миокарда уровень ЛДГ повышается в первый же день, между 3-м и 4-м днем он достигает пика и в среднем через 14 дней возвращается к норме. При проведении электрофореза в крахмальном геле можно выделить пять изоферментов ЛДГ. Разные ткани содержат различные количества этих изоферментов. Изофермент, обладающий наибольшей электрофоретической подвижностью, в основном содержится в миокарде, его обозначают как ЛДГ). Изоферменты, обладающие наименьшей электрофоретической подвижностью, содержатся преимущественно в скелетной мускулатуре и в клетках печени. При остром инфаркте миокарда уровень ЛДГ1 повышается еще до того, как повышается уровень общей ЛДГ, т. е. может наблюдаться повышение содержания ЛДГ) при нормальном содержании общей ЛДГ. Следовательно, выявление повышенного уровня ЛДГ| является более чувствительным диагностическим тестом при остром инфаркте миокарда, чем уровень общей ЛДГ, его чувствительность превышает 95 %.
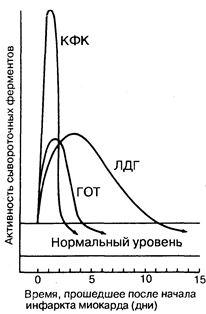
Рис.190-1. Динамика сывороточных ферментов после типичного инфаркта миокарда.
КФК — креатинфосфокиназа; ЛДГ — лактатдегидрогеназа; ГОТ — глутаматрксалоацетаттрансаминаза.
Особую клиническую значимость представляет тот факт, что увеличенный в 2—3 раза уровень общей КФК (но не MB—КФК) может быть следствием внутримышечной инъекции. Возможны случаи парадоксальной диагностики острого инфаркта миокарда у больных, которым была сделана внутримышечная инъекция наркотика в связи с болями в грудной клетке, не связанными с патологией сердца. Кроме того, потенциальными источниками повышенного уровня КФК могут быть: 1) заболевания мышц, в том числе мышечные дистрофии, миопатии, полимиозиты; 2) электроимпульсная терапия (кардиоверсия); 3) катетеризация сердца; 4) гипотиреоидизм; 5) инсульт мозга; 6) хирургические вмешательства; 7) повреждения скелетных мышц при травмах, конвульсиях, длительной иммобилизации. Хирургические вмешательства на сердце и электроимпульсная терапия часто могут приводить к повышению уровня изофермента КФК.
Известно, что существует корреляция между количеством выброшенного в кровь фермента и размером инфаркта миокарда. Продемонстрировано, что масса миокарда, подвергшегося некрозу, может быть определена по кривой концентрация — время в том случае, если известны кинетика высвобождения фермента, его распада, распределения и пр. Анализ кривой концентрация — время для MB — КФК позволяет определить величину инфаркта миокарда в граммах. В то время как площадь под кривой изменения концентрации MB — КФК во времени отражает размеры инфаркта миокарда, абсолютные значения концентрации этого фермента и время до достижения максимума концентрации связаны с кинетикой вымывания MB — КФК из миокарда. Появление просвета в окклюзированной венечной артерии, происходящее либо спонтанно, либо под влиянием механического воздействия или фармакологических препаратов в ранние сроки острого инфаркта миокарда, вызывает быстрый рост концентрации фермента. Пик концентрации достигается через 1—3 ч после реперфузии. Общая площадь под кривой «концентрация — время» при этом может быть меньше, чем без реперфузии, что отражает меньшие размеры инфаркта миокарда.
Характерное возрастание концентрации ферментов наблюдается более чем у у 95 % больных с клинически доказанным инфарктом миокарда. При нестабильной стенокардии содержание КФК, ЛДГ, СГОТ обычно не повышается. У многих больных с подозрением на инфаркт миокарда исходный уровень ферментов в крови сохраняется в пределах нормы, при инфаркте миокарда он может повышаться в 3 раза, однако при этом он не превышает верхней границы нормы. Такую ситуацию наблюдают у больных с небольшим инфарктом миокарда. Хотя такое повышение содержания фермента нельзя рассматривать как строгий диагностический критерий острого инфаркта миокарда, оно с высокой вероятностью заставляет подозревать его. Практическую помощь в такой ситуации может оказать определение изоферментов.
Для диагностики острого инфаркта миокарда или оценки его тяжести могут оказаться полезными радионуклидные методы (гл. 179). Сцинтиграфию в острой фазе острого инфаркта миокарда (изображение «горячего пятна») выполняют с 99m'Тс-пирофосфатом, содержащим двухвалентное олово. Сканограммы обычно дают положительный результат со 2-го по 5-й день после начала инфаркта миокарда, чаще у больных с трансмуральным инфарктом миокарда. Несмотря на то что метод дает возможность определить локализацию инфаркта миокарда и его размеры (с. 887), в плане диагностики он менее точен, чем определение содержания КФК. Изображения миокарда с помощью таллия-201, который захватывается и концентрируется жизнеспособным миокардом, выявляет дефект перфузии («холодное пятно») у большинства больных в первые часы после развития трансмурального инфаркта миокарда. Эта локализованная область. сниженной радиоактивности может заполняться в течение последующих часов. Тем не менее дифференцировать острый инфаркт от старых Рубцовых изменений с помощью данного метода невозможно. Таким образом, сканирование таллием — весьма чувствительный метод для выявления инфаркта миокарда, однако оно неспецифично для острого инфаркта миокарда. Применяя радионуклидную вентрикулографию с эритроцитами, меченными 99mТе, у больных с острым инфарктом миокарда можно выявлять нарушения сократимости и снижение фракции выброса левого желудочка. Радионуклидная вентрикулография весьма ценна при оценке нарушенной гемодинамики при остром инфаркте миокарда и при необходимости установления диагноза инфаркта миокарда правого желудочка, когда снижается фракция выброса правого желудочка. Однако в целом специфичность этого метода низка, поскольку измененные радионуклидные вентрикулограммы регистрируют не только при остром инфаркте миокарда, но и при других патологических состояниях сердца.
В оценке состояния больных острым инфарктом миокарда может оказаться полезной также двухмерная эхокардиография. При этом можно легко выявить нарушения сократимости, в особенности в области перегородки и задненижней стенки. И хотя с помощью эхокардиографии нельзя дифференцировать острый инфаркт миокарда от нарушений сократимости вследствие наличия рубцов или выраженной острой ишемии миокарда, простота и безопасность этого метода позволяют рассматривать его как важный этап обследования больных с острым инфарктом миокарда. Кроме того, эхокардиография может быть весьма информативной для диагностики инфаркта миокарда правого желудочка, аневризмы левого желудочка и тромба в области левого желудочка.
