Кафедра патологической физиологии
СЕВЕРО-ЗАПАДНЫЙ ГОСУДАРСТВЕННЫЙ МЕДИЦИНСКИЙ УНИВЕРСИТЕТ ИМЕНИ И.И. МЕЧНИКОВА
Кафедра патологической физиологии
В.И. Николаев, М.Д. Денисенко
ПАТОФИЗИОЛОГИЯ ПОЧЕК
Учебно-методическое пособие
Санкт-Петербург
2015 г.
УДК 616 – 092.18
ББК 52.5
В.И. Николаев, М.Д. Денисенко Патофизиология почек. Учебно-методическое пособие. – СПб.: Издательство ГБОУ ВПО СЗГМУ им. И.И. Мечникова, 2015. – 54 с.
Рецензент: заведующий кафедрой медицинской биологии д.м.н. профессор Костюкевич С.В.
В учебно-методическом пособии рассматриваются вопросы нарушения функции почек, анализируются механизмы развития патологии почек, описываются основные синдромы, связанные с заболеваниями почек.
Учебно-методическое пособие предназначено для студентов третьего курса обучающихся по ФГОС ВПО по направлению подготовки (специальности) 060101 лечебное дело
Утверждено
в качестве учебно-методического пособия Методическим
советом ГБОУ ВПО СЗГМУ им. И.И. Мечникова
протокол № _2 от «05» декабря 2014 г.
© В.И.Николаев, М.Д.Денисенко
© Издательство СЗГМУ им. И. И. Мечникова, 2015
1.Тема«Патофизиология почек»
2.Контингент учащихся – студенты, обучающиеся по ФГОС ВПО по направлению подготовки (специальности) 060101 лечебное дело.
3. Продолжительность занятий – 4 часа (в академических часах).
4. Структура практического занятия
1. Функции почек. Роль почек в поддержании гомеостаза.
2. Характеристика процессов, лежащих в основе работы почек:
· механизмы процесса фильтрации в норме и при патологии;
· механизмы процесса реабсорбции в норме и при патологии;
· механизмы процесса секреции в норме и при патологии.
3. Основные ренальные симптомы нарушения функции почек:
· изменение суточного объема мочи;
· изменение удельного веса мочи;
· изменение ритма мочеиспускания;
· изменение состава мочи.
4. Протеинурия: виды, механизмы развития.
5. Гематурия: виды, механизмы развития.
6. Цилиндрурия: виды, механизмы развития.
7. Этиопатогенетическая классификация заболеваний почек.
8. Основные патогенетические синдромы заболеваний почек:
· нефритический синдром: этиология, патогенез, клинические проявления, осложнения;
· нефротический синдром: этиология, патогенез, клинические проявления, осложнения;
· острая почечная недостаточность: виды, этиопатогенез, исходы;
· хроническая почечная недостаточность: этиология, патогенез, исход. Уремия.
9. Хроническая болезнь почек.
10. Принципы патогенетической коррекции заболеваний почек.
11. Лабораторная диагностика патологии почек:
· исследование очистительной функции почек (клиренс);
· проба Реберга-Тареева;
· проба по Зимницкому;
· проба по Нечипоренко;
· проба Аддиса-Каковского.
5. Содержание практического занятия
Почки, являясь жизненно важным органом, играют немаловажную роль в сохранении постоянства внутренней среды организма. Поддержание гомеостаза реализуется как за счет непосредственно экскреторной (выделительной) функции почек, так и за счет выполнения почками других – неэкскреторных – функций. Почки участвуют в процессах:
1. регуляции водно-солевого обмена (поддержание объема циркулирующей крови (ОЦК), интерстициальной и внутриклеточной жидкости, концентрации Na+, K+, Mg2+, Cl-, Ca2+ и других электролитов путем влияния на размер экскреции воды и электролитов);
2. регуляции кислотно-щелочного равновесия (за счет реакций ацидогенеза, аммониогенеза, реабсорбции или выведения бикарбонатов, выделения слабых органических кислот в неизмененном виде);
3. регуляции системного артериального давления (за счет регуляции ОЦК, за счет активации ренин-ангиотензин-альдостероновой системы (РААС), влияющей не только на внутрисосудистый объем жидкости, но и (посредством ангиотензина) на общее периферическое сопротивление сосудов (ОПСС), за счет синтеза простагландинов, также изменяющих сосудистый тонус);
4. регуляции гемопоэза (за счет синтеза эритропоэтинов, лейко- и тромбопоэтинов);
5. витаминного обмена (за счет синтеза vitD3);
6. обмена гормонов (за счет синтеза ренина).
И, естественно, почки осуществляют процесс удаления из плазмы крови токсичных продуктов, в том числе лекарственных препаратов, конечных продуктов обмена, но препятствуют выделению с мочой белков и глюкозы.
Функциональной единицей почек является нефрон (представляющий собой клубочек, канальцы – проксимальные и дистальные – и собирательные трубочки), в котором благодаря процессам фильтрации, реабсорбции и секреции и осуществляется образование мочи.
Процесс фильтрации осуществляется в начальной части нефрона – почечных клубочках, где образуется первичная моча, представляющая собой ультрафильтрат плазмы в объеме 180-200 л/сутки.
Движущей силой, обусловливающий процесс фильтрации, является фильтрационное давление (ФД). ФД создается в результате разности между гидростатическим давлением в капиллярах клубочка (ГДкл. = 50-55 мм рт. ст.), способствующим прохождению элементов плазмы крови через трехслойную мембрану в просвет капсулы Боумена, и противоположно действующими силами, создаваемыми онкотическим давлением плазмы крови (ОД = 20-28 мм рт. ст.) и давлением в капсуле Боумена (Дкапс. = 12 мм рт. ст.).
Гидростатическое давление в капиллярах клубочка является величиной, зависящей главным образом от мышечного тонуса стенок приводящей и отводящей артериол. Онкотическое давление плазмы крови зависит от содержания в ней белков. Давление в полости капсулы Боумена определяется проходимостью почечных канальцев и мочевыводящих путей; кроме того, оно зависит от внутрипочечного давления. В среднем фильтрационное давление составляет 18 мм рт.ст.
Фильтрующая мембрана состоит из трех слоев: эндотелия капилляров, базальной мембраны и эпителиальных клеток внутренней части капсулы (подоцитов). Она способна пропускать почти все имеющиеся в плазме крови вещества с молекулярным весом ниже 70 000 Д, а также небольшую часть альбуминов.
Кроме фильтрационного давления, на объем образующегося ультрафильтрата влияет площадь фильтрации, зависящая от количества функционирующих нефронов, а также проницаемость фильтрующей мембраны.
Нарушение фильтрации может выражаться в ее уменьшении или увеличении независимо от объема поступившей в организм жидкости.
К уменьшению объема фильтрации могут приводить как почечные, так и внепочечные факторы.
К почечным причинам снижения фильтрации относятся:
· уменьшение числа функционирующих клубочков вследствие замещения их фиброзной тканью или вследствие деструктивных процессов в почках;
· снижение проницаемости фильтрующей мембраны в связи с прорастанием соединительной тканью, осаждением на ней иммунных комплексов, аутоантител;
· склеротические изменения в приносящих артериолах;
· увеличение давления в полости капсулы Боумена по причине повышения внутрипочечного давления при отеке интерстиция или нарушения проходимости канальцев и мочевыводящих путей.
Внепочечными причинами уменьшения фильтрации могут быть:
· снижение системного кровяного давления (например, в связи с сердечной недостаточностью, шоком любой этиологии, обезвоживанием). При падении систолического артериального давления ниже 50 мм рт.ст. фильтрация прекращается полностью;
· повышение онкотического давления плазмы крови в результате увеличения концентрации белков, что может произойти при повышенном их синтезе (например, при миеломной болезни), введении белковых препаратов или сгущении крови.
Критическое уменьшение объема клубочковой фильтрации может произойти внезапно (например, при острой почечной недостаточности) или явиться результатом длительно развивающейся болезни, приводящей к гибели клубочков.
Несмотря на большой объем первичной мочи, у человека за сутки выделяется около 1,5 литров окончательной мочи. Такое резкое уменьшение объема выделяемой почками жидкости объясняется тем, что в канальцах нефрона происходит процесс усиленной реабсорбции воды, а также электролитов, глюкозы, аминокислот и др. Поступление этих веществ через стенку канальцев в интерстиций и затем в околоканальцевые капилляры осуществляется с помощью разных механизмов:
1) активный транспорт веществ с затратой энергии против электрохимического или концентрационного градиента специфическими переносчиками;
2) пассивный транспорт веществ по концентрационному, осмотическому или электрохимическому градиентам (таким образом транспортируются вода, бикарбонаты, мочевина, ионы Cl-);
3) транспорт белков, осуществляемый главным образом путем пиноцитоза.
Наиболее интенсивно процессы реабсорбции происходят в проксимальном канальце. Здесь всасывается 60-65% воды и натрия, а также высокий процент К+, Са2+, Mg2+, SO42-, HPO42-, Cl-, HCO3-; практически полностью реабсорбируются белки, витамины, аминокислоты, глюкоза, в значительном количестве – мочевина и мочевая кислота (рис. 1).
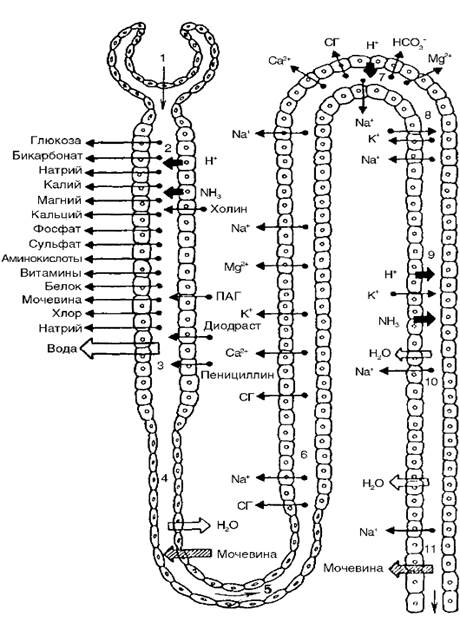
Рисунок 1. Процессы реабсорбции и секреции в нефроне (по Е.М. Тарееву): 1 – клубочек; 2 – проксимальный извитой каналец; 3 – проксимальный прямой каналец; 4 – тонкое нисходящее колено петли Генле; 5 – изгиб петли Генле; 6 – толстое восходящее колено петли Генле; 7 – дистальный извитой каналец; 8 – связующий отдел; 9 – собирательная трубка наружного мозгового вещества; 10 – собирательная трубка внутреннего мозгового вещества почки; 11 – Беллини проток. Стрелка, обращенная из просвета канальца, – реабсорбция вещества, в просвет канальца – секреция.
В проксимальном канальце всасывание электролитов и других веществ происходит с эквивалентным количеством воды, и поэтому содержимое канальца остается изотоничным плазме.
Процессы реабсорбции продолжаются в дистальном канальце и собирательной трубочке. Здесь всасываются Na+, Cl-, Са2+, Н2О и мочевина. Особенностью функционирования этих отделов является то, что здесь процессы реабсорбции и секреции регулируются различными гормонами и зависят от потребностей организма. Такой вид всасывания называется факультативным в отличие от облигатного типа реабсорбции в проксимальном отделе нефрона.
Наряду с реабсорбцией в канальцах осуществляются процессы секреции,т.е. активного выделения ряда веществ в канальцевую жидкость, при этом одни из выделяемых веществ образуются в самом почечном эпителии (Н+ и NH3), а другие извлекаются эпителием из внеклеточной жидкости с помощью специфических транспортных систем. В проксимальном отделе нефрона секретируются в канальцевую жидкость Н+, NH3, щавелевая, мочевая и желчные кислоты, адреналин, ацетилхолин, гистамин, серотонин, тиамин, а также парааминогиппуровая кислота, различные лекарственные вещества (например, пенициллин, индометацин, салициловая кислота, фуросемид и др.).
Нарушение процессов реабсобрцбии, экскреции и секреции в канальцах может быть связано с:
· изолированным повреждением ферментных систем (что имеет место при наследственных и приобретенных тубулопатиях);
· дистрофическими изменениями канальцевого эпителия;
· структурными изменениями в окружающем интерстиции;
· расстройствами гуморальной регуляции.
Тубулопатии – это заболевания, обусловленные нарушением транспортных функций эпителия почечных канальцев в связи с отсутствием или качественными изменениями белков-переносчиков, тех или иных ферментов, рецепторов для гормонов или дистрофическими процессами в стенке канальцев.
По этиологии различают первичные(наследственные) и вторичные(приобретенные) тубулопатии. К первичным тубулопатиям относится, например, нефрогенная форма несахарного диабета. Вторичные тубулопатии могут развиться под действием лекарственных препаратов; при отравлении солями лития, висмута, ртути, свинца, кадмия; при обширных ожогах; гиперпаратиреозе; злокачественных опухолях различных органов; миеломной болезни и др.
В зависимости от локализации дефекта различают проксимальные и дистальные тубулопатии.
Нефротический синдром
Нефротический синдром – синдром, включающий массивную протеинурию (более 3 г/сутки), гипопротеинемию, отеки и гиперипидемию.
Этиология: выделяют первичный нефротический синдром (при врожденных нарушениях липидного обмена) и вторичный нефротический синдром. В любом случае, нефротический синдром – вторичное поражение почек, осложняющее течение многих заболеваний – как первично почечных, так и заболеваний других систем организма.
К возможным причинам вторичного нефротического синдрома относят:
1. Первичные заболевания почек:
· гломерулонефриты;
· гломерулосклероз;
· токсические поражения и др.
2. Заболевания других органов и систем:
· сахарный диабет;
· амилоидоз;
· хронические инфекции (например, бронхоэктатическая болезнь, остеомиелит и др.);
· злокачественные опухоли;
· коллагенозы и др.
Патогенез. На начальном этапе развития нефротического синдрома действуют механизмы, вызывающие повреждение мембран и клеток клубочков под действием причинного фактора. Общим для большинства форм нефротического синдрома является увеличение проницаемости клубочкового фильтра для белка вследствие снижения электрического заряда мембран и постепенно ухудшающаяся реабсорбция белка в канальцах нефронов. Протеинурия может иметь как селективный, так и неселективный характер. При этом количество теряемого организмом с мочой белка всегда более 3 г за сутки.
Следствием макропротеинурии является гипопротеинемия, которая, в свою очередь, влечет за собой развитие отеков первоначально по гипоонкотическому механизму: снижение онкотического давления крови приводит к усилении процесса фильтрации в капиллярах и ухудшению процесса реабсорбции, в результате чего жидкость скапливается в межтканевом пространстве. В ответ на гиповолемию и ишемию почек включается в работу РААС: увеличивается секреция альдостерона, интенсивно реабсорбируется Na+, вслед за этим увеличивается секреция АДГ и задерживается вода (наблюдается олигоурия), что изначально носит компенсаторный характер для восполнения дефицита ОЦК. Однако весь объем реабсорбируемой жидкости в сосудах не задерживается: вследствие низкого онкотического давления крови жидкость выходит в интерстициальное пространство, еще более увеличивая уже имеющиеся отеки, замыкая «порочный круг».
Гиперлипидемия (повышение содержание атерогенных фракций липопротеинов – ЛПНП, ЛПОНП – и холестерина) при нефротическом синдроме объясняется несколькими механизмами:
1. дефицит альбуминов (транспортных белков для ЛПНП и ЛПОНП) приводит к увеличению ЛПНП и ЛПОНП в крови;
2. в результате гипопротеинемии компенсаторно увеличивается активность синтетических процессов в печени, однако происходит не только активный синтез альбуминов, но и атерогенных фракций липопротеинов;
3. развивается нарушение ферментативных систем липидного обмена – в первую очередь, липопротеинлипазы, что приводит к накоплению ЛПОНП и ЛПНП;
4. развивающаяся недостаточность функции щитовидной железы из-за потери тиреоглбулинов с мочой способствует нарушению процессов этерификации холестерина в результате отсутствия суммарного эффекта тиреоидных гормонов с катехоламинами.
Осложнениянефротического синдрома:
· потеря с мочой трансферрина приводит к развитию железодефицитной анемии;
· потеря с мочой факторов комплемента и легких цепей иммуноглобулинов приводит к иммунодефициту (нарушается резистентность к инфекциям);
· потеря антикоагулянтов и ослабление активности фибринолитической системы вследствие снижения содержания плазминогена приводит к наиболее опасному осложнению – тромбофилитическому синдрому с развитием тромбоэмболий.
Уремия
Уремия – клинический синдром прогрессирующей почечной недостаточности, характеризующийся разнообразными нарушениями метаболизма и полиорганной недостаточностью.
Клинические проявления уремии:
1) Астенический синдром:
· слабость;
· быстрая утомляемость;
· бессонница.
2) Поражения кожи:
· зуд;
· расчесы;
· землисто-серый цвет;
· сухость и шелушение;
· запах мочевины и аммиака;
· гнойничковые поражения.
3) Нарушения со стороны сердечно-сосудистой системы:
· артериальная гипертензия;
· аритмии;
· перикардит;
· сердечная недостаточность (острая и хроническая).
4) Поражения дыхательной системы:
· уремический пневмонит;
· острая пневмония;
· плеврит.
5) Поражения желудочно-кишечного тракта и печени:
· тошнота;
· рвота;
· диарея;
· гастрит;
· энтероколит;
· язвы слизистой желудка и двенадцатиперстной кишки;
· желудочно-кишечные кровотечения;
· печеночная недостаточность.
6) Нарушения со стороны системы крови:
· анемия (гипопластическая, гемолитическая);
· геморрагический синдром;
· иммунодефицит.
7) Костно-суставной синдром:
· остеопороз;
· фиброзная остеодистрофия;
· остеомаляция.
8) Нарушения со стороны мышечной системы:
· мышечные подергивания;
· тремор;
· судороги.
9) Нарушение зрения:
· ретинопатия;
· дистрофические изменения роговицы.
10) Нарушение нервной системы:
· энцефалопатия;
· полиневриты.
11) Нарушения водно-солевого обмена:
· отеки;
· гипо- (вначале) / гипернатриемия (на более поздних этапах);
· гиперкалиемия;
· гипокальциемия;
· гиперфосфатемия.
12) Нарушения кислотно-щелочного равновесия:
· ацидоз (метаболический, выделительный).
Нарушение экскреторной функции почек приводит к накоплению в крови креатинина и мочевины, в результате чего конечные продукты азотистого обмена начинают выделяться через потовые железы, пищеварительный тракт, дыхательные пути, а также через серозные оболочки и в полость суставов. В развитии уремии роль эндогенных токсинов общепризнанна. Первоначально к эндотоксинам относили продукты азотистого обмена, однако в экспериментах на животных была доказана слабая токсичность мочевины. Креатинин сам по себе также маотоксичен, но повреждающее действие оказывают продукты его распада – саркозин, метиламин, N-метилгидантоин. Главный токсический эффект связывают с накоплением в крови фенолов и «средних молекул» (олигопептиды с молекулярной массой от 300 до 5000 Да). Роль универсального уремического токсина отводится паратгормону, гиперпродукция которого связана с развивающейся гипокальциемией и гиперфосфатемией. Гипокальциемия вызвана нарушением образования в проксимальных канальцах витамина D3, при недостатке которого снижается всасывание Ca2+ в кишечнике. Вместе с тем снижение клубочковой фильтрации и выделение с мочой неорганических фосфатов приводит к гиперфосфатемии. Избыток фосфатов в крови сопровождается образованием нерастворимой фосфорно-кальциевой соли, которая откладывается в мягких тканях, в том числе и в почках.
Аутоинтоксикация является причиной снижения активности ряда ферментов, нарушения проведения нервных импульсов, развития иммунодефицитного состояния. В механизме уремической комы, наряду с нарушением водно-солевого, кислотно-щелочного обменов, токсического воздействия метаболитов на ткань ЦНС, немаловажное значение имеет гипоксия, являющаяся следствием сердечной, сосудистой, дыхательной недостаточности и неизбежно развивающейся при уремии анемии.
Анемия при уремии связана как с нарушением синтеза эритропоэтинов (гипопластическая анемия), так и с повышенным разрушением эритроцитов в условиях ацидоза (гемолитическая анемия).
Ацидоз (метаболический и выделительный, к которому может присоединяться и респираторный при развитии дыхательной недостаточности) оказывает влияние на активность различных ферментов (тем самым изменяя направленность биохимических реакций), тонус и проницаемость сосудов (что становится дополнительным фактором в развитии отеков и гипоксии), способствует катаболизму белков.
Гиперкалиемия является причиной для нарушения ритма сердца (наиболее характерны атриовентрикулярные блокады), гипернатриемия – артериальной гипертензии и отеков. Развивающаяся сердечная недостаточность может приводить к кардиогенной печеночной недостаточности, к дыхательной недостаточности (вследствие отека легких).
Поражения дыхательной системы связаны как с непосредственным токсическим воздействием метаболитов (уремический пневмонит, перикардит), так и с развитием иммунодефицита, являющегося причиной для присоединения вторичной инфекции, например, пневмонии. Кроме того дыхательная недостаточность присоединяется к сердечной при развитии кардиогенного отека легких.
Снижение активности иммунной системы (подавление как специфического иммунного ответа, так и неспецифического) развивается в результате нарушения синтеза лейкопоэтинов, а также в результате тотального энергодефицита.
Поражения желудочно-кишечного тракта при уремии обусловлены в основном интоксикацией и нарушение электролитного баланса. Они представлены токсическими гастритом, энтеритом, колитом, а также эрозивно-язвенными изменениями слизистых оболочек желудка и кишечника, проявляющимися диспептическими расстройствами и кровотечениями.
Хроническая болезнь почек
В современной медицине, общее признание получила концепция хронической болезни почек (ХБП, CKD – chronic kidney disease), предложенная американскими нефрологами в 2002 году. Под ХБП следует понимать наличие любых маркеров повреждения почек, персистирующих в течение более трех месяцев вне зависимости от нозологического диагноза.
Маркерами повреждения почек считают любые изменения, выявляющиеся при клинико-лабораторном обследовании, которые связаны с наличием патологического процесса в почечной ткани (например, протеинурия, гематурия, снижение скорости клубочковой фильтрации и т.д.). Трехмесячное ограничение (критерий «стойкости») в качестве временного параметра определения ХБП было выбрано потому, что в данные сроки острые варианты развития дисфункции почек, как правило, завершаются выздоровлением или приводят к очевидным клинико-морфологическим признакам хронизации процесса.
Классификация ХБП основана на двух показателях – скорости клубочковой фильтрации (СКФ) и признаках почечного повреждения. В зависимости от их сочетания выделяют пять стадий ХБП.
Классификация ХБП
| Стадия | Описание | СКФ, мл/мин |
| Признаки нефропатии, нормальная или повышенная СКФ | > 90 | |
| Признаки нефропатии, легкое снижение СКФ | 60 – 89 | |
| Умеренное снижение СКФ | 30 – 59 | |
| Выпаженное снижение СКФ | 15 – 29 | |
| Почечная недостаточность | < 15 |
Стадии 3-5 соответствуют определению хронической почечной недостаточности (снижение СКФ 60 мл/мин и менее). Стадия 5 соответствует терминальной хронической почечной недостаточности (уремии).
Диагноз «ХБП» (даже при отсутствии снижения СКФ) подразумевает неизбежное дальнейшее прогрессирование процесса и призван привлечь внимание врача. Именно потенциальная возможность утраты функции почек является главным моментом в понимании термина «хроническая болезнь почек».
ХБП – понятие наднозологическое, и в тоже время оно не является формальным объединением хронических повреждений почек различной природы. Причины выделения этого понятия базируются на единстве основных патогенетических механизмов прогрессирования патологического процесса в почках, общности многих факторов риска развития и прогрессирования патологии почек при их повреждении различной этиологии. С точки зрения соответствия задачам нефропротекции термин «ХБП» можно назвать более универсальным, нежели понятие «хроническая почечная недостаточность», поскольку в классификации ХБП представлены все стадии заболевания почек, включая начальные.
Нарушения иммунологических параметров наблюдаются не только при гломерулонефрите. Развитие гиперчувствительности замедленного типа свойственно тубулоинтерстициальному нефриту. Нарушения иммунной реактивности могут быть основой развития микробно-воспалительного процесса в органах мочевой системы, что позволяет использовать в рамках патогенетического лечения иммуномодуляторы и иммуностимуляторы.
В случае декомпенсации хронической почечной недостаточности проводят диализ (гемо-, перитонеальный, гастроинтестинальный диализ). Во время гемодиализа происходит удаление находящихся в крови веществ путём диффузии и конвекции, которые зависят от свойств гемодиализной мембраны (полупроницаемой), а также удаление лишней воды из организма (ультрафильтрация). Применение диализа позволяет нормализовать на небольшое время ряд параметров организма, определяющих гомеостаз. Однако гемодиализ не заменяет всех функций почек. Радикальным способом лечения является трансплантация почки. Первая успешная трансплантация почки у животных была выполнена в 1902 году, а у человека (от однояйцевого близнеца) – в 1950 году.
Литература.
Основная:
· В.В. Новицкий, Е.Д. Гольдберг, О.И. Уразова. Патофизиология: учебник: 4-е издание, перераб. и доп. – М.: ГЭОТАР-Медиа, 2009. – Т. 2, – С. 317-351.
· Патофизиология органов и систем. Учебно-методическое пособие для самостоятельной работы студентов под ред. проф. Николаева В.И. – СПб: СПбГМА им. И.И. Мечникова, 2008. – С. 4-9.
Дополнительная:
· А.Д. Адо. Патологическая физиология. – М.: Триада-Х, 2000. – С. 547.
· П.Ф. Литвицкий. Патофизиология: учебник: 4-е издание, перераб. и доп. – М.: ГЭОТАР-Медиа, 2007. – С. 574-591.
· В.Ю. Шанин. Клиническая патофизиология. – СПб: Специальная Литература, 1998. – С. 351-372.
7. Материалы для контроля.
Тестовые задания.
1. К ПАТОЛОГИЧЕСКОЙ ПРОТЕИНУРИИ ОТНОСЯТСЯ СЛЕДУЮЩИЕ ВАРИАНТЫ:
а) клубочковая
б) маршевая
в) ортостатическая
г) гистурия
д) канальцевая
е) постстрессорная
МЕХАНИЗМ РАЗВИТИЯ ГИПООНКОТИЧЕСКОГО ОТЕКА ПРИ НЕФРОТИЧЕСКОМ СИНДРОМЕ. ВЫБЕРИТЕ ПРАВИЛЬНУЮ ПОСЛЕДОВАТЕЬНОСТЬ: 1 – ГИПОПРОТЕИНЕМИЯ; 2 – ПЕРЕМЕЩЕНИЕ ЖИДКОЙ ЧАСТИ КРОВИ ИЗ СОСУДА ВО ВНЕКЛЕТОЧНОЕ ПРОСТРАНСТВО; 3 – НАРУШЕНИЕ РЕАБСОРБЦИИ БЕЛКА; 4 – СНИЖЕНИЕ ОНКОТИЧЕСКОГО ДАВЛЕНИЯ КРОВИ; 5 – МАКРОПРОТЕИНУРИЯ; 6 – ОТЕК.
а) 3-5-1-4-2-6
б) 3-4-1-5-2-6
в) 2-4-3-5-1-6
3. КЛИНИКО-ЛАБОРАТОРНЫЕ ПРИЗНАКИ УРЕМИЧЕСКОЙ СТАДИИ ХРОНИЧЕСКОЙ ПОЧЕЧНОЙ НЕДОСТАТОЧНОСТИ:
а) полиурия
б) анурия
в) скорость клубочковой фильтрации составляет 50-70% от должной
г) скорость клубочковой фильтрации составляет менее 5% от должной
д) гиперкалиемия
е) гипокалиемия
ж) полисерозит токсического генеза
з) концентрация креатинина в крови в пределах нормы
и) зуд кожи, шелушение, землисто-серый оттенок
к) бактериурия
4. ПРИЧИНЫ ПРЕРЕНАЛЬНОЙ ОСТРОЙ ПОЧЕЧНОЙ НЕДОСТАТОЧНОСТИ:
а) острый гломерулонефрит
б) мочекаменная болезнь
в) острая кровопотеря
г) ожоговая болезнь
д) профузная диарея
е) острый интерстициальный нефрит
ж) опухоль мочевого пузыря
з) истинный кардиогенный шок
и) острый пиелонефрит
к) гемолитический шок
5. ПО КАЧЕСТВУ ВЫДЕЯЕМОГО С МОЧОЙ БЕЛКА ОПРЕДЕЛЯЮТ СЛЕДУЮЩИЕ ВИДЫ ПРОТЕИНУРИИ:
а) селективная
б) неселективная
в) микропротеинурия
г) макропротеинурия
д) физиологическая
е) патологическая
6. ОСНОВНЫЕ КЛИНИЧЕСКИЕ ПРИЗНАКИ НЕФРОТИЧЕСКОГО СИНДРОМА:
а) гипоонкотические отеки
б) артериальная гипертензия
в) гипопротеинемия
г) лихорпадка
д) пиурия
е) гиперлипидемия
ж) макрогематурия
з) макропротеинурия
и) никтурия
к) гипостенурия
л) увеличение концентрации С-реактивного белка
7. Наглядный материал.
Экспериментальные модели.
Опыт 1. Определение клиренса по креатинину.
Цель опыта: определить клиренс у интактного и подопытного животных; используя полученные данные, дать оценку функционального состояния почек.
Методика. 2 мл сыворотки смешивают в пробирке с 6 мл насыщенного раствора пикриновой кислоты и через 5 мин ставят смесь в кипящую водяную на 15 мин. Затем содержимое пробирки центрифугируют или фильтруют. К 4 мл центрифугата (фильтрата) добавляют 0,2 мл 10% раствора NaOH и тщательно смешивают. Если раствор после подщелачивания мутнеет, его снова центрифугируют (фильтруют). Затем его доводят до объема 10 мл дистиллированной водой.
Через 10 мин пробу калориметрируют при зеленом светофильтре (длина волны 500-600 нм) в кювете с шириной слоя 20 мм, результаты калориметрировании сравнивают с аналогичными данными контрольных проб. Последние готовят следующим образом: к 3 мл раствора пикриновой кислоты добавляют 0,2 мл 10% раствора NaOH и доводят объем до 10 мл, доливая дистиллированную воду. Калориметрируют.
Постановка стандартной пробы: к 1 мл рабочего стандартного раствора креатинина добавляют 3 мл пикриновой кислоты и через 5 мин помещают смесь в кипящую водяную баню на 15 мин. Затем не центрифугируя (не фильтруя) прибавляют к пробе 0,2 мл 10% раствора NaOH и 5,8 мл дистиллированной воды. Калориметрируют в тех же условиях, что и опытную пробу. Содержание креатинина рассчитывают по формуле:
ЕОП.
Р (ммоль/л) = ЕСТ. *0,088 ммоль/л,
где Р – содержание креатинина в сыворотке (плазме) крови, ЕСТ. – экстинкция стандартных проб (за вычетом значений оптической плотности контрольных проб), ЕОП. – экстинкция опытных проб; 0,088 ммоль/л – концентрация креатинина в стандартной пробе.
Ход определения содержания креатинина в моче. В мерном цилиндре объемом 100 мл смешивают 0,5 мл мочи с 3 мл пикриновой кислоты. Смесь тщательно встряхивают и добавляют к ней 0,2 мл 10% раствора NaOH. Доведя объем смеси дистиллированной водой до 100 мл, выдерживают содержимое цилиндра при комнатной температуре в течение 10 мин. Экстинкцию измеряют на ФЭКе в кювете с толщиной слоя 10 мм при зеленом светофильтре (длина волны 500-560 нм), результаты сравнивают с данными контрольных проб.
Контрольные пробы готовят следующим образом. К 3 мл раствора пикриновой кислоты добавляют 0,2 мл 10% раствора NaOH. Затем пробу обрабатывают так же, как и опытную.
Содержание креатинина в моче рассчитывают по формуле:
ЕОП.
U (ммоль/л) = ЕСТ. *8,8 (ммоль/л),
где U – содержание креатинина в моче, ЕСТ – экстинкция стандартной пробы, ЕОП. – экстинкция опытной пробы, 8,8 ммоль/л – концентрация основного стандартного раствора креатинина.
Полученные величины содержания креатинина в сыворотке (плазме) крови и в моче подставляют в формулу клиренса.
Пример. В течение 60 мин выделилось 50 мл мочи. Минутный диурез (U) равен: 50:60 = 0,83 (мл). Концентрация креатинина в моче равна 130 мг%, или 11,4 ммоль/л (коэффициент пересчета старых единиц в рекомендуемые СИ – 0,88). Коэффициент концентрации креатинина равен 130/1,02 = 127,4. Клиренс креатинина равен 127,4 – 0,83 = 105,7 мл. Клубочковая фильтрация (F) равна 105,7 мл. Реабсорбция (R) воды в канальцах равна F – R = 105,7 – 0,83 = 104,87 мл. Реабсорбция первичной мочи R = (104,87/105,74)*100 = 99,2%.
Опыт 2. Получение острой почечной недостаточности у крыс при отравлении глицерином (глицеролом).
Цель опыта: получить у животных острую почечную недостаточность. Определить количество мочевины в крови и моче у опытных и контрольных животных, вычислить показатель очищения (клиренс).
Методика. Острую почечную недостаточность у крыс вызывают внутримышечным введением 50% раствора глицерина в дозе 10 мл на 100 г массы тела животного. Через 2 ч развивается острая почечная недостаточность. Крыс (контрольных и опытных) помещают в обменные клетки и собирают мочу в течение часа. Затем производят забор крови. В крови и моче определяют концентрацию креатинина.
8. Методический материал.
Клинические ситуационные задачи.
Задача №1. Больной П., 28 лет, находился в клинике по поводу развившегося осложнения язвенной болезни. Было сделано переливание крови – 300 мл, после чего наступило резкое ухудшение состояния: появились боли в пояснице, одышка, холодный пот, рвота, падение АД (90/60 мм рт. ст.). Через сутки после трансфузии крови развилась анурия. Был сделан биохимический анализ крови – выявлено резкое увеличение креатинина и мочевины. На 3-и сутки появилась моча почти черного цвета. Удельный вес – 1009-1010. Белок в моче – 0,6 г/л. В осадке: большое количество L, много гиалиновых и зернистых цилиндров, Er – 10-15 в поле зрения.
· Оцените функциональное состояние почек. Укажите форму и стадию нефропатии.
· Объясните этиологию и патогенез данного заболевания, механизмы синдромов и симптомов.
Задача №2. У больной Р., 22 лет, спустя 2 недели после заболевания тяжелой формой ангины, появились боли в области поясницы, одышка, сердцебиение, головная боль. За 4 дня пациентка прибавила в весе 9 кг.
Объективно: лицо бледное, веки мешкообразные, вздутые, глазные щели сужены, голени и стопы пастозны. Границы сердца расширены. АД – 180/95 м рт. ст., ЧСС – 100/мин. В крови повышены титры анти-О-стрептолизина и антигиалуронидазы; повышено содержание фракций глобулинов, а содержание альбуминов и фракций комплемента снижено. СОЭ – 26 мм/час. Положительный симптом Пастернацкого. Суточный диурез – 0,8 л. Удельный вес мочи – 1029. Моча мутная, цвета «мясных помоев». В моче: Er – в большом количестве, L – 6-8 в поле зрения. Белок в моче – 1,5 г/л (молекуляпная масса менее 70 000).
· Какая форма патологии почек развилась у данной больной? Ответ обоснуйте.
· В чем причина и каковы механизмы нарушения функции почек?
· Каковы механизмы симптомов и синдромов, развившихся у больной?
Задача №3. Больной Б., 42 лет, госпитализирован вследствие обострения хронического гломерулонефрита с жалобами на постоянные головные боли распирающего характера, ослабление зрения, боли в сердце, одышку, тошноту, частую рвоту с примесью крови, диарею, гиперсаливацию, постоянную жажду, зуд кожи, боли в костях.
Объективно: состояние тяжелое. Больной истощен, вялый, апатичный. Лицо отечно, землисто-серого цвета. Кожа сухая, со следами расчесов, с геморрагическими высыпаниями. Чувствуется запах аммиака в выдыхаемом больным воздухе, отмечаются непроизвольны мышечные подергивания. АД – 210/120 мм рт. ст., ЧСС – 100/мин, шум трения перикарда. На ЭКГ – признаки гипертрофии левого желудочка, нарушение проводимости, экстрасистолия. Дыхание шумное и глубокое, признаки застойных явлений в легких.
Лабораторные данные: остаточный азот крови – 285,5 ммоль/л, мочевина – 22 ммоль/л, креатинин – 280 мкмоль/л. В клиническом анализе крови: Er – 2,1·1012/л, Hb – 80 г/л. Показатели КЩР: рН – 7,25; ВЕ – -11 ммоль/л. Повышено содержание калия, магния, снижена концентрация натрия и хлора. Суточный диурез значительно снижен – 80 мл/сутки.
· Оцените функциональное состояние почек.
· Объясните этиологию и патогенез данного заболевания, механизмы синдромов и симптомов.
· Какова должна быть тактика врача?
Задача №4. Больной К., 27 лет, поступил с жалобами на резкую слабость, отеки и уменьшение количества мочи.
