Глава 18. Болезни сердечнососудистой системы
Артериальное давление и его регуляция
Артериальное давление(АД) является важнейшим системным показателем сердечнососудистой системы и зависит от состояния трех ее компонентов: сердечного выброса, тонуса артериальных сосудов и объема циркулирующей крови. Функциональный гомеорез этих компонентов поддерживается центральными и местными прессорными и депрессорными нейрогуморальными механизмами (Рис.25).
Механизмы гомеореза АД
Рис.25
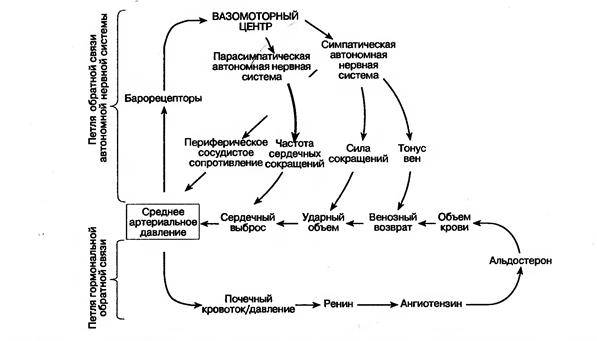
Мгновенные адаптивные изменения АД реализуются прессорными и депрессорными нервными вегетативными механизмами и составляют систему его пропорциональной регуляции. Афферентный отдел пропорциональной системы представлен барорецепторами дуги аорты и каротидных синусов.
При снижении АД сигналы от них поступают в продолговатый мозг и активируют нейроны сосудодвигательного центра, которые инициируют эфферентную норадренергическую стимуляцию α-адренорецепторовмиоцитов артерий, вызывая их сужение. Одновременная катехоламиновая активация β1-адренорецепторовмиокарда повышает его инотропизм и частоту сердечных сокращений, увеличивая минутный выброс сердца. Срабатывание этих механизмов обеспечивает возвращение пониженного АД к норме.
При повышении АД афферентные сигналы активируют центральныеα-адренорецепторы нейронов кардиоингибирующего центра, которые мгновенно подавляют высокочастотную нейрональную активность сосудодвигательного центра. В результате от них на периферию подаются низкочастотные сигналы, стимулирующие β2-адренорецепторымиоцитов артерий, что вызывает их расширение. Одновременно эфферентная холинергическая импульсация нейронов кардиоингибирующего центра активирует М-холинорецепторы миокарда, тормозя пейсмейкерную активность синусового узла и сердечный ритм. Так обеспечивается развитие депрессорного эффекта и возвращение повышенного АД к норме.
Долгосрочная прессорная регуляция АД реализуется интегральной ренин-ангиотензин-альдостероновой гуморальной системой. Ее сенсорный аппарат представлен юкстагломерулярными клетками (ЮГ-клетки) клубочков нефронов, которые активируются разными входными сигналами: чрезмерной β-адренергической сосудорасширяющей стимуляцией артериол клубочков, системным снижением АД, уменьшением ОЦК, ΡgЕ2, гипонатриемией и гиперкалиемией. В ответ ЮГ-клетки секретируют в кровь протеолитический фермент ренин, который инициирует каскад реакций, завершающихся образованием в эндотелии сосудов (главным образом легочных) мощного вазоконстрикторного фактора - ангиотензина II (из ангиотензина I под действием ангиотензинпревращающего фермента). Поступая в кровь, ангиотензин II активирует ангиотензиновые АТ- рецепторы сердца и миоцитов, запуская их сократительные механизмы. Помимо этого он активирует симпатоадреналовую систему, центр жажды и секрецию надпочечниками альдостерона. Последний стимулирует реабсорбцию Νа и вместе с ним воды в канальцевой системе нефрона, увеличивая ОЦК и повышая АД.
Противовесом прессорного ангиотензинового механизма интегративной системы является депрессорный, реализуемый плазменным пептидом брадикинином. Реакция образования прессорного ангиотензина ΙΙ и разрушения депрессорного брадикинина катализируется одним и тем же ангиотензинпревращающим ферментом (АПФ), определяя состояние обоих механизмов: при высокой активности АПФ превалирует прессорный эффект, а при низкой – депрессорный.
Важными депрессорными механизмами являются:
♦- система вазодилататорных и натрийуретических почечных простагландинов А и Е;
♦- система гипоталамического- и предсердных натрийуретических пептидов;
♦- система оксида азота.
Повышение активности прессорных механизмов и/или снижение эффективности депрессорных лежат в основе формирования артериальной гипертензии.
Гипертоническая болезнь
Гипертоническая болезнь (ГБ, первичная артериальная гипертензия, эссенциальная артериальная гипертензия) – хроническое заболевание, обусловленное первичными и разнообразными рассогласованиями прессорных и депрессорных механизмов регуляции АД. Ею болеют 20 – 30% населения экономически развитых стран, причем на ее долю приходятся 90 – 95% всех случаев артериальной гипертензии. Остальные 5-10% составляют вторичные, симптоматические гипертензии, сопутствующие основному заболеванию: тиреотоксическому зобу, гломерулонефриту, феохромоцитоме, болезни Конна и др.
Согласно ВОЗ показатели АД в покое оцениваются следующим образом:
◊- АД=100/60 мм рт.ст. – 139/89 мм рт.ст. – норма (последний показатель более характерен для пожилого возраста);
◊- АД=140/90 мм рт.ст. - 159/94 мм рт.ст. – пограничная гипертензия (группа риска ГБ, хотя такой подъем АД у молодых людей часто совпадает с началом I стадии болезни);
◊- АД=160/95 мм рт.ст. и выше - гипертоническая болезнь.
Основу этиологии ГБ составляет сочетание ряда факторов риска: наследственной предрасположенности к гипертензии, атеросклероза, психоэмоционального перенапряжения и избыточного употребления с пищей натрия хлорида. Два последних фактора играют провоцирующую роль, демаскируя скрытый наследственный субстрат патологии.
Наследственная предрасположенность, на основании последних исследований, состоит в аномальной сборке мембранных белков, выстилающих натриевые и кальциевые каналы нейронов сосудодвигательного центра и миоцитов артерий. Такие дефекты мембранных каналов создают условия для повышенного поступления в клетки ионов Νа и Cа, что вызывает «частичную деполяризацию» их мембран. В клинически непроявленной форме эти нарушения компенсируются повышенной активностью мембранных АТФ-аз, работающих на пределе своих функциональных возможностей. В результате в эффекторных клетках и структурах создаются благоприятные условия для реализации активирующей сигнализации. В часности:
♦-повышается реактивность нейронов сосудодвигательного центра к слабым афферентным стимулам;
♦- в симпатических терминалях повышается готовность к синаптическому выбросу норадреналина и ослаблению его «обратного захвата»;
♦- повышается чувствительность β адренорецепторови АТ-рецепторов миокарда к катехоламинам и ангиотензинуII;
♦- в мембранах миоцитов артериол повышается чувствительность α-адренорецепторов и АТ-рецепторов;
♦- повышается готовность контрактильного аппарата миоцитов артерий к тоническому сокращению.
На этом высокореактивном фоне провокационные факторы легко истощают компенсаторные АТФ-азные механизмы и переводят латентную патологию в проявленную форму.
Патогенез ГБ представляет собой стадийный процесс, характеризующийся прогрессирующим нарастанием АД и полиорганных морфофункциональных нарушений (Рис. 26).
Стадии ГБ
Рис. 26

Патогенез ГБ в I стадию болезни обусловливается возросшей активностью симпатоадреналовой системы и стимуляцией катехоламинами адренергических рецепторов эффекторных органов. Активация β1-адренорецепторов миокардиоцитов инициирует высокую пейсмейкерную активность клеток синусового узла, частый сердечный ритм и увеличенный минутный выброс крови. Активация a1-адренорецепторов миоцитов артериол запускает механизм их сокращения и сужения просвета, а β2-адренорецепторов – расслабления и расширения. В системном, суммарном итоге катехоламиновой стимуляции сосудов превалирует эффект сужения, хотя сосуды мозга, коронаров, почек, скелетных мышц расширяются - в них больше β2-адренорецепторов.
В результате формируется гиперкинетическийтип кровообращения с характерным увеличенным минутным выбросом сердца и ускоренным артериальным кровотоком. Возникает гипертензия, преимущественно систолического типа с повышением АД до160/95 – 179/104 мм рт.ст. Вклад в формирующуюся гипертензию интегративной прессорной системы пока еще невелик. Стадия характеризуется отсутствием органических изменений в органах и относительной легкостью лекарственной коррекции (рис.27).
Общий патогенез I стадии ГБ
Рис.27 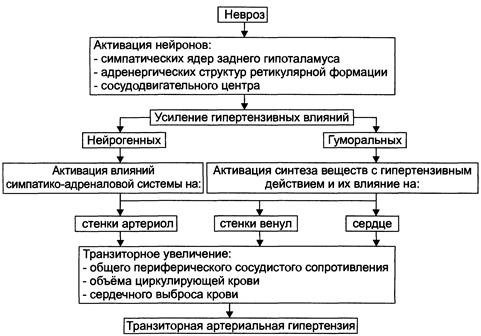
В I стадию ГБ выделяют две фазы: транзиторную и лабильную.
Транзиторная фаза характеризуется подъемом АД до160/95 мм рт.ст. и полной его нормализацией по мере прекращения действия провоцирующих гипертензию факторов. В этом заслуга, главным образом, пропорциональной депрессорной системы и в меньшей степени - интегральной.
Лабильная фаза характеризуется подъемом АД до 179/104 мм рт.ст. и отсутствием полной его нормализации, несмотря на высокое напряжение пропорциональной и интегральной депрессорных систем.
Патогенез II стадии ГБ – стадии стойкой гипертензии обусловлен, главным образом, чрезмерной активацией интегральной прессорной системы и снижением эффективности депрессорных механизмов.
В основе активации ренин-ангиотензинной системы при ГБ лежит механизм «переключения почки», направленный на уменьшение гломерулярной фильтрации, возросшей при гиперкинетическом кровообращении и угрожающей организму опасными солевыми потерями. Основными входными сигналами для его активации являются значительное увеличение объемного гломерулярного кровотока и снижение содержания в плазме ионов Νа. В ответ на это ЮГ-клетки адекватно усиливают секрецию ренина, запускающего каскад образования ангиотензина II, призванного нивелировать эти нарушения. Вместе с тем ангиотензин II суживает не только артериолы клубочков, но и все артерии мышечного типа, внося свой вклад в системное повышение АД. Одновременно активируется альдостеронзависимая реабсорбция натрия и воды, компенсируя возросшую фильтрацию.
Снижение активности депрессорных систем в эту стадию ГБ присходит, главным образом, по следующим причинам:
1 – усиленного разрушения брадикинина из-за высокой активности АПФ;
2 – ослабленного в условиях нарастающей циркуляторной гипоксии циклоксигеназного механизма образования почечных вазодилататорных Ρg А и Е.
В результате усиления интегративных прессорных и снижения депрессорных механизмов гипертензия в эту стадию ГБ приобретает все более вазоконстрикторный характер, проявляющийся ростом диастолического давления. Для неё характерно высокое и стойкое значение АД, достигающее 200/114 мм рт.ст. и наличие функционально компенсированных органических изменений внутренних органов (Рис.28).
