Глава 8. Патология водно-электролитного обмена и КЩС
Водно-электролитный обмен и его регуляция
Вода с растворенными в ней электролитами и неэлектролитами составляет примерно 55% массы тела. В организме она содержится во внутриклеточном и внеклеточном секторах (компартментах), разграниченных между собой биологическими мембранами (рис.15).
Распределение воды в организме
Рис. 15
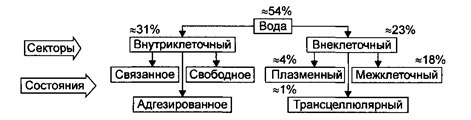
В каждом секторе она находится в трёх состояниях: свободном, связанном с гидрофильными органическими и неорганическими низкомолекулярными веществами и адгезированном – притяженном к поверхности коллоидных молекул. Наиболее мобильна свободная вода: она без затруднений перемещается через разграничительные биомембраны секторов по осмотическому градиенту. Менее подвижна связанная вода: ее перемещение зависит от активного трансмембранного транспорта растворенных в ней ионов. Практически не способна к перемещению адгезированная вода коллоидов, что предопределяет ее назначение – поддерживать объемы секторов в физиологических параметрах. В ходе окислительного метаболизма углеводов, жиров и белков в каждом секторе образуется метаболическая (конституционная) вода, которая является своеобразным резервом всех других ее форм.
Качественно водно-солевой состав секторов различен, но стабилен. Количественно он постоянно меняется из-за перемещений своих мобильных компонентов. Обмен водой между клетками и интерстицием осуществляется по осмотическому градиенту, создаваемому, в основном, деятельностью мембранных Νа, К – помп. Между интерстицием и сосудистым сектором вода перемещается еще и по гидростатическому градиенту, создаваемому разницей давлений в системе капилляров микроциркуляторного русла и межклеточного пространства. Динамичный сосудисто-интерстициальный водно-электролитный гомеостаз - гомеорез постоянно поддерживается поступлением воды и солей в организм с пищей и удалением их из организма с мочой (1,5л/сутки), с потом и выдыхаемыми парами (750 – 1000мл), с фекалиями (200мл). Важную роль в его формировании играют процессы секреции - резорбции пищеварительных соков (до 10л/сутки) и фильтрации - реабсорбции первичной мочи в нефронах почек (150л/сутки). Колебания водно-электролитного баланса зависят также от интенсивности метаболизма, температуры тела, климатических влияний, количества и состава пищи.
Регуляция водно-электролитного гомеореза осуществляется афферентными волюмо-, баро- и хеморецепторами, гипоталамическим центром жажды и эфферентными нейро-гуморальными механизмами, реализуемыми, главным образом, в структурах нефронов почек. Их действие направлено на выведение избытков Να и воды из организма (гипоталамический натрийуретический гормон и атриопептиды) и на реабсорбцию натрия и воды при их дефиците (альдостерон, ионообменный механизм, АДГ).
Если вода представляет собой транспортную систему и метаболическую среду, то электролиты играют значительную роль в реализации клеточных функций: возбудимости, сократимости, секреции, резорбции и соответствующего им уровня метаболизма - углеводного, липидного, белкового, энергетического, медиаторного. В составе буферных систем организма некоторые электролиты обеспечивают гомеостаз рН, необходимый для поддержания оптимальной активности ферментов, а в виде микроэлементов они непосредственно формируют их активные каталитические центры.
Водно-электролитный дисбаланс может привести к тяжелым метаболическим и функциональным последствиям, а будучи нераспознанным и неустранённым – к летальному исходу.
Нарушения водного обмена
Нарушения водного обмена – дисгидрии могут развиваться в двух основных направлениях: водной перегрузки – гипергидратации, или водного дефицита – гипогидратации.
8.2.1. Гипогидратация (обезвоживание, крайняя степень - эксикоз) возникает при значительных водных потерях и протекает в трех вариантах: изотонического, гипотонического и гипертонического.
Изотоническая гипогидратация возникает при потерях жидкости, изотоничной (изоосмолярной) плазме крови и интерстициальной жидкости. Наиболее частыми ее причинами являются кровопотеря и плазморея при ожогах и травмах. Она характеризуется уменьшением объемов внутрисосудистого и интерстициального секторов без изменений в их осмолярности. В ее клинической картине доминируют снижение массы тела, ослабление кожного тургора, уменьшение систолического объёма сердца, снижение систолического и некоторое повышение диастолического давления, тахикардия, олигоурия. Начальные симптомы появляются уже при 3% потерях жидкости. Снижение её в объёме 5-7% массы тела сопровождается тяжелыми гемодинамическими нарушениями, а свыше 10 – 15% - может оказаться смертельной.
Коррекция изотонической гипогидратации осуществляется внутревенной инфузией физиологического раствора, крови, плазмы и плазмозаменителей.
Гипотоническаягипогидратация развивается в результате потерь жидкостей, обогащенных электролитами (гиперосмолярные потери). Это может происходить при некоторых формах почечной патологии, сопровождающихся усилением гломерулярной фильтрации и уменьшением канальцевой реабсорбции, диарее, гипопродукции АДГ и альдостерона. Для этого типа гипогидратации характерно снижение осмолярности плазмы, а затем и интерстиция. В результате свободная вода начинает повышенно перемещаться во внутриклеточный сектор, инициируя развитие внутриклеточного отека.
Коррекцияэтого расстройства базируется на устранении основной патологии и одновременного дозированного восполнения специфических электролитных потерь и воды.
Гипертоническая гипогидратация развивается в результате потерь жидкостей, обедненных электролитами (гипоосмолярные потери) при обильном потоотделении у лихорадящих больных , неукротимой рвоте, диарее и полиурии (особенно при сахарном диабете). Для этого типа гипогидратации характерно повышение осмолярности внеклеточного сектора, что влечет перемещение в интерстиций свободной воды из клеток, вызывая их обезвоживание. Гипоосмолярные водно-электролитные потери сопровождаются гиповолемией, сладжированием крови, повышением риска тромбообразования, нарушениями центрального и периферического кровообращения. В тканях развивается гипоксия и метаболический ацидоз, что усугубляет тяжесть состояния.
Коррекцию умеренных гипоосмолярных потерь (до 5% массы тела/сутки) обычно производят внутривенной инфузией 5% глюкозы. Значительные гипоосмолярные потери (до 10л/сутки) требуют обязательного восполнения возникшего сопутствующего специфическго электролитного дефицита.
8.2.2. Гипергидратация (положительный водный баланс) возникает при чрезмерном введении в организм воды и/или электролитов, а также при ограничении их выведения. Возможны три ее варианта: гипотоническая гипергидратация, изотоническая гипергидратация и гипертоническая гипергидратация.
Гипотоническая гипергидратация или водное отравление развивается при утолении жажды большими объемами пресной воды, превышающими максимальную выделительную функцию почек. Она часто сопутствует почечной, печеночной и сердечной недостаточности, при которых затруднено выведение жидкости из организма. Она формируется одновременно во внеклеточном и внутриклеточном секторах (тотальная дисгидрия). Во внутриклеточном секторе она сопровождается грубыми нарушениями ионного и кислотно-щелочного баланса с последующими функциональными расстройствами. Для водного отравления характерны тошнота, многократная рвота, нарушения сознания, судороги, гемолиз форменных элементов крови, гипоомолярная кома.
Коррекцию водной интоксикации осуществляют внутривенной инфузией мочегонных средств и небольших количеств гипертонических растворов (не более 300 мл 3% раствора хлорида натрия).
Изотоническая гипергидратация возможна, например, при передозировке изотонических растворов (физиологический раствор хлорида натрия и др.). Эта гипергидрия носит, как правило, временный характер при условии нормальной работы почек. В противном случае она сопровождается увеличением объёма сосудистого и интерстициального секторов, провоцируя острую сердечную недостаточность и интерстициальные отеки.
Коррекция этого вида нарушения водно-электролитного баланса сводится, в основном, к форсированию диуреза, что достигается назначением диуретиков - натрийуретиков.
Гипертоническая гипергидратация развивается при вынужденном использовании морской воды в качесте питьевой и при введении в организм больших количеств гипертонических растворов электролитов (хлорида натрия, гидрокарбоната натрия и др.) на фоне имеющейся почечной недостаточности. Эта гипергидрия характеризуется быстрым нарастанием осмолярности интерстициального сектора, так как плазмолемма не пропускает избыток ионов в клетку. По этой причине свободная вода начинает перемещаться из клеток в межклеточное пространство, вызывая их обезвоживание. Этот тип водно-электролитного нарушения, как и гипертоническая дегидратация, сопровождается мучительной жаждой, что заставляет вновь пить соленую воду. Со временем увеличивается объем внутрисосудистого сектора, создавая условия для объемной гипертензии.
Коррекция этой гипергидрии заключается в ограничении введения солей и жидкостей и применении мочегонных средств - натрийуретиков.
8.2.3. Отек. Этот типовой патологический процесс характеризуется повышенным накоплением воды в клетках или в интерстиции. В первом случае развивается внутриклеточный отек, во втором – межклеточный.
Внутриклеточный отек – опасное следствие больших гипоосмолярных водных потерь и гипотонической гипергидрии. Он сопровождается набуханием клетки и ее ультраструктур, их значительными функциональными расстройствами и, финально, осмотическим цитолизом.
Интерстициальный отек – широко распространенная форма нарушения обмена воды между плазмой крови и периваскулярной жидкостью. Некоторые виды отеков имеют специфическое название: анасарка - отек подкожной клетчатки, асцит - скопление жидкости в брюшной полости, гидроторакс – скопление жидкости в плевральной полости.
Патогенетические механизмы интерстициального отека достаточно разнообразны и представлены следующими вариантами:
1.Гемодинамический механизм - обусловлен повышенным давлением в венозном отделе капилляров, уменьшающим реабсорбцию жидкости из интерстиция.
2.Онкотический механизм – обусловлен либо гиперонкией интерстиция, либо гипоонкией плазмы, что увеличивает связывание воды в первом случае и фильтрацию ее свободной формы – во втором.
3.Осмотический механизм – обусловлен либо гиперосмией интерстиция, либо гипоосмией плазмы и создающий осмотический градиент для перемещения свободной воды.
4.Мембраногенный механизм – обусловлен повышением проницаемости капилляров для свободной воды под действием медиаторов воспаления и аллергии, токсинов, гипоксии и ацидоза.
5.Лимфогенный механизм – обусловлен затруднением резорбции воды и крупных метаболических блоков из интерстиция в лимфатические сосуды при их тромбозе и сдавливании.
В зависимости от этиологии различают сердечный, почечный, кахектический, эндокринный, воспалительный, аллергический и токсические отеки.
8.2.3.1.Сердечный отёк возникает в результате сердечной недостаточности, появляющейся прогрессирующим снижением минутного выброса сердца и нарастающей артериальной гипотензией. Одновременно падает венозный возврат крови в сердце, сопровождающийся ее застоем в венах нижней части тела, повышением в них давления, гипоксией и ацидозом тканей. Таким образом, в начальной стадии патогенеза сердечного отека доминируют гемодинамический и мембраногенный механизмы. По мере формирования отека и сдавления им лимфатических сосудов - присоединяется лимфогенный, а при активации прессорной ренин-ангиотензин-альдостероновой системы в ответ на артериальную гипотензию и - осмотический механизмы. Венозный застой в печени и возникающие в ней дистрофические процессы, результируют снижение ее белковосинтетической функции, гипоонкию плазмы и подключение к патогенезу отека еще и онкотического механизма. В итоге «сердечный» имеет сложный, смешанный патогенез.
Принципы терапии сердечного отёка базируются на повышении сократительной функции миокарда сердечными гликозидами и усилении выведения воды и натрия мочегонными препаратами - натрийуретиками.
8.2.3.2.Почечный отек в свом патогенезе может иметь три варианта: гломерулярный (нефритический), тубулярный (нефротический) и смешанный.
Нефритический отек развивается при диффузном аутоаллергическом поражении капилляров клубочков нефрона. В его патогенезе вначале доминирует мебраногенный механизм, а по мере нарастания нарушения кровообращения и гипоксии присоединяется осмотический, вызванный активацией прессорного каскада - ренин-ангиотензин-альдостерон-АДГ.
Нефротический отек развивается при поражении эпителия канальцев нефрона. При этом падает реабсорбция белка из первичной мочи и возникает массивная протеинурия. Если потери белка с мочой не компенсируются белковосинтетической функцией печени (30 – 50г/сутки), то развивается гипоонкия плазмы и запускается онкотический механизм формирования отека.
Смешанный патогенез почечный отек приобретает при одновременном поражении гломерулярного и тубулярного отделовт нефрона.
Почечный отёк нефритического типа устраняют диуретиками, причем предпочтение отдают препаратам, блокирующим эффекты альдостерона, который является конечным звеном порочного круга патологии. Необходимо помнить, что сама по себе борьба с почечными отёками не приведёт к восстановлению функций пораженных почек. Поэтому, главные усилия медикаментозного воздействия должны быть направлены на лечение самой почечной болезни.
8.2.3.3.Кахектический(марантический) отёк развивается при разнообразной и тяжелой патологии, сопровождающейся дефицитом плазменных и соединительнотканных белков: алиментарной белковой недостаточности, злокачественном росте, печеночной недостаточности, тяжелой диареи и др. Таким образом, основу его патогенеза составляют гипоонкия плазмы и повышение капиллярной проницаемости для воды и электролитов из-за дефектов их базальных мембран.
Коррекция отёков этого вида сводится главным образом к лечению основных заболеваний.
8.2.3.4.Эндокринныйотёк или микседема развивается при выраженной гипофункции щитовидной железы и имеет специфическую метаболическую особенность. Она состоит в том, что при дефиците тиреоидных гормонов тормозится катаболизм соединительнотканных белков, а в синтезе преобладает образование муцина. Муцин является высоко гидрофильным белком и, накапливаясь в коже и мышцах, вызывает задержку в них воды и развитие отёка.
Отёк этого типа устраняют заместительной терапией тиреоидными гормонами.
8.2.3.5.Воспалительный и аллергический отеки развиваются в результате повышения капиллярной проницаемости под действием медиаторов и изначально являются мембраногенными. В дальнейшем присоединяется осмотический механизм, обусловленный нарастающей гиперонкией и гиперосмией интерстиция.
Устранение отеков этого типа осуществляется патогенетической терапией воспаления и аллергии (главы 5 и 7).
8.2.3.6.Токсические отёки вызывают вещества отравляющего действия (хлор, фосген, люизит и др.), токсины насекомых, рептилий и бактерий (дифтерии, сибирской язвы). В местах альтерации они повышают капиллярную проницаемость и нарушают обменные процессы, вызывая накопление осмотически активных веществ: аммиака, мочевины, недоокисленных продуктов. Таким образом, в патогенезе токсических отеков участвуют еще мембраногенный и осмотический механизмы.
Лечение токсических отёков заключается в применении противоядий (антидотов), стабилизации капиллярных мембран и нормализации обменных процессов в тканях.
Отеки воспалительного, аллергического и токсического типов чаще всего бывают локальными, а сердечные, почечные, кахектические и эндокринные - генерализованными. Отеки являяются частью патогенеза основных заболеваний. Они отягощают их течение, так как сдавливают сосуды нервы, нарушая трофику клеток и способствуя их гибели.
