Ферменты: общие свойства и механизм действия
Ферменты – это биологические катализаторы, характеризующиеся высокой активностью и специфичностью. Благодаря этим свойствам ферментативный катализ выступает в качестве механизма биологической регуляции химических процессов в живой клетке. Закономерности биохимических процессов можно понять только на базе четких представлений о структуре и свойствах катализирующих их ферментов.
В клинико-лабораторной практике широко используется определение активности ферментов в крови, моче и клетках для диагностики и прогнозирования течения многих заболеваний, а также для контроля за эффективностью применяемых методов лечения.
Цель изучения раздела: уметь использовать знания о структуре и функциональном многообразии белков, об изменении белкового состава органов и тканей в норме и при болезнях для объяснения нормальных функций организма и их нарушений при патологии. Применять знания о свойствах ферментов и ферментативном составе органов и тканей при последующем изучении метаболизма и функций органов и для решения вопросов диагностики.
Студенту необходимо:
знать:
структуру аминокислот, пептидной связи;
– значение первичной структуры белков, определяющей их структурное и функциональное многообразие;
– уровни структурной организации белков;
– химические и энергетические особенности связей и взаимодействий, стабилизирующих различные уровни организации молекулы;
– причины и следствия денатурации белков, факторы вызывающие денатурацию;
– примеры использования денатурирующих факторов в медицине;
– основные методы разделения и очистки белков;
– классификацию и номенклатуру ферментов;
– структурно-функциональную организацию ферментов;
– механизм действия ферментов;
– кинетику ферментативных реакций;
– общие свойства ферментов;
– принципы применения препаратов белка и ферментов в медицине.
уметь:
выполнять качественные и количественные реакции определения белка;
-определять активность некоторых ферментов в биологических жидкостях.
Рекомендуемые темы реферативных сообщений
1.Рибозимы – биологические катализаторы небелковой природы.
2. Кофакторы ферментов.
3.Особенности строения, кинетики и регуляции активности аллостерических ферментов.
4.Сериновые протеазы. Применение ингибиторов протеолиза в медицине.
5. Теории ферментативного катализа
6.Твердофазный иммуноферментный анализ (ELISA) и его использование в клинической и экспериментальной биохимии.
7.Изоферменты в диагностике заболеваний.
8.Иммобилизованые ферменты в диагностике.
Методические указания к самоподготовке.
Вопросы раздела.
1. Химическая природа ферментов. Проферменты.
2. Кофакторы ферментов: химическая природа, классификация.
3. Коферменты: химическая природа, классификация, роль витаминов и их коферментная функция.
4. Структурно-функциональная организация ферментных белков: активный центр, его свойства. Контактный и каталитический участки активного центра ферментов.
5. Регуляторные (аллостерические) центры ферментов. Зависимость активности ферментов от конформации белков.
6. Общие свойства ферментов. Зависимость активности ферментов от реакции среды и температуры: биологическое и медицинское значение этих свойств ферментов.
7. Зависимость скорости ферментативной реакции от концентрации субстрата и фермента. Уравнение Михаэлиса-Ментен.
8. Общие принципы механизма действия ферментов.
9. Принципы качественного и количественного определения активности ферментов.
10. Номенклатура и классификация ферментов.
11. Особенности ферментативного состава у детей разных возрастных периодов.
12. Энзимопатии, определение.
13. Виды энзимопатий.
При подготовке к занятию необходимо вспомнить материал, изучавшийся в курсе общей химии - катализ, факторы, влияющие на катализ, химическая кинетика. Успешное усвоение материала невозможно без детальных знаний о структуре и свойствах простых и сложных белков. Переходя к разбору ферментов, необходимо обратить внимание на доказательства белковой природы энзимов, сопоставить свойства ферментов и неорганических катализаторов. Необходимо иметь четкие представления о типах специфичности ферментов, разобраться в закономерностях зависимости ферментативного катализа от температуры, рН среды.
Знание строения и свойств ферментов является необходимым для понимания механизмов протекания и регуляции всех биохимических процессов, а также для дальнейшего изучения изменений биохимического статуса при патологических состояниях и механизмов воздействия лекарственных веществ.
С целью лучшего усвоения материала выполнить следующие задания согласно таблице 4 и рисунку 5.
Таблица 4. Свойства ферментов
| Задание | Указания к выполнению задания | |
| 1.Изучите химическую природу ферментов, их сходство и различие с неорганическими катализаторами. | 1. Дайте определение понятию «ферменты», перечислите доказательства белковой природы ферментов. 2. Что такое энергия активации? Вспомните, что катализатор приводит к уменьшению энергии активации процесса, в ходе чего скорость биохимической реакции в присутствие фермента возрастает. Заполните таблицу, отражающую сходства и различия ферментов и неорганических катализаторов. | |
| Свойства | Ферменты | Неорганические катализаторы |
| Сравнение влияния на скорость реакции Влияние на подвижное равновесие Снижение энергии активации Адсорбция на поверхности Образование промежуточных соединений Каталитическая активность Специфичность | ||
| Влияние температуры Влияние рН среды Влияние активаторов и ингибиторов Влияние концентрации катализатора Влияние концентрации субстрата | ||
| Изучите структурную организацию энзимов. | 1. Разберите понятия - кофермент, апофермент, холофермент, активный центр, аллостерический центр. 2. Отметьте, чем представлены активные центры ферментов простых и сложных белков. 3. Помимо белков, могут ли обладать ферментативной активностью молекулы других классов биополимеров? Назовите витамины, активной формой которых является НАД. Назовите витамин, активной формой которого является ФАД. | |
| Изучите специфичность ферментов. | 1.Выпишите понятия специфичности фермента и подумайте, чем обусловлена специфичность ферментов. Объясните биологический смысл специфичности. 2. Приведите примеры ферментов с абсолютной, групповой и стереохимической специфичностью. 3. Вспомните теории энзим - субстратных взаимодействий Фишера и Кошленда и дайте определение, какая из этих теорий приемлема на современном уровне для объяснения специфичности ферментов. | |
| Изучите зависимость ферментативной реакции от температуры. | 1. Графически изобразите зависимость активности ферментов от температуры. 2. Охарактеризуйте состояние фермента при 00С и при 1000С. 3. Приведите примеры термолабильных и термостабильных ферментов. 4. Какое практическое значение имеют знания зависимости активности ферментов от температуры. | |
| Изучите зависимость ферментативной активности от рН среды. | 1. Изобразите графическую зависимость от рН среды активности пепсина, трипсина, амилазы слюны, кислой и щелочной фосфатазы. 2. Выделите три ведущих фактора, объясняющие зависимость ферментативного катализа от рН среды. 3. Поясните, для чего специалисту медицины необходимо знать свойства ферментов. | |
| Изучите современную классификацию и номенклатуру ферментов. | 1. Приведите классификацию ферментов. На чем основана классификация ферментов? 2. Напишите примеры типов реакций, катализируемых каждым из 6 классов ферментов, дайте ферментам систематические названия. 3. Определите, к какому классу, относятся ферменты: α-амилаза, щелочная фосфатаза, холинэстераза, моноаминооксидаза. |
| ФЕРМЕНТЫ – БИОКАТАЛИЗАТОРЫ БЕЛКОВОЙ ПРИРОДЫ |
| СВОЙСТВА, ОБУСЛОВЛЕННЫЕ БЕЛКОВОЙ ПРИРОДОЙ |
| СПЕЦИФИЧНОСТЬ |
| ВЫСОКАЯ КАТАЛИТИЧЕСКАЯ АКТИВНОСТЬ |
| ТЕРМОЛАБИЛЬНОСТЬ |
| ЗАВИСИМОСТЬ ОТ рН |
| имеют АКТИВНЫЙ ЦЕНТР – связывание субстрата и его превращение |
| некоторые имеют АЛЛОСТЕРИЧЕСКИЙ ЦЕНТР – связывание эффекторов, регуляция активности |
| абсолютная |
| групповая |
| стереохимическая |
| тепловая денатурация |
| влияние на заряд |
| изменение конформации |
Рисунок 5. Схема «Общие свойства ферментов»
Примеры заданий для контроля исходного уровня знаний
Выберите один наиболее верный ответ.
1. АБСОЛЮТНОЙ СПЕЦИФИЧНОСТЬЮ ОБЛАДАЕТ
1) протеиназа
2) липаза
3) уреаза
4) α-амилаза
2. К КОФЕРМЕНТАМ ОТНОСИТСЯ
1) пируват
2) НАД+
3) витамин В1
4) тирозин
3. ФЕРМЕНТЫ УВЕЛИЧИВАЮТ СКОРОСТЬ РЕАКЦИИ ПОСКОЛЬКУ
1) снижают энергию активации
2) повышают энергию активации
3) изменяют константу равновесия реакции
4) уменьшают изменение свободной энергии реакции
Выберите несколько ответов.
4.ФЕРМЕНТ ОТ НЕОРГАНИЧЕСКОГОКАТАЛИЗАТОРА ОТЛИЧАЕТ
1) способность ускорять реакцию
2) высокая специфичность
3) выход из реакции в неизменном состоянии
4) термолабильность
5) действие в малых концентрациях
5. ВЛИЯНИЕ рН НА ХОД РЕАКЦИИ, КАТАЛИЗИРУЕМОЙ ФЕРМЕНТОМ ЗАКЛЮЧАЕТСЯ В ТОМ, ЧТО
1) [Н+] изменяет направление реакции
2) [Н+] определяет степень ионизации аминогрупп
3) экстремальные значения рН вызывают денатурацию фермента
4) [Н+] определяет степень ионизации карбоксильных групп и субстрата
5) [Н+] вызывает высаливание фермента
.
Эталоны ответов к заданиям
1.-3); 2. –2); 3. –1);
4. – 2),4); 5. -1),2),3),4).
Примеры обучающих задач
Задача 1.Трипсин – фермент, часто используемый в препаративной биохимии для очистки белковых препаратов в ходе анализа. Объясните, почему молекулы трипсина не атакуют друг друга, ведь трипсин относится к протеолитическим ферментам, гидролизующим пептидные связи, а сам трипсин - белок?
Задача 2.Экспериментальные данные свидетельствуют, что в некоторых случаях при полном насыщении фермента субстратом тепловая денатурация фермента наступает при более высоких температурах. Чем объясняется протективное действие высоких концентраций субстрата против тепловой денатурации?
Задача 3.В отдельную группу металлоферментов выделены энзимы, содержащие ионы металлов в качестве простетической группы. Примерами таких ферметов являются цитохромоксидаза, каталаза, пероксидаза, апофермент которых связан с гемовым железом, Zn2+-содержащая карбоангидраза и многие другие ферменты. Объясните, почему в роли кофактора чаще всего выступают переходные металлы?
Задача 4.. Студент получил задание – охарактеризовать активный центр 3 ферментов Е1, Е2, Е3. Для этого он использовал вещества: диизопропилфторфосфат (ДФФ, специфический необратимый ингибитор «сериновых» ферментов) и монойодуксусную кислоту (необратимый неспецифический ингибитор ферментов), а также субстраты этих ферментов. Проведя свои опыты, студент сделал вывод, что Сер присутствует в активном центре ферментов Е1 и Е2, а в активном центре Е1, Е3 и Е2 он определил наличие аминокислотного остатка Цис.
Оцените достоверность результатов, полученных студентом.
Для ответа на вопрос:
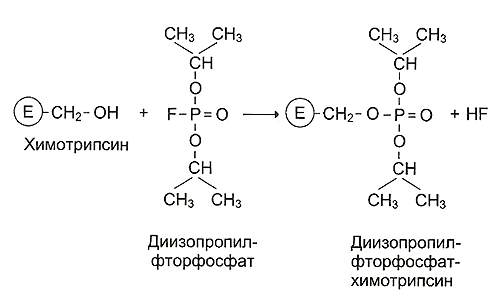
а) укажите, почему в работе студент использовал ДФФ и монойодуксусную кислоту; представьте схемы, объясняющие механизм их взаимодействия с ферментом;
б) опишите, как студент мог определить активность ферментов; укажите, в каких единицах измеряется активность ферментов.
Эталоны ответов на задачи
Задача 1.Как и большинство протеолитических ферментов, трипсин обладает специфичностью действия - этот фермент активен в отношении пептидных связей, образованных карбоксильной группой аргинина и лизина. Молекулы трипсина не атакуют друг друга, т.к. аминокислотные последовательности на поверхности молекулы трипсина не соответствуют его специфичности.
Задача 2.Согласно теории индуцированного соответствия (теории Кошленда), связываясь с активным центром, субстрат вызывает изменение пространственной формы молекулы фермента и переводит его в более устойчивую, стабильную конформацию.
Задача 3.Наличие сильного положительного заряда, большое число свободных орбиталей (следовательно, способность связывать большое число лигандов обусловливают их участие в биокатализе в качестве кофакторов.
Задача 4:
а) ДФФ относится к специфическим необратимым ингибиторам «сериновых» ферментов, т.к. он образует ковалентную связь с гидроксильной группой серина в активном центре фермента при условии определенного окружения радикала серина – Асп, Сер, Глу. Вывод, сделанный студентом, о наличии в активном центре ферментов Е1 и Е2 серина, правильный.
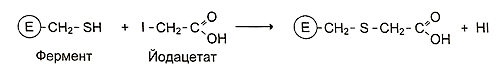
Использовать монойодуксусную кислоту для установления структуры функциональных групп активного центра фермента нельзя. Это вещество относится к необратимым неспецифическим ингибиторам ферментов и образует ковалентные связи со свободными SH-группами цистеина, занимающими любое положение в молекуле белков. Вывод студента о наличии SH-группы в активном центре ферментов Е1, Е2 и Е3 необходимо проверить, применяя специфические ингибиторы;
б) Добавляя субстрат в реакционную смесь, уже содержащую фермент и ДФФ или монойодуксусную кислоту, он смог оценить ингибирующее действие этих веществ по снижению скорости расходования субстрата или образования продукта. Результаты опытов показали снижение активности всех ферментов (Е1, Е2, Е3).
Удельная активность фермента = S (мкмоль) /τ (мин) · m (мг).
Задача 5.
а) Конкурентное ингибирование; из-за схожести химических структур сульфаниламидов и ПАБК.
б) Конкурентные ингибиторы увеличивают Км, не изменяют Vmax; сульфаниламиды как структурные аналоги ПАБК связываются в активном центре фермента дигидроптеоратсинтазы (вместо ПАБК), ингибируя ее.
в) Конкурентное ингибирование можно ослабить или полностью прекратить, повысив концентрацию субстрата (ПАБК), поэтому при высокой концентрации ПАБК сульфаниламиды неэффективны.
г) Это делают для того, чтобы за короткий промежуток времени достичь большой концентрации сульфаниламидов в крови, большинство молекул дигидроптеоратсинтазы будет ингибировано (при конкурентном ингибировании степень ингибирования пропорциональна отношению концентраций ингибитора и субстрата: чем оно выше, тем полнее ингибирование). Таким образом, бактерии теряют способность синтезировать нуклеиновые кислоты, размножаться и погибают.
д) Нет, т.к. сульфаниламиды влияют на синтез фолиевой кислоты. На процессы усвоения и образования коферментных форм фолиевой кислоты в организме человека сульфаниламидные препараты не воздействуют.
