Биотрансформация лекарственных веществ
Большинство лекарственных веществ в организме претерпевают биотрансформацию – подвергаются метаболизму. Из одного и того же вещества могут образовываться не один, а несколько метаболитов, иногда десятки, как это показано, например, для аминазина. Осуществляется биотрансформация лекарственных веществ, как правило, под контролем ферментов (хотя возможно и неферментное их превращение, например химическое - путем гидролиза). В основном метаболизирующие ферменты локализованы в печени, хотя немаловажную роль в метаболизме лекарственных веществ могут играть и ферменты легких, кишечника, почек, плаценты и других тканей. Регулируя такие фармацевтические факторы как вид лекарственной формы (суппозитории вместо таблеток, в/в инъекция вместо пероральных лекарственных форм), можно в значительной степени избежать на первых порах прохождения вещества через печень и, следовательно, регулировать биотрансформацию.
Образование токсических метаболитов можно, также, значительно уменьшить регуляцией фармацевтических факто ров. Например, при метаболизме амидопирина в печени, образуется канцерогенное вещество – диметилнитрозамин. После ректального введения соответствующих лекарственных форм этого вещества отмечается интенсивное всасывание, превосхо-дящее в 1,5 - 2,5 по интенсивности таковое при пероральном приеме, что позволяет снизить дозировку вещества при сохранении терапевтического эффекта и снижении уровня токсичного метаболита.
Биотрансформация обычно приводит к снижению или исчезновению биологической активности, к инакгивации лекарств. Однако с учетом фармацевтического фактора - простая химическая модификация, в ряде случаев можно достигать образования более активных или менее токсичных метаболитов. Так, противоопухолевый препарат фторафур в организме отщепляет гликозидный остаток, высвобождая активный противоопухолевый антиметаболит - фторурацил. Сложный эфир левомицетина и стеариновой кислоты безвкусен в отличие от горького левомицетина. В желудочно-кишечном тракте происходит ферментативный гидролиз неактивного эфира, а высвободившийся левомицетин всасывается в кровь. Плохо растворимый в воде левомицетин переводом в сложный эфир с янтарной кислотой (сукцинат) превращается в хорошо растворимую соль - новая химическая модификация, используемую уже и для в/м и в/в введения. В организме в результате гидролиза этого эфира, достаточно быстро отделяется сам левомицетин.
Для снижения токсичности и улучшения переносимости синтезирована простая химическая модификация изониазида - фтивазид (гидразон изониазида и ванилина). Постепенное высвобождение вследствие биотрансформации противотуберку-лезной активной части молекулы фтивазида – изониазида, уменьшает частоту и выраженность побочных эффектов, характерных при приеме чистого изониазида. То же характерно и для салюзида (гидразон изониазида, полученный конденса-цией его с 2-карбокси-3, 4- диметил бензальдегидом), который в отличие от изониазида можно вводить парентерально.
Экскреция (выведение) лекарственных веществ и их метаболитов
Основными путями экскреции лекарственных веществ и их метаболитов является выделения с мочой и калом, наряду с этим вещества могут выводиться из организма с выдыхаемым воздухом, с секретом молочных, потовых, слюнных и других желез.
Регулируя соответствующим образом фармацевтические факторы для ряда лекарственных веществ можно регулировать и процессы экскреции. Так, увеличивая рН мочи (одновременным введением с лекарственными веществами - слабыми кислотами - щелочнореагирующих компонентов, таких, как натрия гидрокарбонат и др. соответствующих вспомогательных веществ) можно существенно повысить выделение (экскрецию) почками ацетилсалициловой кислоты, фенобарбитала, пробени-цида. Для лекарственных веществ - слабых оснований (новокаин, амфетамин, кодеин, хинин, морфин и др.) имеет место обратная картина - слабые органические основания лучше ионизируются при низких значениях рН (кислой моче), при этом они в ионизированном состоянии плохо реабсорбируются канальцевым эпителием и быстро выделяются с мочой. Введение их вместе со вспомогательными веществами, понижающими рН мочи, (алюминия хлорид, например) способствует быстрому выделению их из организма.
Многие лекарственные вещества проникают из крови в паренхиматозные клетки печени. К этой группе веществ относится левомицетин, эритромицин, олеандомицин, сульфаниламиды, ряд противотуберкулезных веществ и др.
В клетках печени лекарственные вещества частично подвергаются биотрансформации и в неизменном виде или в виде метаболитов (в том числе и коньюгатов) выводятся с желчью или возвращается в кровь. Экскреция лекарственных веществ желчью зависит от ряда факторов, таких как молекулярная масса, совместное применение веществ усиливаю-щих экскрецию желчи - сульфат магния, питуитрин, или секреторную функцию печени - салицилаты, рибофлавин.
Другие пути выведения лекарственных веществ - с потом, слезами, молоком менее существенны для всего процесса выделения.
Исследования всасывания, распределения, биотрансформа-ции и выведения многих лекарственных веществ показали, что способность лекарственного вещества оказывать лечебное действие является лишь его потенциальным свойством, которое может значительно изменяться в зависимости от фармацевтических факторов.
Применяя различное исходное сырье, различные вспомога-тельные вещества, технологические операции и оборудование, можно менять не только скорость высвобождения лекарственного вещества из лекарственной формы, но и скорость и полноту его всасывания, особенности биотрансформации и выделения, а в конечном итоге его терапевтическую эффективность
Таким образом, на все отдельные звенья транспорта лекарственных веществ в организме оказывают влияние различные фармацевтические факторы. А так как терапевтическая эффективность и побочные эффекты лекарств зависят от концентрации всосавшегося лекарственного вещества в крови, органах и тканях, от длительности пребывания вещества там, от особенностей его биотрансформации и выделения, то тщательное изучение влияния фармацевтических факторов на эти процессы, профессиональное, научное регулирование этих факторов на всех стадиях создания и исследования лекарств будет способствовать оптимизации фармакотерапии – повышению ее эффективности и безвредности.
ЛЕКЦИЯ 5
ПОНЯТИЕ БИОЛОГИЧЕСКОЙ ДОСТУПНОСТИ ЛЕКАРСТВ. МЕТОДИКИ ЕЕ ИССЛЕДОВАНИЯ.
Биофармация наряду с тестом фармацевтической доступности предлагает устанавливать специфический критерий для оценки влияния фармацевтических факторов на всасывае-мость лекарственногосредства - биологическую доступность - степень, в которой лекарственное вещество всасывается из места введения в системный кровоток и скорость, с которой этот процесс происходит.
Первоначально критерием степени всасывания лекарствен-ного вещества был взят относительный уровень в крови, создающийся при введении вещества в изучаемой и стандартной форме. Сравнивали, как правило, максимальные концентрации лекарственного вещества. Однако такой подход к оценке всасывания веществ неадекватен по целому ряду причин.
Во-первых, потому что выраженность биологического действия многих лекарственных веществ обусловлена не только их максимальным уровнем, но и временем, в течение которого концентрация вещества превышает минимальный уровень, необходимый для реализации фармакологического эффекта. Во-вторых, эмпирическая оценка момента максимума концентрации вещества в крови может оказаться неверной. В-третьих, эта оценка может быть не точной из-за ошибок определения. Все это побудило исследователей характеризовать степень всасыва-ния не отдельными точками, а фармакокинетической кривой
С = f ( t ) в целом.
А так как интегральное представление о кривой проще получить, измеряя площадь, ограниченную этой кривой с осью абсцисс, то и было предложено характеризовать степень всасывания лекарственноговещества величиной площади под соответствующей фармакокинетической кривой.
Отношение площадей под кривыми, полученными при введении лекарственного вещества в изучаемой и стандартной формах получило название степени биологической доступности:
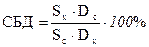 , где:
, где:
Sx - площадь под ФК-кривой для исследуемого вещества в изучаемой лекарственной форме;
Sc - площадь под ФК-кривой для этого же вещества в стандартной лекарственной форме;
Dc и Dx – соответственно дозы вещества в испытуемой и стандартной лекарственных формах.
Исследования биологической доступности проводятся в виде сравнительных экспериментов “in vivo”, в которых лекарство сравнивается со стандартной (наиболее доступной) лекарственной формой этого же активного вещества.
Различают абсолютную и относительную биологическую доступность. В качестве стандартной лекарственной формы, при определении «абсолютной» биологической доступности применяется раствор для внутривенного введения. Внутривенная инъекция дает наиболее четкие результаты, так как доза поступает в большой крут кровообращения и биологическая доступность препарата в этом случае является наиболее полной - практически стопроцентной.
Однако, более распространено и, возможно, более целесообразно определение относительной биологической доступности. При этом стандартной лекарственной формой, как правило, служит раствор для внутреннего употребления и лишь в случаях, когда вещество нерастворимо или неустойчиво в водном растворе может использоваться другая лекарственная форма для приема внутрь, которая хорошо охарактеризована и хорошо всасывается, например, суспензия микронизированного вещества или микронизованный препарат, заключенный в желатиновую капсулу.
Опыт биофармации показал, что характеристика всасыва-ния лекарственного вещества степенью, в которой оно всасывается, недостаточна. Дело в том, что даже при полном всасывании лекарственного вещества его концентрация в крови может не достигать минимального эффективного уровня, если скорость всасывания невелика по сравнению со скоростью выделения (элиминации) этого вещества из организма. На рис. (рис 5.1.) представлены некоторые из возможных ситуаций, возникающих при введении препаратов А, В, С, содержащих одинаковую дозу одного и того же лекарственного вещества, различающихся примененными в процессе их создания фармацевтическими факторами.
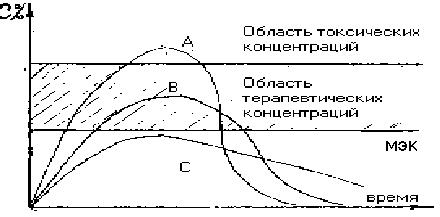
Рисунок 5.1
Изменение концентрации лекарственного вещества в биологической жидкости после введения лекарственных форм, различающиеся фармацевтическими факторами.
При введении препарата А и В концентрация лекарствен ного вещества в крови превышает минимальную эффективную концентрацию (МЭК) в первом случае больше, чем во втором, а при введении препарата С концентрация лекарственного вещества так и не достигает минимальной эффективной концентрации, хотя величины площадей под ФК-кривыми во всех 3-х случаях одинаковы. Таким образом, видимые различия в фармакокинетике лекарственного вещества после его введения в формах А, В, С обусловлены неодинаковой, скоростью всасывания. Вот почему при определении биологической доступности с 1972 г. (Riegelman L.) введено обязательное установление и скорости всасывания, т.е. скорости, с которой вещество поступает из места введения в системный кровоток.
Таким образом, в определении биологической доступности нашли свое отражение интегральный (степень всасывания) и кинетический (скорость всасывания) аспекты оценки процесса всасывания.
При определении биологической доступности производят последовательный забор проб необходимых жидкостей (крови, мочи, слюны, лимфы и др.) в течение строго обусловленного периода времени и определяют в них концентрацию вещества (см. учебник Муравьева И.А., I960 г., ч.1, стр.295, I и 2 абзацы - определение БД на здоровых добровольцах).
Пробы для определения биологической доступности берут из различных мест в зависимости от терапевтического применения лекарстенных веществ. Обычно для этого используют венозную и артериальную кровь или мочу. Имеются, однако, лекарства, биологическую доступность которых целесообразнее определять на месте фактического воздействия лекарстеного вещества. Например, лекарства, которые действуют в желудочно-кишечном тракте или лекарственные формы для нанесения на кожные покровы.
Полученные данные содержания веществ (или их метаболитов) в биожидкостях вносят в таблицы, на основании которых строят графики зависимости концентрации лекарственного вещества в биожидкостях от времени ее обнаружения - (ФК-кривые) C = f (t).
Таким образом, любая разница в биологической доступности сравниваемых лекарств отражена в кривой концентрации веществ в крови или в схеме его выделения с мочой. При этом надо учитывать, что на концентрацию лекарственного вещества в крови влияют и другие переменные факторы: физиологические, патологические (эндогенные) и экзогенные.
Поэтому, чтобы повысить точность исследований необходимо учитывать все переменные величины. Влияние таких факторов как возраст, пол, генетические различия в метаболизме лекарственных веществ, а также наличие патологических состояний, можно в значительной степени контролировать с помощью метода «перекрестного эксперимента».
Влияние факторов, которые непосредственно могут быть проконтролированы исследователем (прием пищи, одновременное введение или прием других лекарств, количество выпитой воды, рН мочи, физическая активность и др.) доводят до минимума путем строгой стандартизации условий эксперимента.
МЕТОДЫ ОЦЕНКИ БИОЛОГИЧЕСКОЙ ДОСТУПНОСТИ. ОЦЕНКА СТЕПЕНИ ВСАСЫВАНИЯ. ИССЛЕДОВАНИЯ С ПРИМЕНЕНИЕМ ОДНОКРАТНОЙ ДОЗЫ.
Степень всасывания чаще определяется по результатам исследования содержания вещества в крови после однократного его назначения.
Преимущества этого метода в том, что при применении однократных доз здоровые люди в меньшей степени подвергаются воздействию лекарства.
Однако концентрацию лекарственного вещества нужно проследить минимально в течение трех полупериодов его нахождения в организме (или дольше). При внесосудистных способах введения препарата необходимо установление времени (tmax.) достижения максимальной концентрации – Сmax.
Для построения кривой C = f (t) зависимости концентрации веществ в крови от времени необходимо получить, по крайней мере, три точки на восходящей и столько же на нисходящей ветвях кривой. Поэтому требуется большое количество проб крови, что является определенным неудобством для лиц, участвующих в опыте.
Расчет степени биологической доступности ведут по формуле:
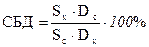 , где:
, где:
Sx и Dx - площадь под кривой и доза исследуемого вещества в испытуемой лекарственной форме;
Sc и DC - площадь под кривой и доза этого же вещества в стандартной лекарственной форме.
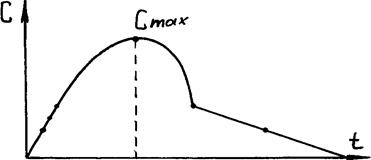 |
Рисунок 5.2
Зависимость концентрации веществ в крови от времени.
В исследованиях степени биологической доступности с применением однократной дозы совершенно необходимы специфические и высоко чувствительные аналитические методы. Необходимо также подробное знание фармакокине-тических характеристик лекарственного вещества. Этот метод может оказаться непригодным в тех случаях, когда лекарственное вещество имеет сложные фармакокинетические свойства. Например, когда выделение с желчью сопровождается повторным всасыванием лекарственного вещества, что приводит к его циркуляции в печени.
ИССЛЕДОВАНИЯ С ПРИМЕНЕНИЕМ ПОВТОРЯЮЩИХСЯ ДОЗ.
В отдельных случаях, в частности для правильной оценки степени биологической доступности лекарств, предназначенных для длительного применения, проводят исследование с повторными дозами.
Этот метод предпочтительнее в условиях клиники, где исследования проводятся на больных, получающих лекарство регулярно в соответствии с курсом лечения. По существу больной проходит лечение препаратом, эффективность которого контролируется по его содержанию в биожидкостях.
Пробы на анализ при этом методе можно получать лишь после того, как будет достигнута устойчивая концентрация вещества в крови. Она достигается обычно после 5-10 доз и зависит от полупериода нахождения вещества в организме. После достижения устойчивой концентрации вещества в крови, время достижения его максимальной концентрации становится постоянным. В этом случае определяют максимальную концентрацию для стандартной лекарственной формы, а затем через установленный интервал времени назначают вещество в исследуемой лекарственной форме и также определяют его максимальную концентрацию в крови.
Расчет степени биологической доступности ведут по формуле:
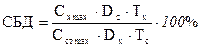 , где:
, где:
Сх - максимальная концентрация для исследуемого препарата;
Сст - максимальная концентрация для стандартного препарата;
Dx и Dc – дозы соответствующих препаратов;
Тх и Тс - время достижения максимальной концентрации после назначения исследуемой и стандартной лекарственной формы.
Степень биологической доступности здесь может быть рассчитана и с использованием значений площади под кривой или значений максимальных концентраций. Площадь под кривой, в этом случае, измеряется в течение только одного интервала между дозами, после достижения устойчивой концентрации.
Положительной стороной методики назначения повторяющихся доз веществ является сравнительно высокое содержание вещества в крови, что облегчает проведение аналитических определений и повышает их точность.
ИССЛЕДОВАНИЯ ПО ОПРЕДЕЛЕНИЮ СОДЕРЖАНИЯ ВЫДЕЛЯЕМОГО С МОЧОЙ ВЕЩЕСТВА ИЛИ ЕГО МЕТАБОЛИТА.
Определение степени биологической доступности по содержанию выделяемого с мочой вещества предусматривает выполнение ряда условий:
1) выделение хотя бы части вещества в неизменном виде;
2) полное и тщательное опорожнение мочевого пузыря при каждом заборе проб;
3) Время сбора мочи, как правило, равняется 7-10 полупериодам нахождения препарата в организме. Именно за этот период успевает выделиться из организма 99,9% введенного лекарственного вещества. Желательны наиболее частые заборы проб на анализ, так как это позволяет более точно определить концентрацию вещества, расчет степени биодоступности ведут по формуле:
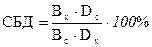 , где:
, где:
В - количество выделенного с мочой неизмененного вещества после назначения исследуемой (х) и стандартной (с) лекарственной формы;
Dx и Dc – дозы соответствующих препаратов.
ОПРЕДЕЛЕНИЕ СКОРОСТИ ВСАСЫВАНИЯ ЛЕКАРСТВЕННЫХ ВЕЩЕСТВ. ЭЛЕМЕНТЫ МОДЕЛИРОВАНИЯ ФАРМАКОКИНЕТИКИ.
Существующие методы оценки скорости всасывания лекарственных веществ основываются на допущении линейнос-ти кинетики всех процессов поступления, переноса и элиминации лекарств в организме.
Простейшим методом определения константы скорости всасывания является метод Dost (1953 г.), основанный на использовании соотношения между константами элиминации и всасывания и временем максимума концентрации на фармакокинетической кривой.
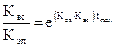 , где:
, где:
е - основание натурального логарифма = 2,71828...;
tmax - время достижения максимального уровня концентра-ции вещества в организме.
К этой формуле составлена специальная таблица зависимости произведения Кэл·tmax и функции E, которая вычисляется затем по формуле:
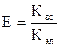 , отсюда Квс=Кэл·Е
, отсюда Квс=Кэл·Е
Фрагмент таблицы и пример вычисления.
| Е | Кэл·tmax |
| 0,01 | 4,652 |
| 0,02 | 3,992 |
| 2,5 | 0,912 |
| 2,5 | 0,872 |
Так, если Кэл = 0,456, а tmax = 2 часа, то их произведение = 0,912. По таблице это соответствует величине функции Е 2,5. Подставляя это значение в уравнение: Квс=Кэл·Е = 0,456·2,5 = 1,1400 ч-1;
Предложена также следующая формула для вычисления константы всасывания (на основе одночастевой модели; Saunders, Natunen, 1973 г.)
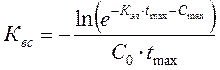 , где:
, где:
е = 2,71828;
Сmax - максимальная концентрация, устанавливаемая через время tmax;
Сo - концентрация вещества в организме в нулевой момент времени, при предположении, что все вещество (доза) поступит в организм и мгновенно распределится в крови, органах и тканях.
Вычисление указанных величин, носящих название параметры фармакокинетики, проводят несложным графичес-ким методом. С этой целью строят кривую фармакокинетики в так называемой полулогарифмической системе координат. На оси ординат откладывают значения lgСt - экспериментальным путем установленные величины концентрации вeщecтвa в биoлoгичec-кoй жидкости за время t, а на оси абсцисс - время достижения этой концентрации в натуральных величинах (сек, мин или часах). Отрезок оси ординат, отсекаемый продолжением (на графике это штриховая линия) линеаризованной кривой дает значение Сo, а величина тангенса угла наклона линеаризованной кривой к оси абсцисс численно равна константе элиминации. tgω=Kэл•0,4343
По найденным значениям константы элиминации и величине Сo можно вычислить и ряд других параметров фармакокинетики для одночастевой модели.
Объем распределения V - условный объем жидкости, необходимый для растворения всей дозы введенного вещества до получения концентрации равной Сo. Размерность - мл, л.
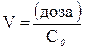
Общий клиренс (плазменный клиренс) CIt, - параметр, характеризующий скорость "очищения" организма (плазмы крови) от лекарственного вещества в единице времени. Размерность - мл/мин, л/час.
CIt=V•Kэл
Период полуэлиминации (полусуществования) Т1/2 или t1/2 - время элиминации из организма половины введенной и всосавшейся дозы вещества.
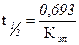
Площадь под фармакокинетической кривой АUС0-¥
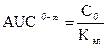 или
или 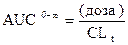
Это площадь фигуры на графике, ограниченной фармакокинетической кривой и осью абсцисс.
Истинный уровень максимальной концентрации Сmax вещества в организме и время ее достижения tmax вычисляют из уравнения:
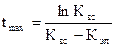
Из этого уравнения следует, что время достижения максимального уровня вещества в организме не зависит от дозы и определяется только соотношением между константами всасывания и элиминации.
Величину максимальной концентрации находят по уравнению:
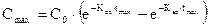
Определение параметров фармакокинетики и, в частности, константы скорости всасывания, для двухчастевой модели рассматривают на курсе фармакотерапии
Определение параметров ФД, БД и фармакокинетики проводятся обычно в процессе разработки или совершенство-вания лекарственного препарата, при сравнительной оценке одного и того же препарата, выпускаемого на различных предприятиях, в порядке постоянного контроля качества и стабильности лекарственных препаратов.
Установление биологической доступности лекарств имеет огромное фармацевтическое, клиническое и экономическое значение.
Рассмотрим материалы о влиянии различных переменных факторов на параметры фармацевтической и биологической доступности.
ЛЕКАРСТВЕННЫЕ ФОРМЫ И ИХ ЗНАЧЕНИЕ В ПОВЫШЕНИИ ФАРМАЦЕВТИЧЕСКОЙ И БИОЛОГИЧЕСКОЙ ДОСТУПНОСТИ
Водные растворы в виде микстур, сиропов, эликсиров и др., как правило, обладают наиболее высокой фармацевтической и биологической доступностью активных ингредиентов. Для повышения БД отдельных видов жидких лекарственных форм строго регулируют количество и природу вводимых стабилиза-торов, корректоров вкуса, цвета и запаха.
Высокой биологической доступностью отличаются и жидкие перорально назначаемые микрокристаллические (размер частиц менее 5 мкм) суспензии. Недаром водные растворы и микрокристаллические суспензии используются в качестве стандартных лекарственных форм при определении степени всасывания.
Капсулы имеют преимущество перед таблетками, так как обеспечивают более высокую фармацевтическую и биологичес-кую доступность включаемых лекарственных веществ. Большое влияние на скорость и степень всасывания веществ из капсул оказывает размер частиц помещенного в капсулу ингредиента, природа наполнителей (скользящих, красящих и т.д.), используемых обычно для улучшения расфасовки сыпучих компонентов в капсулы.
По данным Зак А.Ф. (1987 г.) капсулы рифампицина по 150 мг, изготовленные различными фирмами, различаются по скорости перехода антибиотика в раствор в 2-10 раз. При сравнении биодоступности капсул рифампицина, выпущенных фирмами А и Д, установлено, что количество антибиотика в крови добровольцев на протяжении 10 часов наблюдения, после приема капсул фирмы А, было в 2,2 раза выше, чем после приема капсул фирмы Д. Максимальные уровни рифампицина в первом случае определялись через 117 минут и равнялись 0,87 мкг/мл, во втором - через 151 минуты и равнялись 0,46 мкг/мл.
Таблетки, приготавливаемые методом прессования могут в значительной степени различаться фармацевтическая и билогическая доступность включенных веществ, так как состав и количество вспомогательных веществ, физическое состояние ингредиентов, особенности технологии (виды гранулирования, давление прессования и др.), определяющие физико-механические свойства таблеток, могут значительно изменить как скорость высвобождения и всасывания, так и общее количество вещества, достигшего кровяного русла.
Так, при идентичности состава, установлено, что биодоступность салициловой кислоты и фенобарбитала в таблетках зависела от величины давления прессования; амидопирина, альгина - от типа грануляции; преднизолона, фенацетина - от природы гранулирующей жидкости; гризеофульвина и хинидина - от материала прессующего устройства (пресс-инструмента) табле-точной машины и, наконец, параметры биодоступности фенилбутазона и хинидина в форме таблеток зависели от скорости работы таблеточной машины, запрессовывающей или полностью выдавливающей из прессуемой массы воздух.
В сложном комплексе взаимовлияния различных факторов на биодоступность веществ в форме таблеток разобраться подчас трудно. Тем не менее во многих случаях удается точно установить влияние конкретных факторов на параметры биодоступности. В первую очередь это касается двух важнейших стадий процесса таблетирования - гранулирования и прессования.
Стадия влажной грануляции является наиболее ответственной за изменение физико-механических свойств таблеток, химическую стабильность компонентов. Применение склеивающих, скользящих, разрыхляющих вспомогательных веществ на этой стадии, перемешивание, контакт увлажненной массы с большим числом металлических поверхностей, наконец, смена температур в процессе сушки гранул - все это может послужить причиной полиморфных превращений лекарственных веществ с последующим изменением параметров их биодоступности.
Так, скорость и степень всасывания в желудочно-кишечном тракте натрия салицилата существенно различается в зависимости от того, какой тип грануляции или способ таблетирования используется в производстве таблеток. При влажной грануляци кинетика всасывания натрия салицилата характеризуется медленным повышением концентрации салицилатов в крови, которая не достигает даже минимальной эффективной концентрации (МЭК). В то же время из таблеток, полученных методом прямого прессования отмечается быстрое и полное всасывание натрия салицилата.
Как ни при каком способе гранулирования в процессе влажной грануляции возможно течение разнообразных превра-щений лекарственных веществ - реакции гидролиза, окисления и др., что приводит к изменению биологической доступности. Примером может служить информация о таблетках с алкалоидами раувольфии. Влажная грануляция приводит к частичной деструкции и биологическая доступность их в форме таблеток снижается практически на 20% в сравнении с таблетками, полученными прямым прессованием.
Давление прессования существенно влияет на характер связи между частицами в таблетке, на размер этих частиц, возможность полиморфных превращений и поэтому способно существенно изменять не только фармацевтическая доступность, но и фармакокинетические параметры и биологическая доступность. Наличие крупных или прочных агрегатов частиц лекарственных веществ, малодоступных воздействию содержимого желудочно-кишечный тракт в конечном итоге отражается на интенсивности растворения, всасывания и уровне концентрации вещества в крови.
Так, при значительных давлениях прессования образуются крупные агломераты ацетилсалициловой кислоты, возрастает твердость таблеток и уменьшается время растворимости (высвобождения) вещества. А уменьшение растворимости малорастворимых лекарственных веществ отрицательно сказывается на их биологической доступности.
Согласно данным (Welling, I960 г.) биофармацевтических исследований в 6 американских клиниках (штат Нью-Йорк) наблюдали увеличение частоты инсультов, после того, как стали применять таблетки с фентанилом (анальгетик) другой фирмы-изготовителя. Выяснилось, что это явление связано с изменением биодоступности у новых таблеток вследствие изменения природы вспомогательного вещества и давления прессования измельченных кристаллов фентанила.
Многие исследователи показали, что имеющиеся за рубежом в продаже таблетки дигоксина, изготовленные по различающейся технологии с применением различных вспомогательных веществ и видов грануляции, могут очень существенно различаться по биодоступности - от 20% до 70%. Проблема биодоступности таблеток дигоксина оказалась настолько острой, что в США после биофармацевтических исследований была запрещена продажа таблеток около 40 фирм-изготовителей, посколько их параметры биодоступности оказались весьма низкими. Кстати, таблетки дигоксина, выпускаемые в СНГ, оказались по биодоступности на уровне лучших мировых образцов (Холодов Л.Е. и др., 1982 г.).
Нерационально осуществленный подбор переменных (технологических) факторов при производстве таблеток может стать причиной усиления побочного действия, присущего данному лекарственному веществу. Так, в случае с ацетилсали-циловой кислотой, вызывающей, как известно при приеме внутрь желудочные и кишечные кровотечения, наиболее значительные кровотечения - 2; 3 мл ежедневно в течение 7 дней отмечается после назначения таблеток, спрессованных без буферных добавок, а для так называемых "забуференных" - только 0,3 мл.
Для нашей страны проблема биоэквивалентности таблетированных препаратов не так актуальна, как за рубежом, поскольку таблетки одного наименования выпускаются одним или реже двумя-тремя предприятиями по одинаковому технологическому регламенту. Продукция поэтому оказывается однородной по всем параметрам, включая и биодоступноеть.
При усовершенствовании технологии, замене одних вспомогательных веществ другими и пр. проводятся обязательные исследования биодоступности веществ из таблеток. Например, при изготовлении таблеток нитроглице-рина тритурационным методом биодоступность стала в 2,1 раза больше, чем у таблеток, получаемых по прежней технологии, причем время достижения максимальной концентрации в крови равнялось уже 30 мин (ранее 3 часа), (Лепахин В.К., и др., 1982 г.).
За рубежом наиболее значительные различия в биодоступности веществ в форме таблеток, обнаружены, кроме дигоксина, для хлорамфеникола, окситетрациклина, тетрацик-лина, гидрохлортиазида, теофиллина, рибофлавина и некоторых др.
Поэтому при закупке по импорту или воспроизводстве технологии таблеток по лицензиям возникает также необходи-мость установления параметров фармацевтической и особенно биологической доступности. Для примера приводим результаты исследования (Холодов Л.Е. и др., 1982 г.) биодоступности противосклеротического вещества 2,6-пиридиндиметанол-бисметилкарбамат из его таблеток-аналогов по 0,25: пармидина (улучшение микроциркуляции при атеросклерозе сосудов мозга и сердца) (Россия), ангинина (Япония) и продектина (Венгрия). Установлено, что концентрация вещества в сыворотке крови при приеме пармидина и ангинина приблизительно одинакова, в то же время прием продектина приводит к примерно вдвое более низкой концентрации. Кажущаяся начальная концентрация С0 и площадь под кривой "концентрация - время" у пармидина и ангинина не различаются достоверно, и примерно вдвое выше, чем у продектина. На основании полученных данных сделано заключение, что биодоступность 2,6-пиридиндиметанол-бисметилкарбамата при приеме продектина (таблетки из ВНР) примерно в 2 раза меньшая, чем для таблеток пармидина и ангинина.
Ректальные лекарственные формы – суппозитории, ЖРК, микроклизмы и другие. Углубленными биофарма-цевтическими и фармакокинетическими исследованиями установлены значительные преимущества ректального назначения различных лекарственных препаратов с веществами, относящимися практически ко всем известным фарма-кологическим группам.
Так, для послеоперационной профилактики тромбоэмбо-лий рекомендуются суппозитории с бутадионом, введение которых обеспечивает более высокий уровень вещества в крови и снижение числа побочных действий этого вещества, чем после пероралъного приема таблеток (Thuele и др., 1981 г.).
Ректальное введение индометацина, фенилбутазона обеспечивает кроме высокой биологической доступности и пролонгирование действия этих противовоспалительных средств (Тенцова Л.И., 1974 г.;Reinicre 1984-85 гг.).
Ректальное введение морфина гидрохлорида в дозе 0,3 мг/кг женщинам перед гинекологическими операциями по показателю биодоступности и эффективности не уступает в/м инъекциям этого вещества (Westerling I984).
Ректальные лекарственные формы с препаратами сердечных гликозидов представляют исключительный интерес при значительных нарушениях функции сердечно-сосудистой системы. Суппозитории, микроклизмы, ректоаэрозоли обеспечи-вают не только быстроту доставки активных ингредиентов в организм, но и способствуют снижению их нежелательного побочного действия.
Так, строфантин и коргликон в ректальных суппозиториях (Пешехонова Л.Л., 1982-84) имеют весьма высокие значения биодоступности, при этом отмечается существенное снижение их побочного нежелательного действия, характерного для инъекционных препаратов.
Особого внимания заслуживает установление параметров биодоступности вещества в ректальных лекарственных форм для проведения вводного наркоза у детей. Ряд авторов отмечают более высокую биологическую доступность флунитразепама в ректальных суппозиториях в сравнении с в/м инъекцией. Установлено, что ректальная премедикация флунитразепамом обеспечивает хорошую адаптацию детей к наркозу, без побочных проявлений.
Описаны результаты успешной премедикации у детей композициями транквилизаторов и барбитуратов в форме суппозиториев и микроклизм.
Вид суппозиторной основы, природа примененного ПАВ, физическое состояние введенного лекарственного вещества (раствор, суспензия, эмульсия), интенсивность и вид технологической переработки (плавление, выливание, прессова-ние и др.) оказывают существенное влияние не только на скорость и полноту всасывания различных веществ из ректальных лекарственных форм, но и на уровень побочного действия, характерного для некоторых веществ.
Отмечается значимое влияние природы суппозиторной основы на фармацевтическую и биологическую доступности аминофиллина, эуфиллина, дипрофиллина, парацетамола и других веществ в суппозиториях. Причем биологическая доступность парацетамола в форме суппозиториев может варьировать от 68% до 87% в зависимости от применяемой технологии и суппозиторной основы (Feldman, 1985). Для ацетилсалициловой кислоты отчетливо прослеживается снижение уровня элиминации с мочой после введения больным суппозиториев, содержащих крупные кристаллы этого вещества с покрытием защитной оболочкой.
Мази - наиболее распространенная лекарственная форма в дерматологической практике. Путем введения лекарственных веществ в различные основы, применением всевозможных вспомогательных веществ (солюбилизаторов, диспергаторов, ПАВ, ДМСО и пр.) удается резко повысить интенсивность (скорость и степень) всасывания лекарственных веществ или, наоборот, значительно уменьшить ее.
Так, сульфаниламидные вещества оказывают наибольший терапевтический эффект при введении их в эмульсионные мазевые основы. Добавлением твина-80 удается повысить всасывание норсульфазола из мазевой основы (вазелин) с 0,3% до 16,6%. Добавками различных не неионогенных ПАВ удается резко увеличить бактерицидное действие мазей с фенолом, некоторыми антибиотиками и сульфаниламидами.
Биофармацевтические исследования разработанных на кафедре технологии лекарств ЗГМУ мазей с фенхизолом и мази «Бутамедрол» подтвердили значительную зависимость биодоступности действующих веществ из мазей от природы мазевой основы. Полиэтиленоксидная мазевая основа обеспечивала не только интенсивное высвобождение ингредиентов, но и способствует значительно более высокому уровню биологической доступности хиназопирина и бутадиона в сравнении с другими гидрофильными и гидрофобными основами. При сравнении импортной мази "Бутадион" (ВНР) и разработанной на кафедре (Л.А. Пучкан) мази "Бутамедрол" достоверно установлено, что по силе противовоспалительного действия, благодаря научно-обоснованному выбору носителя, последняя превосходит импортный препарат в 1,5 - 2,1 раза.
Станоева Л. с соавт. подтвердили значительное влияние природы мазевой основы на биодоступность этакридина лактата в форме мази, ряд авторов установили влияние мазевой основы на биологическую доступность дексаметазона (Moes-Henschel 1985), салициловой кислоты и др.
К примеру, при одной и той же дозе анестетика панакаина в мази, сила обезболивающего эффекта мази с ним в зависимос-ти от природы основы колебалась от 10 до 30 раз.
Таким образом, в биофармацевтическом эксперименте установлено влияние на параметры фармацевтической и биологической доступностей и вида лекарственных форм. Степень влияния лекарственной формы на процессы высвобождения и всасывания определяются ее составом, физическим состоянием компонентов, технологическими особенностями приготовления и другими переменными факторами, что особенно проявляется для моделированных лекарственных форм. Согласно Gibaldi (1980) по фармацев-тической доступности все основные лекарственные формы можно расположить в следующем порядке: растворы > микрокристаллические суспензии > РЛФ > капсулы > таблетки > таблетки, покрытые оболочками.
Лекция 6
