Адсорбционные равновесия и процессы на неподвижных границах раздела фаз.
Задания для самостоятельной работы
10.7. При уменьшении концентрации раствора новокаина с 0,2 моль/л до 0,15 моль/л поверхностное натяжение возросло с 6,9 10-2Н/м до 7,1 10-2Н/м, а у раствора кокаина с 6,5 10-3Н/м до 7,0 10-2Н/м. Сравните величины адсорбции двух веществ в данном интервале концентраций (T = 298 К).
10.11. Оцените, во сколько раз поверхностная активность пентанола будет больше поверхностной активности этанола в разбавленных растворах одинаковой концентрации.
10.15. Площадь поперечного сечения молекулы этилацетата равна 2,2 10-19м2. Определите длину молекулы данного вещества (плотность этилацетата 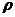 = 0,9 г/мл).
= 0,9 г/мл).
10.16. Величина предельной адсорбции высших предельных спиртов составляет 7,69 10-6моль/м2. Определите длину молекулы пропанола и бутанола. Какова площадь поперечного сечения молекулы спиртов этого ряда? (Плотность пропанола и бутанола равна соответственно 0,804 г/мл и 0,809 г/мл).
10.17. Плотность поперечного сечения молекулы олеата натрия составляет 2,8 10-19м2. Вычислите объем раствора 5 г вещества в 1 л бензола, требуемый для покрытия монослоем (после испарения бензола) 2 м2водной поверхности?
10.27. К водному раствору этилацетата объемом 70,00 мл с поверхностным натяжением 50 мН/м добавили активированный уголь массой 2 г. После установления адсорбированного равновесия поверхностное натяжение увеличилось до 56 мН/м. Определите величину адсорбции этилацетата на активированном угле (см. изотерму поверхностного натяжения водного раствора этилацетата при 298 К).
Занятие 10
Получение и устойчивость дисперсных систем.
Дата_________Лабораторная работа № ______
Способы получения дисперсных систем. Коагуляция золей электролитами.
Цель работы: Изучить способы получения и очистки коллоидных растворов, их оптические свойства. Приобрести навыки измерения порогов коагуляции золей и коагулирующей способности электролитов, научится пептизировать осадки электролитами.
Оборудование и реактивы:Проекционный фонарь; горелка газовая; пробирки; капельницы; воронка; пипетки глазные; фильтровальная бумага; бюретки.
Раствор канифоли в этаноле; растворы: гексацианоферрата(II) калия, нитрата серебра, сульфата меди; раствор танина. Гидрозоль гидроксида железа(III); раствор сульфата натрия (с(Na2SO4)= 0,0025 моль/л); раствор гексацианоферрата(III) калия (с(К3[Fe(CN)6])=0,0025 моль/л); растворы хлорида железа(III) (с(FeCl3) = 0,5 моль/л и насыщенный); раствор аммиака и соляная кислота, с(HCl)=0,1 моль/л.
Ход работы:
Опыт 1.Получение гидрозоля канифоли методом замены растворителя.
В пробирку наливают приблизительно 10 мл (1/2 пробирки) дистиллированной воды и добавляют 5 капель раствора канифоли в этаноле.
Смесь энергично перемешивают и, зажав пробирку в держателе, нагревают до кипения для удаления избытка этанола.
Для наблюдения эффекта Фарадея-Тиндаля пробирку с коллоидным раствором помещают на пути луча света проекционного фонаря. Рассматривают пробирку под углом 900 к направлению падающего луча. Результаты наблюдений записывают в таблицу.
Опыт 2. Получение гидрозоля гидроксида железа(III) методом гидролиза.
В пробирку наливают приблизительно 10 мл (1/2 пробирки) дистиллированной воды и нагревают до кипения; в кипящую воду добавляют 5 капель раствора хлорида железа (III) и продолжают нагревание до появления красно- бурой окраски. Наблюдают, образуется ли конус Фарадея-Тиндаля при пропускании пучка света через полученный раствор.
Уравнение реакции:
Схема строения мицеллы:
Опыт 3. Получение гидрозоля серебра методом восстановления.
В пробирку наливают приблизительно 10 мл дистиллированной воды и добавляют 4-5 капель 0,1% раствора нитрата серебра; полученный раствор нагревают до кипения и по каплям, с интервалами в 1 мин, добавляют 1% раствор танина до появления устойчивой желтой окраски.
Наблюдают, образуется ли конус Фарадея-Тиндаля при пропускании пучка света через полученный раствор. Золь серебра выливают в специальную склянку. Результаты наблюдений записывают в таблицу.
Экспериментальные данные.
| Опыт | Золь | Метод получения | Внешний вид | Наблюдение конуса рассеяния света | ||
| Физический или химический | Диспергирование или конденсация | В проходящем свете | В отраженном свете | |||
Опыт 4. Определение порогов коагуляции.
1. Проводят последовательно два опыта с растворами электролитов Na2SO4 и К3[Fe(CN)6]. Готовят исходные растворы электролита различных концентраций, смешивая в пяти пробирках отмеренные с помощью бюреток исходный раствор электролита и дистиллированную воду в соотношениях, указанных в таблице.
2. В пять хорошо вымытых пробирок отмеривают из бюретки по 5,0 мл гидрозоля железа(III). Во все пробирки с золем приливают по возможности одновременно приготовленные растворы электролита и тотчас же перемешивают. Через 10 мин отмечают, в каких пробирках наблюдается помутнение или образование осадка. Результаты наблюдений записывают в таблицу: знаком «+» отмечают наличие коагуляции, знаком «─» отсутствие.
Экспериментальные данные.
| Пробирка | Объем, мл | Результаты наблюдений Коагулирующий электролит | |||
| Раствор электролита | Вода | Na2SO4 | К3[Fe(CN)6]. | ||
| 2,5 | 0,5 | ||||
| 2,0 | 1,0 | ||||
| 1,5 | 1,5 | ||||
| 1,0 | 2,0 | ||||
| 0,5 | 2,5 |
