Изомерия комплексных соединений
Изомерия комплексных соединений связана
1) с возможным различным расположением лигандов и внешнесферных частиц,
2) с различным строением самой комплексной частицы.
К первой группе относится гидратная (в общем случае сольватная) и ионизационная изомерия, ко второй – пространственная и оптическая.
Гидратная изомерия связана с возможностью различного распределения молекул воды во внешней и внутренней сферах комплексного соединения, например: [Cu(H2O)2Br2] (цвет красно-коричневый) и [Cu(H2O)4]Br2 (цвет голубой).
Ионизационная изомерия связана с возможностью различного распределения ионов во внешней и внутренней сфере, например: [Co(NH3)5Br]SO4 (пурпурного цвета) и [Co(NH3)5SO4]Br (красного цвета). Первое из этих соединений образует осадок, реагируя с раствором хлорида бария, а второе – с раствором нитрата серебра.
Пространственная (геометрическая) изомерия, иначе называемая цис-транс изомерией, характерна для квадратных и октаэдрических комплексов (для тетраэдрических невозможна). Пример: цис-транс изомерия квадратного комплекса [Pt(NH3)2Cl2]
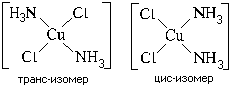
Оптическая (зеркальная) изомерия по своей сути не отличается от оптической изомерии в органической химии и характерна для тетраэдрических и октаэдрических комплексов (для квадратных невозможна).
 Комплексное (координационное) соединение, комплексная частица, комплексообразователь, лиганды, дентатностьлиганда, координационное число, координационный полиэдр, внутренняя сфера, внешняя сфера, аквакомплексы, гидроксокомплексы, аммиакаты, ацидокомплексы, гидридные комплексы, карбонильные комплексы, анионгалогенатные комплексы, спектрохимический ряд лигандов
Комплексное (координационное) соединение, комплексная частица, комплексообразователь, лиганды, дентатностьлиганда, координационное число, координационный полиэдр, внутренняя сфера, внешняя сфера, аквакомплексы, гидроксокомплексы, аммиакаты, ацидокомплексы, гидридные комплексы, карбонильные комплексы, анионгалогенатные комплексы, спектрохимический ряд лигандов
 1.В следующих комплексных соединениях укажите центральный атом, лиганды, внутреннюю и внешнюю сферы; определите заряд комплексной частицы, степень окисления центрального атома и его координационное число. Назовите эти соединения и укажите к какому классу комплексов относятся комплексные частицы, входящие в состав соединений и к какому классу химических веществ относится каждое из этих соединений.
1.В следующих комплексных соединениях укажите центральный атом, лиганды, внутреннюю и внешнюю сферы; определите заряд комплексной частицы, степень окисления центрального атома и его координационное число. Назовите эти соединения и укажите к какому классу комплексов относятся комплексные частицы, входящие в состав соединений и к какому классу химических веществ относится каждое из этих соединений.
а) [Zn(NH3)4](NO3)2; б) [Cr(CO)6]; в) K3[Co(NO3)6].H2O; г) Ca[Cr(NH3)2(NCS)4]2; д) [Cu(NH3)4]SO4.H2O; е) [K(H2O)6][Cr(H2O)6](SO4)2; ж) [H3O]3[FeCl6].H2O; и) K[Ag(CN)2]; к) Na3[FeF6]; л) Na[Sb(OH)6]; м) K2[HgI4]; н) [Cr(H2O)6]Cl3; п) [Cr(H2O)4Cl2]Cl.2H2O; р) Cs[ICl4]; с) H[AuCl4]; т) K[I(I)2]; у) Li[AlH4]; ф) [Cu(NH3)4](OH)2; х) [N(CH3)4]Cl; ц) [P(C6H5)4][B(C6H5)4]; ?) [H3O][AuBr4].4H2O; o) [PCl4][PCl6]. 2.Составьте формулы следующих комплексных соединений:
гексахлоропалладат(IV) аммония;
дихлороаргентат(I) цезия;
гидроксотрихлороаурат(III) оксония;
гексабромоиридат(III) калия;
сульфат дихлоротетраамминкобальта(III);
тетрагидридоборат цезия;
гексакарбонилхром.
3.Молекула гидразина способна присоединять один или два протона и образовывать соли с сильными кислотами. Составьте структурные формулы двух разных сульфатов гидразиния.
4.Если возможно присоединение протона к молекуле воды с образованием иона оксония, то почему не происходит присоединение второго протона с использованием второй неподеленной пары электронов атома кислорода?
5.Объясните, почему невозможна следующая реакция: Fe3 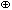 + 6H3O
+ 6H3O 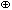 = [Fe(H3O)6]9
= [Fe(H3O)6]9 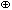 .
.
6.Из водного раствора, содержащего 0,04 моля комплексного соединения состава PtCl4.3NH3, при добавлении нитрата серебра осаждается 0,04 моля хлорида серебра. По результатам этого опыта составьте координационную (предельно упрощенную структурную) формулу соединения.
7.Из водного раствора, содержащего 0,2 моля комплексного соединения состава CoBr3.5NH3, при добавлении избытка раствора нитрата серебра осаждается 0,4 моля бромида серебра. По результатам этого опыта составьте координационную формулу соединения.
8.Составьте схему валентных орбиталей центрального атома, определите тип гибридизации АО этого атома и строение следующих комплексных частиц:
а) [Pb(OH)3] 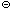 ; б) [Sb(OH)6]
; б) [Sb(OH)6] 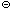 ; в) [Zn(CN)4]2
; в) [Zn(CN)4]2 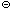 ; г) [Al(H2O)6]3
; г) [Al(H2O)6]3 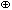 ; д) [Zn(H2O)4]2
; д) [Zn(H2O)4]2 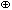 ; е) [Fe(CN)6]3
; е) [Fe(CN)6]3 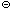 ; ж) [Mn(CN)6]3
; ж) [Mn(CN)6]3 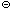 ; и) [Mg(H2O)6]2
; и) [Mg(H2O)6]2 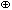 ; к) [Be(H2O)4]2
; к) [Be(H2O)4]2 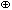 ; л) [Ag(NH3)2]
; л) [Ag(NH3)2] 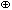 ; м) [Cu(NH3)2]
; м) [Cu(NH3)2] 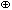 ; н) [Au(CN)2]
; н) [Au(CN)2] 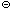 ; п) [Cu(NH3)4]2
; п) [Cu(NH3)4]2 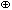 ; р) [MnCl6]2
; р) [MnCl6]2 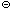 ; с) [Cu(CN)2]
; с) [Cu(CN)2] 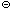 ; т) [SnF3]
; т) [SnF3] 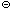 ; у) [Be(OH)4]2
; у) [Be(OH)4]2 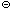 ; ф) [Sn(OH)6]2
; ф) [Sn(OH)6]2 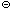 ; х) [Fe(H2O)6]3
; х) [Fe(H2O)6]3 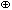 ; ц) [Ni(H2O)6]2
; ц) [Ni(H2O)6]2 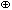 ; ч) [Au(CN)4]
; ч) [Au(CN)4] 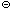 .
.
9.Определите общее число возможных изомеров комплексного соединения CrCl3.5H2O, составьте их формулы и названия. 10.Осуществите следующие превращения:
а) CuSO4 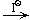 CuI
CuI 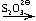 Na3[Cu(S2O3)2]
Na3[Cu(S2O3)2] 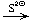 Cu2S;
Cu2S;
б) Cu2O 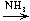 [Cu(NH3)2]OH
[Cu(NH3)2]OH 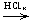 H[CuCl2];
H[CuCl2];
в) CuSO4 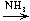 (CuOH)2SO4
(CuOH)2SO4 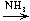 [Cu(NH3)4]SO4
[Cu(NH3)4]SO4 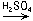 CuSO4;
CuSO4;
г) AgNO3 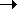 AgCl
AgCl 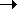 [Ag(NH3)2]Cl
[Ag(NH3)2]Cl 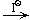 AgI
AgI 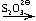 Na3[Ag(S2O3)2]
Na3[Ag(S2O3)2] 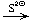 Ag2S;
Ag2S;
д) FeCl3 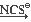 Na3[Fe(H2O)4(NCS)2]
Na3[Fe(H2O)4(NCS)2] 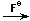 Na3[FeF6];
Na3[FeF6];
е) CoCl2 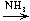 [Co(NH3)6]
[Co(NH3)6] 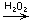 [Co(NH3)6]Cl2(OH);
[Co(NH3)6]Cl2(OH);
ж) Hg(NO3)2 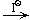 HgI2
HgI2 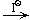 [HgI4]2
[HgI4]2 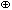
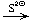 HgS.
HgS.
 Опыт 1. Образование аквакомплекса. 1 микрошпатель безводного сульфата меди поместить в пробирку и по каплям добавить воду. Наблюдать происходящие изменения. Составить химические уравнения протекающих процессов.
Опыт 1. Образование аквакомплекса. 1 микрошпатель безводного сульфата меди поместить в пробирку и по каплям добавить воду. Наблюдать происходящие изменения. Составить химические уравнения протекающих процессов.
Опыт 2. разрушение аквакомплекса. 1 микрошпательгептагидрата сульфата никеля поместить в пробирку. Пробирку закрепить в штативе и сначала осторожно, а затем интенсивно нагреть на открытом пламени. Отметить изменения цвета соли. Зная, что на первом этапе удаляется одна молекула воды, а на втором шесть, составить, структурную формулу исходного соединения.
Опыт 3. Образование аммиакатов. К раствору сульфата меди, полученному в первом опыте, добавить 5 - 6 капель раствора аммиака. Наблюдать изменение окраски. То же проделать с раствором сульфата никеля. Составить ионные уравнения реакции.
Опыт 4. Разрушение аммиаката. К раствору, содержащему аммиакат меди, полученный в предыдущем опыте, добавить несколько капель разбавленной серной кислоты до изменения окраски раствора. Составит уравнения реакций и объяснить происходящие изменения.
Опыт 5. Образование и разрушение гидроксокомплекса. K ?anoai?onoeeoeiea (3-4 капли) добавить по каплям ?anoaвор щелочи. Наблюдать образование и дальнейшее растворение осадка. Затем в полученный раствор по каплям добавить соляную кислоту до растворения первоначально выпадающего осадка. Составит уравнения реакций и объяснить происходящие изменения.
Опыт 6. Получение ацидокомплексов. К 2-3 каплям раствора хлорида железа(III) добавить iieaieyi 8 eaiaeu ?anoai?aoeioeaiaoa (роданида) аммония. Затем добавить раствор фторида натрия до обесцвечивания. Составить уравнения реакций и объяснить изменение цвета раствора.
Опыт 7. Получение полигалогенида. 2-3 кристаллика йода поместить в пробирку и добавить в нее 2 капли воды. Что происходит? Добавить в пробирку 5-6 капель раствора йодида калия и перемешать. Наблюдать происходящие изменения.оставить уравнение реакции.
Самостоятельная работа
1. Составьте формулы комплексных солей, обозначьте заряды ионов:
AgNO3 + 2NH3 = … ([Ag+(NH3)2]NO3–),
PtCl4 + 2KCl = … (K2+[Pt4+Cl6]2–).
2. Cвязи во внутренней сфере комплексного соединения между комплексообразователем и лигандами:
а) донорно-акцепторные; б) ионные;
в) ковалентные неполярные; г) водородные.
Ответ. а.
3. Проверьте предложенные названия комплексных соединений. Если название неправильное, дайте верный вариант.
[Аl(Н2О)6]Сl3 – хлорид гексаакваалюминия (верно),
K2[PtCl6] – гексахлоридплатинат(IV) калия (надо: гексахлороплатинат(IV) калия),
Na2[Zn(OH)4] – тетрагидроксоцинкат натрия (верно),
[Сu(NH3)4](OH)2 – гидроксидтетрааммиакат меди (надо: гидроксид тетраамминмеди(II)),
NH4Cl – хлорид аммония (верно),
[Ag(NH3)2]Cl – хлориддиаммин серебра(I) (надо: хлорид диамминсеребра(I)).
Тезисы сообщений учащихся выглядят следующим образом.
Гальванические покрытия предназначены для защиты одного металла другим. Например, медью покрывают железо. Покрытие наносят с помощью комплексных соединений, тогда медь крепко соединяется с железом.
Электролитическое получение металлов удобно рассмотреть на примере алюминия. Алюминий получают электролизом раствора Al2O3 в расплаве криолита Na3[AlF6] при 900–950 °С. Из расплавов соединений комплексных солей получают также металлические Nb, Tl, Th, Mg.
Защита металлов от коррозии. Ингибиторы – комплексные органические вещества или комплексные соли, замедляющие коррозию металлических изделий.
В аналитической химии комплексные соединения находят применение как реактивы, индикаторы, которые помогают распознать вещества или ионы.
